2. 城市水资源与水环境国家重点实验室(哈尔滨工业大学), 哈尔滨 150090
2. State Key Laboratory of Urban Water Resource and Environment(Harbin Institute of Technology), Harbin 150090, China
厌氧氨氧化工艺因无需外加碳源、污泥产量低等优点成为目前已知最为节能、经济的脱氮途径[1-3], 而作为厌氧氨氧化前段工艺的亚硝化的稳定运行一直是研究的热点和难点[4-5].目前,亚硝化反应器类型的研究正在由SBR向连续流反应器转变, 而CSTR(恒流搅拌反应器)作为典型的连续流反应器备受重视.目前,文献中提到的亚硝化的控制因素主要有pH、温度[6]、基质浓度[7]、超声波处理[8]、投加抑制剂[9]、溶解氧(DO)、水力停留时间(HRT)[10]、缺氧/好氧[11]等.然而, 在污水处理厂的实际运行中, pH、温度、基质浓度属于原水自然属性,难以人为改变; 投加抑制剂在工程上的可行性和经济性仍有质疑; 超声波处理对亚硝化的影响还存在较大争议.相比之下, 协同控制HRT和DO以及缺氧/好氧的运行方式在实际工程中的可行性和经济性更强.然而, 在对实际生活污水的处理上, 针对以上两种方式的研究还很少, 对二者进行比较的研究更是鲜有报道.
为此, 采用两组2级CSTR, 1#采用协同控制DO和HRT的方式运行, 2#采用缺氧/好氧的策略运行, 对两种运行效果进行比较, 以期提出亚硝化较快的启动策略及较稳定的运行策略, 为亚硝化的工程应用提供技术支持.
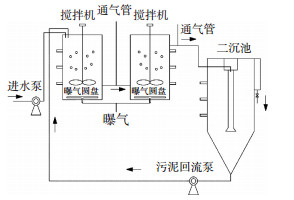
1 实验 1.1 实验装置和方法实验在北京某污水厂进行, 采用两组相同的2级CSTR (1#、2#), 如图 1所示.2级CSTR中各级的有效容积为7 L, 通气管的目的是使2级CSTR水流通畅, 每一级底部设置曝气沙盘, 通过可调式气泵为反应过程提供溶解氧, 由转子流量计控制气量.
|
图 1 反应器装置示意 Figure 1 Schematic diagram of the experimental equipment |
启动前5 d为固定1#2级DO确定HRT阶段, 采用试算法, 即设置1#2级DO分别为0.6~0.8和0.2~0.4 mg/L, 根据经验数据初定1#的HRT为6 h, 试运行5 d, 期间测定出水NH4+-N、NO2--N、NO3--N的变化情况, 若氨氧化率在90%以上, 则将HRT每次缩短0.5 h直到氨氧化率在(70±5)%为止.为使1#和2#的亚硝化效果更具可比性, 最终确定5.5 h作为1#和2#共同的HRT.
1.2 实验用水和接种污泥如表 1所示, 1#和2#共同经历了3个阶段, 即启动阶段S1(第6~55天)、以原水经AO除磷出水为进水阶段S2(第56~75天)和以原水经AO除磷出水为进水但NH4+-N质量浓度下降的适应阶段S3(第76~95天), 各阶段进水NH4+-N质量浓度和运行参数见表 1.
在启动阶段S1采用人工模拟生活污水.向自来水中投加(NH4)2SO4至NH4+-N质量浓度为95~100 mg/L, 投加NaHCO3提供碱度, 碱度与NH4+-N质量比为10∶1, pH为7.5~8.0, 每1 L模拟废水中含有0.136 g KH2PO4, 同时含有微生物生长必需的微量元素.在S2阶段采用城市污水厂原污水经AO除磷后的出水为进水, 即NH4+-N质量浓度为35~43 mg/L, COD<50 mg/L(几乎全部是微生物难降解的物质), ρ(NOx--N)<2 mg/L.在S3阶段继续采用原污水经AO除磷后的出水, 但由于降雨的稀释作用和亚硝化前段AO除磷反应器中NH4+-N的损失,使得亚硝化进水中NH4+-N质量浓度下降到27~33 mg/L, COD<50 mg/L, ρ(NOx--N)<5 mg/L, 磷的质量浓度为1~2.3 mg/L.此时NH4+-N质量浓度的下降和孙艳等[12]的调研结果(北京地区的污水处理厂在7~9月份进水NH4+-N质量浓度下降)相吻合.因此,研究两种运行方式对于进水NH4+-N质量浓度下降的适应性, 可为实际工程中“如何应对原水中NH4+-N的波动”这一不可避免的问题提供宝贵经验.1#和2#的接种污泥来自A2O曝气池, MLSS为3 750 mg/L, MLVSS为2 850 mg/L, 污泥沉降性能良好, SVI为95 mL/g.
| 表 1 各阶段反应器参数变化 Table 1 Parameter variations of each stage |
定期检测反应器内混合液的MLSS、SV30及进出水NH4+-N、NO2--N、NO3--N的质量浓度等参数, 通过WTW便携式测定仪测定DO、pH和水温等.水样分析中NH4+-N测定采用纳氏试剂光度法, NO2--N采用N-(1-萘基)乙二胺光度法, NO3--N采用紫外分光光度法, COD采用快速测定仪[13].
氨氧化率RA、亚硝化率RN和游离氨(FA)按下式计算:
| $ {R_{\rm{A}}}=\frac{{\rho ({\rm{NH}}_4^ +-{\rm{N}})}}{{{\rho _{{\rm{in}}}}({\rm{NH}}_4^ +-{\rm{N}})}} \times 100\%.$ | (1) |
式中:ρin(NH4+-N)为进水NH4+-N质量浓度, mg/L; ρ(NH4+-N)为进出水NH4+-N质量浓度差, mg/L.
| $ {R_N}=\frac{{\rho (NO_2^--N)}}{{{\rho _{{\rm{in}}}}(NO_2^--N) + \rho (NO_3^--N)}} \times 100\%. $ | (2) |
式中:ρ(NO2--N)为进出水NO2--N的质量浓度差, mg/L; ρ(NO3--N)为进出水NO3--N的质量浓度差, mg/L.
| $ \rho (FA)=\frac{{17 \times {\rho _{{\rm{inner}}}}(NH_4^ +-N) \times {{10}^{{\rm{pH}}}}}}{{14 \times ({e^{6344/(273 + T)}} + {{10}^{{\rm{pH}}}})}}. $ | (3) |
式中:ρinner(NH4+-N)为反应器内NH4+-N质量浓度, mg/L; T为水温, K.
2 结果与讨论 2.1 启动时间的比较根据AOB的氧饱和常数为0.2~0.4 mg/L, NOB氧饱和常数为1.2~1.8 mg/L [14], 设置1#的2级DO分别为0.6~0.8和0.2~0.4 mg/L, 第一级中DO较高的目的是抑制接种污泥中的厌氧杂菌, 同时更好地利用2级DO梯度实现NO2--N的积累[15].2#中第一级只搅拌不曝气, 不控制DO, 经过测定其DO在0~0.1 mg/L, 第二级搅拌并曝气, 控制DO为0.6~0.8 mg/L.
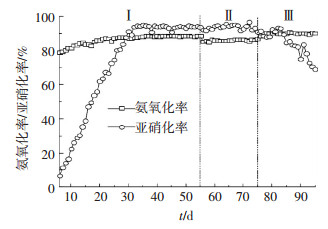
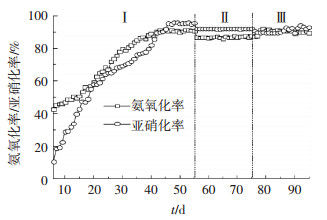
如图 2所示, 1#经过26 d(第5~31天)的运行, 氨氧化率达86.94%, 亚硝化率达93.10%.如图 3所示, 2#经过41 d(第5~46天)的启动,氨氧化率变为88.31%, 亚硝化率变为93.02%.说明两种方式都可以成功启动亚硝化, 但启动快慢有差异.亚硝化启动的实质是AOB的富集以及NOB等其他杂菌的被抑制并淘洗的过程.因为两种运行方式都提供了适宜AOB但不适宜甚至抑制NOB等其他细菌生存的环境, 即低DO(0.2~0.8 mg/L)、充足的基质NH4+-N ((95±5) mg/L)、较高FA(1.0~3.74 mg/L)等条件, 最终都会实现亚硝化的启动.
二者的启动时间相差15 d, 主要原因是2#中缺氧/好氧的运行方式在第一级只搅拌不曝气, DO在0~0.1 mg/L不能为AOB提供充足的溶解氧, 使得在第6~31天, 2#中NH4+-N氧化平均值比1#少23.79 mg/L, NO2--N积累的平均值少13.98 mg/L.在其他条件相同时, 溶解氧成为2#中AOB生长的限制因素, 导致其富集较慢, 启动时间也相对较长.
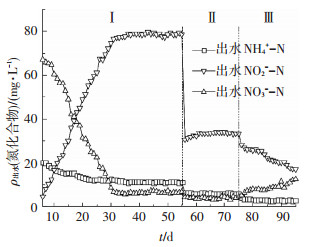
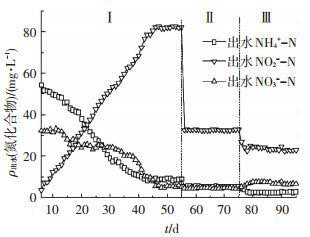
如图 4、5所示, 在第6天时1#和2#出水NO3--N分别为67.20和32.31 mg/L, 说明开始阶段缺氧/好氧运行方式能更好地抑制NOB, 基于上述分析能否在2# 2级CSTR总体积不变且进水负荷一定的条件下, 通过相对增大好氧段体积或者提高好氧段内的DO,达到既能够抑制NOB,又能为AOB提供充足的DO使其快速富集, 进而快速启动亚硝化有待进一步研究.
|
图 2 1#亚硝化率及氨氧化率变化 Figure 2 Variation of ammonia oxidation rate and nitrite accumulation rate in 1# |
|
图 3 2#亚硝化率及氨氧化率变化 Figure 3 Variation of ammonia oxidation rate and nitrite accumulation rate in 2# |
|
图 4 1#出水NH4+-N、NO2--N、NO3--N变化 Figure 4 Variation of NH4+-N, NO2--N and NO3--N concentration in effluent in 1# |
|
图 5 2#出水NH4+-N、NO2--N、NO3--N变化 Figure 5 Variation of NH4+-N, NO2--N and NO3--N concentration in effluent in 2# |
启动历程表明, 与缺氧/好氧的运行方式相比, 控制DO/HRT能更快地启动亚硝化.
2.2 原水稳定运行阶段的比较 2.2.1 亚硝化效果的比较在1#和2#亚硝化启动成功后, 为强化亚硝化效果, 从第46~55天继续采用人工模拟废水且水质保持不变, 1#和2#在第46~55天亚硝化率均在90%以上, 说明两者亚硝化效果均已得到很好维持.此后, 为了比较两种运行方式对生活污水处理上的差异, 进行了S2阶段(第56~75天)的研究, 从第56天转变进水为原水经AO除磷后的出水, 随着进水NH4+-N质量浓度的下降, 如表 1所示1#、2#的HRT降低到3 h, 而1#在第56~75天氨氧化率和亚硝化率的平均值为85.74%和93.39%, 与1#相似, 2#分别为86.80%、91.76%, 说明经过驯化后的AOB可以适应AO除磷出水低NH4+-N的环境, 同时说明协同控制DO/HRT和缺氧/好氧这两种运行方式在以原水经AO除磷出水(NH4+-N质量浓度为35~43 mg/L)为进水时均能维持稳定的亚硝化效果.
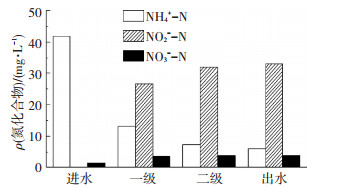
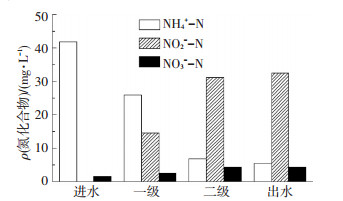
为深入分析1#和2#在S2阶段稳定运行的原因, 对二者2级的NH4+-N、NO2--N、NO3--N质量浓度进行测定, 结果如图 6、7所示, 在1#的第一级中NO2--N积累量达26.10 mg/L, 第二级达31.91 mg/L, 但是NO2--N转化为NO3--N的量很少, 原因在于通过控制DO介于AOB和NOB氧饱和常数之间使NOB被成功抑制, 此时, 协同控制HRT使得NH4+-N氧化为NO2--N时出水能维持较稳定的亚硝化效果.与1#相似, 2#的第1级和第2级中NO3--N的增加都很少,分别为0.31和2.81 mg/L, 说明在低NH4+-N条件下缺氧/好氧方式的亚硝化效果也较好, 这与Kornaros等[16]的研究相符, 对于缺氧/好氧下亚硝化稳定的机理在2.3部分进行说明.
|
图 6 1# S2阶段NH4+-N、NO2--N、NO3--N变化 Figure 6 Variation of NH4+-N, NO2--N and NO3--N concentration in pathway during S2 period in 1# |
污水处理厂曝气能耗约占处理成本的40%~50%[17], 因此,对两种运行方式下的曝气能耗进行比较非常必要.在S2阶段(第56~75天), 1#2级的曝气量分别为2.5~2.7和0.7~0.8 L/min, 2#第一级只搅拌不曝气, 第二级的曝气量为2.5~2.7 L/min.与1#相比, 2#节省的曝气能耗介于$\frac{{0.7}}{{2.7 + 0.7}}=20.59\% $和$\frac{{0.8}}{{2.5 + 0.8}}=24.24\% $[17], 而在具体的实验过程中曝气量是有波动的,因此,在二者亚硝化效果基本相同的前提下, 2#比1#节省了约20%的曝气能耗.
|
图 7 2# S2阶段NH4+-N、NO2--N、NO3--N变化 Figure 7 Variation of NH4+-N, NO2--N and NO3--N concentration in pathway during S2 period in 2# |
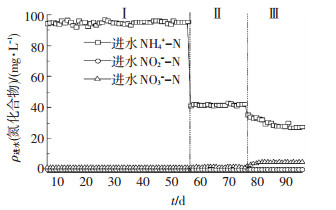
有研究表明, 北京地区的污水处理厂在7~9月份普遍发生进水NH4+-N质量浓度下降的现象, 主要是由于夏季雨水导致进水流量增大, 污染物质量浓度因为稀释作用而降低[12].因此,比较两种运行方式对NH4+-N质量浓度下降的适应性对于亚硝化应用到实际工程中有借鉴意义.如图 8所示, 在本实验的第76天进水NH4+-N也发生了下降的现象, 由43 mg/L左右持续下降到27 mg/L左右.进水NH4+-N质量浓度下降有2个原因, 一是原污水厂进水NH4+-N质量浓度下降, 二是在AO除磷反应器中污泥龄较长导致部分硝化菌未被淘汰, 使得少量NH4+-N被氧化为NO3--N.
|
图 8 进水NH4+-N、NO2--N、NO3--N变化 Figure 8 Variation of NH4+-N, NO2--N and NO3--N concentration in influent |
为了比较两种运行方式在对进水NH4+-N质量浓度下降适应性上的差异, 进行S3阶段(第76~95天)的研究.此阶段保持1#和2#的曝气量不变,考察二者对NH4+-N质量浓度下降的适应性.如表 1所示, 在第76~95天, 1#2级DO分别变为0.8~1.0、0.3~0.5 mg/L, 2# 2级DO变为0~0.1、0.8~1.0 mg/L.如图 2所示,在第95天1#的氨氧化率在90%左右, 而亚硝化率却由88.59%下降到67.39%说明亚硝化已经失稳.与1#不同, 2#在此阶段氨氧化率一直在90%以上, 亚硝化率也维持在88%以上, 这说明2#对于进水NH4+-N下降的适应性更强.
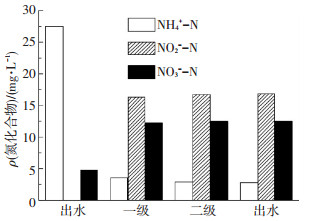
如图 9所示,以第95天为例, 在1#的第一级NH4+-N已经被氧化了87.00%, NO3--N增加到13.8 mg/L, 说明在NH4+-N质量浓度下降而HRT不变的条件下, NH4+-N在更短的时间被氧化, 1#和2#2级DO的上升也证明了这一现象.此时, NOB和NO2--N、DO接触时间变长, 为其生长提供了有利条件, 在长期的运行过程中NOB得到增殖, 亚硝化遭到破坏.这同时说明通过对DO/HRT的控制在进水NH4+-N质量浓度下降较大(由43 mg/L下降到27 mg/L)时很难维持连续流亚硝化的稳定.
|
图 9 1#第95天NH4+-N、NO2--N、NO3--N变化 Figure 9 Variation of NH4+-N, NO2--N and NO3--N concentration in pathway in 1# on 95th day |
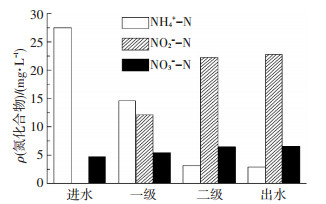
然而, 值得思考的是,如图 10所示,在进水水质、负荷等其他条件与1#都相同的2#也经历了进水NH4+-N质量浓度的下降, 其NH4+-N被氧化的时间也会缩短, 也有可能导致亚硝化失稳,但实际上并未发生这一现象.Yu等[18]的研究表明, 从缺氧到好氧过程中AOB能够比NOB更快地恢复活性, 原因在于二者对“饥饿”的动力学反应不同, Bournazou[19]和Kornaros等[16]进行了类似实验, 结果表明, 从缺氧到好氧的过程中NOB的生长速率下降很大.以上结论均为本实验的结果“缺氧/好氧的运行方式在进水NH4+-N质量浓度下降很大时能够抑制亚硝化向全程硝化转化”提供有力支撑.
本实验由于客观上进水只发生了NH4+-N质量浓度下降的现象, 而生活污水水量大、水质波动较大的特点使得污水处理厂进水NH4+-N也有突然上升的情况, 而此时缺氧/好氧运行能否依然维持较好的亚硝化效果还有待进一步研究.但是, 有一点是肯定的, 即本实验的条件下, 在进水NH4+-N质量浓度下降较大时, 与协同控制DO/HRT的运行方式相比, 缺氧/好氧运行确实维持了更好的亚硝化效果, 同时节省了约20%的曝气能耗.
|
图 10 2#第95天NH4+-N、NO2--N、NO3--N变化 Figure 10 Variation of NH4+-N, NO2--N and NO3--N concentration in pathway in 2# on 95th day |
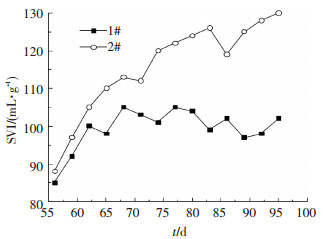
污泥膨胀一直是污水处理的一大难题[20], 研究表明, NO2--N的大量积累容易引起污泥的膨胀[21-22].因此, 有必要对两种运行方式下SVI进行比较.如图 11所示, 1#在第56~95天时SVI平均值为99 mL/g, 最大值为105 mL/g, 2#在这一过程中SVI平均值为115 mL/g, 最大值为130 mL/g.两种运行方式污泥沉降性能良好, 均未引起污泥膨胀, 2#沉降性能没有1#好的原因在于进水COD中仍有少量的可供异养菌降解的物质, 为丝状菌提供了一定的碳源, 且2#第一级中只搅拌不曝气的条件DO很低, 丝状菌氧饱和常数很低, 这样的条件为丝状菌提供了繁殖的可能, 使SVI增大, 但是最终并未引起污泥的膨胀.
以上分析说明两种运行方式污泥沉降性能良好, 这在一定程度上也说明了A/O除磷+亚硝化+厌氧氨氧化整套工艺在处理生活污水上的优势.
|
图 11 SVI变化 Figure 11 Variations of SVI |
1)在常温18~22℃、NH4+-N质量浓度为95~100 mg/L的条件下, 采用缺氧/好氧工艺与协同控制DO/HRT工艺分别用了41和26 d成功启动了亚硝化.
2)采用水质较稳定的AO除磷出水为进水时(NH4+-N质量浓度为35~43 mg/L), 两种运行方式均能维持较稳定的亚硝化, 且缺氧/好氧的运行方式节省了约20%的曝气能耗.
3)当进水NH4+-N质量浓度发生明显下降(由43 mg/L下降到27 mg/L)时, 缺氧/好氧运行方式亚硝化较稳定, 亚硝化率保持在88%以上, 而协同控制HRT和DO的方式亚硝化率下降到67.39%.
4)协同控制DO/HRT与缺氧/好氧运行的方式污泥沉降性能良好, 均未引起污泥膨胀.
| [1] |
TURK O, MAVINIC D S. Preliminary assessment of a shortcut in nitrogen removal from wastewater[J].
Canadian Journal of Civil Engineering,1986, 13 (6) : 600-605.
DOI: 10.1139/l86-094 ( 0) 0)
|
| [2] |
BARTROLI A, PEREZ J, CARRERA J. Applying ratio control in a continuous granular reactor to achieve full nitritation under stable operating conditions[J].
Environmental Science and Technology,2010, 44 (23) : 8930-8935.
DOI: 10.1021/es1019405 ( 0) 0)
|
| [3] |
STAR W, ABMA W R, DENNIS B, et al. Startup of reactors for anoxic ammonium oxidation: experiences from the first full-scale anammox reactor in Rotterdam[J].
Water Research,2007, 41 (18) : 4149-4163.
DOI: 10.1016/j.watres.2007.03.044 ( 0) 0)
|
| [4] |
CHUANG H P, OHASHI A, IMACHI H, et al. Effective partial nitrification to nitrite by down-flow hanging sponge reactor under limited oxygen condition[J].
Water Research,2007, 41 (2) : 295-302.
DOI: 10.1016/j.watres.2006.10.019 ( 0) 0)
|
| [5] |
FUX C, BOEHLER M, HUBER P, et al. Biological treatment of ammonium-rich wastewater by partialnitritation and subsequent anaerobic ammonium oxidation (anammox) in a pilot plant[J].
Journal of Biotechnology,2002, 99 (3) : 295-306.
DOI: 10.1016/S0168-1656(02)00220-1 ( 0) 0)
|
| [6] |
GABARRO J, GANIGUE R, GICH F, et al. Effect of temperature on AOB activity of a partial nitritation SBR treating landfill leachate with extremely high nitrogen concentration[J].
Bioresource Technology,2012, 126 : 283-289.
DOI: 10.1016/j.biortech.2012.09.011 ( 0) 0)
|
| [7] |
PENG Y, ZHANG S, ZENG W, et al. Organic removal by denitritation and methanogenesis and nitrogen removal by nitritation from landfill leachate[J].
Water Research,2008, 42 (4) : 883-892.
( 0) 0)
|
| [8] |
ZHENG M, LIU Y, XU K, et al. Use of low frequency and density ultrasound to stimulate partial nitrification and simultaneous nitrification and denitrification[J].
Bioresource Technology,2013, 146 : 537-542.
DOI: 10.1016/j.biortech.2013.07.044 ( 0) 0)
|
| [9] |
SANHA B, ANNACHHATRE A P. Partial nitrification—operational parameters and microorganisms involved[J].
Reviews in Environmental Science and Bio/Technology,2007, 6 (4) : 285-313.
DOI: 10.1007/s11157-006-9116-x ( 0) 0)
|
| [10] |
ZENG W, WANG X, LI B, et al. Nitritation and denitrifying phosphorus removal via nitrite pathway from domestic wastewater in a continuous MUCT process[J].
Bioresource Technology,2013, 143 : 187-195.
DOI: 10.1016/j.biortech.2013.06.002 ( 0) 0)
|
| [11] |
KORNAROS M, MARAZIOTI C, LYBERATOS G. A pilot scale study of a sequencing batch reactor treating municipal wastewater operated via the UP-PND process[J].
Water Science and Technology,2008, 58 (2) : 435-438.
DOI: 10.2166/wst.2008.366 ( 0) 0)
|
| [12] |
孙艳, 张逢, 胡洪营, 等. 北京市污水处理厂进水水质特征的统计学分析[J].
给水排水,2014, 1 : 177-181.
SUN Yan, ZHANG Feng, HU Hongying, et al. Statistical analysis of influent quality characteristics of municipal wastewater treatment plants in Beijing, China[J]. Water & Wastewater Engineering,2014, 1 : 177-181. (  0) 0)
|
| [13] |
张肖静, 李冬, 梁瑜海, 等. MBR-SNAD工艺处理生活污水效能及微生物特征[J].
哈尔滨工业大学学报,2015, 47 (8) : 87-91.
ZHANG Xiaojing, LI Dong, LIANG Yuhai. Performance and microbial characteristic of SNAD process for treating domestic sewage in a membrane bioreactor[J]. Journal of Harbin Institute of Technology,2015, 47 (8) : 87-91. (  0) 0)
|
| [14] |
郭海娟, 马放, 沈耀良. DO和pH值在短程硝化中的作用[J].
环境污染治理技术与设备,2006, 7 (1) : 37-40.
GUO Haijuan, MA Fang, SHEN Yaoliang. Effects of DO and pH on nitrosofication[J]. Techniques and Equipment for Environmental Pollution Control,2006, 7 (1) : 37-40. (  0) 0)
|
| [15] |
张昭, 李冬, 邱文新, 等. 城市污水部分亚硝化的实现与稳定运行[J].
中南大学学报(自然科学版),2013, 44 (7) : 3066-3071.
ZHANG Zhao, LI Dong, QIU Wenxin, et al. Achievement and stable operation of partial nitritation for municipal wastewater[J]. Journal of Central South University(Science and Technology),2013, 44 (7) : 3066-3071. (  0) 0)
|
| [16] |
KORNAROS M, DOKIANAKIS S N, LYBERATOS G. Partial nitrification/denitrification can be attributed to the response of nitrite oxidizing bacteria to periodic anoxic disturbances[J].
Environmental Science & Technology,2010, 44 (19) : 7245-7253.
( 0) 0)
|
| [17] |
GUO J H, PENG Y Z, PENG C Y, et al. Energy saving achieved by limited filamentous bulking sludge under low dissolved oxygen[J].
Bioresource Technology,2010, 101 (4) : 1120-1126.
DOI: 10.1016/j.biortech.2009.09.051 ( 0) 0)
|
| [18] |
YU R, CHANDRAN K. Strategies of Nitrosomonas europaea 19718 to counter low dissolved oxygen and high nitrite concentrations[J].
BMC Microbiology,2010, 10 (5) : 1-11.
( 0) 0)
|
| [19] |
BOURNAZOU M N C, HOOSHIAR K, ARELLANO-GARCIA H, et al. Model based optimization of the intermittent aeration profile for SBRs under partial nitrification[J].
Water Research,2013, 47 (10) : 3399-3410.
DOI: 10.1016/j.watres.2013.03.044 ( 0) 0)
|
| [20] |
郝晓地, 朱景义, 曹秀芹. 污泥膨胀形成机理及控制措施研究现状和进展[J].
环境污染治理技术与设备,2006, 7 (5) : 1-9.
HAO Xiaodi, ZHU Jingyi, CAO Xiuqin. Situation and development of bulking sludge study:general theories and control measures[J]. Techniques and Equipment for Environmental Pollution Control,2006, 7 (5) : 1-9. (  0) 0)
|
| [21] |
MUSVOTO E V, LAKAY M T, CASEY T G, et al. Filamentous organism bulking in nutrient removal activated sludge systems[J].
Water Sa,1999, 25 : 397-407.
( 0) 0)
|
| [22] |
MA Y, PENG Y, WANG S, et al. Achieving nitrogen removal via nitrite in a pilot-scale continuous pre-denitrification plant[J].
Water Research,2009, 43 (3) : 563-572.
DOI: 10.1016/j.watres.2008.08.025 ( 0) 0)
|
 2016, Vol. 48
2016, Vol. 48


