随着工业化程度的提高以及人类社会的不断进步,寻求一种新的能源材料,是21世纪以来人类急需解决的重大发展问题之一[1].为解决这一问题,各国研究者们都在努力地寻找和开发具有环保、高能的新能源[2].在对新型能源的探索和研究过程中,化学能源逐渐成为人们关注的焦点.锂离子电池较传统的电池有明显的优势,目前已被广泛应用于手机、笔记本等小型移动设备中[3-5].探索并开发出能够满足多方面功能需求的锂离子电池,已经成为全球各个国家研究发展的重心[6-10].据粗略估计[11],在假定材料物理参数固定的情况下,锂离子电池的正极材料容量每提高一倍,电池体系的能量密度可以提高大约57%.因此,要想在锂离子电池方面有新的突破,就必须开发包括新一代正极材料体系在内的新型电极材料体系.三元正极材料LiNixCoyA11-x-yO2相较于LiCoO2,减少了对Co的使用,降低了成本,实际放电比容量更高,被认为是能够替代LiCoO2的第二代绿色锂离子电池正极材料.
在电池的充电末期,层状镍系正极材料中的Ni处于高氧化价态,具有很强的氧化性,会与电解液发生副反应,产生气体和放出热量,破坏电解液的功能,从而导致电池失效.为了改善层状镍系正极材料存在的这种问题,采用表面包覆技术,对层状镍系正极材料进行适当的改性处理.表面包覆技术是一种有效提高电池材料性能的手段,具有以下作用[12-15]:1) 可以改善材料的界面效应,降低电池的阻抗;2) 可以有效地提高材料的热稳定性和改善材料的大电流充放电性能;3) 在充电截止电位较高时,可以明显改善材料的循环稳定性.因此,壳结构复合技术作为一种全新的包覆技术,在锂离子电池正极材料的发展上具有突破性意义.
LiNixCoyA11-x-yO2的研究对于开拓锂离子电池正极材料市场、改善生态环境具有重要意义.因此,研究和发展具有应用前景的富镍系锂离子电池正极材料具有重要的现实意义和应用价值.
1 实验 1.1 实验材料制备镍钴铝氢氧化物前驱体的制备:以NiSO4·6H2O、CoSO4·7H2O和A12(SO4) 3·18H2O为原料,按照摩尔比Ni:Co:A1=0.8:0.15:0.05的比例,用蒸馏水配制成金属离子总浓度一定的硫酸盐溶液,以一定浓度的NaOH溶液为沉淀剂,浓氨水为络合缓冲剂,氢氧化钠和氨水按照氨碱比为1:2混合配制成溶液,将两种溶液分别通过蠕流泵并流加入反应釜中.控制体系温度为55 ℃,搅拌强度为600 r/min,pH值为11.0.待反应结束后,将生成物取出,静置、洗涤、抽滤、干燥,得到所需的镍钴铝氢氧化物前躯体.
正极材料的制备:以Ni0.8Co0.15Al0.05(OH)2为核,在其表面包覆一层Ni1/3Co1/3Mn1/3(OH)2壳,按7:3的配比合成实验.实验以购买的金天公司生产的Ni0.8Co0.15Al0.05(OH)2前驱体为原料,配置Ni1/3Co1/3Mn1/3(OH)2前驱体溶液,按1:1:1的摩尔比配制硫酸镍、硫酸锰和硫酸钴的的混合硫酸盐溶液,以NaOH为沉淀剂,氨水为络合剂,按照氨碱比为1:2的比例配制NaOH和氨水的混合溶液.将Ni0.8Co0.15Al0.05(OH)2前驱体溶液倒入反应釜中,以700 r/min的转速运行,待反应釜中温度升至55 ℃,调整溶液pH值为11.1,开始滴加混合硫酸盐溶液和NaOH与氨水的混合溶液,控制pH值为11.1.待实验结束后,将反应产物静置、抽滤、干燥.将包覆Ni1/3Co1/3Mn1/3(OH)2外壳的Ni0.8Co0.15Al0.05(OH)2前驱体,充分干燥研磨后,与碳酸锂按摩尔比混合,在行星球磨机中以180 r/min的转速,充分球磨混料15 h,将其取出干燥、研磨,在气氛炉中750 ℃焙烧15 h,得到正极材料.
1.2 材料的表征实验采用德国布鲁克公司生产的Bruker D8 X-射线粉末衍射仪分析材料晶体结构,测试条件为:Cu靶Kα射线,λ=1.5406×10-10 m,石墨单色器,工作电压为40 kV,工作电流为300 mA,步长0.01°,扫描角度的范围为10°≤2θ≤90°;采用Philips XL-30E型场致发射扫描电子显微镜对材料表面形貌进行表征.
1.3 电化学性能测试按照质量百分比为80%:10%:10%,称取正极材料、乙炔黑、聚偏四氟乙烯 (PVDF),以N-甲基吡咯烷酮为溶剂,在研钵中充分混合搅拌均匀,将其均匀地涂布在铝箔上.在真空烘箱中80 ℃烘干,最后制作成电极片.扣式电池组装过程在充满氩气的手套箱中进行,保持手套箱中严格的干燥、氩气环境.以金属锂片为负极,采用Celgard 2400隔膜,电解液为LiPF6/EC+DMC,做成CR2025型扣式电池.将组装好的扣式电池静置12 h以上,进行充放电测试.实验采用的测试系统是深圳新威尔电子公司生产的BTS (5 V, 50 mA) 电池测试系统,采用恒电流放电和恒流-恒压充电测试.
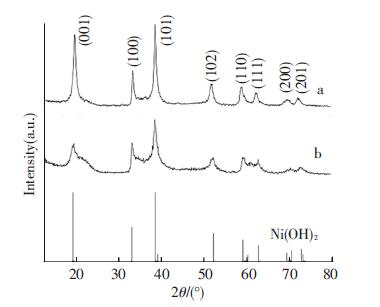
2 结果与讨论 2.1 前驱体包覆产物的表征图 1为对前驱体进行包覆前后的Ni0.8Co0.15Al0.05(OH)2前驱体与氢氧化镍标准衍射峰的XRD对比图,a曲线为包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体,b曲线为没有包覆的Ni0.8Co0.15Al0.05(OH)2前驱体.对比图 1中的曲线a、b可知,包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体的特征峰明显,峰较为尖锐,与氢氧化镍的标准衍射峰对应的很好,且无杂峰,峰的强度较大,说明结晶较好,Ni0.8Co0.15Al0.05(OH)2前驱体经包覆改性反应后,结构较为明确,通过包覆,没有改变主体相结构.
|
图 1 包覆前后的Ni0.8Co0.15Al0.05(OH)2前驱体与Ni (OH)2的XRD对比图 Figure 1 XRD patterns of coated Ni0.8Co0.15Al0.05(OH)2 precursor and Ni0.8Co0.15Al0.05(OH)2 precursor (a—coated Ni0.8Co0.15Al0.05(OH)2 precursor; b—Ni0.8Co0.15Al0.05(OH)2 precursor |
图 2为Ni0.8Co0.15Al0.05(OH)2前驱体包覆前与表面包覆Ni1/3Co1/3Mn1/3(OH)2前驱体后的扫描电镜图,图 2(a)、(b)分别为Ni0.8Co0.15Al0.05(OH)2前驱体包覆前的扫描电镜图,可以看到,Ni0.8Co0.15Al0.05(OH)2前驱体主要呈球形或接近于球形,球形度较好,前驱体表面较光滑,大小均匀.

|
图 2 Ni0.8Co0.15Al0.05(OH)2前驱体表面包覆前后的SEM图 Figure 2 SEM of coated Ni0.8Co0.15Al0.05(OH)2:(a, b) Ni0.8Co0.15Al0.05(OH)2 precursor; (c, d) coated Ni0.8Co0.15Al0.05(OH)2 precursor |
图 2(c)、(d)分别为Ni0.8Co0.15Al0.05(OH)2前驱体表面包覆Ni1/3Co1/3Mn1/3(OH)2后的扫描电镜图片,由图 2(c)可以看到,有部分小颗粒生成,可能是包覆反应搅拌过程中,新生成的Ni1/3Co1/3Mn1/3(OH)2前驱体,也可能是Ni0.8Co0.15Al0.05(OH)2前驱体的小碎颗粒.包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体表面较粗糙,出现了覆盖物,表面发生了明显的颗粒变化.因此, 对比可得,Ni0.8Co0.15Al0.05(OH)2前驱体的表面发生了明显变化,说明包覆物质已经形成.
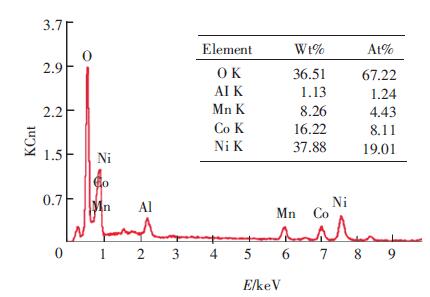
Ni0.8Co0.15Al0.05(OH)2前驱体表面用Ni1/3Co1/3Mn1/3(OH)2包覆后,取其微小区域进行EDX能谱检测.图 3能谱图显示,Ni0.8Co0.15Al0.05(OH)2前驱体进行表面包覆后,合成的物质元素比,既不符合Ni0.8Co0.15Al0.05(OH)2前驱体的元素比,也不与Ni1/3Co1/3Mn1/3(OH)2中三者的元素比相匹配,而是处于两者之外的其他元素比,说明所取的物质是二者的混合体,初步肯定了包覆的存在.
|
图 3 包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体样品表面的EDX谱图 Figure 3 EDX of coated Ni0.8Co0.15Al0.05(OH)2 |
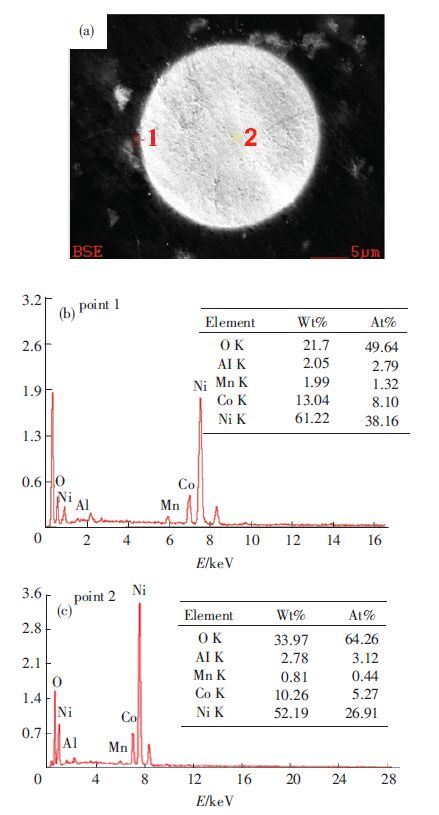
将Ni1/3Co1/3Mn1/3(OH)2包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体样品用树脂制样,将细小颗粒剖开横切面后,进行颗粒切面边缘及颗粒中心的EDX能谱分析.图 4(b)和(c)为1点和2点的能谱图.对比两点可看出,1点的锰元素含量明显高于2点,说明锰离子大量存在于颗粒外部,2点的Al元素含量高于1点,可以验证表面确实Ni1/3Co1/3Mn1/3(OH)2的包覆层形成.
|
图 4 包覆后的前驱体切面边缘及中心的EDX能谱图 Figure 4 EDX of Margin and center of coated Ni0.8Co0.15Al0.05(OH)2 |
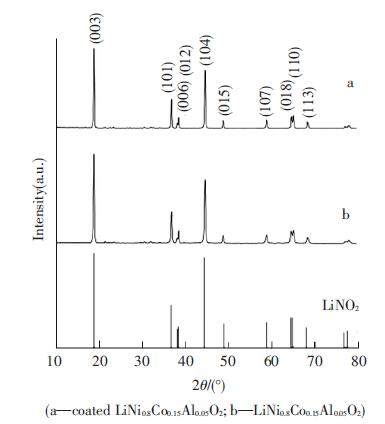
图 5为在750 ℃条件保温15 h,烧结得到的正极材料的XRD谱图,a曲线为包覆后的正极材料,b曲线为未包覆的正极材料.两种材料的XRD衍射峰与LiNO2标准衍射峰对比,可知两种材料的特征峰明显,且峰较为尖锐,对应准确,无杂峰,说明烧结后正极材料结晶度较好,结构未发生变化,为典型的a-NaFeO2层状结构.峰 (003) 和峰 (104),是强度较高的两个峰,且I003和I104的对比,用来判定材料的混排程度,图 5显示,峰强对比明显,表明材料混排较少,为良好的电化学性能提供了必要的条件.
|
图 5 750 ℃烧结的正极材料的XRD谱图 Figure 5 XRD patterns of LiNi0.8Co0.15Al0.05O2 and coated LiNi0.8Co0.15Al0.05 O2 at 750 ℃ (a—coated LiNi0.8Co0.15Al0.05O2; b—LiNi0.8Co0.15Al0.05O2) |
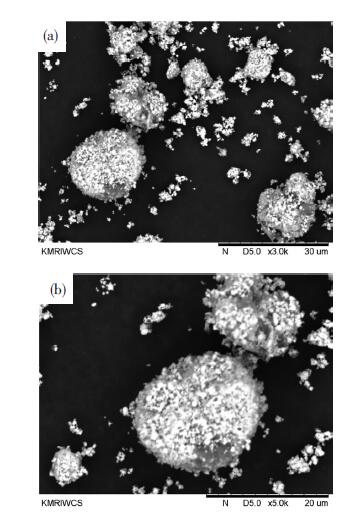
包覆后的正极材料烧结后,通过扫描电镜观察其形貌,结果如图 6所示.
|
图 6 包覆改性的正极材料烧结后的SEM图 Figure 6 SEM of coated LiNi0.8Co0.15Al0.05O2 |
由图 6可知,正极材料大部分仍然保持球形结构,颗粒表面粗糙,大颗粒周围有一些零散、较小的碎片,分析可能是由于球磨时间过长的缘故.
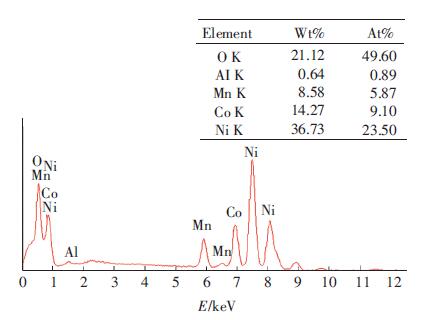
包覆后的正极材料烧结后,取其微小区域,进行EDX能谱检测.图 7能谱图显示,包覆后的正极材料烧结后,合成的物质元素比,既不符合LiNi0.8Co0.15 Al0.05O2的元素比,也不与LiNi1/3Co1/3Mn1/3O2中三者的元素比相匹配,而是处于两者之外的其他元素比,说明所取的物质是二者的混合体.由Ni1/3Co1/3Mn1/3(OH)2包覆后的Ni0.8Co0.15Al0.05(OH)2前驱体的EDX图可知, 确实形成了包覆层,而包覆后的正极材料烧结后的EDX图也显示物质元素比处于两者之外的其他元素比,由此肯定了烧结后包覆依然存在.
|
图 7 包覆改性的正极材料烧结后的EDX图 Figure 7 EDX of coated LiNi0.8Co0.15Al0.05O2 |
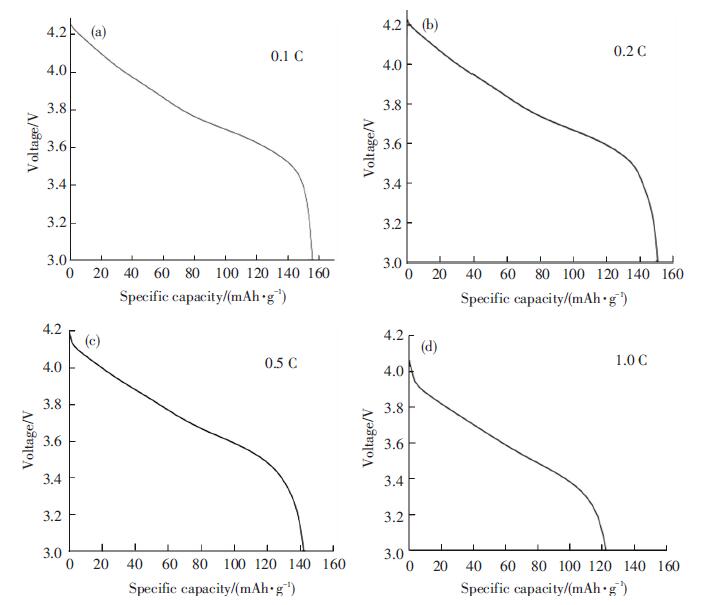
图 8是未包覆改性的LiNi0.8Co0.15Al0.05O2正极材料在0.1、0.2、0.5、1 C倍率下的首次放电曲线,电压范围为2.75~4.3 V.由图 8可知,在0.1、0.2、0.5、1 C倍率下,材料的首次放电比容量分别为157、150.6、141.8、122.3 mAh·g-1.由0.1到1 C,放电比容量降低了34.7 mAh·g-1,衰减了22.1%,衰减较为明显.
|
图 8 LiNi0.8Co0.15Al0.05O2材料在不同倍率下首次循环的放电比容量图 Figure 8 Discharge curves of LiNi0.8Co0.15Al0.05O2 tested after 1 cycle at different rate |
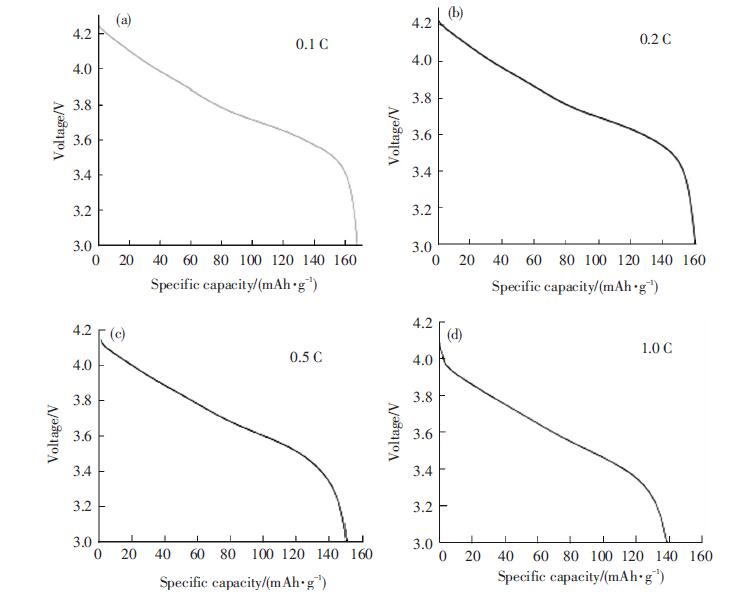
图 9是包覆改性后的正极材料在0.1,0.2,0.5,1 C倍率下的首次放电曲线,电压范围为2.75~4.3 V.由图 9可知,在0.1 C倍率下,材料的首次放电曲线较平滑,放电比容量可达167.6 mAh·g-1,在0.2、0.5、1 C倍率下,材料的首次放电比容量分别为160.1、150.4、138.5 mAh·g-1.由0.1到1 C,放电比容量降低了29.1 mAh·g-1,衰减了17.4%.
|
图 9 包覆改性后的LiNi0.8Co0.15Al0.05O2材料在不同倍率下首次循环的放电比容量图 Figure 9 Discharge curves of coated LiNi0.8Co0.15Al0.05O2 tested after 1 cycle at different rate |
图 10为包覆改性前后的正极材料在不同倍率下的倍率性能和循环性能的比较图以及包覆改性后的正极材料在0.5 C倍率下的充放电曲线.由图 10(a)可知,包覆改性后的正极材料总放电比容量得到了提高,这说明包覆改性后的正极材料改善了未包覆LiNi0.8Co 0.15 A10.05O2正极材料的循环稳定性,提高了高倍率下的放电比容量.由图 10(b)可得,材料的首次放电比容量为150.4 mAh·g-1,经过20次循环后放电比容量为140.4 mAh·g-1,循环稳定性好.这是因为通过表面包覆改性,合成核壳结构的正极材料,材料的稳定性得到提高,同时,在高温作用下,包覆在正极材料表面的元素,在正极材料上发生了高温扩散和化学反应,起到掺杂改性的作用.

|
图 10 不同倍率下包覆改性前后的正极材料倍率性能和循环性能的比较图 (a),以及包覆改性后的正极材料在0.5C倍率下的充放电曲线 (b) Figure 10 Rate capability and cyclic performances of the bare and coated LiNi0.8Co0.15Al0.05O2 electrodes at 0.1 C, 0.2 C, 0.3 C, 0.5 C and 1 C rates (a), and discharge-charge curves of coated LiNi0.8Co0.15Al0.05O2 tested at 0.5 C (b) |
本文以LiNi0.8Co0.15Al0.05O2正极材料为研究对象,采用共沉淀法合成氢氧化物前驱体,并对LiNi0.8Co0.15Al0.05O2正极材料进行包覆改性,在前驱体的基础上进行包覆,制备合成具有核壳结构的正极材料.电化学结果表明:
1) 未包覆改性的LiNi 0.8Co0.15Al0.05O2正极材料在0.1、0.2、0.5、1 C倍率下的首次充放电比容量分别为157,150.6,141.8,122.3 mAh·g-1.包覆改性后正极材料在相同倍率下,材料的首次放电比容量分别为167.6,160.1,150.4,138.5 mAh·g-1.
2) 由0.1到1 C,包覆改性前后的正极材料的放电比容量衰减量由34.7 mAh·g-1降为29.1 mAh·g-1,容量衰减百分比由22.1%降低到17.4%.
经包覆改性后的正极材料,在放电比容量和容量衰减率方面均有改善.
| [1] | 雷永泉, 万群, 石永康. 新能源材料[M]. 天津: 天津大学出版社, 2000: 1-143. LEI Yongquan, WAN Qun, SHI Yongkang. New energy materials[M]. Tianjin: Tianjin University Press, 2000 : 1-143. |
| [2] | XU Bo, QIAN Danna, WANG Ziying, et al. Recent progress in cathode materials research for advanced lithium ion batteries[J]. Materials Science and Engineering R, 2012, 73: 51–65. DOI: 10.1016/j.mser.2012.05.003 |
| [3] | 雷永泉, 万春荣, 姜长印. 锂离子二次电池[M]. 北京: 化学工业出版社, 2002: 2-5. LEI Yongquan, WAN Chunrong, JIANG Changyin. Li-ion secondary battery[M]. Beijing: Chemical Industry Press, 2002 : 2-5. |
| [4] | ETACHERI V, MAROM R, ELAZZRI R. Challenges in the development of advanced Li-ionbatteries:a review[J]. Energy & Environmental Science, 2011, 4(9): 3243–3262. |
| [5] | 郭炳现, 徐徽, 王先友. 锂离子电池[M]. 长沙: 中南大学出版社, 2002: 36-55. GUO Bingxian, XU Hui, WANG Xianyou. Li-ion battery[M]. Changsha: Central South University Press, 2002 : 36-55. |
| [6] | THACKERAY M. Structural considerations of layered and spinellithiated oxides for lithium ion baaery[J]. J Electrochem Soc, 1995, 142(8): 2558–2563. DOI: 10.1149/1.2050053 |
| [7] | RITCHIE A G. Recent developments and likely advances in lithium rechargeable batteries[J]. J Power Sources, 2004, 136(2): 285–289. DOI: 10.1016/j.jpowsour.2004.03.013 |
| [8] | 吴川, 吴锋, 陈实. 锂离子电池正极材料研究进展[J]. 电池, 2000, 30(1): 36–39. WU Chuan, WU Feng, CHEN Shi. Cathode materials research for Li-ion battery[J]. Battery, 2000, 30(1): 36–39. |
| [9] | 屈平, 方芳. 锂离子电池的技术与市场[J]. 国际电源商情, 2004, 9: 32–35. QU Ping, FANG Fang. Technology and market for Li-ion battery[J]. International Power Business, 2004, 9: 32–35. |
| [10] | 万传云. 锂离子电池正负极材料市场发展趋势[J]. 电池工业, 2005, 10(6): 369–371. WAN Chuanyun. Market development trends of the anode and cathode materials for Li-ion batteries[J]. Chinese Battery Industry, 2005, 10(6): 369–371. |
| [11] | TARASCON J M. Key challenges in future Li-battery research[J]. PhilosophicalTransanctions of the Royal.Socioty A, 2010, 368: 3227–3241. |
| [12] | 陈宏浩. 锂离子电池正极材料层状锂镍钻氧化物掺杂研究: [D]. 武汉: 武汉大学, 2005 CHEN Honghao. Layered lithium-nickel-cobalt oxide doping of the cathode materials for Li-ion batteries[D]. Wuhan: Wuhan University, 2005. |
| [13] | KANNAN A M, RABENBERG L, MANTHIRAM A. High capacity surface-modified LiCoO2cathodes for lithium-ion batteries[J]. Electrochemical and Solid StateLett, 2003, 6(1): A16–A18. DOI: 10.1149/1.1526782 |
| [14] | CHEN Zhaohui, DAHN J R. Methods to obtain excellent capacity retention in LiCoO2cycled to 4.5V[J]. Electrochem Acta, 2004, 49(7): 1079–1090. DOI: 10.1016/j.electacta.2003.10.019 |
| [15] | KWEON H J, PARK D G. Surface modification of LiSr0.002Ni0.9Co0.1O2by overcoating with a magnesuim oxide[J]. Electrochemical and Solid-State Letters, 2000, 3(3): 128–130. |
 2017, Vol. 25
2017, Vol. 25


