目前广泛应用于导电浆料中的导电填料可分为银基、钯-银、金基、铂基、铜基、镍基及其它金属填料,导电填料的导电性和抗氧化性直接影响着导电浆料性能的优劣[1].与其他导电填料相比,铜作为贱金属代表,其价格低廉,且导电性仅次于银,而且铜不会发生电子迁移现象,因此,铜基浆料是银基浆料最理想的替代材料[2-3].
但微米级片状铜粉具有很大的比表面积,表面能大且表面活性高,因此,在空气中易被氧化,生成铜的氧化物[4-5],且导电浆料在烧结过程中,会加速铜粉的氧化.将表面被氧化的铜粉做为导电填料可能会出现许多问题,小则引起电子浆料电阻率急速升高,出现断路现象,影响使用,大则出现局部电阻太大,产生大量热量,引起事故.
近年来各国研究人员在铜粉表面抗氧化性研究取得了许多重要进展,主要包括金属包覆法(如银包铜粉)、非金属包覆法(主要包括缓蚀剂法、偶联剂法、磷化处理法等方法)以及其他抗氧化法[6-8].
金属包覆法是指在铜粉表面完整地包覆一层性能稳定、导电性好的其他金属层,防止铜粉与空气直接接触,以提高铜粉抗氧化性和导电性.吴懿平[9]等采用三次镀银法,在一次镀银后利用稀硫酸除去铜粉表面的铜氨络合物,然后利用重复镀银的方法来解决镀层不均匀问题.通过反复进行银包覆工艺虽然实现了铜粉银包覆,但该方法操作复杂、成本高,很难被实际应用.此外,一些研究人员也试图通过给超细铜粉表面包覆Ni、Sn等金属的方法,以提高铜的抗氧化性和导电性[10-11],虽然取得了一定的研究成果,但与表面包覆Ag相比导电性较差.
非金属包覆法是相对于金属包覆法而言,主要分为无机物包覆和有机物包覆两类.文献[12-13]研究发现,采用直接添加硅烷偶联剂法,制备得到的铜电子浆料具有良好的抗氧化性和导电性,分析原因主要是由于铜粉和偶联剂的相互作用需要一段时间,在铜粉与偶联剂尚未完全作用前将铜电子浆料印刷在陶瓷基片上,随着偶联剂与铜粉的进一步作用,会在铜粉表面形成保护膜,将铜颗粒与空气隔绝开,从而保证了铜粉不被氧化,而且还不影响铜粉的导电性.由于偶联剂在一定温度下性能稳定,可以有效隔绝铜粉与氧气,提高铜导电浆料的抗氧化性[14],但对烧结后的导电铜膜进行导电性测试,发现与其他几种抗氧化方法相比导电性较差.
其他抗氧化法如罗艳[15]等将铜粉在甲醇-油酸混合溶液中进行油酸预包覆,然后以正硅酸乙酯原料,在Ar气保护下采用溶胶-凝胶法对油酸预包覆的铜粉进行SiO2-A1(其主要成分为SiO2,相当于利用硅酸溶胶进行二次包覆)系薄膜的二次包覆.研究结果表明:铜粉具有良好的导电性和抗氧化能力.李利君[16]等人利用正硅酸乙酯在碱性条件下水解制备得到硅酸溶胶,在氮气保护用溶胶-凝胶法对铝颜料进行包覆,以此方法提高铝颜料的耐碱性和抗氧化性.利用硅酸溶胶对粉体材料进行溶胶-凝胶包覆可以提高材料抗氧化性能,其弊端在于硅酸溶胶不易包覆在粉体材料表面,容易出现包覆不全的现象.
目前国内采用溶胶-凝胶法对粉体材料进行包覆的,大多数采用的是硅酸溶胶或者二氧化钛溶胶,除上述研究外,夏志伟[17]、闫军[18]等人,他们都是利用钛酸丁酯水解制备二氧化钛溶胶对材料进行溶胶-凝胶包覆.近年来,在国外应用溶胶-凝胶法制备涂层的研究非常活跃,Supplit R[19]利用正硅酸乙酯和乙烯基三乙氧基硅烷的水解制备得到硅酸溶胶对铝颜料进行溶胶-凝胶包覆以提高其抗腐蚀性和抗氧化性.Juha等[20]则利用SiO2-ZrO2溶胶对铜金属包覆以提高其表面耐腐蚀性.总的来说,国内的溶胶主要集中在单一的硅酸溶胶,国外则是二氧化硅与其他氧化物的复合溶胶.
针对铜粉高温环境下易氧化问题,本文采用正硅酸乙酯和硼酸三丁酯的双水解来制备硼酸和硅酸的复合溶胶,它不仅纯度高,而且均匀度高,其均匀程度可达分子或原子水平[21-22],这样不但可以充分的包覆在铜粉表面,同时它还具有较低的介电性能,与金、银和铜的匹配性好.通过硼硅酸凝胶薄膜包覆铜粉来防止铜粉氧化,获得了较为满意的效果.这种溶胶制备方法及硼硅酸凝胶包覆法对铜粉的抗氧化研究在文献中还未见报道.
将凝胶包覆到经过表面酸洗的铜粉上,获得实验所需的铜粉.将包覆后的铜粉制成浆料并印刷到陶瓷基板上,600 ℃烧结后获得铜导电膜层,通过四探针测试仪测量膜层的烧结后的电阻,并换算成其相对电导率.在SEM下观察凝胶包覆后铜粉的表面形貌.将满足实验导电率要求的铜粉经过700 ℃高温烧结,并利用XRD考查其氧化情况.利用示差扫描量热仪研究实验制备的铜粉在高温情下的热失重及氧化情况.
1 试验 1.1 试剂与分析仪器采用分析纯的稀盐酸、无水乙醇、正硅酸乙酯、硼酸三丁酯、吗啉和铜粉为实验原料,所需实验仪器为自蔓延燃烧合成反应釜、四探针测试仪、电子天平、X射线衍射仪(XRD)、扫描电子显微镜(SEM)、热重分析仪(TGA).
1.2 铜粉表面的清洗铜粉颗粒表面的氧化物主要是CuO和Cu2O,本文采用无机酸洗的方法去除铜粉表面氧化物,具体反应方程为
| $ \begin{array}{l} 2{\rm{HCl}}\left( {稀} \right) + {\rm{CuO }} = {\rm{CuC}}{{\rm{l}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}},\\ 2{\rm{HCl}}\left( {稀} \right) + {\rm{C}}{{\rm{u}}_{\rm{2}}}{\rm{O}} = {\rm{Cu + CuC}}{{\rm{l}}_{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}} \end{array} $ |
通过观察发现,当铜粉表面呈现鲜红色时,说明铜粉表面的氧化物已经被完全除去.如果此时的铜粉裸露在空气中,极易被氧化,为了避免铜粉被再次被氧化,当铜粉表面的氧化物被去除后,快速用蒸馏水冲洗铜粉冲洗数次,待到没有明显刺鼻气味后再用无水乙醇进行包覆,然后将铜粉放在真空环境下进行干燥,干燥温度为100 ℃,时间为2 h.
1.3 SiO2-B2O3溶胶的制备按照一定量的比例称取正硅酸乙酯和无水乙醇,并将其混合均匀后加入到滴定管中,称为A溶液.与此同时,按照设计的比例称量一定量的去离子水和稀盐酸,称为B溶液,打开磁力搅拌器使B溶液混合均匀并加热.当温度稳定在50 ℃时,打开滴定管阀门,让A液均匀的加入B液中,水解反应正式开始,反应时间为20~30 min.
观察水解物状态,当水解到一定程度时,用吗啉试剂进行检测,观察其形成凝胶的时间.取4.5 mL水解液置于10 mL带刻度的试管,加入0.5 mL吗啉,震摇试管,同时开始计时,待完全胶凝时停止计时.当正硅酸乙酯胶凝时间为250~280 s时,说明正硅酸乙酯水解程度达到60%左右,此即为实验所需正硅酸乙酯水解液.将准备好的一定量的硼酸三丁酯溶液加入正硅酸乙酯水解液中进行水解,通过磁力搅拌器使正硅酸乙酯溶液和硼酸三丁酯混合均匀,并均匀加热.重复前面的方法,用吗啉试剂再次检测其水解程度,当烧杯中的溶液变为一种无色透明胶状液体时,说明硼酸三丁酯与正硅酸乙酯的混合液水解度达到80%以上,此即为实验所需的SiO2-B2O3溶胶,且制备出来的溶胶性能稳定、无沉淀.
正硅酸乙酯的水解缩合反应过程如下.
第1步:水解反应
| $ {\rm{Si(O}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{{\rm{)}}_{\rm{4}}}{\rm{ + 4}}{{\rm{H}}_{\rm{2}}}{\rm{O}} = {\rm{Si}}{\left( {{\rm{OH}}} \right)_{\rm{4}}}{\rm{ + 4}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{OH}}. $ |
第2步:缩聚反应
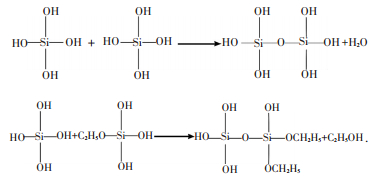
|
第3步:聚合反应
| $ n\left( {—{\rm{Si}}—{\rm{O}}—{\rm{Si}}—} \right) \to {\left( {—{\rm{Si}}—{\rm{O}}—{\rm{Si}}—} \right)_n}. $ |
正硅酸乙酯的水解总反应式可表示为
| $ {\rm{Si(O}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{)4 + 2}}{{\rm{H}}_{\rm{2}}}{\rm{O}} = {\rm{Si}}{{\rm{O}}_{\rm{2}}}{\rm{ + 4}}{{\rm{C}}_{\rm{2}}}{{\rm{H}}_{\rm{5}}}{\rm{O}}{{\rm{H}}^{\left[ {23 - 24} \right]}} $ |
硼酸三丁酯的水解缩合反应过程如下.
第1步:水解反应
| $ {\rm{B(O}}{{\rm{C}}_{\rm{4}}}{{\rm{H}}_{\rm{9}}}{\rm{) + 3}}{{\rm{H}}_{\rm{2}}}{\rm{O = B}}{\left( {{\rm{OH}}} \right)_{\rm{3}}}{\rm{ + 3}}{{\rm{C}}_{\rm{4}}}{{\rm{H}}_{\rm{9}}}{\rm{OH}}. $ |
第2步:缩聚反应
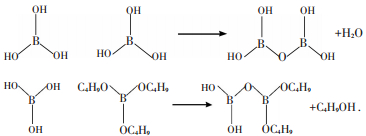
|
第3步:聚合反应
| $ n\left( {—{\rm{B}}—{\rm{O}}—{\rm{B}}—} \right) \to {\left( {—{\rm{B}}—{\rm{O}}—{\rm{B}}—} \right)_n}. $ |
硼酸三丁酯的水解总反应式为
| $ {\rm{2B(O}}{{\rm{C}}_{\rm{4}}}{{\rm{H}}_{\rm{9}}}{\rm{)3 + 3}}{{\rm{H}}_{\rm{2}}}{\rm{O = }}{{\rm{B}}_{\rm{2}}}{{\rm{O}}_{\rm{3}}}{\rm{ + 6}}{{\rm{C}}_{\rm{4}}}{{\rm{H}}_{\rm{9}}}{\rm{OH}}{\rm{.}} $ |
在对铜粉进行溶胶包覆前,取适量甲醛于烧杯中,将经过盐酸酸洗过的铜粉倒入甲醛中浸泡约15 min.
采用甲醛对铜粉进行预处理,主要作用有两点:一是去除在实验过程中铜粉表面可能产生的氧化物;二是作为湿润剂使硼硅酸凝胶能均匀的包覆在铜粉表面[25].待铜粉被充分湿润后,按照硼硅酸凝胶与铜粉的质量比为6%、8%、10%、12%、16%称取SiO2-B2O3凝胶分别加入到铜粉中.随后充分进行搅拌,保证SiO2-B2O3凝胶完全均匀的包覆在铜粉表面,再将包覆后的铜粉放置在有N2保护的反应釜中进行干燥,干燥温度为200 ℃.
2 结果及讨论 2.1 铜粉包覆率分析由表 1可知,当m(SiO2-B2O3):m(Cu)=10%时,铜导电膜层的相对电导率最高,为57%.
| 表 1 铜导电膜层的相对电导率 Table 1 Relative conductivity of copper conductive film |
当m(SiO2-B2O3):m(Cu) < 10%时,随着溶胶的质量分数的降低,铜导电膜层的相对导电率随之下降,原因是加入的凝胶过少,以至于溶胶不能完全的包覆在铜粉表面形成完整的保护膜,制成浆料并印刷到陶瓷基板上600 ℃高温烧结后,裸露出来的铜粉会与空气中的氧气反应生成CuO和Cu2O,从而影响铜粉的导电性.在此范围内加入的溶胶越少,裸露出来的铜粉就越多,高温烧结后铜粉被氧化的就越多,导电膜层的导电性也就越差.
相反,当m(SiO2-B2O3):m(Cu)>10%时,随着加入溶胶的量的增加,铜导电膜层的导电性降低,原因在于加入的凝胶过多,导致包覆在铜粉表面的溶胶层过厚,且溶胶有可能堆积在铜粉颗粒之间,制备成导电膜层后,过厚的凝胶层以及堆积在铜粉之间的凝胶,阻碍铜粉与铜粉之间形成导电网络.加入的溶胶越多,堆积在铜粉之间的凝胶就越多,铜粉之间就越难形成导电网络,因而铜导电膜层的导电性能越差.
2.2 SEM显微分析本实验分为5组.分别取按5种不同质量分数溶胶配比制得的铜粉,然后在400 ℃真空下焙烧,随后放入JMF-6700F型扫描电镜下扫描,放大倍数为10 000倍,铜粉的SEM照片见图 1.

|
图 1 铜粉的原始形貌图以及不同质量分数溶胶包覆后的铜粉的SEM照片 Figure 1 SEM photographs of the original morphology of copper powder and copper powder coated by different gel concentration: (a) original morphology of copper powder; (b) 16%; (c)12%; (d)10%; (e)8%; (f)6% |
对比图 1(b)~(d)可知,当m(SiO2-B2O3):m(Cu) > 10%时,随着加入溶胶量的增加,烘干后凝胶在铜粉表面形成的膜层越来越厚,堆积在铜粉间的凝胶也越来越多,说明此时的溶胶加入量过高.虽然凝胶含量的增多有利于将铜粉包覆的更完整、更光滑,有利于提高其抗氧化性,但过剩的凝胶会堆积在铜粉之间并使保护膜层变厚而阻碍铜粉颗粒之间的连接,这势必会影响铜粉的导电性.
同样,对比图 1(d)~(f)发现,当m(SiO2-B2O3):m(Cu) < 8%时, 铜粉表面不光滑,甚至有铜粉直接裸露出来,这说明了凝胶的添加量不足,以至于凝胶不能完全包覆在铜粉表面形成保护膜,出现包覆不全得情况,将此铜粉高温烧结后势必会有部分铜粉与氧气发生氧化反应而影响铜粉的导电性.
而当m(SiO2-B2O3):m(Cu)=8%~10%时,观察图 1(d)和(c),可见铜粉表面光滑、平整,此时铜粉表面被溶胶恰好均匀包覆而无多余凝胶堆积于铜粉之间,而且厚度薄厚适中且均匀.通过以上分析,得出结论:当m(SiO2-B2O3):m(Cu)=8%~10%之间时,符合设计要求.
2.3 X-射线衍射分析经过盐酸酸洗以及甲醛浸泡的铜粉,基本上可以完全去除铜粉表面的氧化物(CuO、Cu2O).由铜导电膜层电导率的测定以及铜粉的表面形貌可知,当m(SiO2-B2O3):m(Cu)=8%~10%时,此时溶胶包覆后的铜粉满足实验要求,因此本次实验是取m(SiO2-B2O3):m(Cu)=10%溶胶包覆后的铜粉置于干燥箱中干燥,干燥环境为自然条件,设置温度为700 ℃,干燥时间2 h,随后取出样品,采用D/max2200PC型X射线衍射仪考察其氧化情况.
任何一种结晶物质都具有特定的晶体结构.在一定波长的X-射线照射下, 每种晶体物质都有自己特有的衍射特征(衍射线的位置和强度).因此我们可以通过观察样品的XRD图来分析样品在高温烧结后的氧化情况.
由图 2可知,样品只在2θ为43.25°、50.37°、73.99°出现衍射峰,分别对应的是铜的(111)、(200)、(220) 晶面.但在2θ为36.41°、61.34°处出现的衍射峰,正好对应Cu2O的衍射峰(111)、(220) 晶面,该衍射峰极为微弱,说明只有极少量的铜粉被氧化,这表明经该方法处理后的铜粉在高温下也具有良好的抗氧化能力.

|
图 2 700 ℃烧结后的铜粉XRD谱图 Figure 2 XRDdiagrams of copper powder sintered at 700 ℃ |
同样,取m(SiO2-B2O3):m(Cu)=10%溶胶包覆后的铜粉作为样品进行热失重分析.在干燥环境下,如果样品的质量增加了,可以推断其原因是Cu与氧气反应得到了CuO和Cu2O而造成质量增加.所以,我们可以用样品在干燥条件下质量增加的趋势来判断和计量Cu被氧化的情况.
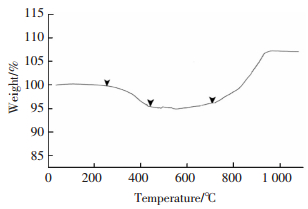
由图 3铜粉热失重曲线图可知,凝胶包覆铜粉的热失重过程可分为4个阶段:第1阶段,室温到249.17 ℃,此阶段样品几乎无变化,说明此时铜粉的氧化率基本为零:第2阶段,从249.17 ℃到417.86 ℃,这个过程中铜粉质量开始缓慢下降,分析原因为这个过程中主要是铜粉表面包覆的溶胶失去水分,以及凝胶中的部分物质挥发,但是它们的含量都是很低的,所以可以基本断定这个阶段也无铜粉被氧化;第3阶段,从417.86 ℃到716.56 ℃,曲线缓慢上升,说明此时样品的质量开始增加,但是增加的不明显,说明此时有少量的铜粉被氧化而导致的质量增加;第4阶段从716.56 ℃到832.51 ℃,曲线开始急剧上升,说明样品重量显著增加,主要原因是在该阶段温度过高,达到了凝胶的熔点,以至于包覆在铜粉表面的凝胶开始融化流动,导致大量的铜粉裸露出来而被氧化.
|
图 3 溶胶包覆后铜粉热重曲线 Figure 3 thermogravimetric curve of copper powder coated by sol |
综上分析发现,从室温到716.26 ℃,经溶胶包覆的铜粉基本无氧化,说明该铜粉在高温下具有良好的抗氧化性.
从铜粉的SEM图像分析、XRD物相分析和热重分析可知,当m(SiO2-B2O3):m(Cu)=8%~10%时,可以在铜粉表面形成均匀、完整的硼硅酸凝胶,此时铜粉在700 ℃以下无明显氧化.图 4为溶胶包覆铜粉700 ℃烧结前后的宏观图片,可以看出铜粉烧结前后表面色泽几乎无差异,都呈鲜红色,只是烧结后颜色有些许变暗,原因是有部分铜粉表面被氧化所致.这说明了硼硅酸凝胶包覆后的铜粉在高温烧结后依然具有优良的抗氧化性.

|
图 4 铜粉的宏观图 Figure 4 Macro photographs of copper powders: (a) before sintering; (b) after sintering |
1) 以正硅酸乙酯和硼酸三丁酯等为原料,制备适合于包覆铜粉的硼硅酸溶胶,且制备出来的溶胶均匀、无沉淀.
2) 在m(SiO2-B2O3):m(Cu)=8%~10%时,铜粉表面包覆的硼硅酸凝胶均匀、完整.
3) 当m(SiO2-B2O3):m(Cu)=10%时,600 ℃烧结后铜导电膜层的相对电导率为57%.
4) 在700 ℃条件下烧结后,铜粉表面仅有极少量Cu2O的生成,制备出的铜粉具有良好的抗氧化性.
5) 对制得铜粉进行热重检测,发现当m(SiO2-B2O3):m(Cu)=10%时,处理过的铜粉具有良好的抗氧化性,在温度低于700 ℃时铜粉表面只有极少量的氧化物生成,说明经凝胶包覆的铜粉在高温下具有良好的抗氧化性.
| [1] |
刘新峰, 屈银虎, 郑红梅, 等. 铜电子浆料的抗氧化研究和进展[J]. 应用化工, 2014, 43(8): 1493–1496.
LIU Xinfeng, QU Yinhu, ZHENG Hongmei, et al. Progress on oxidation resistance of copper paste[J]. Applied Chemical Industry, 2014, 43(8): 1493–1496. |
| [2] |
谭富彬, 谭浩巍. 电子元器的发展及其对电子浆料的需[J]. 贵金属, 2006, 27(1): 64–68.
TAN Fubin, TAN Haowei. Development of electronic components and its repuirements to electronic.pastes[J]. Precious Metals, 2006, 27(1): 64–68. |
| [3] | FINEH R G. Thick film materials[J]. Thin Solid Films, 1969, 3: 189–199. DOI: 10.1016/0040-6090(69)90029-7 |
| [4] | IRFAN M, KUMAR D. Recent advances in isotropic Conductive adhesives for electronics packaging applications[J]. International Journal of Adhesion and Adhesives, 2008, 28(7): 362–371. DOI: 10.1016/j.ijadhadh.2007.10.004 |
| [5] |
刘志杰, 赵斌, 张宗涛, 等. 铜超微粉末的表面改性及其抗氧化性[J]. 华东理工大学学报, 1996, 26(3): 270–275.
LIU Zhijie, ZHAO Bin, ZHANG Zongtao, et al. Study on the modification of surface property and oxidation resistance of ultramicro copperparticles[J]. Journal of East China University of Science and Technology, 1996, 26(3): 270–275. |
| [6] | SEHOEH K F. Conductive adhesives for electronics packaging[J]. IEEE Electrical Insulation Magazine, 2003, 19(2): 46–46. |
| [7] | ZHANG R W, MOON K S, LIN W, WONG CP. Preparation of highly conductive polymer nanocomposites by low temperature sintering of silver nanoparticles[J]. J Mater Chem, 2010, 20: 2018–2023. DOI: 10.1039/b921072e |
| [8] | MIZUNO M, SAKA M, AHE H. Mechanism of electrical conduction through anisotropically conductive adhesive films[J]. IEEE Transactions on Components, Packaging and Manufactring Technology Part A, 1996, 19(4): 546–553. DOI: 10.1109/95.554936 |
| [9] |
吴懿平, 吴大海, 袁忠发, 等. 镀银铜粉导电胶的研究[J]. 电子元件与材料, 2005, 24(4): 32–35.
WU Yiping, WU Dahai, YUAN Zhongfa, et al. Research of silver plating copper filled conductive adhesive[J]. Electronic Components and Materials, 2005, 24(4): 32–35. |
| [10] | SHERMAN R D, MIDDLEMAN L M, JACOBS S M. Electron transport processes in conductor-filled polymers[J]. Polymer Engineering and Science, 1983, 23(1): 36–46. DOI: 10.1002/(ISSN)1548-2634 |
| [11] | ZHAO Bin, LIU Zhijie, ZHANG Zongtao, et al. Improvement of oxidation resistance of ultrfine copper powders by phosphating treatment[J]. Journal of Solid State Chemistry, 1997, 130(1): 157–160. DOI: 10.1006/jssc.1997.7276 |
| [12] |
何益艳, 范修涛, 陆瑞卿, 等. 铜粉表面包覆硅偶联剂改性研究[J]. 腐蚀与防护, 2006, 27(2): 69–72.
HE Yiyan, FAN Xiutao, LU Ruiqing, et al. Anti-oxidation silane coupling agent enwrapped in the surface of copper powder[J]. Corrosion and Protection, 2006, 27(2): 69–72. |
| [13] |
喻冬梅, 陈明涛, 程江, 等. 碳纤维体系导电涂料的制备工艺[J]. 化工新型材料, 2007, 35(11): 65–67.
YU Dong, CHEN Mingtao, CHENG Jiang, et al. Conductive paint technology of modified carbon fibers/acrylic resin composite[J]. New Chemical Materials, 2007, 35(11): 65–67. DOI: 10.3969/j.issn.1006-3536.2007.11.024 |
| [14] |
施冬梅, 杜仕国, 田春雷, 等. 铜系电磁屏蔽涂料防氧化技术研究进展[J]. 现代涂料与涂装, 2003, 38(3): 33–34.
SHI Dongmei, DU Shiguo, TIAN Chunlei, et al. Research progress of Anti-oxidization technology of copper-based electromagnetic shielding coatings[J]. Modern Paint and Finishing, 2003, 38(3): 33–34. |
| [15] |
罗艳, 周康根, 肖妍艳, 等. 导电浆料用铜粉的表面改性及其性能[J]. 材料与冶金学报, 2006, 5(2): 119–124.
LUO yan, ZHOU Kanggen, XIAO Yanyan, et al. Surface modification and properties of copper powder for conductive paste[J]. Journal of Materials and Metallurgy, 2006, 5(2): 119–124. |
| [16] |
李利君, 皮丕辉, 文秀芳, 等. 溶胶-凝胶法制备纳米SiO包覆的铝颜料[J]. 华南理工大学学报(自然科学版), 2007, 35(11): 72–76.
LI Lijun, PI Pihui, WEN Xiufang, et al. Nano-sized SiO2-coated aluminum pigments prepared by sol-gel method[J]. Journal of South China University of Technology (Natural Science Edition), 2007, 35(11): 72–76. DOI: 10.3321/j.issn:1000-565x.2007.11.015 |
| [17] | 夏志伟. 玻璃微珠表面纳米二氧化钛薄膜包覆及其隔热性能研究[D]. 广州: 华南理工大学, 2015. XIA Zhiwei.Research on nano-TiO2 films coated hollow glass microspheres and their thermal insulation property[D]. Guangzhou:South China University of Technology, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10561-1015988103.htm |
| [18] |
闫军, 催海萍, 杜仕国, 等. 溶胶-凝胶法应用于Cu粉抗氧化工艺研究[J]. 特种制造及有色金属, 2006, 26(7): 459–462.
YAN Jun, CUI Haiping, DU Shiguo, et al. Sol-gel process for improving the oxidation-resistance of copper powder[J]. Special Casting and Nonferrous Alloys, 2006, 26(7): 459–462. |
| [19] | SUPPLIT R, SCHUBERT U. Corrosion protection of aluminum pigments by sol-gel coatings[J]. Corrosion Science, 2007, 49(8): 3325–3332. DOI: 10.1016/j.corsci.2007.03.014 |
| [20] | JUHA N, JUHA M, RITTA M, et al. Sol-gel based protective coatings for copper products[J]. Journal of Coatings Technology and Research, 2008, 5(3): 335–344. DOI: 10.1007/s11998-007-9069-1 |
| [21] | FATHI A S, VASANTHA R W A. Sol-gel coating of powders for processing electronic ceramics[J]. Journal of the American Ceramic Society, 1988, 71(11): 934–937. DOI: 10.1111/jace.1988.71.issue-11 |
| [22] | JONES R W. Fundamental principles of sol-gel technology[J]. Institute of Metals, 1990, 25(11): 1429–1434. |
| [23] |
林健. 催化剂对正硅酸乙醋水解-聚合机理的影响[J]. 无机材料学报, 1997, 12(3): 363–368.
LIN Jian. The effect of catalysts on teos hydrolysis-condensation mechanism[J]. Journal of Inorganic Materials, 1997, 12(3): 363–368. |
| [24] | 高建东. 无机富锌底漆固化剂影响因素的研究[J]. 涂料工业, 1998(3): 11-13. GAO Jiandong.Study on the hardener of inorganic zinc-primer[J].1998(3):11-13. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=tlgy803.003&dbname=CJFD&dbcode=CJFQ |
| [25] | 刘新峰. 高温烧结型铜电子浆料抗氧化性研究[D]. 西安: 西安工程大学, 2015. LIU Xinfeng.Study for anti-oxidation of copper electrical paste sintered in high temperature[D].Xi'an:Xi'an Polytechnic University, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10709-1015393997.htm |
 2017, Vol. 25
2017, Vol. 25


