2. 贵州省功能材料化学重点实验室(贵州师范大学), 贵阳 550001
2. Key Lab for Functional Materials Chemistry of Guizhou Province(Guizhou Normal University), Guiyang 550001, China
锂离子电池以其高工作电压、高比容量、循环寿命长以及对环境友好等优点而广泛应用于各种便携式电子产品中[1-3].但随着锂离子电池在电动汽车和储能领域等大型设备中的应用,对其能量密度和循环性能提出了更高的要求.负极材料是锂电池的关键材料之一,决定了电池的基本性能.目前商业化锂电池中普遍使用的负极材料是石墨,其优点是制备成本低廉,性能比较稳定,但是石墨的理论比容量仅为372 mAh/g[4],这在一定程度上限制了其在电动汽车等新领域方面的应用.因此,开发更高容量的负极材料成为目前锂离子电池研究领域的热点之一.
近年来,金属氧化物负极材料,尤其是纳米SnO2材料,因其具有较高的理论容量(782 mAh/g)和低嵌锂电势等优点,成为锂离子电池负极的最佳替代材料之一[5-7].但纳米SnO2材料仍存在许多问题有待解决,如充放电过程中体积效应、导电率差等问题[8].研究发现,通过调控纳米SnO2的合成条件,可获得具有更大比表面积的特殊纳米结构(如核-壳、多孔、花瓣状等结构)[9-13],能有效缓冲体积膨胀效应,缩短锂离子的迁移路径,从而改善电化学性能.WU等[14]合成了由超薄SnO2纳米片组成的多层花瓣状球体结构,该结构与商业的SnO2纳米颗粒比较,表现出更高的可逆容量和更好的循环性能.因此,本文以锡酸钠为原料,采用水热法,以不同表面活性剂合成3种纳米结构的SnO2负极材料,利用SEM、XRD、电化学测试仪等对材料的形貌、结构及电化学性能进行研究.
1 实验 1.1 化学试剂Na2SnO3·4H2O(分析纯),聚乙烯吡咯烷酮(PVP-K30, 优级纯),Zn(Ac)2·2H2O(分析纯),尿素(分析纯),十二烷基硫酸钠(电泳级),均来自国药集团.
1.2 材料制备将3.75 mmol聚乙烯吡咯烷酮(PVP) (尿素(urea)、十二烷基硫酸钠(SDS))分别溶解于100 mL水-乙醇(体积比1:1) 的混合溶液中,加入0.15 mmol的Zn(Ac)2和2.1 mmol Na2SnO3 ·4H2O搅拌4 h后,将混合溶液转移至反应釜中180 ℃加热24 h.待反应釜冷却至室温后,进行离心过滤,依次用去离子水与无水乙醇洗涤2~3次后在真空干燥箱中70 ℃干燥12 h获得样品.
1.3 材料表征采用日本理学公司生产的D/Max-2200型X射线粉末衍射仪对SnO2粉末进行物相分析表征,辐射源为Cu靶,扫描范围10°~80°.采用德国蔡司Supra 55型场发射扫描电子显微镜观察样品表面形貌,加速电压5 kV.采用北京中科HYA2010-C2比表面积测试仪测试SnO2材料的比表面积,测试结果见表 1.
| 表 1 使用不同表面活性剂制备的纳米SnO2材料的比表面积 Table 1 Specific surface area of nano-SnO2 obtained with different surfactants |
将所制备的纳米SnO2负极材料、导电剂乙炔黑、粘结剂聚偏氟乙烯(PVDF)按质量比70:20:10混合,以N-甲基吡咯烷酮(NMP)为分散剂,球磨混合均匀,涂布于铜集流体上,120 ℃烘干后得到负极极片.与金属锂片、聚丙烯多孔膜(Celgard 2400)、1 mol/L的LiPF6/EC(乙烯碳酸酯)+DMC(碳酸二甲酯)(1:1,by volume)电解液,在氩气气氛手套箱中装配成CR2025扣式模拟电池.使用武汉Land-CT2001A电池测试系统测试恒流充放电性能,电压范围0.01 ~3.0 V电流密度200 mA/g,测试温度30 ℃.使用武汉科思特仪器有限公司生产的型号为,CS350的电化学工作站进行循环伏安测试,电压扫描范围0.01~3.0 V,扫描速度为0.1 mV/s.
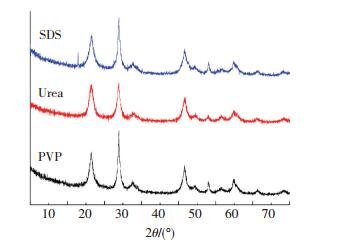
2 结果与分析 2.1 微观结构分析图 1为使用不同表面活性剂制备的纳米SnO2材料的XRD谱图,由图可知,所有样品的特征衍射峰如(110)、(101)、(200)、(211) 等峰出现位置基本一致,都很好的对应正方金红石结构的SnO2(JCPDS:41-1445),衍射峰比较尖锐并且没有观察到其它杂质峰,表明所制备的材料具有较高的纯度且结晶度良好.
|
图 1 使用不同表面活性剂制备的纳米SnO2材料的XRD谱图 Figure 1 XRD pattern of nano-SnO2 obtained with different surfactants |
图 2为无表面活性剂与不同表面活性剂修饰的SnO2材料SEM图,从图中可知,经表面活性剂修饰后,材料的晶粒形貌变化较大.无表面活性剂修饰的SnO2材料(如图 2(a)),其颗粒生长无规律,分散性较差;以尿素为表面活性剂的SnO2(如图 2(b))其晶体结构均呈球形且分散均匀,无明显的颗粒团聚现象,晶粒半径约100~200 nm.以SDS为表面活性剂制备的纳米SnO2(如图 2(c)),其晶粒结构为表面粗糙的类球形,半径约400 nm,晶粒生长不均匀,周围夹杂有少量非规整的晶粒,并且稍有团聚.以PVP为表面活性剂制备的纳米SnO2(如图 2(d)),可以看出,其形貌与前面两种截然不同,该晶粒均由几十个纳米长的纳米棒组装呈花球状结构.不同形貌的纳米SnO2材料可能是由于不同表面活性剂导致晶体生长机制不同所致.

|
图 2 无表面活性剂与不同表面活性剂修饰的SnO2材料的SEM图 Figure 2 SEM images of nano-SnO2 obtained with different surfactants: (a) no surfactant; (b) urea; (c)SDS; (d) PVP |
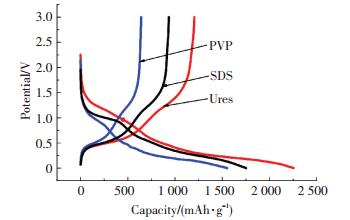
图 3为使用不同表面活性剂制备的纳米SnO2负极材料的首次充放电曲线图.从图可知,材料均在0.9 V附近出现放电平台,这主要归因于固体电解质界面(SEI)膜的形成及SnO2与Li反应生成Sn和Li2O的过程[15-16].从图还可得出尿素为表面活性剂制备的纳米SnO2材料的首次充放电比容量明显高于SDS和PVP为表面活性剂制备的纳米SnO2材料,这是由于尿素作表面活性剂制备的材料拥有更大的比表面积,从而克服了SnO2本身比表面积低、体积膨胀效应等缺陷[17],进而在一定程度上改善其电化学性能.
|
图 3 使用不同表面活性剂制备的纳米SnO2材料的首次充放电曲线 Figure 3 Charge-discharge curves of nona-SnO2 obtained with different surfactants |
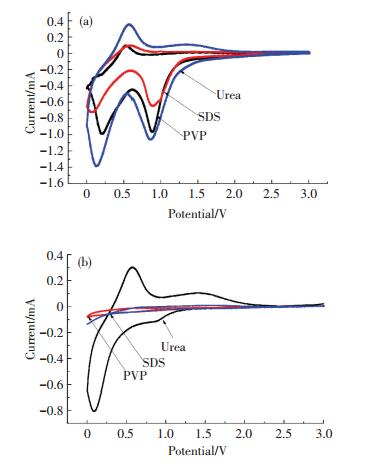
图 4为使用不同表面活性剂制备的纳米SnO2负极材料的首圈和第二圈循环伏安曲线.从图 4(a)可以看出,首圈循环伏安曲线在0.9 V附近均出现明显的还原峰,这主要对应于Sn和Li2O的生成和SEI膜的形成过程,与3种材料的首次充放电曲线得到的结果吻合.从图 4(b)观察发现,0.9 V附近的还原峰强度很弱,表明SnO2与Li反应的可逆程度很低,这正是致使材料首次不可逆容量大的原因.另一个还原峰出现在0.2 V附近,该峰对应于Li-Sn合金的形成过程.在0.5 V附近均出现氧化峰,氧化峰的出现是由于去合金化过程产生的.还从图 4(b)得出尿素为表面活性剂制备的纳米SnO2材料在0.5 V的氧化峰远大于其他两种材料.
|
图 4 使用不同表面活性剂制备的纳米SnO2材料的循环伏安曲线 Figure 4 Cycling voltammgram of nona-SnO2 obtained with different surfactants: (a) first cycle; (b) second cycle |
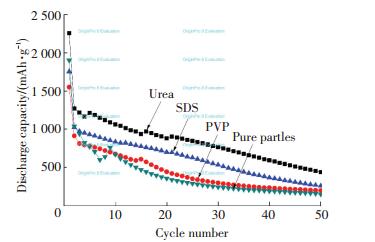
图 5分别为PVP、SDS、尿素3种表面活性剂制备的纳米SnO2负极材料在电流密度为200 mA/g,电压范围在0.01~3 V下,50次循环的放电循环曲线,其中PVP、SDS、尿素为表面活性剂制备的纳米SnO2材料的首次放电比容量分别为1 551.3、1 751.2、2 256.6 mAh/g,50次循环后分别为200.5、260.8和440.1 mAh/g,从数据可得出3种材料的容量衰减都很大.相比之下,尿素为表面活性剂制备的材料其循环稳定性较好,容量较高,这是因为尿素作表面活性剂制备的材料其形貌为表面较光滑的球体,颗粒分散性良好,尺寸大小均匀,拥有更大的比表面积和更多的活性位点,有效抑制了体积膨胀效应,有利于电子在脱嵌锂过程中的传递,进而拥有较好的电化学性能.
|
图 5 使用不同表面活性剂制备的纳米SnO2材料的放电循环性能曲线 Figure 5 Cycling performance of nona-SnO2 obtained with different surfactants |
以锡酸钠为原料,聚乙烯吡咯烷酮、尿素、十二烷基硫酸钠分别作为表面活性剂,采用水热法制备了具有纳米结构的SnO2负极材料.结果表明,以尿素为表面活性剂制备出半径在100~200 nm具有良好分散性的纳米SnO2球形颗粒.材料组装成锂离子模拟电池在0.01~3.0 V,以200 mA/g进行充放电,首次放电容量2 256.6 mAh/g,经过50次循环后,放电容量保持在440 mAh/g,表现了较好的循环性能.
| [1] | CHOI N S, CHEN Z, FREUNBERGER S A, et al. Challenges facing lithium batteries and electrical double-layer capacitors[J]. Angewandte Chemie, 2012, 51(40): 9994–10024. DOI: 10.1002/anie.201201429 |
| [2] | SIMON P, GOGOTSI Y. Materials for electrochemical capacitors[J]. Nature Materials, 2008, 7(11): 845–854. DOI: 10.1038/nmat2297 |
| [3] | REDDY M V, SUBBA RAO G V, CHOWDARI B V. Metal oxides and oxysalts as anode materials for Li ion batteries[J]. Chemical Reviews, 2013, 113(7): 5364–457. DOI: 10.1021/cr3001884 |
| [4] | LIAN P, ZHU X, LIANG S, et al. Large reversible capacity of high quality graphene sheets as an anode material for lithium-ion batteries[J]. Electrochimica Acta, 2010, 55(12): 3909–3914. DOI: 10.1016/j.electacta.2010.02.025 |
| [5] | PARK M S, KANG Y M, KIM J H, et al. Effects of low-temperature carbon encapsulation on the electrochemical performance of SnO2, nanopowders[J]. Carbon, 2008, 46(1): 35–40. DOI: 10.1016/j.carbon.2007.10.032 |
| [6] | YUAN L, WANG J, CHEW S Y, et al. Synthesis and characterization of SnO2 -polypyrrole composite for lithium-ion battery[J]. Journal of Power Sources, 2007, 174(2): 1183–1187. DOI: 10.1016/j.jpowsour.2007.06.179 |
| [7] | LI H, HUANG X, CHEN L. Anodes based on oxide materials for lithium rechargeable batteries 1[J]. Solid State Ionics, 1999, 123(1-4): 189–197. DOI: 10.1016/S0167-2738(99)00081-8 |
| [8] | XIONG W L, CHANG M L, ARCHER L A. Designed Synthesis of Coaxial SnO2 @carbon Hollow Nanospheres for Highly Reversible Lithium Storage[J]. Advanced Materials, 2009, 21(24): 2536–2539. DOI: 10.1002/adma.v21:24 |
| [9] | MENG X, ZHOU M, LI X, et al. Synthesis of SnO2, nanoflowers and electrochemical properties of Ni/SnO2, nanoflowers in supercapacitor[J]. Electrochimica Acta, 2013, 109(11): 20–26. |
| [10] | ZHANG J, JING G, XU H, et al. Reactive-template fabrication of porous SnO2 nanotubes and their remarkable gas-sensing performance[J]. Acs Applied Materials & Interfaces, 2013, 5(16): 7893–7898. |
| [11] | TALEBIAN N, JAFARINEZHAD F. Morphology-controlled synthesis of SnO2, nanostructures using hydrothermal method and their photocatalytic applications[J]. Ceramics International, 2013, 39(7): 8311–8317. DOI: 10.1016/j.ceramint.2013.03.101 |
| [12] | GAO Y, TANG Z. Design and application of inorganic nanoparticle superstructures: current status and future challenges[J]. Small, 2011, 7(15): 2133–2146. DOI: 10.1002/smll.v7.15 |
| [13] | SHI W, SONG S, ZHANG H. Hydrothermal synthetic strategies of inorganic semiconducting nanostructures[J]. Chemical Society Reviews, 2013, 42(13): 5714–5743. DOI: 10.1039/c3cs60012b |
| [14] | WU H B, CHEN J S, LOU X W, et al. Synthesis of SnO2 hierarchical structures assembled from nanosheets and their lithium storage properties[J]. Journal of Physical Chemistry C, 2011, 115(50): 24605–24610. DOI: 10.1021/jp208158m |
| [15] | BALAN L, SCHNEIDER R, GHANBAJA J, et al. Electrochemical lithiation of new graphite-nanosized tin particle materials obtained by SnCl2, reduction in organic medium[J]. Electrochimica Acta, 2006, 51(17): 3385–3390. DOI: 10.1016/j.electacta.2005.09.045 |
| [16] | ZOU L, GAN L, LV R, et al. A film of porous carbon nanofibers that contain Sn/SnOx, nanoparticles in the pores and its electrochemical performance as an anode material for lithium ion batteries[J]. Carbon, 2011, 49(1): 89–95. DOI: 10.1016/j.carbon.2010.08.046 |
| [17] |
齐涛, 张永超, 石海英, 等. TiO2包覆SnO2光阳极的制备及其对DSSC性能的影响[J]. 人工晶体学报, 2015, 44(10): 2847–2851.
QI Tao, ZHANG Yongchao, SHI Haiying, et al. Preparation of SnO2-TiO2 photoanode and its effect on the property of DSSC[J]. Journal of Synthetic Crystals, 2015, 44(10): 2847–2851. DOI: 10.3969/j.issn.1000-985X.2015.10.037 |
 2017, Vol. 25
2017, Vol. 25


