过氧化氢(H2O2)具有强氧化性,作为高效消毒灭菌剂和漂白剂,广泛应用于食品卫生、环保、纺织、化工等领域[1],但H2O2的过量残留会对人体健康及生态环境造成严重危害[2].因此,对H2O2进行准确、快速、灵敏的检测显得尤为重要.目前,测定H2O2的方法有分光光度法、化学发光法、荧光光度法、色谱法等.但这些方法存在灵敏度低、操作复杂、仪器分析方法费用较高,且难于进行现场监测等缺点,因此建立一种痕量H2O2的快速测定方法具有重要意义[3-4].电化学生物传感器具有操作简单、灵敏度高、线性范围宽、快速而稳定的响应信号等优点,受到广泛关注.在已有报道的电化学H2O2传感器中,大多要利用辣根过氧化物酶(HRP)的高效催化功能.而酶是一种具有活性的蛋白质,价格昂贵且易变性失活,对保存、检测条件要求也较苛刻,使其实际应用价值受到限制[5-6].
纳米材料由于其独特的结构和形态,表现出良好的光电活性、磁性及催化性能.近年来,利用纳米材料进行传感器研究已经引起了人们的广泛兴趣[7-8].自2007年Fe3O4纳米颗粒被报道具有类过氧化物酶活性以来,铁氧化物磁性纳米材料在电化学传感研究领域中占据非常重要的地位.然而,未经修饰的尖晶型铁磁颗粒很容易团聚,极不稳定,其应用也面临着巨大挑战[9].石墨烯是一种只有1个碳原子厚度的二维材料,当把零维的铁磁纳米颗粒负载到石墨烯上,这种杂化的纳米结构不但可以保持其原有的单一材料性能,而且会展现出更好的协同作用[10-11].同时,将具有良好生物相容性和稳定性的贵金属与上述材料形成复合材料,构成一个友好的电化学传感界面,对于H2O2的快速、简便检测具有重要意义[12].
本文采用一步原位法合成尖晶型铁磁/石墨烯纳米复合材料(Fe3O4/rGO),将该复合材料修饰到玻碳电极表面,再利用电化学沉积的方法将贵金属Pd沉积到材料表面,形成新型磁性纳米复合材料.
1 实验 1.1 仪器与试剂CHI760A型电化学工作站(上海辰华仪器有限公司);扫描电子显微镜(SEM,Hitachi,S-4800);能谱仪(EDS, Falcon, EDAX);三电极体系:玻碳电极为工作电极,铂网电极为对电极,饱和甘汞电极为参比电极.所有电化学实验都在0.1 mol/L磷酸盐缓冲溶液中进行(pH=7.4).
石墨粉、氯化铁(FeCl3·6H2O)、氯化钯(PdCl2)、过氧化氢(H2O2)购于国药集团化学试剂有限公司;D-葡萄糖(Glu)、L-抗坏血酸(AA)、多巴胺(DA)、尿酸(UA)购于Sigma-Aldrich公司.其他试剂均为分析纯,实验用水为二次蒸馏水.
1.2 Fe3O4/rGO纳米复合材料的制备首先利用改进的Hummers方法制备氧化石墨烯[13];然后将30 mg氧化石墨烯加入到置有20 mL一缩二乙二醇溶剂的反应装置中,超声1 h,使氧化石墨烯均匀分散于溶剂中;接着,向反应装置中加入120 mg FeCl3·6H2O,并在氮气保护下220 ℃加热搅拌0.5 h;最后,向混合物中迅速加入5 mL NaOH/DEG储备液,并于220 ℃下加热反应1 h,最终产物离心分离并洗涤,置于40 ℃烘箱中干燥过夜.
1.3 Fe3O4/rGO修饰电极的制备直径3 mm的玻碳电极依次用1.0、0.3、0.05 μm的氧化铝粉末抛光,再分别用硝酸以及超纯水对电极表面进行超声清洗.然后以新制备的0.1 mol/L H2SO4为底液,用循环伏安法扫描15圈,电压-0.25~1.25 V,扫描速度50 mV/s,经处理后的电极干燥后用超纯水洗涤后干燥待用.将1 mg Fe3O4/rGO分散于1 mL无水乙醇中,取10 μL该分散液于玻碳电极表面,置于室温中干燥,该电极记为Fe3O4/rGO/GCE.
1.4 Pd/Fe3O4/rGO修饰电极的制备以Fe3O4/rGO/GCE为工作电极,饱和甘汞电极(SCE)为参比电极,铂网电极为辅助电极,在0.1 mol/L KCl和0.5 mmol/L Pd前驱物的混合溶液中,控制-0.8~0.5 V电位内,采用循环伏安法扫描50周,扫描速度50 mV/s.取出,用超纯水冲洗并自然干燥,得到Pd/Fe3O4/rGO纳米复合材料修饰电极,该电极记为Pd/Fe3O4/rGO/GCE,即为基于Pd沉积铁磁/石墨烯纳米复合材料的传感器.
2 结果与讨论 2.1 Pd/Fe3O4/rGO纳米复合材料的表征将Pd纳米颗粒利用电化学方法沉积到Fe3O4/rGO纳米复合材料表面以后,利用扫描电子显微镜(SEM)和能谱仪(EDS)分别对样品的形貌和组成进行了表征,结果见图 1.
|
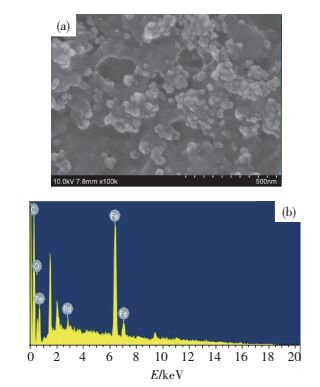
图 1 Pd/Fe3O4/rGO的扫描电镜照片(a)和X射线能谱(b) Figure 1 SEM images of Pd/Fe3O4/rGO on GCE (a) and the EDS of Pd/Fe3O4/rGO composite (b) |
由图 1(a)可以观察到,较深的黑色衬底表面,分布着粒径为50 nm左右的白色球状物质.EDS能谱分析结果(图 1(b))也表明,复合材料中有Pd和Fe的存在,说明Pd纳米颗粒已经成功沉积到了Fe3O4/rGO纳米复合材料表面.
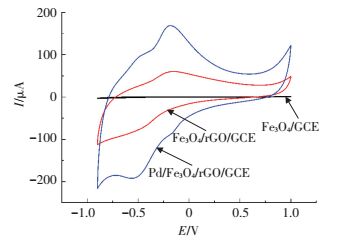
2.2 修饰电极的电化学性能表征图 2显示了不同材料修饰电极Fe3O4/GCE、Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE在0.1 M PBS(pH 7.4, 含有0.1 M KCl)中的循环伏安曲线.从图 2可以观察到:Fe3O4/GCE没有明显的氧化还原峰,但Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE都显示出一对完整的氧化还原峰;并且Pd/Fe3O4/rGO/GCE的峰值电流(ΔIp)是Fe3O4/rGO/GCE的3倍之多,这也说明了石墨烯和Pd纳米颗粒的引入赋予了传感器更为优异的电子转移能力.
|
图 2 Fe3O4/GCE、Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE在0.1 M PBS (pH 7.4, 含有0.1 M KCl)中的CV曲线 Figure 2 Cyclic voltammograms of Fe3O4/GCE、Fe3O4/rGO/GCE and Pd/ Fe3O4/rGO/GCE in 0.1 M PBS, pH 7.4 (containing 0.1 M KCl) at scan rate of 50 mV/s |
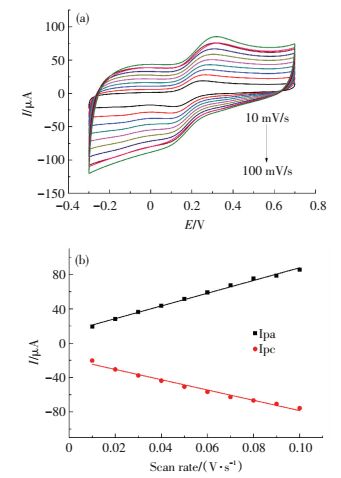
随后研究了Pd/Fe3O4/rGO/GCE在含有5 mM Fe(CN)63-/4-的0.1 M PBS(0.1 M KCl)溶液中,不同扫描速度与峰电流之间的关系,扫苗速度范围10~100 mV/s.如图 3所示,随着扫描速度的增加,峰与峰之间的电位ΔEp以及峰电流ΔIp也同步增加,且阳极峰电流和阴极峰电流均与扫速成良好的线性关系,表明电极反应是一个表面控制过程.
|
图 3 Pd/Fe3O4/rGO/GCE在0.1 M PBS(pH 7.4, 含有0.1 M KCl)溶液中不同扫描速度下的CV图(a)和氧化还原电流值和扫速的关系(b) Figure 3 Cyclic voltammograms of the Pd/Fe3O4/rGO/GCE in in 0.1 M PBS, pH 7.4 (containing 0.1 M KCl) at different scan rates (a) and the dependence of redox peak currents on the scan rate (b) |
图 4比较了Pd/Fe3O4/rGO/GCE在有/无0.1 m M H2O2存在时的循环伏安行为.对于Pd/Fe3O4/rGO/GCE而言,-0.1 V处的还原峰归属于Pd的电还原信号.当溶液中加入0.2 mM H2O2储备液后,Pd/Fe3O4/rGO/GCE传感器在-0.1 V的还原峰电流增大,表明了制备的电极对H2O2有较好的电化学响应.

|
图 4 Pd/Fe3O4/rGO/GCE在0.1 M PBS (pH 7.4)溶液中,扫速50 mV/s时加入/不加入H2O2的CV曲线 Figure 4 CV curves of Pd/Fe3O4/rGO/GCE in 0.1 M PBS (pH 7.4) with the absence and presence of H2O2 at scan rate of 50 mV/s |
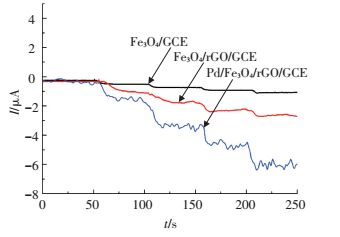
为进一步说明石墨烯片层结构和Pd纳米颗粒的引入对传感器电催化性能的影响,利用计时电流法,在检测电位为-0.1 V时,向0.1 M PBS(pH 7.4, 包含0.1 M KCl)溶液中等时间间隔加入同浓度的H2O2,比较Fe3O4/GCE、Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE对检测物响应大小.如图 5所示,通过修饰Fe3O4/GCE,当连续加入等浓度的H2O2、Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE对H2O2都产生一个快速响应.值得注意的是Fe3O4/rGO/GCE和Pd/Fe3O4/rGO/GCE产生的电流响应分别约为Fe3O4/GCE电流响应的3倍和5倍.修饰电极电流响应信号的增强可能归结于石墨烯良好的二维层状结构可以为Fe3O4磁性纳米颗粒和Pd提供良好的固定环境;同时,Pd纳米颗粒的引入可以提高传感器的催化性能和稳定性,这样便形成了完美的整体结构,这种结构是一种导电网络,可以缩短电子和离子运输的途径,提高电子传递速度.
|
图 5 检测电位-0.1 V时,向0.1 M PBS (pH 7.4, 包含0.1 M KCl)溶液中等时间间隔加入0.2 mM H2O2,不同修饰电极对检测物响应 Figure 5 Current-time response of Fe3O4/GCE、Fe3O4/rGO/GCE and Pd/Fe3O4/rGO/GCE upon successive addition of 0.2 mM H2O2 in 0.1 M PBS, pH 7.4 (containing 0.1 M KCl) at an applied potential of -0.1 V |
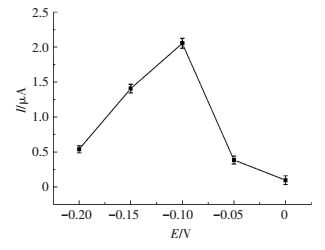
用计时电流法考察传感器性能之前,先对传感器检测电位进行优化.因为合适的检测电位对传感器灵敏度有很大影响.如图 6所示,在-0.2 ~0 V内,向溶液中加入0.1 mM H2O2后,检测电极在-0.1 V电位下的安培响应最大,因此-0.1 V为最优检测电位,故以下测试均在此电位下进行.
|
图 6 Pd/Fe3O4/rGO/GCE在不同检测电位下对H2O2的电流响应 Figure 6 Current responses of the Pd/Fe3O4/rGO/GCE upon H2O2 at different applied potentials |
图 7记录了采用计时电流法记录检测电位为-0.1 V时,向搅拌的0.1 M PBS(pH 7.4, 含有0.1 M KCl)溶液中连续滴加不同浓度H2O2时的安培电流响应曲线.由图 7可知,随着不断加入H2O2,电流响应呈现阶梯性的增大,电极对检测物的响应时间约为5 s.在50~1 000 μM和1 000~2 600 μM范围内,H2O2的浓度与电流响应呈现良好的线性关系,灵敏度分别为3.685和2.810 μA/mM.由以上数据可看出,Pd/Fe3O4/rGO/GCE传感器对于H2O2的检测有较高的灵敏度和较宽的线性范围.

|
图 7 Pd/Fe3O4/rGO/GCE电极在检测电位-0.1 V,向搅拌的0.1 M PBS (pH 7.4, 含有0.1 M KCl)溶液中连续滴加不同浓度H2O2时的安培电流响应曲线;内插图为电流与H2O2浓度的标准曲线 Figure 7 Amperometric response of the Pd/Fe3O4/rGO/GCE for the successive addition of different concentration of H2O2 into constantly stirred 0.1 M PBS, pH 7.4 (containing 0.1 M KCl). Applied potential: -0.1 V; Insert: the calibration line of the response current vs. the H2O2 concentration |
选择性是一项评价传感器性能优劣的重要指标,实验测试了常见干扰物L-抗坏血酸(AA)、多巴胺(DA)、D-葡萄糖(Glu)以及尿酸(UA)对H2O2传感器选择性的影响.实验结果如图 8所示,可以看出,以上干扰物对H2O2检测的影响较小,可忽略不计,这说明Pd/Fe3O4/rGO纳米复合材料修饰电极可以避免其他物质干扰, 用于实际样品的检测.

|
图 8 外源性干扰物对电极检测H2O2性能的影响(图中箭头表示加入0.1 mM H2O2、0.5 mM UA、0.5 mM AA、0.5 mM DA和0.5 mM Glu的计时电流曲线) Figure 8 Effect of the possible interferents in H2O2 biosensor. The arrows show the each moment at the successive addition of 0.1 mM H2O2、0.5 mM UA、0.5 mM AA、0.5 mM DA and 0.5 mM Glu |
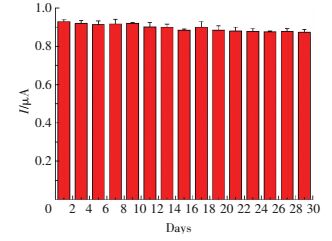
接着考察了Pt/Fe3O4/rGO修饰电极的重复性和稳定性.挑选新制备的5根电极,利用计时电流法对0.2 mM的H2O2进行检测,记录每根电极的安培电流响应,计算得到5根电极电流的相对标准偏差为3.2%,结果表明,制备的修饰电极具有良好的一致性,可用于H2O2的可重复性检测.此外,同样利用计时电流法研究了传感器的稳定性,考察4周内同一根电极对相同浓度H2O2测定的电流变化,结果见图 9,发现经过数周使用后Pt/Fe3O4/rGO修饰电极30天后仍保持95.2%以上的灵敏度.Pt/Fe3O4/rGO纳米复合材料的稳定结构有效保持了传感器的稳定性.
|
图 9 Pt/Fe3O4/rGO修饰电极的长期稳定性测试结果 Figure 9 Long-term stability of the Pt/Fe3O4/rGO/GCE |
1) 本文利用电化学沉积的方法将Pd纳米颗粒沉积到Fe3O4/rGO纳米复合材料修饰的玻碳电极表面,形成了直接测定H2O2的无酶传感器.该复合结构集合了石墨烯和Pd纳米颗粒的性能优越性,提高了传感器对H2O2的检测灵敏度,降低了检测限,在50~1 000 μM和1 000~2 600 μM范围内,H2O2的浓度与电流响应呈现良好的线性关系,灵敏度分别为3.685和2.810 μA/mM.
3) 该传感器经过数周使用后仍保持95.2%以上的灵敏度,常见干扰物质也对H2O2检测的影响较小,因此具有一定的实际应用价值.
| [1] | CHEN Wei, CAI Shu, REN Qiongqiong, et al. Recent advances in electrochemical sensing for hydrogen peroxide: a review[J]. Analyst, 2012, 137(1): 49–58. DOI: 10.1039/C1AN15738H |
| [2] | LI Jianping, LI Yuping, ZHANG Yun, et al. Highly sensitive molecularly imprinted electrochemical sensor based on the double amplification by an inorganic prussian blue catalytic polymer and the enzymatic effect of glucose oxidase[J]. Analytical Chemistry, 2012, 84(4): 1888–1893. DOI: 10.1021/ac2026817 |
| [3] | ZHU Zhigang, GARCIA-GANCEDO L, CHEN Cheng, et al. Enzyme-free glucose biosensor based on low density CNT forest grown directly on a Si/SiO2 substrate[J]. Sensor and Actuators B: Chemical, 2013, 178(3): 586–592. |
| [4] | ZHU Xiang, NIU Xiangheng, ZHAO Hongli, et al. Doping ionic liquid into prussian blue-multiwalled carbon nanotubes modified screen-printed electrode to enhance the nonenzymatic H2O2 sensing performance[J]. Sensor and Actuators B:Chemical, 2014, 195(5): 274–280. |
| [5] | CHEN Lijian, WANG Nan, WANG Xindong, et al. Protein-directed in situ synthesis of platinum nanoparticles with superior peroxidase-like activity, and their use for photometric determination of hydrogen peroxide[J]. Microchimica Acta, 2013, 180(15): 1517–1522. |
| [6] | GAO Lizeng, ZHUANG Jie, NIE Leng, et al. Intrinsic peroxidase-like activity of ferromagnetic nanoparticles[J]. Nature Nanotechnology, 2007, 2(9): 577–583. DOI: 10.1038/nnano.2007.260 |
| [7] | GEORGIA G, ANTHEMIDIS A N. Magnetic materials as sorbents for metal/metalloid preconcentration and/or separation. A review[J]. Analytica Chimica Acta, 2013, 789(14): 1–16. |
| [8] | HAO Rui, XING Ruijun, XU Zhichuan, et al. Synthesis, functionalization, and biomedical applications of multifunctional magnetic nanoparticles[J]. Advanced Materials, 2010, 22(25): 729–2742. |
| [9] | ZHANG Zhanxia, ZHU Hui, WANG Xiaolei, et al. Sensitive electrochemical sensor for hydrogen peroxide using Fe3O4 magnetic nanoparticles as a mimic for peroxidase[J]. Microchimica Acta, 2011, 174(1): 183–189. |
| [10] | AMBROSI A, CHUA C K, BONANNI A, et al. Electrochemistry of graphene and related materials[J]. Chemical Reviews, 2014, 114: 7150–7188. DOI: 10.1021/cr500023c |
| [11] | JIANG Lili, FAN Zhuangjun. Design of advanced porous graphene materials: from graphene nanomesh to 3D architectures[J]. Nanoscale, 2014, 6: 1922–1945. DOI: 10.1039/C3NR04555B |
| [12] | CHEN Shihong, YUAN Ruo, CHAI Yaqin, et al. Electrochemical sensing of hydrogen peroxide using metal nanoparticles: a review[J]. Microchimica Acta, 2013, 180: 15–32. DOI: 10.1007/s00604-012-0904-4 |
| [13] | MARCANO D C, KOSYNKIN D V, BERLIN J M, et al. Improved synthesis of graphene oxide[J]. ACS Nano, 2010, 4(8): 4806–4814. DOI: 10.1021/nn1006368 |
 2017, Vol. 25
2017, Vol. 25


