2. 东华大学 材料科学与工程学院,上海 201620;
3. 越南国立河内科学大学 化学学院,越南 河内 1000000;
4. 上海应用技术大学 材料科学与工程学院,上海 201418
2. School of Materials Science and Engineering, Donghua University, Shanghai 201418, China;
3. Faculty of Chemistry, VNU University of Science, Vietnam National University, Hanoi 1000000, Vietnam;
4. School of Materials Science and Engineering, Shanghai Institute of Technology, Shanghai 201418, China
光解水制氢是光催化和洁净能源领域极其重要的研究课题,具有长远的战略应用前景.自1972年Fujishima等[1]发现TiO2单晶可用于光催化分解水以来,半导体异相催化技术得到了深入的研究和发展.迄今已发现的可用于光解水的催化剂材料主要有钛、钽、铌、镓的氧化物和硫化物等材料[2-3].其中,具有钙钛矿结构的钛酸锶(SrTiO3)作为一种具有典型钙钛矿结构(ABO3)的复合金属氧化物,由于其结构明确,物化性质稳定,具有高度的化学匹配性以及合适的禁带宽度(3.2 eV),应用于光催化领域而被熟知[4-5].紫外光能激发其价带位置的电子至导带位置而产生电子-空穴对;而钛酸锶的导带位置比二氧化钛导带位置低200 mV,使得钛酸锶可与二氧化钛进行配对产生能带电势差以增强其光电化学性能[6].Zhang等[7]发现, 在光电化学电池系统中通过使SrTiO3与TiO2纳米管进行复合能够促进光激发下电子与空穴的有效分离,从而提高相应的光电流与光电压,预测SrTiO3/TiO2异质结结构可被应用于染料-光敏电池、二氧化碳催化还原或光催化分解水制氢领域.Cao等[8]成功合成了SrTiO3/TiO2纳米颗粒,并发现此材料在紫外光照射下降解罗丹明B发挥更加显著的光催化性能.受上述结果启发,SrTiO3/TiO2一维结构纳米管理论上也可在光催化分解水中发挥改善的作用.然而,关于SrTiO3/TiO2纳米结构中电子激发载流子特性的理论研究仍不充分.此外,在TiO2纳米管中添加Sr提供了一种途径来研光催化活性的目的.另外,SrTiO3具有优异的化学稳定性.耦合SrTiO3与TiO2可以预期通过带边偏移引入强界面电场,有效加速了光生载体的分离,提高了TiO2的光催化性能.
已经通过多种方法合成了SrTiO3,包括溶胶-凝胶法、水热合成、常规固相反应、反胶团微乳液法、熔盐合成法和非水法.具有钙钛矿型结构的化合物作为重要构象从水热反应出现[8-12].因此,需要开发具有可控形态和尺寸的SrTiO3/TiO2异质结构的一般方法.此外,非均相催化剂的活性基本上受到晶相、尺寸、表面积、结晶度,特别是暴露的晶面的影响, 它们的形态和外表面也影响它们的光催化活性.在这方面,SrTiO3尺寸和形状的精确控制对于评估形状依赖性光反应性和开发高性能光催化剂至关重要.然而,尽管以前的种种努力,对其尺寸和形状的这种精确控制已经分散和限制.关于SrTiO3/TiO2及负载贵金属异质结构界面厚度和不同形态对氢气产生的影响的研究尚未有报道[12-20].
本文通过简单水热法首先合成一定锶钛物质的比的SrTiO3/TiO2异质结结构纳米颗粒,采用XRD、SEM、UV-vis方法对其进行表征,通过“光催化还原沉积方法”制备不同质量分数的纳米铂颗粒(0、1%、2%、5%),探究其光催化分解水产氢性能测试催化活性的变化.
1 实验 1.1 TiO2纳米颗粒的制备称取0.1 mol钛酸四丁酯入烧杯中,在剧烈搅拌过程中连续缓慢滴加0.4 mol质量分数37%的浓HCl.持续剧烈搅拌2 h至体系混合反应至澄清透明后,把整个体系转入水热釜中,于200 ℃恒温连续反应24 h后自然降至室温,将所得到的白色粉体经去离子水和无水乙醇离心洗涤数次后放入干燥箱,于60 ℃下干燥12 h,最终得到TiO2白色粉末.
1.2 制备SrTiO3/TiO2异质结结构纳米颗粒称取0.02 mol上述TiO2白色粉末于烧杯中,物质的量比n(Sr)/n(Ti)=0.4,同时在烧杯中加入0.008 mol Sr(OH)2·8H2O,并向其中加入65 mL去离子水超声分散5 min并剧烈搅拌1 h,至混合液搅拌均匀后置入水热反应釜中,于160 ℃恒温连续反应20 h后自然降至室温,所得到的白色粉体经去离子水和无水乙醇离心洗涤数次后放入干燥箱于60 ℃下干燥12 h,最终得到SrTiO3/TiO2白色粉末.
1.3 Pt负载SrTiO3/TiO2异质结结构纳米颗粒称取上述SrTiO3/TiO2样品0.5 g于100 mL烧杯中,加入50 mL去离子水超声分散均匀并搅拌,然后按质量分数0、1%、2%、5%向其中加入H2PtCl6·6H2O分别为0、0.009、0.018、0.044 g.将整个体系至于紫外氙灯光照下持续搅拌至水分完全挥发,残余物离心洗涤干燥后得到4组样品.
1.4 样品的表征采用PANalytical公司X′pert Pro XRD型射线衍射仪检测样品的晶体结构,用高分辨率透射电子显微镜(JEOL JEM-2011)观察形貌、尺寸及其晶格结构,用日本岛津公司SHIMADZU UV-3600紫外可见分光光度计上测试样品的紫外-可见吸收光谱,扫描范围为200~800 nm.采用X-射线光电子能谱分析仪器(XPS,ESCALAB250Xi)分析样品.
1.5 光解水性能测试所有催化剂样品全部用于紫外光下的光催化分解水实验.每份样品分别取0.1 g分散于100 mL含甲醇浓度6 mol/L的水溶液中(甲醇提供电子牺牲剂).300 W高压氙灯(北京中教金源有限公司,总输出功率50 W,紫外输出功率6.6 W,其中实测光功率为5.93 mW,所对应的光密度为7.89 mW/cm3)作为紫外光源, 灯口高于水平面10 cm.反应温度恒定保持在5 ℃.
上述整个体系可被作为一套光化学电池系统,并用于光解水测试实验.产生的氢气采用北京中教金源有限公司的带有热传导探测器的GC-7900型气相色谱(高纯氮气作为载流气)进行分析.
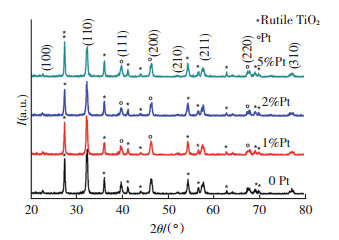
2 结果及分析 2.1 样品表征分析图 1为不同Pt纳米颗粒负载量0、1%、2%、5%)的SrTiO3/TiO2异质结纳米颗粒XRD谱图.由图 1可知:n(Sr)/n(Ti)=0.4时,水热反应160 ℃下20 h后,在谱图中出现了SrTiO3特征峰,分别是2θ=22.68°、32.34°、39.88°、46.43°、57.74°、67.81°和77.12°,分别对应SrTiO3的(100)、(110)、(111)、(200)、(211)、(220)和(310)晶面,与JCPDS01-074-1296卡片(晶格常数为a=b=c=0.390 nm)基本吻合,证明合成的样品中含有SrTiO3,结晶良好,属立方晶系;2θ=27.44°、36.08°、39.19°、41.24°、44.05°、54.32°、56.63°、62.76°、64.05°、69.01°、69.80°、72.42°和76.54°分别对应金红石型TiO2(110)、(101)、(200)、(111)、(210)、(211)、(220)、(002)、(310)、(301)、(112)、(311)和(202)晶面,与JCPDF01-089-0552卡片(晶格常数为:a=b=0.460 nm,c=0.296 nm)基本吻合,证明合成的样品中含有TiO2,结晶良好,属四方晶系.谱图中2θ=39.80°、46.34°、67.21°对应了Pt的(111)、(200)、(210)的衍射峰,与JCPDS00-004-0802卡片(晶格常数为:a=b=c=0.392 nm)基本吻合,证明合成的样品中含有Pt纳米颗粒,结晶良好,属立方晶系,表明实验成功合成了PtPt纳米颗粒负载具有SrTiO3/TiO2复合纳米颗粒结构[21-23].
|
图 1 负载Pt纳米颗粒质量分数分别为0、1%、2%、5%的SrTiO3/TiO2异质结纳米颗粒XRD谱图 Figure 1 XRD patterns of SrTiO3/TiO2 heterojunction nanoparticles loaded with 0, 1%, 2%, 5% Pt |
表 1列出了不同质量分数Pt纳米颗粒负载SrTiO3/TiO2的平均晶粒尺寸、晶格常数、晶粒尺寸以及晶格常数根据Debye-Sc和Debye-Scherrer公式计算.
| 表 1 不同质量分数Pt纳米颗粒负载SrTiO3/TiO2异质结样品的平均晶粒尺寸以及晶格常数 Table 1 Average crystallite size and lattice constant of the SrTiO3/TiO2 heterojunction samples doped withdifferent amounts of Pt |
由表 1可知,合成的样品主晶相均为纳米尺寸的SrTiO3/TiO2,其晶格常数与标准晶格常数基本吻合.通过精修XRD数据可知,随着负载量的增加,Pt纳米颗粒的平均晶粒尺寸为40.8 nm.
为了表征制备的Pt纳米颗粒负载SrTiO3/TiO2异质结复合纳米颗粒的形貌,采用TEM和HRTEM对Pt纳米颗粒负载SrTiO3/TiO2复合纳米颗粒进行了观察分析.图 2为不同负载Pt后SrTiO3/TiO2纳米颗粒的形貌.由图 2(a)可以看出,经水热反应以及浸渍法负载Pt后得到的SrTiO3/TiO2形貌呈纳米颗粒状,且粗细均一,形貌及分布均匀.在5%Pt负载图中可以清晰地观测到Pt的金属颗粒,并且尺寸均匀.图 2(b)给出了5%Pt纳米颗粒SrTiO3/TiO2异质结结构的高分辨透射电镜TEM照片,可以看出,粒径为20~50 nm的SrTiO3纳米颗粒均匀地分布在TiO2纳米立方体的表面.结合上述XRD谱图及下文的能谱XPS分析可以推断,SrTiO3纳米颗粒能够成功地在TiO2表面生长.另外,由图 2(b)可以看出:在SrTiO3和TiO2间有一层明显的界面,这可能就是所谓的SrTiO3/TiO2异质结结构;在交界处展现出了2种明显不同的晶格条纹,晶格条纹间距是0.326 nm,对应锐钛矿(110)晶面,而另一个是0.277 nm,对应立方相钛酸锶(110)晶面,0.196 nm对应立方相纳米Pt的(200)晶面.

|
图 2 负载Pt纳米颗粒的SrTiO3/TiO2纳米颗粒TEM照片(a)及HRTEM照片(b) Figure 2 TEM (a) and HRTEM (b) images of SrTiO3/TiO2 heterojunction nanocomposites loaded with Pt |
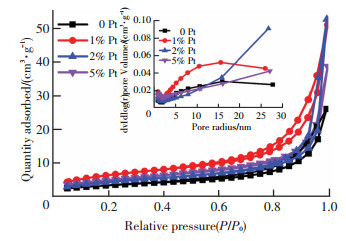
通过氮吸附-解吸附等温线对比,SrTiO3/TiO2和负载Pt纳米颗粒异质结构样品的比表面积,孔结构和尺寸分布进行了表征,结果见图 3.由图 3可以看出,SrTiO3/TiO2异质结构样品对于所有不同的形态显示出介孔结构.氮吸附-解吸等温线可分为Ⅲ型等温线,是典型的介孔材料.根据IUPAC分类,磁滞回线是H3型.通常发现这种类型的滞后是由具有不均匀尺寸和/或形状的形成狭缝状孔的聚集体或颗粒团聚体形成的0.1%Pt纳米颗粒SrTiO3/TiO2异质结构的BET比表面积在23.195 m2/g处最高,并且介孔材料的特征是平均Barrett-Joyner-Halenda(BJH)孔径为13.60 nm,总孔体积为0.079 cm3/g.高BET表面积和大的总孔体积强烈支持SrTiO3/TiO2具有介孔结构的事实.扩大的比表面积将产生更多的反应位点, 以促进反应物的通入.考虑到上述优点,认为SrTiO3/TiO2层状结构对SrTiO3/TiO2异质结构的光催化活性有较好的改善作用.
|
图 3 SrTiO3/TiO2、1%Pt、2%Pt和5%Pt结构的氮吸附-脱附等温线图和孔径分布 Figure 3 Nitrogen adsorption-desorption isotherm plot and pore size distribution of SrTiO3/TiO2, 1%Pt, 2%Pt and 5%Pt structures |
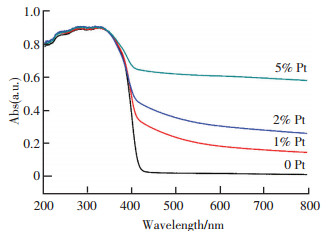
图 4为不同Pt纳米颗粒负载量(0、1%、2%、5%)的锶钛物质的量比0.4时SrTiO3/TiO2异质结纳米颗粒样品的紫外-可见漫反射吸收光谱.由图 4可以看出:SrTiO3/TiO2在紫外区域尤其是在波长小于420 nm的光谱范围内有最强的吸收性能;随着Pt负载量的增加,Pt-SrTiO3/TiO2在紫外-可见光谱范围内均有较好的吸收性能,说明引入Pt纳米颗粒有效提高了SrTiO3/TiO2在可见光范围内的吸收性能.
|
图 4 Pt纳米颗粒负载量质量分数分别为0、1%、2%、5% SrTiO3/TiO2纳米颗粒的UV-vis谱图 Figure 4 UV-Vis spectra of the SrTiO3/TiO2 heterojunction nanoparticles loaded with Pt of different mass fractions 0, 1%, 2%, 5% |
通过计算负载Pt纳米颗粒的SrTiO3/TiO2纳米颗粒样品的禁带宽,利用公式[24-26]
| $ {E_{\rm{g}}} = 1\;240/\lambda ({\rm{nm}}), $ |
计算负载Pt纳米颗粒质量分数为0、1%、2%、5%时SrTiO3/TiO2纳米颗粒的带隙Eg,分别为2.99、2.72、2.29、2.02 eV,意味着均可在紫外光下被激发(如图 5所示); 并且随着Pt纳米颗粒负载量的增加,其带隙逐渐减小,从而大大降低电子跃迁所需要的能量,提高光催化分解水效率.
|
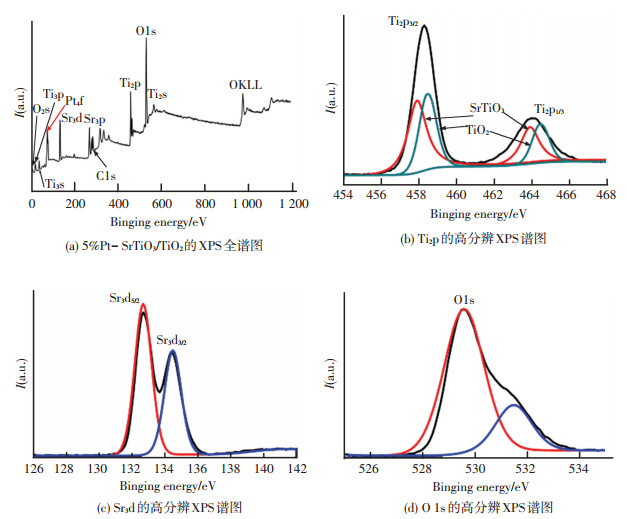
图 5 5%Pt-SrTiO3/TiO2的XPS谱图 Figure 5 XPS of 5% Pt-SrTiO3/TiO2:(a) XPS survey spectra; (b) high-resolution XPS spectrum of Ti2p; (c) Sr3d; (d) O 1s of the 5% Pt-SrTiO3/TiO2 sample |
图 5为5%Pt纳米颗粒负载SrTiO3/TiO2异质结纳米颗粒的XPS谱图.由图 5(a)可知,Pt负载SrTiO3/TiO2的全谱结果显示样品表面只有Sr、Ti、O、C及Pt纳米颗粒5种元素存在,并未检测到其他元素的存在.通过实验数据分析可知,电子结合能为284.6 eV处的峰属于C1s的特征谱峰,来源于样品制备过程中被C污染所造成的,说明样品是由Pt纳米颗粒、SrTiO3与TiO2复合而成,与前面分析的EDS和XRD结果一致.Ti的高分辨XPS如图 5(b)所示,该特征峰在458.63 eV的中心(Ti2p3/2)和464.12 eV(Ti2p1/2),并且Ti2p峰出现了宽化和不对称,结合元素结合能和峰形特征,表示在一个Ti4+的氧化态存在钛酸锶/二氧化钛异质结构中.如图 5(c)所示,该特征峰在132.74 eV的中心(Sr3d5/2)和134.47 eV(Sr3d3/2).在132.74 eV所对应的特征峰为所报道的钙钛矿的SrTiO3,134.47 eV所对应的特征峰为SrO混合物[13].如图 5(d)所示,在529.56 eV出现的特征峰与TiO2和SrTiO3有关,另一个在531.78 eV的中心峰被认为是涉及到吸附的氧气,如碳酸盐和羟基氧化物[14-15].
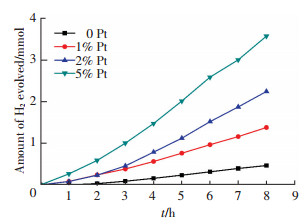
2.2 光催化制氢性能图 6给出了Pt纳米颗粒负载量分别为0、1%、2%、5%的锶钛物质的量比为0.4时的SrTiO3/TiO2异质结纳米颗粒光催化分解水产生氢气随时间的变化曲线,表 2为SrTiO3/TiO2纳米颗粒在Pt负载量质量分数分别为0、1%、2%和5%时的产氢结果.
|
图 6 SrTiO3/TiO2异质结Pt纳米颗粒负载量质量分数分别为0、1%、2%和5%的产氢曲线 Figure 6 H2 generation amount of the SrTiO3/TiO2 heterojunction nanoparticles at different Pt loaded mass fractions 0, 1%, 2% and 5% |
| 表 2 SrTiO3/TiO2,1%Pt,2%Pt和5%Pt的BET表面积和孔径尺寸 Table 2 BET surface area and crystallite size of SrTiO3/TiO2, 1%Pt, 2%Pt and 5%Pt structures |
由表 3可以看出:当Pt负载量为5%时,其SrTiO3/TiO2纳米颗粒到达最优催化活性,此时在紫外光照下8 h分解水产生氢气为3.574 mmol;当样品中负载Pt纳米颗粒后,催化效率明显高于未负载的SrTiO3/TiO2纳米颗粒.此结果证明负载贵金属元素可以显著降低催化剂的肖特基能级,提高产品的光催化活性.
| 表 3 SrTiO3/TiO2异质结负载Pt纳米颗粒质量分数分别为0、1%、2%和5%的产氢结果 Table 3 H2 generation amount of the SrTiO3/TiO2 heterojunction nanoparticles with different Pt loaded mass fraction 0, 1%, 2% and 5% |
此外,虽然负载质量分数5%的Pt纳米颗粒后SrTiO3/TiO2纳米颗粒催化活性最高,但从性价比方面来考虑,其性价比最低.因为从表 3得出,负载5%Pt后的产氢效率显著低于负载2%Pt纳米颗粒后产氢效率的2.5倍,同时也显著低于负载1%Pt后产氢效率的5倍,因此从经济效益方面来说,负载1%Pt后的SrTiO3/TiO2纳米颗粒其性价比为最优.
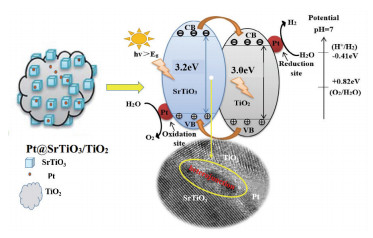
图 7为负载Pt纳米颗粒的SrTiO3/TiO2异质结纳米颗粒光催化分解水机理图.在紫外光的照射下,电子在SrTiO3内从价带激发到了导带,SrTiO3中被激发至导带的电子通过SrTiO3/TiO2界面被传输到了TiO2的导带位置上,同时TiO2中价带上的光生空穴也转移到了SrTiO3的价带上.从而使电子和空穴得到有效分离.
|
图 7 紫外光照射下负载Pt纳米颗粒的SrTiO3/TiO2纳米颗粒光催化剂上电子转移及生成氢气示意图 Figure 7 Schematic photoexcited electron transfer and H2 evolution on Pt-loaded SrTiO3/TiO2 heterojunction nanoparticles photocatalyst under UV irradiation |
为了进一步了解Pt纳米颗粒负载SrTiO3/TiO2异质结的光催化响应的机制,在能量角度及钛酸锶和二氧化钛之间的电荷转移进行了讨论.半导体材料的VB和CB边缘电位可根据式(1)和(2)进行计算.
| $ {E_{{\rm{VB}}}} = X-{E_{\rm{e}}} + 0.5{E_{\rm{g}}}, $ | (1) |
| $ {E_{{\rm{CB}}}} = {E_{{\rm{VB}}}}-{E_{\rm{g}}}. $ | (2) |
式中:EVB和ECB分别为VB和CB的边缘电位;X是半导体的电负性,TiO2和SrTiO3的X为5.81和4.94 eV;Ee为对氢比例(4.5 eV)的自由电子的能量;Eg为半导体的带隙能量.
TiO2和SrTiO3的ECB计算结果为-0.29和-1.16 eV(相对于标准氢电极,NHE).在紫外光的激发下,TiO2和SrTiO3的VB上的电子被激发,后转移到其对应的CB上,在VB上留下各自的空穴.当SrTiO3纳米颗粒接触TiO2时,纳米结构异质结形成.一方面,钛酸锶的CB比二氧化钛更负时,光生电子快速地从钛酸锶的CB传送到二氧化钛,同时,对TiO2的VB中的光生空穴直接移动到钛酸锶的VB; 另一方面,TiO2的费米能级被向上移动(朝向负电势),而钛酸锶的费米能级向下移动(朝正电位),直至平衡状态成立,导致钛酸锶的变速的费米水平/二氧化钛纳米管异质更负的电位.在平衡状态在异质结界面建立能够进一步促进激发光生载流子迁移的内电场.
根据以上结果和讨论可知,优秀的光电化学活动可归因于负的协同效应在异质移位费米水平和降低的光生载流子复合率.由于贵金属Pt纳米颗粒的负载,Pt纳米颗粒具有稳定的化学性质和良好的导电性,大大降低了光催化所需的肖特基能级,从而显著提升了SrTiO3/TiO2纳米颗粒的光催化性能[26-30].
3 结论负载贵金属Pt量越大,相应的催化剂催化活性越高,其中,负载5% Pt的SrTiO3/TiO2异质结纳米颗粒光催化8 h产氢量为3.574 mmol,平均产氢效率为0.447 mmol/(gcat·h).但从性价比的角度来考虑,其催化效率远不及负载1%Pt纳米颗粒的SrTiO3/TiO2纳米颗粒催化效率的5倍,因此虽然负载5%Pt纳米颗粒的SrTiO3/TiO2纳米颗粒光催化效率最高,但是性价比却最低,相反,负载1%Pt纳米颗粒的SrTiO3/TiO2异质结纳米颗粒的光催化性价比最高.它应该有极大的潜力在光催化、太阳能电池、光阴极应用保护环境甚至抗菌材料等.
| [1] | FUJISHIMA A, HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238(5358): 37–38. DOI: 10.1038/238037a0 |
| [2] | KUDO A. Development of photocatalyst materials for water splitting[J]. International Journal of Hydrogen Energy, 2006, 31(2): 197–202. DOI: 10.1016/j.ijhydene.2005.04.050 |
| [3] | MAEDA K, DOMEN K. New non-oxide photocatalysts designed for overall water splitting under visible light[J]. J Phys Chem C, 2007, 111(22): 7851–7861. DOI: 10.1021/jp070911w |
| [4] | DOMEN K, KUDO A, ONISHI T. Photocatalytic decomposition of water into H2 and O2, over NiO-SrTiO3, powder. 1. structure of the catalyst[J]. J Phys Chem, 1986, 90: 292–295. DOI: 10.1021/j100274a018 |
| [5] | AHUJA S, KUTTY T R N. Nanoparticles of SrTiO3 prepared by gel to crystallite conversion and their photocatalytic activity in the mineralization of phenol[J]. J Photoch Photobio A, 1996, 97(1/2): 99–107. |
| [6] | DIAMANT Y, CHEN S G, MELAMED O, et al. Core-shell nanoporous electrode for dye sensitized solar cells: the effect of the SrTiO3 shell on the electronic properties of the TiO2 core[J]. J Phys Chem B, 2003, 107(9): 1977–1981. DOI: 10.1021/jp027827v |
| [7] | ZHANG J, BANG J H, TANG C C, et al. Tailored TiO2-SrTiO3 heterostructure nanotube arrays for improved photoelectrochemical performance[J]. ACS Nano, 2010, 4(1): 387–395. DOI: 10.1021/nn901087c |
| [8] | CAO T P, LI Y J, WANG C H, et al. A facile in situ hydrothermal method to SrTiO3/TiO2 nanofiber heterostructures with high photocatalytic Activity[J]. Langmuir, 2011, 27(6): 2946–2952. DOI: 10.1021/la104195v |
| [9] | HUANG Z Q, RACITI D, YU S N, et al. Synthesis of platinum nanotubes and nanorings via simultaneous metal alloying and etching[J]. J Am Chem Soc, 2016, 138: 6332–6335. DOI: 10.1021/jacs.6b01328 |
| [10] | ZHENG Z K, TACHIKAMA T, MAJIMA T. Single-particle study of Pt-modified Au nanorods for plasmonenhanced hydrogen generation in visible to near-infrared region[J]. J Am Chem Soc, 2014, 136: 6870–6873. DOI: 10.1021/ja502704n |
| [11] | HE W W, WU X C, LIU J B, et al. Pt-guided formation of Pt-Ag alloy nanoislands on Au nanorods and improved methanol electro-oxidation[J]. J Phys Chem C, 2009, 113(24): 10505–10510. DOI: 10.1021/jp9027707 |
| [12] | GUO L M, LIANG K, MARCUS K. Enhanced photoelectrocatalytic reduction of oxygen using Au@TiO2 plasmonic film[J]. ACS Appl Mater Interfaces, 2016, 8: 34970–34977. DOI: 10.1021/acsami.6b14586 |
| [13] | LIU P X, QIN R X, FU G, et al. Surface coordination chemistry of metal nanomaterials[J]. J Am Chem Soc, 2017, 139: 2122–2131. DOI: 10.1021/jacs.6b10978 |
| [13] | LOU Z Z, KIM S, ZHANG P, et al. In situ observation of single Au triangular nanoprism etching to various shapes for plasmonic photocatalytic hydrogen generation[J]. ACS Nano, 2017, 11: 968–974. DOI: 10.1021/acsnano.6b07581 |
| [14] | LOU Z Z, FUJITSUKA M, MAJIMA T. Two-dimensional Au-nanoprism/reduced graphene oxide/Pt nanoframe as plasmonic photocatalysts with multiplasmon mode boosting hot electron transfer for hydrogen generation[J]. J Phys Chem Lett, 2017, 8: 844–849. DOI: 10.1021/acs.jpclett.6b03045 |
| [15] | WENDERICH K, MUL G. Methods, mechanism, and applications of photodeposition in photocatalysis: a review[J]. Chem Rev, 2016, 116: 14587–14619. DOI: 10.1021/acs.chemrev.6b00327 |
| [16] | CHEN X, SHEN S, GUO L, et al. Semiconductor-based photocatalytic hydrogen generation[J]. Chem Rev, 2010, 110(11): 6503. DOI: 10.1021/cr1001645 |
| [17] | HARA S, YOSHIMIZU M, TANIGAWA S, et al. Hydrogen and oxygen evolution photocatalysts synthesized from strontium titanate by controlled doping and their performance in two-step overall water splitting under visible light[J]. J Phys Chem C, 2012, 116: 17458. DOI: 10.1021/jp306315r |
| [18] | IWASHINA K, KUDO A. Rh-doped SrTiO3 photocatalyst electrode showing cathodic photocurrent for water splitting under visible-light irradiation[J]. J Am Chem Soc, 2011, 133: 13272. DOI: 10.1021/ja2050315 |
| [19] | PERDEW J P, BURKE K, ERNZERHOF M. Generalized gradient approximation made simple[J]. Phys Rev Lett, 1996, 77: 3865. DOI: 10.1103/PhysRevLett.77.3865 |
| [20] | BAE S W, BORSE P H, LEE J S. Dopant dependent band gap tailoring of hydrothermally prepared cubic SrTixM1xO3(M= Ru, Rh, Ir, Pt, Pd) nanoparticles as visible light photocatalysts[J]. Appl Phys Lett, 2008, 92: 104107. DOI: 10.1063/1.2897300 |
| [21] | IRIE H, MARUYAMA Y, HASHIMOTO K. Ag+-and Pb2+-doped SrTiO3 photocatalysts: a correlation between band structure and photocatalytic activity[J]. J Phys Chem C, 2007, 111: 1847–1852. DOI: 10.1021/jp066591i |
| [22] | WANG C, QIU H, INOUE T, et al. Highly active SrTiO3 for visible light photocatalysis: a first-principles prediction[J]. Solid State Commun, 2014, 181: 5. DOI: 10.1016/j.ssc.2013.11.026 |
| [23] | ASAHI R, MORIKAWA T, OHWAKI T, et al. Visible-light photocatalysis in nitrogen-doped titanium oxides[J]. Science, 2001, 293: 269. DOI: 10.1126/science.1061051 |
| [24] | WANG B, KANHERE P D, CHEN Z, et al. Anion-doped NaTaO3 for visible light photocatalysis[J]. J Phys Chem C, 2013, 117: 22518. DOI: 10.1021/jp407025r |
| [25] | GUO E, YIN L W. Tailored SrTiO3/TiO2 heterostructures for dye-sensitized solar cells with enhanced photoelectric conversion performance[J]. J Mater Chem A, 2015, 3(25): 13390–13401. DOI: 10.1039/C5TA02556G |
| [26] | TANG R, YIN L W. Enhanced photovoltaic performance of dye-sensitized solar cells based on Sr-doped TiO2/SrTiO3 nanorod array heterostructures[J]. J Mater Chem A, 2015, 3(33): 17417–17425. DOI: 10.1039/C5TA03810C |
| [27] | MATSUI N, ANZAI K, AKAMATSU N, et al. Reaction mechanisms of carbon dioxide reforming of methane with Ru-loaded lanthanum oxide catalyst[J]. Appl Catal A-Gen, 1999, 179(1/2): 247–256. |
| [28] | SUBRAMANIAN V, ROEDER R K, WOLF E E. Synthesis and UV-visible-light photoactivity of noble-Metal-SrTiO3 composites[J]. Ind Eng Chem Res, 2006, 45(7): 2187–2193. DOI: 10.1021/ie050693y |
| [29] | HISATOMI T, KUBOTA J, DOMEN K. Recent advances in semiconductors for photocatalytic and photoelectronchemical water splitting[J]. Chem Soc Rev, 2014, 43: 7520–7535. DOI: 10.1039/C3CS60378D |
| [30] | NG J W, XU S P, ZHANG X W, et al. Hybridized nanowires and cubes: a novel architecture of a heterojunctioned TiO2/SrTiO3 thin film for efficient water splitting[J]. Adv Funct Mater, 2010, 20(24): 4287–4294. DOI: 10.1002/adfm.v20.24 |
 2018, Vol. 26
2018, Vol. 26


