2. 河北科技大学 材料科学与工程学院,石家庄 050000
2. School of Materials Science and Engineering, Hebei University of Science & Technology, Shijiazhuang 050000, China
半导体光催化技术起始于1972年,Fujishima和Honda[1]研究发现TiO2的光催化作用能够将水分解成氢气和氧气,之后这项技术开始应用到污水处理研究中.光催化的过程就是光电子跃迁产生空穴和电子对,与水和其中的氧作用产生羟基自由基·OH,后者将有机物矿化[2-3].
·OH+Organics→CO2+H2O
实际反应可分为光生载流子的产生、捕获以及复合和界面电荷的传输3个阶段[4].其中载流子产生速度是飞秒级,其他两个阶段都是纳秒级,而最后的催化剂表面反应速率则为毫秒级[5],在整个反应的开始和结束阶段还有污染物在催化剂表面吸脱附的物理过程[6].因此,光催化剂的电子结构、反应条件、光电子捕获剂的捕获能力以及催化剂和污染物的吸脱附性质基本决定了光催化反应的速率[7].
在目前的研究工作中,ZnO和TiO2是最常见的两种半导体催化剂,但由于量子效率低,载流子复合率高等问题一直无法大规模应用[8],新型催化剂的成本偏高,因而科研人员的思路逐渐转移到如何改变外部条件来提升光催化工艺的效率上.直到石墨烯和它的氧化物逐渐被引入到光催化材料中,人们的视野才又转回光催化剂材料本身[9].从上文中提到的几个方面来看,首先,石墨烯具有共轭π键结构,电子迁移率为2×105cm2/(V·s),可以作为电子受体,延缓电子空穴对的复合[10];其次,石墨烯超高的比表面积增加了催化剂和预处理物的接触面积,利于吸附[11];最后,相比于纯TiO2,复合材料的费米能级向更正的方向偏移,提高了对更长波光子的利用率[9],也可以抑制材料表面态对光生电子的捕获[12-13].
而相比于石墨烯,氧化石墨烯(GO)具有亲水特性和优异的插层性能[14],吸附能力更强,也更容易获得.GO具备实现光催化的必要结构,有研究显示不同氧化程度的石墨烯具有不同的禁带宽度,约处在2.4~4.3 eV[15-16],对应的本征吸收波长限则是288 nm~516 nm,因而在可见光下可能具有光催化效果.目前的催化剂材料领域的研究重心开始向ZnO、TiO2和还原氧化石墨烯(rGO)复合材料转移[17-20].如Morawski等[18]合成了TiO2和rGO不同占比的材料来降解一丁醇,发现在rGO占比为0.5 wt.%时效果最好,Qin等[19]合成了ZnO和rGO不同占比的材料并用来降解亚甲基蓝,发现rGO占比为4.06 wt.%时效果最好.但对GO在光催化方面的性质以及影响因素的单独研究还未见报道.
在本研究中,我们制作得到GO,并对其进行了表征;然后以亚甲基蓝(MB)作为实验对象,探究了不同催化剂浓度、搅拌、曝气氧气浓度和外加电流条件下GO的光催化效果,并初步分析了这些条件的作用机理.
1 实验 1.1 实验试剂与仪器鳞片石墨(500目)、硝酸钠、浓硫酸、高锰酸钾、双氧水、亚甲基蓝.所有试剂均为分析纯.
SK-G10123K开启式真空/气氛管式电炉,KPS-6005DU Single output DC power supply,商品石墨电极,鱼跃YU300家用增氧机,85-2恒温磁力搅拌器,YS-366000E20可见光型全光谱光源,波长范围为380~780 nm.
1.2 GO及其分散液的准备使用改良的Hummer法[21]制作GO.将2 g鳞片石墨和2 g硝酸钠加入100 mL浓硫酸中,0 ℃搅拌,缓慢加入12 g高锰酸钾,继续搅拌90 min,之后升温到40 ℃继续搅拌2 h,缓慢加入80 mL去离子水和10 mL质量分数为30%的双氧水,搅拌10 min后取出.
将得到的GO用去离子水洗涤,分离干燥,一部分分散于水中,得到浓度为5 mg/mL的GO水溶液,记为M-05;取一部分使用真空炉250 ℃进行2 h还原,记为M-05-250;再取一部分使用真空炉350 ℃进行2 h还原,记为M-05-350.
1.3 样品表征使用型号为Quanta_650FEG扫描电镜(SEM)、JEM-2100F (HR)透射电镜(TEM)和Nicolet-360红外光谱仪进行GO的微观形貌和成分分析.用Nikon N-SIM/STORM超分辨率荧光显微镜对M-05进行扫描,用METASH上海元析仪器UV-9000S紫外可见分光光度计对M-05、M-05-250和M-05-350进行扫描,得到UV-Vis光谱,研究材料的光学吸收特性.使用上海复享光学K-Sens-532 Raman光谱仪得到Raman光谱,对材料进行结构分析.
1.4 光催化实验通过降解MB来评估GO的光催化效率.MB溶液浓度为40 mg/L.实验开始时,在溶液中加入所需含量的催化剂,振荡混匀.将反应体系置于黑色试验箱中,保证不受外界光源的干扰,试验体系与光源的距离保持约30 cm,温度为(30±2) ℃.在试验开始时,先将体系在黑暗中静置5 min,之后光照处理,每隔一定时间振荡混匀,取出6 mL溶液,离心除去光催化剂后进行测试.用UV-9000S型分光光度计确定MB的浓度.
实验中曝气所用气体是空气,气流量为2 L/min.需要改变氧气浓度时将体系和家用保健制氧机连接,通过改变制氧机的模式来提供不同浓度和流量的氧气,分别为90%,1 L/min;50%,2 L/min;40%,3 L/min;30%,5 L/min和21%,4 L/min.通电时在石墨电极两端接入电源,调节电压使电流为15 mA,电流密度为1 mA/cm2.
2 结果与分析 2.1 氧化石墨烯的表征分析 2.1.1 扫描电子显微镜(SEM)与电子能谱(EDS)分析由图 1可以看出,鳞片石墨呈片层结构(图 1(a)),表面平滑,并堆积在一起,GO也是层状结构(图 1(b)),但片层上有典型的石墨烯褶皱和卷曲.EDS能谱分析显示在GO中,C和O的质量比约为2.3:1,氧化程度很高,表明所得GO有较多的含氧官能团.

|
图 1 GO的SEM图像(a)及鳞片石墨的SEM图像(b) Figure 1 SEM image of (a) GO, (b)flake graphit |
采用放大倍数更高的TEM分析GO的形貌.图 2显示GO片层呈薄纱状,边缘处带有褶皱,可以看出经过Hummer法处理,片层剥离情况良好.图 2(b)可以看出GO层数很少,颜色较深部位是褶皱引起的层数增加,这是热力学原因造成的,也是石墨烯材料基本结构的典型特征.

|
图 2 GO的TEM高、低倍图像 Figure 2 TEM image of GO |
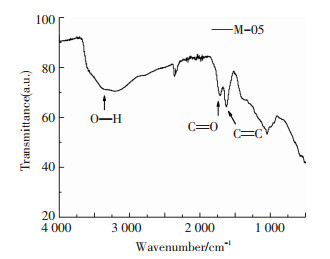
图 3是GO的FT-IR图谱,可以看出GO中含有大量的含氧基团,在3 400 cm-1附近的峰对应于羟基的不对称伸缩振动吸收,峰型较宽说明材料更多地表现出无机物特性,1 720 cm-1处为羧基中羰基的伸缩振动峰,1 620 cm-1处为未氧化的C=C的伸缩振动峰,与EDS能谱结合分析可以看出得到的GO含氧基团种类和数量都比较多.
|
图 3 GO的傅里叶变换-红外谱图 Figure 3 FT-IR spectra of GO |
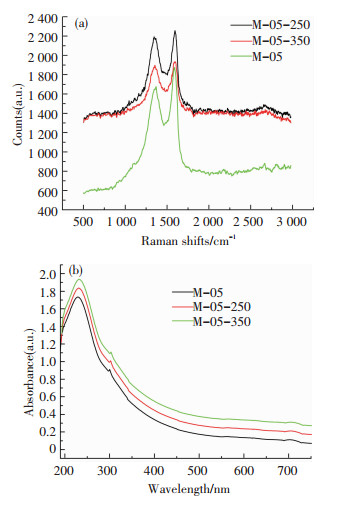
图 4(a)是材料的Raman图谱,图谱显示M-05在1 350 cm-1附近有D峰,1 583 cm-1左右的是G峰,在2 700 cm-1处有不明显的2D峰,ID/IG值约为0.875,显示其存在较多的缺陷,2D峰很小,表明所得到的GO氧化程度较高[22].经过真空炉250和350 ℃还原后,其ID/IG值上升,并与还原温度的变化方向一致,分别达到了0.973和0.980,2D峰也逐渐明显,与文献描述一致[24],这可能是含氧官能团被除去,sp2结构恢复,整体有序度增加造成的.
|
图 4 M-05、M-05-250和M-05-350的拉曼谱图(a)和紫外-可见吸收光谱(b) Figure 4 Raman(a) and UV-vis absorption spectra(b) of M-05, M-05-250&M-05-350 |
图 4(b)是样品的紫外-可见吸收光谱.229 nm处的吸收峰对应于C=C的π-π*跃迁,300纳米处的弱吸收峰对应于C=O的n-π*跃迁,这是GO的特征结构.可以看出随着还原时间的延长,π-π*逐渐红移,且对应的吸光度相对变大,这表明石墨烯的共轭电子结构逐渐得到恢复.结合拉曼光谱,可以看出所得到的GO氧化程度是较高的.
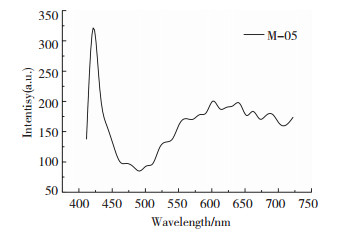
2.1.5 荧光共聚焦激发光谱分析本图谱是用405 nm波长的激光扫描受测物质,然后测量激发光的能量得到.图谱反应出该物质吸收特定波长光线获得激发态的能力.从图中看出实验得到的GO在425 nm处有一个强的发射峰,在500 nm到700 nm光波之间也有很多强度不一的发射峰,说明对这一波长光线,GO确实有吸收光子发生电子跃迁的能力.发射峰的分布说明材料是不同氧化程度的石墨烯的集合,相比单一物质,对光的利用率更高.
2.2 MB的光催化降解图 6(a)是在2 h可见光照射后MB的自降解及加入M-05-350和M-05后的光降解测试结果.
|
图 5 GO的荧光共聚焦激发图谱 Figure 5 Fluorescence confocal spectroscopy of GO |
|
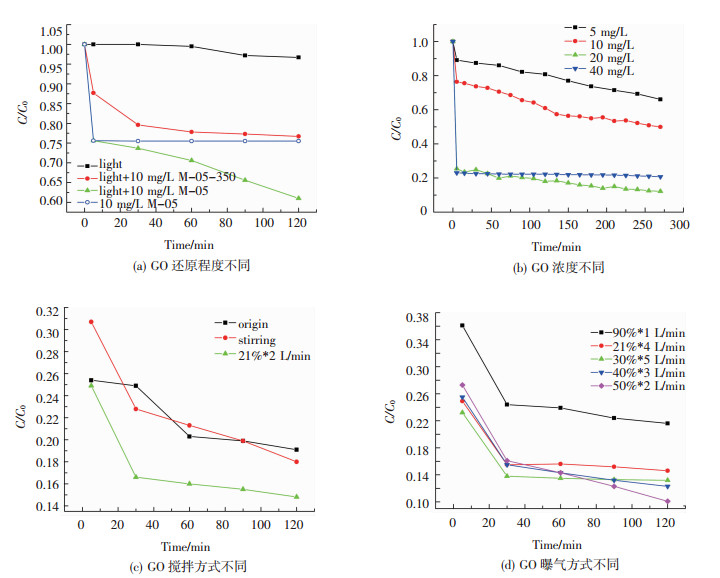
图 6 不同条件下MB的光催化降解 Figure 6 Photocatalytic degradation of MB with(a) different catalysts; (b)GO of different concentration; (c) different forms of agitator; (d)different forms of aeration |
由图 6(a)可以看出,黑暗条件下加入M-05后MB浓度在最初5 min下降了25%,之后保持不变,这是GO对MB的吸附导致的,有文献[23]表明GO对MB的吸附曲线和时间的关系是一条几乎平行于横轴的直线,即在5 min内吸附作用已经完成.当只有光照不添加催化剂时MB浓度在2 h后下降幅度约为5%,在加入GO后,这一数字达到了39%,三者对比说明GO对MB起到了光催化降解的效果.M-05-350是由M-05还原得到,含氧基团数量减少,在水中分散性较差,吸附能力弱,曲线在30 min后逐渐与横坐标轴平行,最终去除率只有22%,推测是由于GO被还原的部分不具有光催化能力.
2.3 催化剂浓度的影响在亚甲基蓝溶液中分别加入0.25、0.5、1和2 mL M-05,使溶液中GO浓度相应分别为5 mg/L(组1)、10 mg/L(组2)、20 mg/L(组3)和40 mg/L(组4),之后使用可见光源照射2小时,降解曲线如图 6(b)所示.
从图中可以看出,随着浓度的增加,GO的吸附效果的变化符合传统的吸附剂浓度效应.在5 min之后,1和2两组曲线斜率相差不大,但都大于3和4两组,并且可以看出组4的曲线在5 min后与横坐标轴基本平行,但最终结果小于组3.这是因为一方面GO浓度增大,对未吸附部分的催化降解效果变强,另一方面,结合试验时的观察可以得出,浓度的增加同样导致了溶液的透光率降低,受光面积减小,当浓度到达40 mg/L时,经历暗吸附的溶液几乎达到了不透光状态,很难实现光催化.
2.4 机械搅拌和曝气的影响目前对于ZnO和TiO2的光催化的研究通常使体系处于搅拌状态,因为搅拌能使催化剂和反应物充分接触,提高反应效率.GO不同于半导体光催化剂,在水中具有良好的分散性,因此我们探究搅拌对其光催化效果的影响.记使用磁力搅拌器的体系为组1,曝气气流量为2 L/min的体系为组2,效果如图 6(c)所示.
可以看出,磁力搅拌器的使用并没有提升降解效果,1组和对比组相差约1%,并且在30 min及以后的测量节点处,两者的数值都很接近.这是因为GO在水中具有良好的分散性,多以单层或双层的薄片存在,超大的比表面积能充分发挥其吸附能力,使催化过程接近于均相催化,搅拌不能提升降解效果.与1组相比,2组的最终去除率增长了5%,是因为曝气增加了氧气浓度[25].
2.5 曝气氧气浓度的影响图 6(c)可以说明曝气能够提升GO的催化效果,受此启发,我们研究了曝气时氧气浓度对反应的影响,结果如图 6(d)所示.
由图中可以看出,随着氧气浓度的增加,曲线斜率逐渐变大,最终去除率逐渐上升,最高达到了89.9%,但在浓度由50%提升到90%时,催化效果大幅下降.这是因为在光催化体系中,氧气可以俘获催化剂表面的光生电子生成过氧化物·O2-,一方面延缓电子-空穴对的复合,另一方面过氧化物不稳定,最终也会生成·OH,提高催化效果.但这种效果不会随着曝气流量的增加而一直提升.当溶解氧达到饱和时,受制于光生电子在界面上被氧捕获的反应速率,持续曝气对于反应速率的影响明显下降[26],并且过量过氧化物生成的H2O2会捕获体系中的·OH生成·O2H,使处理效果下降[27].另外,曝气时会形成悬浮气泡,气泡过多对于光子在溶液中的传播也有影响[28],这是氧气浓度为30%,曝气量为5L/min时,曲线几乎与横坐标轴平行的原因.
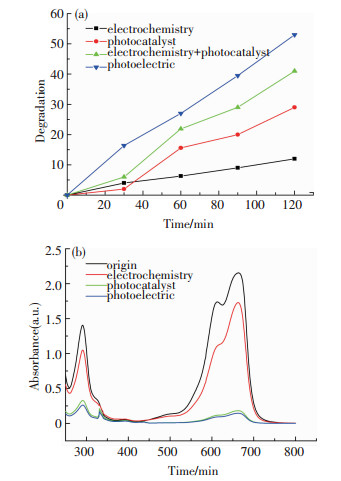
2.6 外加电流的影响作为两种重要的高级氧化技术,电催化和光催化的结合早在1993年就在污水处理领域得到了应用,并被发现具有协同作用[29].在本实验中,通过光催化、电化学催化及光电联合降解MB的比较,探究协同作用在GO的光催化过程中是否存在,结果如图 7(a)所示.
|
图 7 (a) 光催化、电化学及光电联合降解率比较; (b)光催化、电化学及光电联合降解UV-vis图谱 Figure 7 Degradation rates(a) & UV-vis spectra(b) of photocatalytic, electrochemical and photoelectric |
计算MB未被吸附部分的降解率,当外加电流密度为1 mA/cm2时,2 h后单独电化学工艺降解率仅为12.1%.相比之下,单独光催化工艺降解率较高,约为30.1%.当光催化和电化学工艺联合工作时,2 h后降解率达到了53%,大于单独光催化和单独光化学降解率的代数加和,这表明两者产生了协同增强效应,并且总的去除率也达到了87.9%.
在光催化过程中,电子迁移使电子和空穴分离,当辅以电化学工艺时,两者在电流作用下向对应电极移动,降低复合率,提高催化效果;并且电解水可以生成氧气,使溶液中溶解氧浓度提升,提高光催化效果[5].
2.7 机理分析由图 7(a)看出,在仅增加了光照的条件后,MB的降解效率提高了41%,图 7(b)是MB在电催化和光催化后的UV-Vis图谱,经过电催化和光催化降解后,吸收峰的位置基本一致,与文献所述吻合[30],结合之前的研究,可以得出GO对MB的降解是基于光催化原理.光催化技术包含氧化过程和还原过程,综合图 6和图 7来看,曝气和电化学辅助分别直接和间接地增加了溶液中溶解氧的浓度,而溶解氧是主要的光生电子俘获剂,一方面阻止了光生电子和空穴的复合,另一方面与电子结合最终也产生羟基自由基,因而可以推断GO对MB的降解是基于羟基自由基氧化原理.
3 结论用改良的Hummer法制备了氧化石墨烯,探究了不同外界条件对其光催化效果的影响,研究表明在亚甲基蓝浓度为40 mg/L时
1) 在0~20 mg/L范围内,氧化石墨烯浓度提升会使最终催化效果呈上升态势,但浓度超过20 mg/L后会使溶液透光率降低,效果下降.
2) 氧化石墨烯在水中分散性良好,更接近均相催化,搅拌不能提高催化效果.
3) 曝气能提高氧化石墨烯的催化效果,在浓度为0~50%范围内,氧气浓度提升会提高催化效果,但浓度达到90%后会抑制催化作用.
4) 电化学工艺可以和氧化石墨烯光催化产生协同效应,当外加电流密度为1 mA/cm2时,两者联合作用降解率达到了53%,高于两者单独作用的加和42.2%.
5) Hummer法制备氧化石墨烯成本较低,光催化净化污水不具有特定选择性,因而氧化石墨烯的光催化有可能应用到实际污水治理中.
| [1] | FUJISHIMA A, HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature, 1972, 238(5358): 37–38. DOI: 10.1038/238037a0 |
| [2] | PARAMESHWARI R, JOTHIVENKATACHALAM K, BANKS C E, et al. Acid-free co-operative self-assembly of graphene-ZnO nanocomposites and its defect mediated visible light photocatalytic activities[J]. Physica B Condensed Matter, 2017, 506(1): 32–41. |
| [3] | PAWAR R C, LEE C S. Single-step sensitization of reduced graphene oxide sheets and CdS nanoparticles on ZnO nanorods as visible-light photocatalysts[J]. Applied Catalysis B Environmental, 2014, 144(1): 57–65. |
| [4] | GAYA U I, ABDULLAH A H. Heterogeneous photocatalytic degradation of organic contaminants over titanium dioxide: A review of fundamentals, progress and problems[J]. Journal of Photochemistry & Photobiology C Photochemistry Reviews, 2008, 9(1): 1–12. |
| [5] |
张峰. 光催化水处理技术[M]. 北京: 化学工业出版社, 2015.
ZHANG Feng. Photocatalytic water treatment technology[M]. Beijing: Chemical Industry Press, 2015. |
| [6] | MALATO S, BLANCO J, VIDAL A, et al. Photocatalysis with solar energy at a pilot-plant scale: an overview[J]. Applied Catalysis B Environmental, 2002, 37(1): 1–15. DOI: 10.1016/S0926-3373(01)00315-0 |
| [7] |
高濂, 郑珊, 张青红. 纳米氧化钛光催化材料及应用[M]. 北京: 化学工业出版社, 2002.
GAO Lian, ZHENG Shan, ZHANG Qinghong. Nano titania photocatalytic material and its application[M]. Beijing: Chemical Industry Press, 2002. |
| [8] |
宁艳春, 蒲文晶. 纳米二氧化钛的制备及其光催化应用进展[J]. 化工环保, 2004, 24(z1): 117–119.
NING Yanchun, PU Wenjing. Preparation and photocatalytic application of nano TiO2[J]. Environmental protection of chemical industry, 2004, 24(z1): 117–119. DOI: 10.3969/j.issn.1006-1878.2004.z1.035 |
| [9] |
张琼, 贺蕴秋, 陈小刚, 等. 氧化钛/氧化石墨烯复合结构及其光催化性能[J]. 科学通报, 2010, 55(7): 620–628.
ZHANG Qiong, HE Yunqiu, CHEN Xiaogang, et al. Structure and photocatalytic properties of TiO2-Graphene oxide intercalated composite[J]. Chinese Science Bulletin, 2010, 55(7): 620–628. |
| [10] | BEURA R, THANGADURAI P. Structural, optical and photocatalytic properties of graphene-ZnO nanocomposites for varied compositions[J]. Journal of Physics & Chemistry of Solids, 2017, 102: 168–177. |
| [11] | LEI Y, CHEN F, LUO Y, ET AL. Synthesis of three-dimensional graphene oxide foam for the removal of heavy metal ions[J]. Chemical Physics Letters, 2014, 593(6): 122–127. |
| [12] | DUBEY P K, TIWARI R S, TRIPATHI P, et al. Synthesis of reduced graphene oxide-TiO2 nanoparticle composite systems and its application in hydrogen production[J]. International Journal of Hydrogen Energy, 2014, 39(29): 16282–16292. DOI: 10.1016/j.ijhydene.2014.03.104 |
| [13] |
付姚, 曹望和, 田莹. TiO2纳米薄膜电极中光生载流子传输特性研究[J]. 化学学报, 2006, 64(17): 1761–1764.
FU Yao, CAO Wanghe, TIAN Ying. Study on transport properties of photo-generated carriers in nanocrystalline TiO2 film electrode[J]. Acta Chimica Sinica, 2006, 64(17): 1761–1764. DOI: 10.3321/j.issn:0567-7351.2006.17.001 |
| [14] | LIU Z H, WANG Z M, YANG X, et al. Intercalation of organic ammonium ions into layered graphite oxide[J]. Langmuir, 2002, 18(12): 4926–4932. DOI: 10.1021/la011677i |
| [15] | YEH T F, SYU J M, CHENG C, et al. Graphite oxide as a photocatalyst for hydrogen production from water[J]. Advanced Functional Materials, 2010, 20(14): 2255–2262. DOI: 10.1002/adfm.v20:14 |
| [16] | YEH T F, CHAN F F, HSIEH C T, et al. Graphite oxide with different oxygenated levels for hydrogen and oxygen production from water under illumination: the band positions of graphite oxide[J]. Journal of Physical Chemistry C, 2011, 115(45): 22587–22597. DOI: 10.1021/jp204856c |
| [17] | LI B, LIU T, WANG Y, et al. ZnO/graphene-oxide nanocomposite with remarkably enhanced visible-light-driven photocatalytic performance[J]. Journal of Colloid & Interface Science, 2012, 377(1): 114–121. |
| [18] | MORAWSKI A W, KUSIAK-NEJMAN E, WANAG A, et al. Photocatalytic degradation of acetic acid in the presence of visible light-active TiO2 -reduced graphene oxide photocatalysts[J]. Catalysis Today, 2017, 280: 108–113. DOI: 10.1016/j.cattod.2016.05.055 |
| [19] | QIN J, ZHANG X, YANG C, et al. ZnO microspheres-reduced graphene oxide nanocomposite for photocatalytic degradation of methylene blue dye[J]. Applied Surface Science, 2016, 392: 196–203. |
| [20] | LIN L, WANG H, XU P. Immobilized TiO2 -reduced graphene oxide nanocomposites on optical fibers as high performance photocatalysts for degradation of pharmaceuticals[J]. Chemical Engineering Journal, 2017, 310: 389–398. DOI: 10.1016/j.cej.2016.04.024 |
| [21] | Jr W S H, Offeman R E. Preparation of graphitic oxide[J]. Journal of the American Chemical Society, 1958, 80(6): 1339–1339. DOI: 10.1021/ja01539a017 |
| [22] | PAWAR R C, LEE C S. Single-step sensitization of reduced graphene oxide sheets and CdS nanoparticles on ZnO nanorods as visible-light photocatalysts[J]. Applied Catalysis B Environmental, 2014, 144(1): 57–65. |
| [23] | ZHANG W, ZHOU C, ZHOU W, et al. Fast and considerable adsorption of methylene blue dye onto graphene oxide[J]. Bull Environ Contam Toxicol, 2011, 87(1): 86–90. DOI: 10.1007/s00128-011-0304-1 |
| [24] | STANKOVICH S, DIKIN D A, PINER R D, et al. Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J]. Carbon, 2007, 45(7): 1558–1565. DOI: 10.1016/j.carbon.2007.02.034 |
| [25] |
施利毅, 华彬. 二氧化钛超细粒子的制备及其光催化降解含酚溶液[J]. 华东理工大学学报, 1998, 24(3): 291–297.
SHI Liyi, HUA Bin. Photocatalytic destruction of phenol with ultrafine titania particles[J]. Journal of east China University of Science and Technology, 1998, 24(3): 291–297. |
| [26] |
武婕. 含酚废水光催化处理的环境健康风险评价研究[D]. 太原: 太原理工大学, 2005. WU Jie. An environmental health risk assessment research for photcatalytic degradation of wastewater with phenols[D]. Taiyuan: Taiyuan University of Technology, 2005. http://cdmd.cnki.com.cn/Article/CDMD-10112-2005148557.htm |
| [27] |
田园, 陈广春, 王晔. UV-Fenton光催化氧化处理高浓度邻苯二甲酸二辛酯生产废水[J]. 环境工程学报, 2007, 1(7): 71–74.
TIAN Yuan, CHEN Guangchun, WANG Ye. Treatment of high concentration dioctyl phthalate (DOP) production waste water by UV-Fenton process[J]. Chinese Journal of Environment Engineering, 2007, 1(7): 71–74. DOI: 10.3969/j.issn.1673-9108.2007.07.015 |
| [28] | CHONG M N, JIN B, CHOW C W, et al. Recent developments in photocatalytic water treatment technology: a review[J]. Water Research, 2010, 44(10): 2997–3027. DOI: 10.1016/j.watres.2010.02.039 |
| [29] | VINODGOPAL K, KAMAT P V. Enhanced rates of photocatalytic degradation of an azo dye using SnO2/TiO coupled semiconductor thin films[J]. Environmental Science & Technology, 1995, 29(3): 841–845. |
| [30] | LI B, LIU T, WANG Y, et al. ZnO/graphene-oxide nanocomposite with remarkably enhanced visible-light-driven photocatalytic performance[J]. Journal of Colloid & Interface Science, 2012, 377(1): 114–121. |
 2018, Vol. 26
2018, Vol. 26


