2. 新型陶瓷纤维与复合材料重点实验室(国防科技大学),长沙 410082
2. Key Laboratory of New Ceramic Fibers and Composites (National University of Defense Technology), Changsha 410082, China
SiO2气凝胶是一种由纳米量级颗粒相互交联形成的具有三维网络状结构的多孔材料,由于其具有密度低(~0.03 g/cm3)、孔隙率高(>90%)、比表面积高(~1 000 m2/g)和导热系数低(~0.005 W/mK)等优点,在隔热、催化剂载体、电学、声学和声阻等材料领域具有广泛的应用前景[1-2].研究表明,在一定的温度荷载下,SiO2气凝胶纤细的骨架及孔结构会发生剧烈变化,导致其隔热性能和负载能力大幅下降,其他性能也显著降低[3].故而,研究热负载条件对SiO2气凝胶组成、微观结构的影响和程序升温下材料所发生相关反应的动力学及机理,对SiO2气凝胶的组成和微观结构优化、服役条件的选择具有重要意义[4].热重分析是研究固体材料在氧化、热分解等反应过程的动力学和机理的重要手段之一,具有试样用量少、速度快,并能在测量温度范围内研究物质发生反应全过程等优点,受到广泛应用[5-6].
本文首先采用FT-IR、XPS、SEM、TEM等分析方法研究了阶梯升温下不同温度所得SiO2气凝胶的组成和形貌,进而采用热重分析中的无模式函数法,通过研究程序升温下SiO2气凝胶热重行为的变化,从微观角度对材料所发生反应的特征及相关机理进行了系统的研究.
1 实验 1.1 原材料硅酸四乙酯(TEOS,A.R.,国药集团化学试剂有限公司),无水乙醇(EtOH,A.R.,湖南汇虹试剂有限公司),硝酸(HNO3,A.R.,上海振兴化工二厂有限公司),氨水(NH4OH,A.R.,国药集团化学试剂有限公司),去离子水(自制).
1.2 材料制备采用酸—碱两步催化法制备SiO2气凝胶[7],具体过程:将正硅酸乙酯和乙醇按一定比例混合均匀,标记为A溶液;将盐酸和乙醇按一定比例混合均匀,标记为B溶液;在剧烈搅拌下,按比例将B滴加到A中,滴加速度20 mL/h,滴加完毕搅拌2 h,得到C溶液;将氨水、水和乙醇按一定比例混合均匀,标记为D溶液;在剧烈搅拌下,按一定比例将D溶液滴加到C中,滴加速度20 mL/h,滴加完毕搅拌2 h,即得到SiO2溶胶.将所得SiO2溶胶密封后,放入308 K水浴中静置使其凝胶,胶凝后在凝胶表面加入一定量的乙醇液封凝胶并老化24~48 h,以使凝胶骨架牢固.将老化好的湿凝胶转移到超临界干燥装置中,预充一定氩气,然后按室温~573 K、升温速度1 K/min、573 K保温2~4 h的制度进行超临界干燥,然后卸压,装置的压力恢复常压后关闭加热装置,冷却到室温后开釜取样,即得SiO2气凝胶.
将超临界干燥所得SiO2气凝胶在空气气氛中按照10 K/min的升温速率从室温升至目标温度(分别为673、873、1 073和1 273 K),并保温2 h,得到不同温度处理的SiO2气凝胶.
1.3 测试方法用傅里叶变换红外光谱(FT-IR,Avatar360,Nicolet)研究热处理温度对SiO2气凝胶材料中化学键的影响.操作条件:KBr压片,波长范围为4 000~400 cm-1.
采用扫描电子显微镜(SEM,JSM-6700F,Jeol)和透射电子显微镜(TEM,TEM, Philips, Tecnan F20),对不同热处理温度下所得SiO2气凝胶的微观形貌进行表征.
采用X射线光电子能谱(XPS,Thermo Scientific Escalab 250Xi光电子能谱仪),表征不同热处理温度所得SiO2气凝胶中各种化学键的定量分析,操作条件: Al Kα激发源,靶电压和靶电流分别为15 kV和10 mA.
用德国耐驰公司的STA 449C综合热分析仪研究SiO2气凝胶在程序升温下的热重行为,进而探讨其在该过程所发生的反应特征及相关机理.操作条件:空气流量50 mL/min,升温速率为5、10和15 K/min,温度变化范围为室温到1 273 K,采用热天平记录材料质量随温度的变化.
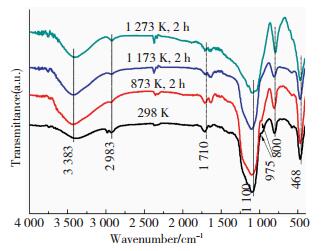
2 结果 2.1 热处理温度对SiO2气凝胶组成的影响图 1为不同温度热处理后所得SiO2气凝胶的红外光谱图.从图 1可以看出,不同温度处理后的试样在1 100、800、468 cm-1处均有吸收,这些吸收峰分别对应Si—O—Si的不对称伸缩振动、对称伸缩振动、弯曲伸缩振动吸收峰[8-9],这表明SiO2气凝胶材料主要由Si—O—Si键组成.
|
图 1 不同温度热处理后SiO2气凝胶的FT-IR谱图 Figure 1 FT-IR spectra of SiO2 aerogel treated at different temperatures |
出现在975 cm-1处的吸收峰,对应Si—OH基团的伸缩振动峰[10],随着热处理温度的升高,其强度逐渐下降,当温度高于873 K,该吸收峰消失,表明样品中的Si—OH键消失.与此同时,800 cm-1处Si—O—Si的吸收峰的强度随温度升高而增强,表明样品中Si—O—Si键的含量增多,这可能是由于气凝胶中Si—OH之间或Si—OH与Si—OC2H5发生缩合所致[11].随着热处理温度的升高,出现在1 710 cm-1处的H—O—H弯曲振动峰强度变弱,表明材料中的水分逐渐减小,这可能由于气凝胶较高的比表面积,且测试过程很难避免与空气接触,故而即使1 273 K处理的试样中仍存在微量的水[12].不同热处理的试样中,在2 893 cm-1处均存一个弱峰,该峰对应于C—H键的反对称伸缩振动吸收[13],而C—H源于未完全水解的Si—OC2H5基团,表明即使温度达到1 273 K,试样中仍存在少量的Si—OC2H5基团.
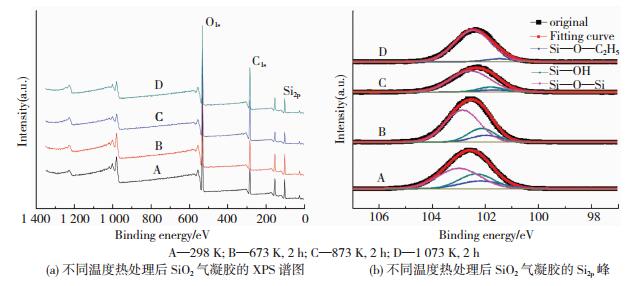
为确定热处理过程中SiO2气凝胶组成的定量变化,本文对不同温度处理所得SiO2气凝胶进行了XPS分析.图 2(a)为不同温度处理后SiO2气凝胶的XPS全谱图,图 2(b)为不同化学环境中Si2p谱峰,采用Peakfit (version 4.12)软件对Si2p峰进行分峰拟合,利用20% Gaussian-80% Lorentzian复合函数进行拟合过程的运算,并依据峰面积计算各官能团的相对含量,具体结果见表 1.
|
图 2 SiO2气凝胶的XPS谱图 Figure 2 XPS spectra of SiO2 aerogels: (a) XPS survey spectra of SiO2 aerogel treated at different temperatures; (b) Si2p spectra of SiO2 aerogels treated at different temperatures |
| 表 1 不同温度热处理后SiO2气凝胶的官能团的含量 Table 1 Quantitative XPS analysis of SiO2 aerogels treated at different temperatures |
从表 1可知,Si—O—Si键中Si2p的结合能位于103.1 eV附近[14-15],Si—OH键中Si2p的结合能位于102.3 eV附近[16],Si—OC2H5键中Si2p的结合能位于102.2 eV附近[17].随热处理温度升高,Si—O—Si键的摩尔分数从室温的50.85%增加到1 073 K时的93.40%,而Si—OH键的摩尔分数从室温的30.09%下降到873 K的12.18%,最后在1 073 K降低到0,即材料中Si—OH基团消失,这与红外结果一致.而Si—OC2H5键摩尔分数的变化趋势与Si—OH键基本一致,但热处理温度达到1 073 K时,试样中仍存在一定量的该类键(6.59%),这可能是由于Si—OC2H5键的空间位阻较大,及O—C键能较高,导致缩合反应难以进行彻底[18].
2.2 SiO2气凝胶微观形貌分析图 3是不同温度热处理后所得SiO2气凝胶材料的SEM和TEM微观形貌照片.由图 3可以看出:未处理的SiO2气凝胶具有开孔结构,主要由纳米级球状颗粒构成类线形团簇,然后以团簇为骨架,进一步构成三维网络多孔结构,颗粒大小较均匀,粒径在7~9 nm;随着热处理温度的升高,颗粒逐渐长大,部分骨架坍塌,导致材料的比表面积降低,当热处理温度达到1 273 K时,颗粒烧结长大(约50 nm),团簇彻底消失,导致气凝胶的比表面积明显下降,导热系数升高,材料基本失去负载能力[19].

|
图 3 不同温度热处理后SiO2气凝胶的SEM和TEM照片(线条代表团簇,方框代表团聚颗粒,圆圈代表孔隙) Figure 3 SEM and TEM images of SiO2 aerogels treated at different temperatures(Symbol of circle stand for pore, square for cluster and line for skeleton) |
采用非等温动力学法研究材料的反应动力学和机理,主要有模式函数法和自由模式法[20],考虑到SiO2气凝胶升温过程所发生反应的复杂性(缩合、氧化、分解等),本文采用自由模式法研究材料在该过程中活化能随其反应转化率的变化,探讨所发生反应的相关机理.自由模式法主要以Flynn-Wal-Ozawa(F-W-O)、Vyazovkin和Friedman-Reich-Levi (F-R-L)等方法为主[21],本文主要采用F-W-O法和Vyazovkin法.
F-W-O方程式:
| $ \lg {\beta _i} = \lg \left( {\frac{{A{E_\alpha }}}{{RG\left( \alpha \right)}}} \right) - 2.315 - 0.4567\frac{{{E_\alpha }}}{R}\frac{1}{{{T_{\alpha , i}}}}. $ | (1) |
Vyazovkin方程式:
| $ \ln \frac{\beta }{{T_\alpha ^2}} = \ln \left[ {\frac{{R{k_{\text{o}}}}}{{{E_\alpha }g\left( \alpha \right)}}} \right] - \frac{{{E_a}}}{R}\frac{1}{{{T_\alpha }}}. $ | (2) |
式中:β为升温速率;A和ko为指前因子;α为转化率;T为绝对温度,K;R为气体常数,J/(mol·K);G(α)和g(α)为反应模式函数的积分形式.对一个α,不同的升温速率βi对应不同的温度Tα, i(见图 3).
对式(1)而言,在α一定的情况下,以lg βi对1/Tα, i作直线,其斜率则为-0.456 7Eα·R-1,这样就可以计算出某一转化率(α)对应的活化能(Eα).对式(2)而言,在α一定的情况下,以ln(β/Tα2)对1/Tα作直线,其斜率则为-Eα·R-1,这样就可以计算出某一转化率g(α)对应的活化能(Eα′).
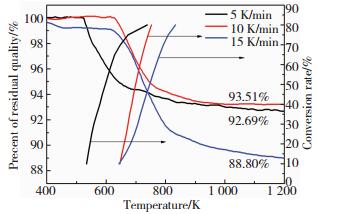
图 4为不同升温速率所得SiO2气凝胶材料的热重曲线,对其进行相应转换,可以得到α-T曲线[22].从该曲线可以获得不同升温速率(βi)时转化率(α)所对应的温度(Tα, i),将数据(βi、α、Tα, i)分别代入式(1)和(2),可得到不同转化率所对应的活化能,结果见图 5.
|
图 4 不同升温速率时SiO2气凝胶的TG和反应转化率(α)曲线 Figure 4 TG and Conversion rate (α)curves of SiO2 aerogel with different heating rates |
|
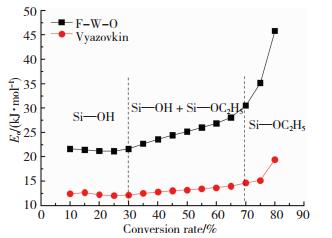
图 5 SiO2气凝胶活化能随转化率变化的关系曲线 Figure 5 Eα as a function of conversion percentage for SiO2 aerogel using the model-free methods |
从图 5可以看出,随转化率的增加,SiO2气凝胶程序升温过程所涉及反应的活化能先缓慢增加而后急速增加.Vyazovkin等对固体发生氧化、分解、缩合等反应的活化能随其转化率变化的现象研究较深入[23],称这种变化的活化能为“有效活化能”,认为当反应为单步反应时,随着转化率的增加,其有效活化能基本不变,而对复杂反应来说,其有效活化能依赖于每一基元反应在不同转化率时对繁杂反应的贡献.
结合FT-IR谱图、XPS谱图及Eα-α曲线(分别对应图 1、图 2和表 1、图 5)的结果,以及相应键能数据(H—O、C—O和Si—O的键能分别为463、358和451 kJ/mol)[24],可以看出,程序升温下,SiO2气凝胶失重过程中,有效活化能与转化率关系的变化主要由以下3种不同的化学过程所控制:
1) 当α < 30%时(低于667 K,10 K/min对应的数据,下同),这一阶段的有效活化能变化不明显且较低,主要是硅羟基(Si—OH)之间的缩合脱水[25],产物为水,该反应主要包括Si—O和O—H键的断裂,以及水的生成,由于O—H的空间位阻较小,故该阶段反应体系的有效活化能较低且变化不大.
2) 当30% < α < 70% (位于673~730 K),这一阶段的有效活化能随转化率升高缓慢增加,主要为硅羟基(Si—OH)和硅乙氧基(Si—OC2H5)之内/之间发生缩合反应[26],反应产物为水或者醇.该阶段反应主要包括Si—O—H中Si—O和O—H键的断裂、S—O—C2H5中Si—O和O—C键的断裂,以及水和醇的生成.虽然O—H的体积小,空间位阻较小,容易发生缩合,但是乙氧基(—OC2H5)的体积较大,空间位阻大,较难发生反应,从而导致本阶段的反应活化能较高,且随转化率的增加,硅乙氧基(Si—OC2H5)之间反应所占总反应的比例逐渐增加,从而导致本阶段反应的有效活化能随转化率升高缓慢增加.
3) 当α>70%时(高于730 K),这一阶段的有效活化能随着转化率升高迅速增加,主要由于Si—OH基团基本消失,反应主要由Si—OC2H5之间的缩合脱醚或与气氛中氧的氧化反应,由于Si—O—C2H5较大的空间位阻,同时颗粒长大,材料致密性增加,导致Si—OC2H5断裂后生成的Si—O键接触难度增加,较难生成Si—O—Si键,两种因素的协同作用导致该过程反应的活化能急剧上升.
图 6为不同升温速率时SiO2气凝胶的DTG曲线.从图 6可以看出,不同升温速率会出现不同的明显失重峰,对升温速度为5 K/min的曲线,其分别在518、569、591和622 K出现失重峰,其中518 K为最高失重峰;对升温速度10 K/min的曲线,其分别在642、676和737 K出现失重峰,其中676 K为最高失重峰;对升温速度为15 K/min的曲线,其分别在704和752 K出现失重峰,其中704 K为最高失重峰.

|
图 6 不同升温速率时SiO2气凝胶的DTG曲线 Figure 6 DTG curves of SiO2 aerogel with different heating rates |
这些数据表明,热负载条件下,SiO2气凝胶的热稳定性与升温速率有较大关系,升温速率越高,则气凝胶发生明显失重所对应的温度也越高,其热稳定性越好.同时也表明,程序升温下,SiO2气凝胶发生的反应较为复杂,为几个基元反应的组合,这与前期的分析结果一致.
3 结论1) 阶梯升温中,随热处理温度的升高,气凝胶中Si—O—Si键摩尔分数逐渐增加,而Si—OH键和Si—OC2H5键的逐渐降低,其中Si—OH在1 073 K基本消失;SiO2气凝胶主要由球状颗粒(7~9 nm)构成类线形团簇,然后以团簇为骨架,进一步构成三维网络多孔结构,随热处理温度的升高,颗粒逐渐长大,部分骨架坍塌,当温度达到1 273 K,颗粒长大至约50 nm,团簇彻底消失,材料发生明显烧结.
2) 程序升温法中,升温速率越高,SiO2气凝胶的热稳定性越好;气凝胶材料的失重主要由于多种反应的组合,当α < 30%时,这一阶段的有效活化能变化不明显且较低,主要是Si—OH之间的缩合,产物为水;30% < α < 70%时,这一阶段的有效活化能随着转化率的升高而缓慢增加,主要是Si—OH与/或Si—OC2H5之间发生缩合反应,反应产物为水或者醇;当α>70%时,这一阶段的有效活化能随着转化率的升高而迅速增加,主要是Si—OC2H5之间的缩合,产物为醇或醚.
| [1] |
蔡龙, 蒲群, 曲康, 等. 酸碱催化剂浓度对柔性硅气凝胶性能和结构的影响[J]. 化工学报, 2016, 67(2): 648–653.
CAI Long, PU Qun, QU Kang, et al. Effects of acid-base catalysts concentration on structures and properties of flexible silica aerogels[J]. CIESC Journal, 2016, 67(2): 648–653. |
| [2] | TANG X B, SUN A H, CHU C Y, et al. A novel silica nanowire-silica composite aerogels dried at ambient pressure[J]. Materials and Design, 2017, 115: 415–421. DOI: 10.1016/j.matdes.2016.11.080 |
| [3] | ISMAIL A A, IBRAHIM I A. Impact of supercritical drying and heat treatment on physical properties of titania/silica aerogel monolithic and its application[J]. Applied Catalysis A: General, 2008, 346: 200–205. DOI: 10.1016/j.apcata.2008.05.031 |
| [4] | ZHOU C L, YANG J, SUI X Y, et al. Impacts of structural change of SiO2 aerogel under different time and high temperature conditions on insulation performance[J]. Journal of Advanced Ceramics, 2014, 5: 11–16. |
| [5] | ZHANG Y Y, LV W, LV X W, et al. Oxidation kinetics of ilmenite concentrate by non-isothermal thermogravimetric analysis[J]. Journal of Iron and Steel Research, 2017, 24: 678–684. DOI: 10.1016/S1006-706X(17)30102-4 |
| [6] | MISHRA G, BHASKAR T. Non isothermal model free kinetics for pyrolysis of rice straw[J]. Bioresource Technology, 2014, 169: 614–621. DOI: 10.1016/j.biortech.2014.07.045 |
| [7] | DUAN Y, JANA S C, LAMA B, et al. Hydrophobic silica aerogels by silylation[J]. Journal of Non-Crystalline Solids, 2016, 437: 26–33. DOI: 10.1016/j.jnoncrysol.2016.01.016 |
| [8] | SHAO Z D, LUO F Z, CHENG X, et al. Superhydrophobic sodium silicate based silica aerogel prepared by ambient pressure drying[J]. Materials Chemistry and Physics, 2013, 141: 570–575. DOI: 10.1016/j.matchemphys.2013.05.064 |
| [9] | SAEED S, SOUBAIHI R M A, WHITE L S, et al. Rapid fabrication of cross-linked silica aerogel by laser induced gelation[J]. Microporous and Mesoporous Materials, 2016, 221: 245–252. DOI: 10.1016/j.micromeso.2015.09.012 |
| [10] | SHAHZAMAIN M, BAGHERI R, MASOOMI M. Synthesis of silica-polybutadiene hybrid aerogels: the effects of reaction conditions on physical and mechanical properties[J]. Journal of Non-Crystalline Solids, 2016, 452: 325–335. DOI: 10.1016/j.jnoncrysol.2016.08.031 |
| [11] | 高庆福.纳米多孔SiO2、Al2O3气凝胶及其高效隔热复合材料研究[D].长沙: 国防科学技术大学, 2009. http://cdmd.cnki.com.cn/Article/CDMD-90002-2010147316.htm |
| [12] | HUANG D M, GUO C N, ZHANG M Z, et al. Characteristics of nanoporous silica aerogel under high temperature form 950 ℃ to 1 200 ℃[J]. Materials & Design, 2017, 129: 82–90. |
| [13] | GARCIA-TORRES B A, AGUILAR-ELGUEZABAL A, ROMAN-AGUIRRE M, et al. Synthesis of silica aerogels microspheres prepared by ink jet printing and dried at ambient pressure without surface hydrophobization[J]. Materials Chemistry and Physics, 2016, 172: 32–38. DOI: 10.1016/j.matchemphys.2015.12.047 |
| [14] | NOCUN M, CHOLEWA-KOWALSKA K, LACZKA M. Structure of hybrids based on TEOS-cyclic forms of siloxane system[J]. Journal of Molecular Structure, 2009, 938: 24–28. DOI: 10.1016/j.molstruc.2009.08.034 |
| [15] | WANG H K, WU Q Z, CAO D X, et al. Synthesis of SnSb-embedded carbon-silica fibers via electrospinning: effect of TEOS on structural evolutions and electrochemical properties[J]. Materials Today Energy, 2016, 1-2: 24–32. DOI: 10.1016/j.mtener.2016.11.003 |
| [16] | GOSTYNSKI R, FRASER R, LANDMAN M, et al. Synthesis and XPS characterization of Si-supported chromium (o) Fischer aminocarbene complexes[J]. Journal of Organometallic Chemistry, 2017, 836-837: 62–67. DOI: 10.1016/j.jorganchem.2017.03.001 |
| [17] | HE S, SUN G X, CHENG X D, et al. Nanoporous SiO2 grafted aramid fiber with low thermal conductivity[J]. Composited Science and Technology, 2017, 146: 91–98. DOI: 10.1016/j.compscitech.2017.04.021 |
| [18] | 曾昭琼. 无机化学[M]. 北京: 高等教育出版社, 2004. |
| [19] | DAN D, ZHANG H, TAO W Q. Effective structure of aerogels and decomposed contributions of its thermal conductivity[J]. Applied Thermal Engineering, 2014, 72(1): 2–9. DOI: 10.1016/j.applthermaleng.2014.02.052 |
| [20] | ZHANG C, BINIENDA W K, ZENG L M, et al. Kinetic study of the novolac resin curing process using model fitting and model-free methods[J]. Thermochimica Acta, 2011, 523: 63–69. DOI: 10.1016/j.tca.2011.04.033 |
| [21] | CEPELIOGULLAR O, HAYKIRI-ACMA H, YAMAN S. Kinetic modelling of RDF pyrolysis: Model-fitting and model-free approaches[J]. Waste Management, 2016, 48: 275–284. DOI: 10.1016/j.wasman.2015.11.027 |
| [22] | GAO P Z, GUO W M, XIAO H N, et al. Model-free kinetics applied to the oxidation properties and mechanism of three-dimension carbon/carbon composite[J]. Materials Science and Engineering A, 2006, 432: 226–230. DOI: 10.1016/j.msea.2006.06.005 |
| [23] | VYAZOVKIN S, WIGHT C A. Model-free and model-fitting approaches to kinetic analysis of isothermal and nonisothermal data[J]. Thermochimica Acta, 1999, 340-341: 53–68. DOI: 10.1016/S0040-6031(99)00253-1 |
| [24] | 唐宗薰. 无机化学热力学[M]. 北京: 科学出版社, 2010. |
| [25] | ZHI L, CHENG X D, SHI L, et al. Flammability and oxidation kinetics of hydrophobic silica aerogels[J]. Journal of Hazardous Materials, 2016, 320: 350–358. DOI: 10.1016/j.jhazmat.2016.07.054 |
| [26] |
师春晓, 张寿春, 姜勇刚, 等. 氧化硅气凝胶的高温性能[J]. 稀有金属材料与工程, 2016, 45(Suppl): 210–213.
SHI Chunxiao, ZHANG Shouchun, JIANG Yonggang, et al. High temperature properties of silica aerogel[J]. Rare Metal Materials and Engineering, 2016, 45(Suppl): 210–213. |
 2018, Vol. 26
2018, Vol. 26


