2. 井冈山大学 化学化工学院,江西 吉安 343009;
3. 井冈山大学 建筑工程学院,江西 吉安 343009
2. School of Chemistry & Chemical Engineering, Jinggangshan University, Ji′an 343009, China;
3. School of Building Engineering, Jinggangshan University, Ji′an 343009, China
尖晶石型锰酸锂具有资源丰富、能量密度高、成本低、无污染、安全性好等优点,被认为是锂离子动力电池理想的正极材料[1-3].由于Jahn-Teller效应和歧化反应造成锰离子的溶解,之后锰离子迁移并沉积到负极上[4-5],造成了LiMn2O4系锂离子电池容量衰减[6-8],特别是在高温下衰减更加剧烈[9-10],严重制约其在动力电池领域的大规模应用.抑制锰溶解是克服锰酸锂系锂电池容量衰减的关键技术之一[1-2].
锰酸锂电池的锰溶解有3个基本过程[4-5, 11]:1)在锂离子电池中,电解质LiPF6发生分解,生成PF5,LiPF6↔LiF(s)+PF5;2)PF5与痕量水生成腐蚀性HF酸,PF5+H2O→POF3+2HF,POF3+3H2O→H3PO4+3HF;3)HF酸与锰酸锂发生歧化反应, 2LiMn2O4+4HF=3MnO2+MnF2+2H2O,MnO2不溶解而留在电极上,MnF2溶解在电解液中.
因此,有2类基本方法抑制锰溶解:1)抑制HF的生成.发现某些添加剂[12-17],如用聚合物电解质替代LiPF6,添加LiBOB、LiBSF等,能在一定程度上抑制HF、H2O的生成.2)对正极材料进行改性[18-21],提高LiMn2O4材料本身的抗HF的能力.
随着温度升高,反应活化能增加,电解质就难免分解生成HF酸,因此材料科学家们更加关注对正极材料进行改性.改性方法有:1)“整体掺杂法”,部分锰离子被阳离子替代后,形成更强的M—O键,但仍保持尖晶石结构(LiMxMn2-xO4,M=Li,Co,Mg,N,Al,Zn),使得平均价态维持在3.5以上,抑制J-Teller效应,改善结构稳定性[18-21].2)“表面包覆法”,在尖晶石表面涂覆一层薄的金属氧化物涂层(SnO2、Co3O4、Al2O3、ZnO、MgO、SiO2)[20-23],防止电解液与LiMn2O4之间的直接接触,抑制电解液在电极界面上发生反应,提高锰酸锂抵抗电解液中HF酸的电化学腐蚀.研究表明,用Al3+、Ti4+等部分替代Mn离子可稳定晶体结构[20, 22, 24],用Ni2+、Co2+等作为掺杂剂可改善锂电池的循环性能[18].但由于Al3+或Ti4+等掺杂离子不具有电化学活性,随着掺量的增加,电池能量密度必定下降;而Ni2+、Co2+等阳离子则具有高化学活性,则可能导致LiMn2O4的安全问题.“表面包覆法”也可能存在一些问题:金属氧化物包覆层与活性尖晶石型LiMn2O4材料之间的异质结构,很容易造成电池循环过程中的相偏析或分离,从而影响LiMn2O4系锂离子电池的电化学性能.
在所有掺杂、包覆材料中,TiO2由于热稳定、结构稳定性能良好,离子能快速进出等特性,受到了广泛关注[24-25].相比TiO2多晶整体掺杂,表面纳米TiO2修饰则有更多的通道,锂离子更容易进出到宿主材料晶体结构中,因此最近成为一种颇受关注的方法[25].使用原子层沉积技术,可制备纳米级二氧化钛和氧化铝的原子层沉积层,该超薄致密包覆层可以减少锰溶解,减缓容量衰减,但该技术成本高、生产率低,主要用于基础研究[26].采用低成本、大规模生成的简便方法来制备超薄覆盖层,具有十分重要的现实意义.虽然近年来对各种类型的金属氧化物涂层及其工艺过程进行了探讨,但阐明包覆层作用的直接证据却很少,缺乏锰酸锂正极材料包覆前后在高温电解液中溶解对比的验证性试验数据.在以往的研究报道中,大多数研究只演示了表面覆盖前后的正极材料,与锂金属组成半电池的电化学循环性能变化,而开展全电池的高温电化学循环性能变化的研究却少见.
基于此,本文提出对尖晶石锰酸锂进行表面掺杂二氧化钛的思路:将包覆后材料经过高温长时间煅烧,使得金属钛离子能扩散到锰酸锂颗粒材料表层中,形成LiTixMn2-xO4尖晶石结构层,既维持了表面晶体结构稳定,又利用表面层钛离子抵抗氢氟酸腐蚀,以抑制锰酸锂材料高温下的锰溶解,提高电化学循环性能的思路.本文将通过锰酸锂正极化成后,在高温电解液进行溶解对比性试验,给出包覆层作用的直接证据,并进行全电池高温环境下电化学循环性能的对比测试.
1 实验 1.1 原料与制备 1.1.1 尖晶石LiMn2O4的合成以MnCO3和Li2CO3为原料,按照n(Mn):n(Li)=2.00:1.05分别称取相应质量的反应物, 充分混合后倒入球磨罐中,加入1/3容量的乙醇作为分散剂,并以500 r/min的转速湿法球磨18 h.将球磨后的产物烘干装入坩埚中,并将坩埚放入马弗炉内,均匀升温3 h后达到预设试验温度750 ℃,并保温10 h.停炉后,样品随炉自然冷却至室温,研磨分散后得到产物尖晶石LiMn2O4.
1.1.2 TiO2表面掺杂采用溶胶-凝胶法制备TiO2水溶胶:C16H36O4Ti首先溶解在乙醇中,形成质量分数20%C16H36O4Ti溶液;然后将溶液缓慢滴入醋酸溶液中,醋酸组成为质量分数10%乙酸、质量分数50%乙醇和质量分数40%水,搅拌15 min后得到溶胶;进一步加入乙醇稀释得到至质量分数5%C16H36O4Ti溶液.采用溶胶-凝胶法,对尖晶石锰酸锂进行二氧化钛表面包覆.将制备的尖晶石LiMn2O4粉末加入到TiO2水溶胶中,磁力搅拌20 min后,置于80 ℃电热鼓风干燥箱中干燥3 h.将干燥后的样品置于马弗炉内,并于750 ℃煅烧6 h,得到表面具有LiMn2-xTixO4掺杂薄层的尖晶石锰酸锂正极材料.
1.1.3 电池的组装将掺杂前后获得的样品作为正极材料,全电池以石墨作为负极,半电池则以金属锂片作为负极,并参照文献[18]制备纽扣电池,整个电池的组装在充满氩气的手套箱中进行.
1.2 样品测试与表征 1.2.1 SEM/EDS分析采用场发射环境扫描电镜(SEM)观察掺杂前后尖晶石LiMn2O4正极材料形貌,并采用能谱分析(EDS)同步测试各样品相应的表面元素,分别选取SEM形貌中3个特征位置进行能谱分析,取其平均值作为最终表面元素的含量.
将组装后的半电池在55 ℃环境下10 C充放电200次后,拆解电池,用碳酸二甲酯(DMC)浸泡电极除去残余的电解液,真空烘干后放入SEM/EDS中,测量正极片表面元素及其含量.
1.2.2 XRD分析采用X射线衍射仪(D/MAX 2550VB3/PC*)对样品进行物相分析.Cu靶Kα辐射,石墨单色滤波器,λ=0.154 18,电压为40 kV,扫描范围为10°~90°,扫描步长为0.02 (°)/s.
1.2.3 ICP-AES分析待掺杂包覆前后的正极组装成纽扣电池,化成形成稳定的SEI膜后,将各自正极片浸泡在55 ℃的锂电池通用电解液中浸泡,采用OPTIMA 3300DV型电感耦合等离子体原子发射仪(ICP-AES)分别测试浸泡不同时间后电解液中的锰离子浓度.
2 结果与讨论 2.1 尖晶石LiMn2O4形貌图 1为掺杂包覆前后尖晶石LiMn2O4的SEM形貌.由图 1(a)可知,经过球磨并高温固化后已生成了典型的尖晶石六面体相结构.这主要是由于在球磨过程中,2种粉末MnCO3和Li2CO3不断地相互摩擦并与球磨罐壁碰撞,使之产生塑性变形而形成若干大小不一的薄片状.随着球磨时间的延长,塑性变形后的粉末由于冷作硬化又导致其碎化,并在球磨罐内被搅拌得更加均匀,粉末颗粒的粒度进一步减小,2种粉体之间接触的面积更大,高温固化反应更加充分.将该产物进行TiO2表面掺杂包覆,其形貌如图 1(b)所示.由图 1(b)可发现,包覆TiO2后的样品颗粒形貌完整地保存了原有的尖晶石相,没有出现偏析和分离的现象,可见,TiO2掺杂包覆工艺过程并没有改变样品的结构,此种方法是可行的.

|
图 1 尖晶石LiMn2O4的SEM形貌 Fig.1 SEM and coated with TiO2 morphology of spinel LiMn2O4 before (a) and (b) doped |
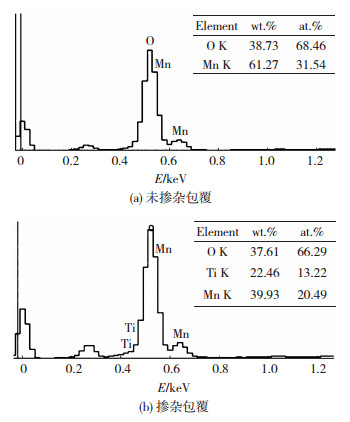
将TiO2掺杂包覆前后获得的尖晶石LiMn2O4材料进行能谱分析,得出各样品的表面元素,如图 2所示.
|
图 2 TiO2掺杂包覆前后尖晶石LiMn2O4表面元素分析 Fig.2 EDS surface elements analysis of spinel LiMn2O4: before (a) and (b) doped and coated with TiO2 |
因Li元素在EDS设备中不能产生特征X射线,图 2无法探测出Li元素及其含量,但分析得到了材料表面的、Mn、Ti元素.图 2(a)中,未掺杂包覆的样品表面的O和Mn的原子个数比为2:1,完全符合LiMn2O4结构,说明MnCO3和Li2CO3粉末经球磨和高温固化后得到了比较完整的尖晶石LiMn2O4相,这与图 1(a)形貌观察相吻合.经过TiO2包覆后(图 2(b)), 除原有的O、Mn元素,还有Ti元素的存在;而且,Ti元素的加入改变了O和Mn元素的原子比,O元素含量变化不大,但Mn元素原子含量明显下降.由此可见,TiO2成功地掺杂包覆到尖晶石LiMn2O4的表面,并形成了与LiMn2O4结构类似的LiMn2-xTixO4表面掺杂层.
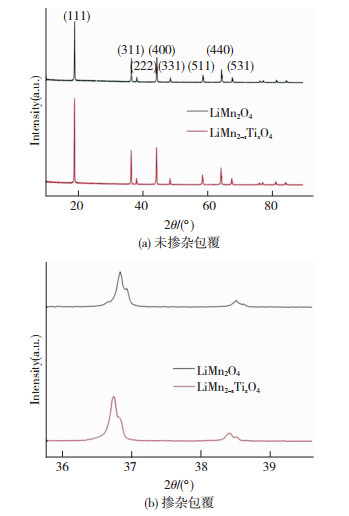
2.3 XRD衍射分析为进一步表征TiO2表面掺杂包覆尖晶石LiMn2O4结构的变化,将掺杂前后的样品进行XRD衍射分析,如图 3所示.
|
图 3 TiO2掺杂包覆前后尖晶石LiMn2O4 的XRD衍射谱图 Fig.3 XRD analysisof spinel LiMn2O4 before (a) and after (b) doped-coated with TiO2 |
2种样品都出现了尖晶石锰酸锂典型的晶面(111)、(311)及(400)等,与锰酸锂的标准谱图相吻合[19],说明合成的锰酸锂材料具有很规整的结构;而且,掺杂包覆后形成的LiMn2-xTixO4与原材料LiMn2O4 的特征衍射线一致,进一步说明TiO2掺杂包覆工艺并没有改变原材料的结构,保持了掺杂层具有较多的离子和电荷的传输通道,这与前面的分析结果是一致的.但是,TiO2掺杂包覆并非对原材料没有丝毫影响,从放大谱图(图 3(b))可以观察到:表面掺杂样品的衍射峰位置比之未掺杂的左移,表明了晶格伸长,说明了晶胞中部分Mn4+被原子半径稍大的Ti4+替代;未进行包覆的LiMn2O4 各衍射峰峰明显尖锐,而包覆TiO2后,衍射峰稍有宽化,这是由于原子半径稍大的Ti4+扩散到了锰酸锂表面微区的晶格中,导致了晶格有些畸变.
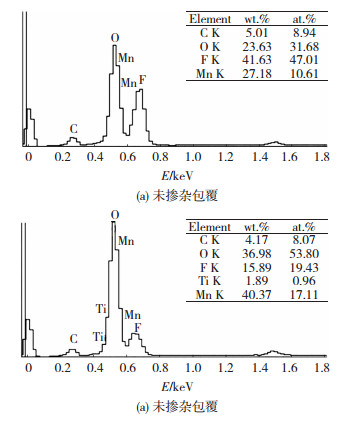
2.4 循环后正极片EDS分析将包覆前后的2种材料组装成电池,为探测循环后正极片的稳定性,将55 ℃、10 C充放电循环200次后半电池的正极片进行EDS表面元素分析,除含有少量的微量元素P、Al外,主要的元素及其含量如图 4所示.
|
图 4 充放电循环后EDS分析 Fig.4 EDS surface elements analysis of spinel LiMn2O4 after charging and discharging circulation before (a) and after (b) doped and coated with TiO2 |
由图 4(b)可知,经TiO2表面掺杂包覆后的正极材料组成的原电池,虽然经过长时间的大电流放电循环,在其表面仍可发现Ti元素的存在,说明包覆的Ti元素在此种环境下具有高度的稳定性.F元素(电解液中含六氟磷酸锂)是表征SEI膜含量的重要标志,F含量越少,SEI膜越稳定.对比图 4(a)和(b)可发现,掺杂包覆样品的F元素含量远远低于未掺杂包覆样品,而且Mn元素含量高于未掺杂包覆样品,这说明TiO2表面掺杂包覆抑制了Mn的溶解,提高了电池SEI膜的稳定性.
2.5 高温电解液中锰溶解为表征TiO2表面掺杂后电池的抗电解液腐蚀能力,将2种化成后的锰酸锂正极浸泡在55 ℃下的电解液中一段时间,分别测浸泡不同时间后电解液中锰离子的质量浓度,其值如图 5所示.由图 5可知:浸泡初期,2种锰酸锂正极溶于电解液中的锰含量均较少;随着浸泡时间的延长,未表面掺杂TiO2的样品LiMn2O4正极在电解液中的Mn质量浓度远远高于表面掺杂后的样品LiMn2-xTixO4;在电解液中浸泡12 d后,未包覆的样品LiMn2O4正极溶于电解液中的锰含量约为LiMn2-xTixO4的3倍.可见,TiO2掺杂包覆形成的LiMn2-xTixO4表面层能够保护锰酸锂抵抗电解液腐蚀,有效抑制了高温环境下锰离子的溶解,提高正极结构稳定性.这与循环后正极材料EDS分析结果是吻合的.这将为开发锰酸锂电极的高容量、高安全性、高稳定性和高电荷传输性能提供参考.

|
图 5 55 ℃下电解液锰离子质量浓度与浸泡时间的关系 Fig.5 The relation of Mn ion in the electrolyte and soaking time at 55 ℃ |
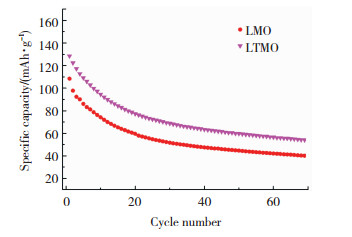
2种材料与石墨组成全电池,在55 ℃环境下0.1 C充放电循环,其放电容量对比如图 6所示.
|
图 6 2种材料全电池55 ℃环境下的放电容量对比 Fig.6 Comparison of discharge capacity of the two materials full cell at 55 ℃ |
70次循环后,LMO的放电容量为40 mAh/g,而LTMO的放电容量为53 mAh/g,比LMO的高出35%.2种材料的全电池容量衰减都比较快,与半电池明显有些不同,但其衰减规律与半电池测试相吻合:包覆后的材料高温电化学循环性能明显优于未包覆材料.
3 结论1) 将2种反应物MnCO3和Li2CO3混合后,以500 r/min的转速湿法球磨18 h,然后在高温固化可得到具有典型结果的尖晶石LiMn2O4原材料.
2) 采用凝胶-溶胶法,将TiO2涂在锰酸锂颗粒表面上后,经过750 ℃煅烧6 h后,成功实现了TiO2表面掺杂包覆尖晶石LiMn2O4材料,Ti元素的加入改变了O和Mn元素的原子个数比,并在表面获得了与其结构类似的纳米级LiMn2-xTixO4结构薄层.
3) TiO2表面掺杂工艺能够显著提高LiMn2O4的电化学性能,保护锰酸锂抵抗电解液的腐蚀,抑制高温环境下锰离子的溶解,提高SEI膜的稳定性,提高锰酸锂系锂电池的使用寿命和高温性能.
| [1] |
ZHAN Chun, LU Jun, JEREMY K A, et al. Mn(Ⅱ) deposition on anodes and its effects on capacity fade in spinel lithium manganate-carbon systems[J]. Nat Commun, 2013, 4: 2437-2445. DOI:10.1038/ncomms3437 |
| [2] |
LU Jun, ZHAN Chun, WU Tianpin, et al. Effectively suppressing dissolution of manganese from spinel lithium manganate via a nanoscale surface-doping approach[J]. Nat Commun, 2014, 5: 5693-5701. DOI:10.1038/ncomms6693 |
| [3] |
LEE H R, SEO H R, LEE B, et al. Spinel-structured surface layers for facile Li ion transport and improved chemical stability of lithium-manganese-oxide spinel[J]. Applied Surface Science, 2017, 392(15): 448-455. |
| [4] |
XIAO Xingcheng, LIU Zhongyi, BAGGETTO L, et al. Unraveling manganese dissolution deposition mechanisms on the negative electrode in lithium ion batteries[J]. Phys Chem Chem Phys, 2014, 16(22): 10398-10402. DOI:10.1039/c4cp00833b |
| [5] |
SHIN H, PARK J, SASTRY A M, et al. Degradation of the solid electrolyte interphase induced by the deposition of manganese ions[J]. Journal of Power Sources, 2015, 284: 416-427. DOI:10.1016/j.jpowsour.2015.03.039 |
| [6] |
陈海辉, 邱新平. 尖晶石锰酸锂电池容量衰减的机理探析[J]. 井冈山大学学报(自然科学版), 2015, 36(4): 34-42. CHEN Haihui, QIU Xinping. Mechanism analysis on capacity fading of spinel lithium manganese oxide cell[J]. Journal of Jianggangshan University (Natural Science), 2015, 36(4): 34-42. DOI:10.3969/j.issn.1674-8085.2015.04.007 |
| [7] |
CHEN Haihui, MA Tianyi, ZENG Yingying, et al. Mechanism of capacity fading caused by Mn (Ⅱ) deposition on anodes for spinel lithium manganese oxide cell[J]. Journal of Wuhan University of Technology-Mater Sci Ed, 2017, 32(1): 1-10. DOI:10.1007/s11595-017-1547-4 |
| [8] |
QIAO Ruimin, WANG Yuesheng, OLALDE-VELASCO P, et al. Direct evidence of gradient Mn(Ⅱ) evolution at charged states in LiNi0.5Mn1.5O4 electrodes with capacity fading[J]. Journal of Power Sources, 2015, 273: 1120-1126. DOI:10.1016/j.jpowsour.2014.10.013 |
| [9] |
WALDMANN T, WILKA M, KASPER M, et al. Temperature dependent ageing mechanisms in Lithium-ion batteries[J]. Journal of Power Sources, 2014, 262(4): 129-135. |
| [10] |
CHOU Weiyu, JIN Yichun, DU Jenqgong, et al. A facile approach to derive binder protective film on high voltagespinel cathode materials against high temperature degradation[J]. Applied Surface Science, 2015, 355: 1272-1278. DOI:10.1016/j.apsusc.2015.08.046 |
| [11] |
SAULNIER M, AUCLAIR A, LIANG G, et al. Manganese dissolution in lithium-ion positive electrode materials[J]. Solid State Ionics, 2016, 294: 1-5. DOI:10.1016/j.ssi.2016.06.007 |
| [12] |
MANCINI M, BEKAERT E, DIEMANT T, et al. Study on the stability of Li2MnSiO4 cathode material in different electrolyte systems for Li-ion batteries[J]. Electrochimica Acta, 2015, 176: 679-688. DOI:10.1016/j.electacta.2015.07.015 |
| [13] |
XU Jingjing, XIA Qingbo, CHEN Fangyuan, et al. Facilely solving cathode/electrolyte interfacial issue for high-voltage lithium ion batteries by constructing an effective solid electrolyte interface film[J]. Electrochimica Acta, 2016, 191: 687-694. DOI:10.1016/j.electacta.2016.01.138 |
| [14] |
KIM S, KIM M, CHOI I, et al. Quercetin as electrolyte additive for LiNi0.5Mn1.5O4 cathode for lithium-ion secondary battery at elevated temperature[J]. Journal of Power Sources, 2016, 336: 316-324. DOI:10.1016/j.jpowsour.2016.10.079 |
| [15] |
WANG Renheng, LI Xinhai, WANG Zhixing, et al. Comparative study of lithium bis(oxalato)borate and lithium bis(fluorosulfonyl)imide on lithium manganese oxide spinel lithium-ion batteries[J]. Journal of Alloys and Compounds, 2015, 624: 74-84. DOI:10.1016/j.jallcom.2014.11.098 |
| [16] |
HU Pu, DUAN Yulong, HU Deping, et al. Rigid-flexible coupling high ionic conductivity polymer electrolyte for an enhanced performance of LiMn2O4/graphite battery at elevated temperature[J]. ACS Appl Mater Interfaces, 2015, 7: 4720-4727. DOI:10.1021/am5083683 |
| [17] |
WANG Renheng, LI Xinhai, WANG Zhixing, et al. Manganese dissolution from LiMn2O4 cathodes at elevated temperature: methylene methanedisulfonate as electrolyte additive[J]. J Solid State Electrochem, 2016, 20: 19-28. DOI:10.1007/s10008-015-2998-1 |
| [18] |
YI Tingfeng, MEI Jie, ZHU Yanrong. Key strategies for enhancing the cycling stability and capacity of LiNi0.5Mn1.5O4 as high-voltage cathode materials for high power lithium-ion batteries[J]. Journal of Power Sources, 2016, 316(1): 85-105. |
| [19] |
TRON A, PARK Y D, MUN J. AlF3-coated LiMn2O4 as cathode material for aqueous rechargeable lithium battery with improved cycling stability[J]. Journal of Power Sources, 2016, 325(1): 360-364. |
| [20] |
WALLER G H, BROOKE P D, RAINWATER B H, et al. Structure and surface chemistry of Al2O3 coated LiMn2O4 nanostructured electrodes with improved lifetime[J]. Journal of Power Sources, 2016, 306(29): 162-170. |
| [21] |
FENG Xiaoyu, ZHANG Jianxin, YIN Longwei. Enhanced cycling stability of Co3(PO4)2-coated LiMn2O4 cathode materials for lithium ion batteries[J]. Powder Technology, 2016, 287: 77-81. DOI:10.1016/j.powtec.2015.09.031 |
| [22] |
LAI Feiyan, ZHANG Xiaohui, WANG Hongqiang, et al. Three-dimension hierarchical Al2O3 nanosheets wrapped LiMn2O4 with enhanced cycling stability as cathode material for lithium ion batteries[J]. ACS Appl Mater Interfaces, 2016, 8: 21656-21665. DOI:10.1021/acsami.6b05640 |
| [23] |
LUO Zhimei, SUN Yanguang, LIU Huiyong. Electrochemical performance of a nano SnO2-modified LiNi1/3Co1/3Mn1/3O2 cathode material[J]. Chinese Chemical Letters, 2015, 26(11): 1403-1408. DOI:10.1016/j.cclet.2015.06.007 |
| [24] |
ZHANG Zhongru, GONG Zhengliang, YANG Yong. Electrochemical performance and surface properties of bare and TiO2-coated cathode materials in lithium-ion batteries[J]. J Phys Chem B, 2004, 108: 17546-17552. DOI:10.1021/jp046980h |
| [25] |
SHANG Yesheng, LIN Xiujing, LU Xu, et al. Nano-TiO2 (B) coated LiMn2O4 as cathode materials for lithium-ion batteries at elevated temperatures[J]. Electrochimica Acta, 2015, 156: 121-126. DOI:10.1016/j.electacta.2015.01.024 |
| [26] |
LEE S, YOON G, JEONG M, et al. Hierarchical surface atomic structure of a manganese-based spinel cathode for lithium-ion batteries[J]. Angew Chem Int Ed, 2015, 54(4): 1153-1158. DOI:10.1002/anie.201408853 |
 2019, Vol. 27
2019, Vol. 27


