非晶态合金,是一类具有原子短程有序、长程无序结构特点的新型材料,在三维空间呈无序拓扑状态排列,由有序结构的原子簇混乱堆积而成,属于热力学上的亚稳态。自Smith[1]首先报道了非晶态合金催化剂的制备及应用以来,国内外催化界和材料界对非晶态合金材料展开了广泛的研究,其中关于镍系非晶态合金的研究尤为活跃[2-5]。
镍系非晶态合金的制备方法主要有骤冷法[1, 6]、化学还原法[7]和化学镀法等[8]。骤冷法制备的镍系非晶态合金具有较高的配位不饱和性和活性位,但该法制备条件苛刻,使用前需经严格复杂的活化处理,催化剂比表面积小,限制了其在工业上的发展;随后出现的化学还原法,虽然解决了骤冷法的不足,但因其活性组分分布不均匀、易团聚,因此,在应用上造成了一些不便;而化学镀法可在一定程度上克服骤冷法、化学还原法的分布不均,易团聚等缺点,适宜工业生产,使其在镍系非晶态材料的制备及应用中备受关注。化学镀法也称无电解镀或自催化镀,是在无外加电流的情况下借助合适的还原剂,使镀液中金属离子还原成金属,并沉积到基体表面的一种镀覆方法。化学镀法制备的镍系非晶态合金催化剂因具有高分散性及高催化活性而被广泛用于不饱和化合物的加氢[9-10]、硼氢化物水解[11]和燃料电池中的电催化氧化[12]等方面。此外,化学镀法制备的镍系合金镀层材料空隙少、镀层致密,能有效密封基体材料而具有优异的耐腐蚀性、耐磨性,因而在表面工程技术中也引起关注。近年来,研究者通过向化学镀液中加入固体颗粒(如氧化物、碳化物、功能陶瓷等)可得到功能性涂层[13-14],从而进一步改善镀层结构和性能,使化学镀法在表面技术中更具优势。
本文对化学镀法的原理及特性进行了阐述,并综述了化学镀镍材料在催化、表面技术等方面的研究应用以及镀液的净化与利用,最后对化学镀法制备的镍系非晶态合金材料的发展进行了展望。
1 化学镀法的原理及其特性化学镀Ni类型丰富,应用广泛。使用不同的还原剂,可以获得不同的镀层成分。如以次磷酸钠为还原剂,可以制备Ni-P,以硼氢化钾为还原剂,则可以得到Ni-B。目前,化学镀法通常以金属诱导镀液分解,在温和条件下制备出性能良好的材料。首先在基材上用Ag、Au、Pd或Pt等金属对基底活化[15-16],使基底表面生成一层具有催化活性的金属粒子作为成核晶种,镀液中含有的还原剂在基底的表面发生还原反应,并通过沉积物本身的吸附作用继续均匀沉积在基底表面上镀覆金属膜。诸多研究人员对Ni的化学镀过程进行研究,并总结出可能的途径或机理。
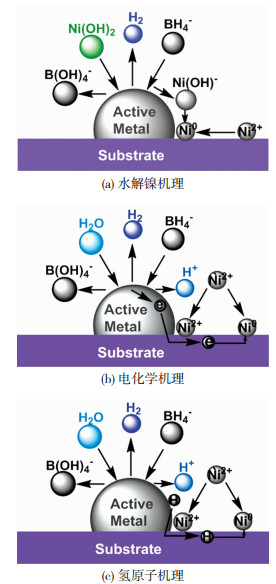
Gorbunova[17]和Mallory等[18]总结前人研究后,得到了Ni-B形成过程的3种可能的机理,用于描述化学镀镍连续沉积生成新核的可能途径,如图 1所示,3种机理可简要描述如下。
|
图 1 载体上的化学镀镍机理[16] Fig.1 Mechanism of nickel deposition on substrates (a) hydrolyzed nickel mechanism; (b) electrochemical mechanism; (c) hydrogen atom mechanism[16] |
1) 水解Ni机理。形成的新核与Ag分离,扩散到镀液中,同时,镍单质可能通过镀液中的电子或H原子还原镍离子而形成。并被载体吸附沉积到基底表面以作为镍沉积的新活性位点。
2) 电化学机理。一些新的催化位点可能是通过电化学机理在基底上用电子还原镍离子而产生的,然而由电子还原的新原子核仅发生在基底上的某些位置,并随着电子在化学镀过程中高度分散,原子核均匀分布。
3))氢原子机理。新的催化核被硼氢化物分解的氢原子还原,当银上发生氢溢流时,新原子核应位于原始原子核(活性金属)附近。这些途径与载体和镀液或活性金属和镀液之间的界面反应的相互作用有关,因此,载体的吸附能力与负载能力有很大的关系。
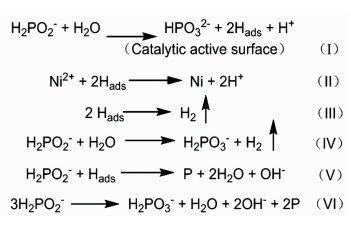
Ni-P的形成过程由于体系复杂,影响因素甚多,因此,研究人员也提出了多种可能的机理,典型的如“原子氢析出理论”[19]、“氢化物理论”[20]和“电化学理论”[21],其中,原子氢析出理论被更广泛认可,反应途径如下。
由图 2(I)式可知, 原子氢由H2PO2-和H2O分别提供,并吸附在催化活性表面将Ni2+还原,生成的H+导致溶液的pH值下降[19-20],由图 2式(V)可知在化学镀Ni-P初期,P的沉积速率缓慢是由于溶液的pH值较高抑制了反应向正方向进行,从而阻碍了P的还原,这也解释了在镀覆初期P含量少的原因。
近年来化学镀法发展极为迅速,一方面作为功能材料,在防腐、耐磨方面,逐渐发展为一种特殊的表面工程技术;另一方面作为催化材料,在加氢、水解等方面逐渐表现出高催化活性。化学镀法的特性主要表现在以下几个方面:1)无需外加直流电源装置;2)化学镀是实现非金属表面金属化、金属表面沉积施镀的重要手段,如在金属、非金属、碳纤维、陶瓷等表面镀覆;3)对于形状复杂的基体亦能得到厚度均匀、空隙少、致密的镀层;4)设备简单,操作容易,反应温度低,镀层与基体结合强度高,镀层厚度可控;5)镀层具有特殊的机械、物理和化学性能[22]。目前,化学镀已发展为一种应用广泛的技术,得到的镀层连续性、均匀性较好,具有高催化活性,耐腐蚀,耐磨损[23]。
2 化学镀法制备镍系非晶态合金的研究及应用化学镀法制备的镍系非晶态材料在催化领域中往往表现出较高的催化活性。同时,又常用于制备防腐蚀材料,不通电的情况下在金属表面镀覆防腐蚀膜,达到与电镀一样的效果。
2.1 催化剂制备中的研究与应用化学镀法制备的镍系非晶态催化剂有着广阔的应用前景,其制备的催化剂分散性好,催化活性高,常用于不饱和化合物的加氢、氧化、水解等催化反应。
2.1.1 不饱和化合物加氢化学镀法制备镍系催化剂过程中,通常采用Ag、Au、Pd或Pt等金属诱导法,由金属离子的诱导在基体上形成高分散性、适宜粒径的催化剂,能暴露出更多的催化活性中心,解决了活性组分的团聚问题,改善了热稳定性,催化活性明显高于非负载的镍系非晶态合金,具有良好的循环使用性能。
程庆彦等[24]采用金属Ag诱导化学镀法制备Ni-P/ZrO2非晶态合金催化剂,用于硝基苯加氢反应中。结果表明:载体ZrO2大大提高了Ni-P非晶态合金的热稳定性,并有效解决了纳米Ni-P催化剂的团聚问题。硝基苯的转化率和苯胺的选择性均为100%,同等条件下,催化加氢活性优于Ni-P催化剂。王丽娜等[25]采用Pd诱导化学镀法制备了负载型Ni-Co-P/γ-Al2O3非晶态合金催化剂,以硝基苯催化加氢反应考察其催化性能,结果表明:Ni-Co-P以非晶态的形式成功沉积在γ-Al2O3小球上。硝基苯的转化率达99.9%,苯胺选择性达99.99%,具有良好的催化活性和循环使用性能。Xie等[26]采用自制的碳纳米纤维为载体,Pd诱导化学镀制备负载型Ni-Co-B/CNF催化剂,以催化硝基苯加氢作为探针反应,结果表明,硝基苯转化为苯胺的转化率可达98.8%,选择性为100%,与Raney-Ni相比,Ni-Co-B/CNF催化剂具有更高的催化活性和稳定性。
另外,可以在化学镀法制备催化剂的过程中引入超声、微波等手段,如葛少辉等[27]在超声波条件下,利用Ag诱导化学镀法制备了非晶态Ni-B合金和负载型Ni-B/MgO催化剂,以环丁烯砜加氢制环丁砜为探针反应。结果表明,环丁烯砜转化率为80.9%,与未引入超声波制备的催化剂相比,催化加氢性能提高30%。超声波的引入能够提高活性组分的分散性,改善活性组分的粒径,且不影响Ni-B的非晶态结构。Wu等[28]在微波辅助下分别以水和乙二醇为溶剂制备了Ni-B/MgO(W)、Ni-B/MgO(EG),以苯乙酮加氢为探针反应,结果表明,Ni-B/MgO(EG)催化苯乙酮转化率为93.2%,苯乙醇的选择性为95.1%,均高于Ni-B/MgO(W),相比于未引入微波辅助制备的Ni-B/MgO(EG),转化率提高了10%以上,由TEM表征可知,非晶态Ni-B颗粒均匀分散在MgO上,微波辐射对Ni-B/MgO(W)中Ni-B的粒径有显着影响。
本课题组采用Ag诱导化学镀法,以KBH4为还原剂,制备了NiCoB/TiO2三元非晶态合金催化剂[10]。结果表明:NiCoB以非晶态的形式负载在TiO2载体上,由图 3可知NiCoB/TiO2分散性较好。将该催化剂应用于松节油催化加氢制备顺式蒎烷,α-蒎烯转化率高达99.23%,顺式蒎烷对应选择性为95.53%,收率达94.80%。
目前化学镀趋势向着多元合金的方向发展,如Ni与Co、Ag、Sn等元素与其他类金属元素P、B等形成合金,可以使镀层具有更高催化活性和热稳定性。但这种多元合金镀层的发展还比较慢,主要原因是多元合金化学镀工艺Ni-P合金难控制。若在化学镀制备过程中引入超声、微波等手段来改善化学镀的工艺,应该可以得到活性、稳定性更高的催化剂。
2.1.2 电催化氧化反应化学镀法制备的镍系催化剂在氧化还原反应中,通常用于电催化氧化反应,在电极表面镀覆Ni基非晶态合金膜后,电催化氧化效果明显高于晶态膜,在酸碱溶液中具有良好的稳定性,较长的使用寿命。通常采用循环伏安法(CV)的峰电流密度作为电催化氧化的活性指标,峰电流密度越高,催化活性越高。
Babu等[29]采用化学镀法在石墨上镀覆Ni-P,研究了纯Ni和Ni-P/石墨两种催化剂在KOH溶液中不同浓度葡萄糖的电氧化性能。与纯Ni相比,化学镀Ni-P/石墨对葡萄糖的氧化具有更高的催化效果,其峰电流密度可达338 mA/cm2。Hassan等[30]通过化学镀法在酸性镀液中成功制备了Ni-B/C电极,并用于甲醇的电催化氧化。XRD、SEM分析表明Ni-B/C镀层在结构上混合有微晶-非晶态,其对甲醇电催化氧化的催化活性约为Pt/C或Ni-P/C电极的两倍。
Cao等[31]以TiO2纳米管为载体通过化学镀法制备了Ni-B/TiO2合金电极。研究表明,Ni-B/TiO2合金电极对碱性介质中的甲醇具有很高的电催化氧化活性。其对电极催化寿命的考察表明,在经过1 300次循环后,Ni-B/TiO2电极依然相对稳定。Wen等[32]采用化学镀法在碱性介质中制备了Ni-B薄膜作为高效电催化剂用于水合肼的电催化氧化。同时,利用电镀法制备Ni薄膜与Ni-B薄膜进行比较,Ni-B薄膜对肼氧化显示更高的电催化活性和稳定性。XRD分析可知,与Ni薄膜相比,Ni-B膜由非晶态和纳米晶态的混合组成。
随着非晶态合金电极的研究进展,三元非晶态合金电极在电催化氧化方面表现出很大的优势。Yuan等[33]利用化学镀法分别制备了纳米孔Ni-Cu-P三元非晶态合金(NP-NiCuP)、纳米孔Ni-Cu晶态合金(NP-NiCu)以及Ni-Cu-P三元非晶态合金(S- NiCuP)电极,并用于甲醇的电催化氧化。结果表明,NP-NiCuP电极比S-NiCuP和NP-NiCu电极对甲醇氧化更具有稳定的氧化还原行为和优异的催化稳定性。在未来的发展中,化学镀制备的多元合金电极必将成为电催化氧化的主流。
2.1.3 水解反应化学镀法制备的镍系催化剂在水解反应中,通常用于析氢反应。在NaBH4水解制氢反应中,通常以非贵金属FeCl2、CoCl2、NiCl2、CuCl2等为催化剂[34]。由于Ni、Co等对氢具有较强的亲和力,通常加氢、析氢反应中都以Ni、Co等为活性组分。
Wang等[35]研究了通过化学镀制备的负载型纳米Ni-B/Cu催化剂对NaBH4水解产氢性能的影响。通过对催化碱性NaBH4溶液的水解动力学研究可知,产氢速率可达4 991.8 mL/(g·min),活化能为36.3 kJ/mol。同时,Ni-B催化剂也表现出较高的稳定性,在5次循环使用后仍可保持其初始值的80.5%。
李忠等[36]以纳米碳纤维(CNFs)为载体,采用化学镀法镀覆Ni-Co-P,用于催化碱性NaBH4水解析氢。结果表明,在55 ℃、5%的硼氢化钠溶液中,产氢速率可以达到30.770 L/(g·min),活化能为51.57 kJ/mol,并表现出优异的循环使用性能。
Li等[37]采用Pd诱导化学镀法制备了Ni-Co-P/γ-Al2O3催化剂,用于催化NaBH4水解产氢。结果表明,Ni-Co-P/γ-Al2O3催化剂在55 ℃时的最大产氢速率为6 599.6 mL/(g·min)。由于Ni、Co和P三者的协同作用,使得Ni-Co-P/γ-Al2O3催化剂具有良好的循环能力和活化能(Ea=52.05 kJ/mol),在经过7次循环使用后,产氢速率仍可达3 994.9 mL/(g·min)。Rakap等[38]采用Pd诱导化学镀法制备了Co-Ni-P/Pd-TiO2催化剂。通过对水解动力学研究可知,活化能(Ea =57.0 kJ/mol),55 ℃下最大产氢速率为3 780 mL/(g·min),在经过5次循环使用后,仍保持其初始催化活性的86.4%。
由表 1所述不同方法制备的催化剂在同一探针反应中,可知化学镀法制备的催化剂要比传统方法制备的活性高。化学镀法制备的三元合金催化剂相比于二元合金具有更高的催化活性。将Co、Cu等对氢具有较强的亲和力的元素,加入化学镀镍溶液中,采用一种或多种还原剂,可以得到多元合金,以改善二元合金的稳定性相对较差的缺陷。
| 表 1 不同方法制备的催化剂的活性对比 Table 1 Activity comparison of catalysts prepared by different methods |
表面工程是表面预处理后,通过表面涂覆、表面改性或多种表面技术复合处理,改变固体金属表面或非金属表面的形态、化学成分、组织结构和应力状况,以获得所需表面性能的系统工程[42]。表面工程技术包括化学转化、阳极氧化、热喷涂、化学镀、激光熔覆等[43],在各种表面工程技术中,化学镀法通过多组分多层次镀覆,有效突破了单一组分薄膜的限制,制备出多组分合金镀层(如镍系合金镀层),它表现出优异的耐腐蚀性、耐磨性,被广泛应用在制备防腐、耐磨材料上。
2.2.1 防腐材料近年来,化学镀法在制备镍系防腐材料方面表现出巨大的优势。化学镀覆在基体上的非晶态合金膜比传统方法制备的更加均匀致密,相比电镀法更经济环保。在化学镀液中添加一些惰性粒子[44]如Al2O3[45]、SiO2[46]和SiC[47-48]等,使惰性粒子与Ni、Cu、Zn和Ni-P合金等共沉积,由此形成的镀层不仅增强了金属基体的强度,而且通过抑制底层金属氧化可起到防腐蚀的作用,使金属基体表面得到改性。
Ma等[47]利用化学镀法在低碳钢基体上制备了Ni-P、Ni-P-SiC镀层,引入超声波分散SiC,共沉积在Ni-P涂层中,可改善镀层的显微硬度,作为延缓Ni-P镀层塑性变形的屏障[49],从而改善Ni-P-SiC纳米复合镀层结构和腐蚀性能。Wang等[48]利用化学镀法在AZ91D镁合金基体上制备了Ni-P/SiC梯度镀层。EIS研究表明,与Ni-P涂层相比,Ni-P/SiC梯度涂层具有更高的电荷转移电阻和较低的电容值,且Ni-P/SiC梯度涂层能够为镁合金基底提供更好的防腐蚀保护。
Sharifalhoseini等[50]在合成Ni-P/ZnO纳米粒子过程中引入了超声波,结果表明,与传统方法相比,引入超声波得到的Ni-P镀层具有更高的抗腐蚀性能。Zou等[51]采用超声波辅助化学镀法制备了Ni-P/Mg-8Li合金,研究表明,Ni-P镀层是非晶态和多晶态混合存在,并与基材粘合良好。动电位扫描极化测试和析氢测试结果表明,超声波辅助可以显著提高Ni-P镀层的耐腐蚀性能,形成均匀致密的微细结构,强化钝化膜。
Seifzadeh等[52]利用化学镀法在AZ91D合金上制备了Ni-Co-P和Ni-Co-P-SiO2纳米复合镀层,并与传统的Ni-P镀层进行比较,结果表明,Ni-Co-P-SiO2复合镀层耐腐蚀性能优于Ni-P和Ni-Co-P镀层,这是由于SiO2在合金表面吸附而形成厚而致密的具有曲折晶界的镀层。通过电化学方法评估镀层的腐蚀行为,Ni-Co-P-SiO2纳米复合镀层表现出优异的抗腐蚀性能。
2.2.2 耐磨材料目前耐磨材料是新技术领域的核心,它在信息技术、生物技术、能源技术等高科技领域和国防建设的中担任着重要角色。因此,众多研究者致力于研究新型耐磨材料的制备方法。而化学镀法制备的非晶态合金膜均匀致密,在各种形貌的基材上呈现出良好的粘附性,因此,具有优良的耐磨性。
Jagatheeshwaran等[53]利用化学镀法以NaH2PO2为还原剂在En8钢上分别镀覆了Ni-P、Ni-P/未经煅烧贝壳颗粒(SSP)、Ni-P/煅烧贝壳颗粒(Cal.SSP)镀层,并对镀层的低摩擦性和耐磨损性的进行了研究。结果表明,3种镀层厚度依次增加,表明耐磨性能依次增加,NiP/Cal.SSP复合镀层具有更好的耐摩擦性能。Madah等[54]通过化学镀法以NaBH4为还原剂,在中碳钢体上镀覆平均厚度为50~60 μm的Ni-B镀层,用XRD、SEM、维氏硬度等测定镀层的结构、形貌、硬度以及硼含量,以滑动距离表示Ni-B镀层的耐磨性。结果表明,由于硼含量相对较高,阻碍了镍相成核,从而使Ni-B镀层以非晶态形式镀覆在碳钢表面,化学镀Ni-B镀层比工具钢、硬铬镀层和Ni-P镀层更耐磨。
与制备耐腐蚀材料相似,在化学镀液中添加一些惰性粒子如SiC,使之与Ni、P、B等共沉积,由此形成的合金镀层可增强金属基体的强度,从而增强基体的耐磨性能。例如Sivandipoor等[55]将WS2颗粒作为固体润滑剂加入化学镀Ni-P中,在低碳钢基体上制备耐摩擦的新型复合镀层Ni-P-WS2,通过测定摩擦系数来评价耐磨性,结果表明,在镀层中使用WS2颗粒降低了硬度并改变了传统Ni-P镀层的磨损行为,摩擦系数从0.6以上降低到约0.1。Franco等[56]将SiC颗粒作为第二相粒子加入化学镀Ni-P中,在铝合金LM24基体上制备耐摩擦的复合镀层Ni-P-SiC,考察了SiC的含量对镀层耐磨性能的影响,并与Ni-P/LM24和LM24基体进行了比较,研究发现嵌入的颗粒压入基体中,这有助于防止复合材料的进一步磨损。
3 镀液净化与再利用随着化学镀的应用范围和生产规模不断扩大以及人们环保意识的日益增强,化学镀废液所致的环境污染已备受重视,研究化学镀液的净化和再利用也就应运而生,近年来经过研究者们的努力,已取得了一些研究成果[57]。研究者多以分离技术如电解沉积法、离子交换法来净化回收化学镀废液,也有研究者使用Fenton法,如UV-Fenton,其是有望成为化学镀废液处理的一把“杀手锏”。
电解法是用镍阳极补充镍离子,用阴极使Ni离子还原为金属镍,以回收镍,采用特种阴极使亚磷酸根还原为次磷酸根[58]。Lee等[59]以电解沉积法回收化学镀镍废液中的镍,研究发现镍的电解沉积受pH值影响很大,如不进行pH值调节,镍回收率仅为30%,电流效率低于20%;然而,当pH=2.0±0.2时,镍回收率超过90%,且电流效率未有下降。但在电解沉积镍之前,需将废液pH值调节至13,除去废液中的铁和锌,以获得高纯度镍产品。但该法无法彻底除去亚磷酸盐,对沉积镍反应仍有影响,当Ni离子浓度低时,电流效率很低,析镍成本变高。因此,此方法尚不成熟,实用案例极少。
离子交换法是处理化学镀镍废液的常用方法,处理过程中常使用氧化剂或强酸破坏配位剂,采用弱酸性阳离子或弱碱性阴离子交换树脂吸附Ni2+,它能有效回收镍离子并回用到镀液中,也能同时除去各种阴、阳离子,使水以纯水形式回用,但缺点是废液中的次磷酸根不能完全回用。Li等[60]采用褐煤离子交换法研究了化学镀镍废液中镍回收的新方法。研究表明,镍离子交换不仅受溶液pH值的影响,而且受废液中存在的阴离子种类的阻碍,尤其是高浓度磷化合物。镍离子交换的最合适pH值为9.0~10.0,使用氢氧化钙沉淀ENP废液中的磷,磷去除率最高达98.2%。控制pH值以防止氢氧化镍的共沉淀,最终可使化学镀镍废液溶液中62%的镍离子交换成褐煤。
不同于以上分离技术回收净化镀液,Liu等[61]采用紫外-Fenton(UV-Fenton)工艺回收净化化学镀废液,以H2O2为氧化剂,去除废镀液中高含量的COD,添加Fe2+以回收次磷酸盐和亚磷酸盐,生成可用作磷酸铁锂电池原料的高纯磷酸铁。结果表明,当使用连续进料模式加入H2O2和Fe2+时,可获得最高的氧化效率,COD去除率约96.1%。同时,次磷酸盐和亚磷酸盐被氧化成磷酸盐,以Fe3+沉淀磷酸盐,可以回收废镀液中约99.9%的磷,且回收的磷酸铁颗粒纯度高、尺寸大。
采用Fenton法在处理化学镀废液时,可获得较高的氧化效率,具有一般化学氧化法无法比拟的优点,但H2O2价格昂贵,单独使用成本太高,因而在实际应用中,通常是与其他处理方法联用,将其用于废水的预处理或最终深度处理。用少量Fenton试剂对废液进行预处理,使废液中的难降解有机物发生部分氧化,改变其可生化性、溶解性和混凝性能,利于后续处理,这将是未来工业废水处理的发展趋势。例如Seo等[62]以UV/H2O2光化学工艺为基础,经过不懈努力,成功联用Advanced Oxidation Process(AOP)技术进行工艺优化,处理高浓度的化学镀镍废液。特别是,Seo等提出了镍以浸出和浓缩来回收的处理方法,此外以UV/H2O2光化学工艺与O3发生器配合使用,将亚磷酸盐和次磷酸盐氧化成易于沉淀的磷酸盐,通过COD和PO4-P转换效率和H2O2的消耗量来评估能耗。研究表明,UV/H2O2工艺与O3发生器配合使用不仅可以节省6 h的处理时间,还可以减少30%的H2O2消耗量。证明了Fenton法与AOP技术联用是可行且高效的。
4 展望近年来,利用化学镀法制备镍系非晶态合金的研究已取得了一些进展,应用于催化方面表现出较高的活性和选择性,但对于其调控机理以及结构与性能之间的关系亟待建立。通过深入研究制备条件,得到B和P与Ni形成合金时的存在状态,B、P的含量对Ni的分散性、粒径大小的影响,结合催化性能,得到“构效关系”,完善镍系非晶态催化剂体系。作为一种表面工程技术,相较于普通的电镀法、阳极氧化法等,化学镀得到的镀层相对致密,具有良好的耐腐蚀性、耐磨性,但要得到无空隙、轻薄的镀层,依然是难题。理论上,可在不影响化学镀液稳定性的情况下,通过增加活性组分,得到多元合金如Ni-Fe-P,从现有技术看,研究多拘泥于常用还原剂,若开发使用新的还原剂或使用多种还原剂,通过调控镀液的pH值、温度、惰性粒子等因素,控制镀层厚度、形貌等,可得到具有特殊用途的多元合金功能材料,然后,再建立组分、还原剂及制备条件之间的构效关系,将为功能材料方面提供更好的参考价值。对于化学镀废液回收、再利用方面,若采用多种净化处理方式相结合,同时回收处理化学镀废液中多种有害元素并降低回收产物的二次污染,将更有利于重金属资源的节约与保护,降低环境净化负担。现阶段,将该方法应用于工业生产,形成一套成熟度高、费用低、能耗小且简单易行的处理方法是非常有必要的。
| [1] |
SMITH G V, BROWER W E, MATYJASZCZYK M S, et al. Metallic glasses: new catalyst systems[J]. Studies in Surface Science & Catalysis, 1981, 7: 355-363. DOI:10.1016/S0167-2991(09)60283-4 |
| [2] |
李辉. 非晶态合金及其催化应用[M]. 北京: 科学出版社, 2014. LI Hui. Amorphous Alloys and its Catalytic Applications[M]. Beijing: Science Press, 2014. |
| [3] |
LI H, ZHANG D, LI G, et al. Mesoporous Ni-B amorphous alloy microspheres with tunable chamber structure and enhanced hydrogenation activity[J]. Chemical Communications, 2010, 46(5): 791-3. DOI:10.1039/b917430c |
| [4] |
SCHUH C A, HUFNAGEL T C, RAMAMURTY U. Mechanical behavior of amorphous alloys[J]. ActaMaterialia, 2007, 55(12): 4067-4109. DOI:10.1016/j.actamat.2007.01.052 |
| [5] |
DENG J F, LI H, WANG W. Progress in design of new amorphous alloy catalysts[J]. Catalysis Today, 1999, 51(1): 113-125. DOI:10.1016/S0920-5861(99)00013-9 |
| [6] |
ÁRPÁDMOLNÁAR, SMITH G V, BARTÓK M. New catalytic materials from amorphous metal alloys[J]. Advances in Catalysis, 1989, 36(6): 329-383. DOI:10.1016/S0360-0564(08)60020-6 |
| [7] |
WONTERGHEM J V, MΦRUP S, KOCH C J W, et al. Formation of ultra-fine amorphous alloy particles by reduction in aqueous solution[J]. Nature, 1986, 322(6080): 622-623. DOI:10.1038/322622a0 |
| [8] |
MALLORY Jr G O. Method of preparing substrate surface for electroless plating and products produced thereby: U.S. Patent 4232060[P]. 1980-11-04.
|
| [9] |
ZHANG S, XIA Z, NI T, et al. Tuning chemical compositions of bimetallic AuPd catalysts for selective catalytic hydrogenation of halogenated quinolines[J]. Journal of Materials Chemistry A, 2017, 5(7): 3260-3266. DOI:10.3866/PKU.WHXB201407141 |
| [10] |
鞠江月, 王亚明, 蒋丽红, 等. NiCoB/TiO2非晶态合金催化松节油加氢反应[J]. 精细化工, 2017, 34(1): 66-73. JU Jiangyue, WANG Yaming, JIANG Lihong, et al. Hydrogenation of turpentine catalyzed by NiCoB/TiO2 amorphous alloy catalysts[J]. Fine Chemicals, 2017, 34(1): 66-73. DOI:10.13550/j.jxhg.2017.01.011 |
| [11] |
WANG Y, LI T, BAI S, et al. Catalytic hydrolysis of sodium borohydride via nanostructured cobalt-boron catalysts[J]. International Journal of Hydrogen Energy, 2016, 41(1): 276-284. DOI:10.1016/j.ijhydene.2015.11.076 |
| [12] |
LI Y, FAN Y, JIAN J, et al. Pt-based structured catalysts on metallic supports synthesized by electroless plating deposition for toluene complete oxidation[J]. Catalysis today, 2017, 281: 542-548. DOI:10.1016/j.cattod.2016.05.022 |
| [13] |
WU Y, LIU H, SHEN B, et al. The friction and wear of electroless Ni-P matrix with PTFE and/or SiC particles composite[J]. Tribology International, 2006, 39(6): 553-559. DOI:10.1016/j.triboint.2005.04.032 |
| [14] |
ISLAM M, AZHAR M R, KHALID Y, et al. Electroless Ni-P/SiC Nanocomposite coatings with small amounts of SiC nanoparticles for superior corrosion resistance and hardness[J]. Journal of Materials Engineering & Performance, 2015, 24(12): 1-9. DOI:10.1007/s11665-015-1801-x |
| [15] |
SUN S, LIU J, YAN C, et al. A novel process for electroless nickel plating on anodized magnesium alloy[J]. Applied Surface Science, 2008, 254(16): 5016-5022. DOI:10.1016/j.apsusc.2008.01.169 |
| [16] |
WU Z, GE S, ZHANG M, et al. Synthesis of nickel nanoparticles supported on metal oxides using electroless plating: controlling the dispersion and size of nickel nanoparticles[J]. Journal of Colloid & Interface Science, 2009, 330(2): 359-366. DOI:10.1016/j.jcis.2008.10.083 |
| [17] |
GORBUNOVA K M, IVANOV M V, MOISEEV V P. Electroless deposition of nickel-boron alloys mechanism of process, structure, and some properties of deposits[J]. Journal of The Electrochemical Society, 1973, 120(5): 613-618. DOI:10.1149/1.2403514 |
| [18] |
MALLORY G O, HAJDU J B. Electroless plating: fundamentals and applications[M]. William Andrew, 1990.
|
| [19] |
KRISHNAN K H, JOHN S, SRINIVASAN K N, et al. An overall aspect of electroless Ni-P depositions——A review article[J]. Metallurgical and Materials Transactions A (Physical Metallurgy and, Materials Science), 2006, 37(6): 1917-1926. DOI:10.1007/s11661-006-0134-7 |
| [20] |
FELDSTEIN N, LANCSEK T S. A New technique for investigating the electrochemical behavior of electroless plating baths and the mechanism of electroless nickel plating[J]. Journal of The Electrochemical Society, 1971, 118(6): 869-874. DOI:10.1080/00202967.1971.11870185 |
| [21] |
AGARWALA R C, AGARWALA V. Electroless alloy/composite coatings: A review[J]. Sadhana, 2003, 28(3-4): 475-493. DOI:10.1007/BF02706445 |
| [22] |
闫晓慧. 化学镀镍磷专利技术综述[J]. 科技视界, 2015(23): 319-322. YAN Xiaohui. Summary of patented technology of electroless nickel phosphorus[J]. Science & Technology Vision, 2015(23): 319-322. DOI:10.3969/j.issn.2095-2457.2015.23.242 |
| [23] |
SUDAGAR J, LIAN J, SHA W. ChemInform abstract: electroless nickel, alloy, composite and nano coatings——A critical review[J]. Cheminform, 2013, 44(31): 183-204. DOI:10.1016/j.jallcom.2013.03.107 |
| [24] |
程庆彦, 张凯, 王延吉, 等. Ni-P/ZrO2非晶态合金催化剂的制备及硝基苯液相加氢性能[J]. 现代化工, 2017, 37(8): 81-85. CHENG Qingyan, ZHANG Kai, WANG Yanji, et al. Preparation of Ni-P/ZrO2 amorphous alloy catalyst and its performance in liquid-phase hydrogenation of nitrobenzene[J]. Modern Chemical Industry, 2017, 37(8): 81-85. DOI:10.16606/j.cnki.issn0253-4320.2017.08.019 |
| [25] |
王丽娜, 李忠, 刘腾宇, 等. 负载型非晶合金催化剂Ni-Co-P/γ-Al2O3的制备及其结构和催化性能表征[J]. 青岛科技大学学报(自然科学版), 2016, 37(1): 41-46. WANG Lina, LI Zhong, LIU Tengyu, et al. Preparation, structure and property characterization of supported amorphous alloy catalysts Ni-Co-P/γ-Al2O3[J]. Journal of Qingdao University of Science and Technology(Natural Science Edition), 2016, 37(1): 41-46. DOI:10.16351/j.1672-6987.2016.01.009 |
| [26] |
XIE G, SUN W, LI W. Synthesis and catalytic properties of amorphous Ni-Co-B alloy supported on carbon nanofibers[J]. Catalysis Communications, 2009, 10(3): 333-335. DOI:10.1016/j.catcom.2008.09.013 |
| [27] |
GE S, WU Z, ZHANG M, et al. Sulfolene hydrogenation over an amorphous Ni-B alloy catalyst on MgO[J]. Industrial & Engineering Chemistry Research, 2006, 45(7): 2229-2234. DOI:10.1021/ie0512542 |
| [28] |
WU Z J, GE S H, ZHANG M H, et al. Synthesis of a supported nickel boride catalyst under microwave irradiation[J]. Catalysis Communications, 2008, 9(6): 1432-1438. DOI:10.1016/j.catcom.2007.12.006 |
| [29] |
BABU G V, PALANIAPPA M, JAYALAKSHMI M, et al. Electroless Ni-P coated on graphite as catalyst for the electro-oxidation of dextrose in alkali solution[J]. Journal of Solid State Electrochemistry, 2007, 11(12): 1705-1712. DOI:10.1007/s10008-007-0347-8 |
| [30] |
HASSAN H B, HAMID Z A. Electroless Ni-B supported on carbon for direct alcohol fuel cell applications[J]. International Journal of Hydrogen Energy, 2011, 36(1): 849-856. DOI:10.1016/j.ijhydene.2010.09.069 |
| [31] |
CAO H, WANG Z, HOU G, et al. TiO2, nanotube-supported amorphous Ni-B electrode for electrocatalytic oxidation of methanol[J]. Surface & Coatings Technology, 2010, 205(3): 885-889. DOI:10.1016/j.surfcoat.2010.08.037 |
| [32] |
WEN X P, DAI H B, WU L S, et al. Electroless plating of Ni-B film as a binder-free highly efficient electrocatalyst for hydrazine oxidation[J]. Applied Surface Science, 2017, 409: 132-139. DOI:10.1016/j.apsusc.2017.03.047 |
| [33] |
YUAN L S, ZHENG Y X, JIA M L, et al. Nanoporous nickel-copper-phosphorus amorphous alloy film for methanol electro-oxidation in alkaline medium[J]. ElectrochimicaActa, 2015, 154: 54-62. DOI:10.1016/j.electacta.2014.12.055 |
| [34] |
徐东彦, 张华民, 叶威. 硼氢化钠水解制氢[J]. 化学进展, 2007, 19(10): 1598-1605. XU Dongyan, ZHANG Huamin, YE Wei. Hydrogen production from sodium borohydride[J]. Progress in Chemistry, 2007, 19(10): 1598-1605. |
| [35] |
WANG Y, LU Y, WANG D, et al. Hydrogen generation from hydrolysis of sodium borohydride using nanostructured Ni-B catalysts[J]. International Journal of Hydrogen Energy, 2016, 41(36): 16077-16086. DOI:10.1016/j.ijhydene.2016.05.258 |
| [36] |
李忠, 王丽娜, 王桂雪, 等. 负载型Ni-Co-P/CNFs催化剂的制备及释氢性能[J]. 燃料化学学报, 2015(3): 372-378. LI Zhong, WANG Lina, WANG Guixue, et al. Hydrogen generation from the hydrolysis of sodium borohydride solution over the supported Ni-Co-P/CNFs catalysts[J]. Journal of Fuel Chemistry and Technology, 2015(3): 372-378. DOI:10.3969/j.issn.0253-2409.2015.03.017 |
| [37] |
LI Z, LI H, WANG L, et al. Hydrogen generation from catalytic hydrolysis of sodium borohydride solution using supported amorphous alloy catalysts (Ni-Co-P/γ-Al2O3)[J]. International Journal of Hydrogen Energy, 2014, 39(27): 14935-14941. DOI:10.1016/j.ijhydene.2014.07.063 |
| [38] |
RAKAP M, KALU E E, ÖZKAR S. Cobalt-nickel-phosphorus supported on Pd-activated TiO2, (Co-Ni-P/Pd-TiO2) as cost-effective and reusable catalyst for hydrogen generation from hydrolysis of alkaline sodium borohydride solution[J]. Journal of Alloys & Compounds, 2011, 509(25): 7016-7021. DOI:10.1016/j.jallcom.2011.04.023 |
| [39] |
徐云, 蒋月秀, 秦祖赠, 等. Ni-P非晶态合金/酸化膨润土的制备及加氢性能[J]. 化工进展, 2017, 36(5): 1719-1726. XU Yun, JIANG Yuexiu, QIN Zuzeng, et al. Preparation and hydrogenation property of Ni-P amorphous alloy/acid-treated bentonite catalysts[J]. Chemical Industry and Engineering Progress, 2017, 36(5): 1719-1726. DOI:10.16085/j.issn.1000-6613.2017.05.021 |
| [40] |
GUO J, HOU Y, LI B, et al. NiB-Ni nanocomposites for improved electrocatalytic activity in methanol oxidation reaction[J]. Journal of Applied Electrochemistry, 2016, 46(12): 1-10. DOI:10.1007/s10800-016-1000-y |
| [41] |
GUO Y, FENG Q, MA J. The hydrogen generation from alkaline NaBH4, solution by using electroplated amorphous Co-Ni-P film catalysts[J]. Applied Surface Science, 2013, 273(2): 253-256. DOI:10.1016/j.apsusc.2013.02.025 |
| [42] |
徐滨士, 谭俊, 陈建敏. 表面工程领域科学技术发展[J]. 中国表面工程, 2011, 24(2): 1-12. XU Binshi, TAN Jun, CHEN Jianmin. Science and technology development of surface engineering[J]. China Surface Engineering, 2011, 24(2): 1-12. DOI:10.3969/j.issn.1007-9289.2011.02.001 |
| [43] |
GRAY J E, LUAN B. Protective coatings on magnesium and its alloys-a critical review[J]. Cheminform, 2002, 336(1): 88-113. DOI:10.1016/S0925-8388(01)01899-0 |
| [44] |
EOM K S, CHO K W, KWON H S. Effects of electroless deposition conditions on microstructures of cobalt-phosphorous catalysts and their hydrogen generation properties in alkaline sodium borohydride solution[J]. Journal of Power Sources, 2008, 180(1): 484-490. DOI:10.1016/j.jpowsour.2008.01.095 |
| [45] |
BALARAJU J N, KALAVATI, RAJAM K S. Electroless ternary Ni-W-P alloys containing micron size Al2O3, particles[J]. Surface & Coatings Technology, 2010, 205(2): 575-581. DOI:10.1016/j.surfcoat.2010.07.047 |
| [46] |
HAZAN Y D, ZIMMERMANN D, Z'GRAGGEN M, et al. Homogeneous electroless Ni-P/SiO2, nanocomposite coatings with improved wear resistance and modified wear behavior[J]. Surface & Coatings Technology, 2010, 204(21-22): 3464-3470. DOI:10.1016/j.surfcoat.2010.04.007 |
| [47] |
MA C, WU F, NING Y, et al. Effect of heat treatment on structures and corrosion characteristics of electroless Ni-P-SiC nanocomposite coatings[J]. Ceramics International, 2014, 40(7): 9279-9284. DOI:10.1016/j.ceramint.2014.01.150 |
| [48] |
WANG H L, LIU L Y, DOU Y, et al. Preparation and corrosion resistance of electroless Ni-P/SiC functionally gradient coatings on AZ91D magnesium alloy[J]. Applied Surface Science, 2013, 286(4): 319-327. DOI:10.1016/j.apsusc.2013.09.079 |
| [49] |
HAMID Z A, EL BADRY S A, AAL A A. Electroless deposition and characterization of Ni-P-WC composite alloys[J]. Surface and Coatings Technology, 2007, 201(12): 5948-5953. DOI:10.1016/j.surfcoat.2006.11.001 |
| [50] |
SHARIFALHOSEINI Z, ENTEZARI M H. Enhancement of the corrosion protection of electroless Ni-P coating by deposition of sonosynthesized ZnO nanoparticles[J]. Applied Surface Science, 2015, 351: 1060-1068. DOI:10.1016/j.apsusc.2015.06.028 |
| [51] |
ZOU Y, ZHANG Z, LIU S, et al. Ultrasonic-assisted electroless Ni-P plating on dual phase Mg-Li alloy[J]. Journal of The Electrochemical Society, 2015, 162(1): C64-C70. DOI:10.1149/2.0841501jes |
| [52] |
SEIFZADEH D, HOLLAGH A R. Corrosion resistance enhancement of AZ91D magnesium alloy by electroless Ni-Co-P coating and Ni-Co-P-SiO2, nanocomposite[J]. Journal of Materials Engineering & Performance, 2014, 23(11): 4109-4121. DOI:10.1007/s11665-014-1210-6 |
| [53] |
JAGATHEESHWARAN M S, ELAYAPERUMAL A, ARULVEL S. The role of calcinated sea shell particles on friction-wear behavior of electroless NiP coating: Fabrication and characterization[J]. Surface & Coatings Technology, 2016, 304: 492-501. DOI:10.1016/j.surfcoat.2016.07.053 |
| [54] |
MADAH F, DEHGHANIAN C, AMADEH A A. Investigations on the wear mechanisms of electroless Ni-B coating during dry sliding and endurance life of the worn surfaces[J]. Surface & Coatings Technology, 2015, 282: 6-15. DOI:10.1016/j.surfcoat.2015.09.003 |
| [55] |
SIVANDIPOOR I, ASHRAFIZADEH F. Synthesis and tribologicalbehaviour of electroless Ni-P-WS2, composite coatings[J]. Applied Surface Science, 2012, 263(48): 314-319. DOI:10.1016/j.apsusc.2012.09.051 |
| [56] |
FRANCO M, SHA W, MALINOV S, et al. Micro-scale wear characteristics of electroless Ni-P/SiC composite coating under two different sliding conditions[J]. Wear, 2014, 317(1-2): 254-264. DOI:10.1016/j.wear.2014.06.013 |
| [57] |
方景礼. 化学镀镍废液处理的现状与ENP-1化镍废液处理剂[J]. 电镀与精饰, 2015(10): 43-47. FANG Jingli. The status of spent electroless nickeling (EN) solution treatment and ENP-1 treating agent of spent EN solution[J]. Plating and Finishing, 2015(10): 43-47. |
| [58] |
崔磊, 王维德, 倪海霞, 等. 化学镀镍废液亚磷酸盐的电解转化研究[J]. 水处理技术, 2006, 32(7): 36-38. CUI Lei, WANG Weide, NI Haixia, et al. al Electrolytic transferring of phosphite in nickel electroplating waste liquor[J]. Technology of water treatment, 2006, 32(7): 36-38. DOI:10.3969/j.issn.1000-3770.2006.07.009 |
| [59] |
LEE H Y. Separation and recovery of nickel from spent electroless nickel-plating solutions with hydrometallurgical processes[J]. Separation Science and Technology, 2013, 48(11): 1602-1608. DOI:10.1080/01496395.2012.756523 |
| [60] |
LI L, TAKAHASHI N, KANEKO K, et al. A novel method for nickel recovery and phosphorus removal from spent electroless nickel-plating solution[J]. Separation & Technology, 2015, 147: 237-244. DOI:10.1016/j.seppur.2015.04.029 |
| [61] |
LIU P, LI C, LIANG X, et al. Recovery of high purity ferric phosphate from a spent electroless nickel plating bath[J]. Green Chemistry, 2014, 16(3): 1217-1224. DOI:10.1039/c3gc41779d |
| [62] |
SEO M, CHO S, LEE S, et al. A Study on the highly effective treatment of spent electroless nickel plating solution by an advanced oxidation process[J]. Journal of the Korean Industrial & Engineering Chemistry, 2015, 26(3): 270-274. |
 2020, Vol. 28
2020, Vol. 28