2. 山西大学 资源与环境工程研究所,太原 030006
2. Institute of Resources and Environmental Engineering, Shanxi University, Taiyuan 030006, China
光催化作为近些年新兴发展的领域,其本质是催化剂在光照条件下进行的光化学反应和催化反应。光催化能将太阳能转变为化学能,例如光解水制氢[1-2]、光催化还原二氧化碳等[3],此外,光催化还可以利用太阳能降解有机污染物、还原重金属离子等,因而是一种理想的环境污水治理技术。含酚废水作为环境污水的一个分支,因高毒性,难降解性已被含中国在内的众多国家列入重点防治名单。所以,利用光催化技术处理含酚废水对于环境保护和污水治理具有重大意义。
光催化技术的核心是光催化剂,目前发现可作为光催化剂的材料众多,包括二氧化钛(TiO2), 氧化锌(ZnO), 氧化锡(SnO2), 二氧化锆(ZrO2),硫化镉(CdS)等多种氧化物、硫化物半导体。相比而言,二氧化钛因稳定的物化性质、极低的毒性、低廉的价格和优异的生物相容性等优点[4-5],这些年广泛受到研究者的喜爱[6]。但是纯二氧化钛作为光催化剂仍有一些不足:1)禁带较宽(锐钛矿型3.2 eV,金红石型3.0 eV),只能被小于400 nm的太阳光所激发,而这部分光仅占太阳光的5%,对太阳光的利用率极低;2)量子效率低,其表面产生的光生电子与空穴对极易发生复合,所以需要对二氧化钛进行改性,以提高其量子效率和太阳光的利用率[7]。对二氧化钛改性的方法包括金属/非金属掺杂[8]、贵金属表面沉积[4, 9]、量子点/有机染料敏化[10-11]、半导体复合等[12],其中,量子点敏化二氧化钛是指将量子点与二氧化钛复合,通过量子点在紫外光与可见光下的感光性,增加光生电子与空穴的数量,扩宽太阳光吸收范围[8],而传统量子点多数都包含有毒重金属离子,生物相容性差,严重会危及人类生命[7, 13]。碳量子点作为近年新兴的一种荧光碳纳米材料,不仅无毒害,制备成本低廉,而且因其优良的光敏性、光诱导电子转移能力以及光致发光效应等特性赋予了其在光催化领域杰出的应用潜力[14-16]。本文以富勒烯碳灰为原料,利用混酸回流法制备了一种发黄蓝光的碳量子点,然后采用一步水热法将碳量子点负载于二氧化钛表面合成了复合光催化剂。借助高分辨透射电子显微镜,红外光谱,紫外可见光光谱,荧光光谱,X射线衍射,X射线光电子能谱分析等表征手段对碳量子点和复合光催化剂进行表征,并以苯酚作为模拟废水进行光催化性能测试。
1 实验 1.1 主要试剂与仪器试剂:纳米二氧化钛P25(德固赛,分析纯)购自上海倍墨实业有限公司,富勒烯炭灰,硝酸,硫酸购自上海国药化学试剂有限公司,均为分析纯。去离子水采用优普实验室超纯水器制备。
仪器:高分辨透射电子显微镜(JEM-2100),日本电子株式会社;傅立叶变换红外光谱仪(VERTEX 70),德国布鲁克科学仪器公司;荧光光谱(日立F-4600);紫外可见漫反射光谱(Varian Cary 50),美国瓦里安有限公司;紫外可见分光光度仪(UV-1601),北京瑞利分析仪器公司;X射线衍射仪(XRD-6000),日本岛津;X射线光电子能谱分析(XSAM800),英国Kratos公司;光催化仪(XPA-7),南京旭江机电厂。
1.2 实验方法 1.2.1 富勒烯炭灰量子点的制备对实验室已有的富勒烯炭灰量子点[17](标记为F-CQDs)进行优化,即调节混酸(硝酸/硫酸)回流比为1/3.2。
1.2.2 F-CQDs/P25复合光催化剂的制备称取0.5 g F-CQDs,加25 mL去离子水溶解,配成浓度为20 mg/mL的量子点母液备用;称取0.4 g P25。然后分别量取量子点母液80、120、160、200、240 μL(即相当于P25质量分数的0.4%,0.6%,0.8%,1.0%,1.2%),滴加在相同体积(120 mL)去离子水中,室温搅拌均匀,然后加入P25继续搅拌均匀,转移至200 mL(装填量60%)聚四氟乙烯做内衬的水热反应釜,恒温干燥箱110 ℃反应2 h,反应结束后自然冷却至室温,离心过滤,去掉上清液,加去离子水多次洗涤离心至上清液无色透明,80 ℃真空干燥箱干燥12 h,即可制得X%-F-CQDs/P25复合光催化剂。
1.2.3 F-CQDs/P25复合光催化剂光催化降解苯酚各量取100 mL,50 ppm的苯酚水溶液于6个规格相同的250 mL的烧杯中,依次加入质量均为0.1 g的未改性P25、0.4%F-CQDs/P25,0.6%F-CQDs/P25,0.8%F-CQDs/P25,1.0%F-CQDs/P25,1.2%F-CQDs/P25,置于恒温磁力搅拌器搅拌,暗吸附2 h,打开500 W氙灯,氙灯与烧杯的垂直距离为70 cm,间隔一定时间取样,每次取样5 mL,8 000 r/min离心15 min,取上清液,利用UV-1601于270 nm处测定紫外吸光度,绘制降解率与时间曲线。在测试范围内,苯酚水溶液的浓度与吸光度符合郎伯比尔定律,降解效率(η)根据以下公式计算:
| $ \eta=\frac{C_{0}-C_{t}}{C_{0}} \times 100 \%=\frac{A_{0}-A_{t}}{A_{0}} \times 100 \%. $ | (1) |
A0、C0分别为光照降解前苯酚的吸光度,质量分数,At、Ct分别为光照降解t时刻苯酚的吸光度,质量分数。
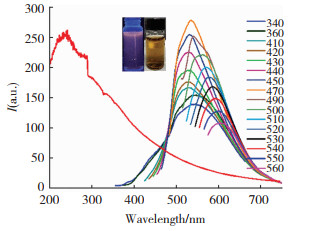
2 结果与讨论 2.1 F-CQDs的荧光特性表征碳量子点最初发现与应用的两个突出特点是荧光特性,紫外区强吸收。图 1是F-CQDs水溶液在不同激发波长下的荧光发射光谱与紫外可见吸收光谱(红色曲线)。从图中可以看出,随着激发波长的增大,发射波长的强度先增大后减小,并且逐渐红移,在470 nm处有最佳发射波长,最强发射峰位置在535 nm,这证明F-CQDs的光致发光性质存在激发波长依赖性。图 1的插图是F-CQDs在365 nm的紫外灯(左)与日光灯下的光学照片,可以看到其在紫外灯下发出明亮的黄蓝光。目前,关于碳量子点的发光机理还没有统一定论,仍需进一步研究[18]。F-CQDs水溶液的紫外可见吸收光谱中(红色曲线),在245 nm处有很明显的特征吸收峰,这是由于C=O键的n→π*跃迁产生的,同时在400~700 nm的可见光区也有长拖尾吸收,这为改性二氧化钛提供了可行性条件[19]。利用荧光光谱仪测定了F-CQDs的荧光寿命与绝对荧光量子产率,其平均荧光寿命τave=3.32 ns,绝对荧光量子产率φ=3.9%。
|
图 1 F-CQDs在不同激发波长下的荧光发射光谱和紫外可见吸收光谱,插图为F-CQDs在365 nm的紫外灯(左)与日光灯下的光学照片 Fig.1 Fluorescence emission spectra at varying excitation wavelengths and UV-visible absorption spectrum of the F-CQDs. Insets are photos of the F-CQDs in aqueous solution under 365 nm UV lamp (left) and room light (right) |
| 表 1 F-CQDs的荧光特性(荧光寿命和绝对荧光量子产率) Table 1 Fluorescence performance (fluorescence lifetimes (τ) and absolute fluorescence quantum yields (φ)) of F-CQDs aqueous solution |
为了表征F-CQDs和复合光催化剂的微观形貌首先进行HRTEM测试。图 2(a)是F-CQDs的HRTEM图片。可以清晰观察到F-CQDs呈无规则球形,且分散均匀无团聚现象,粒径大约在(2~4)nm,图 2(b)是F-CQDs/P25复合光催化剂的HRTEM图片,图中红圈重点标示的是碳量子点,说明F-CQDs被成功负载于P25上。

|
图 2 F-CQDs和F-CQDs/P25高分辨透射电镜图片 Fig.2 HRTEM image of F-CQDs and F-CQDs/P25 |
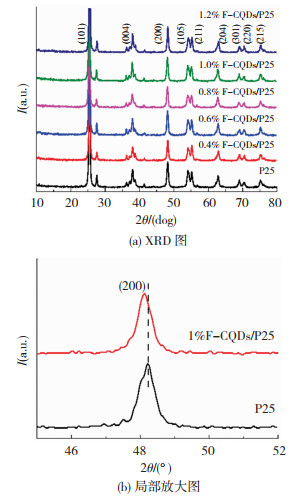
为确定制备样品的晶体结构进行了XRD测试。图 3(a)展示的是P25和不同F-CQDs掺杂量负载P25的复合光催化剂的XRD谱图。其中二氧化钛P25的XRD图谱分别在25.4°,38.1°,48.3°,54.2°,55.4°,62.8°,70.5°和75.3°处出现明显衍射峰,对应于(101),(004),(200),(105),(211),(204),(220)和(215)晶面,这与(JCPDS NO.84-1285)锐钛矿型TiO2的XRD图谱一致,而在69.1°出现的衍射峰属于金红石型二氧化钛的(301)晶面(JCPDS NO.86-0148),说明购买的P25为锐钛矿/金红石混合型。另外发现不同F-CQDs掺杂量负载P25的复合光催化剂的XRD图谱与P25的也近乎完全相同,这表明F-CQDs掺杂P25只是通过表面相互作用结合在一起,而并非进入P25本体,故不会改变P25本体的晶型结构[19]。图 3(b)展示的是P25与1%F-CQDs/P25的(200)晶面放大图。随着F-CQDs含量增加为1%时,其XRD衍射峰从48.24°略微偏移到48.13°,这可能是在制备过程中加热这个宏观残余应力引起晶格各向异性收缩造成的。
|
图 3 P25和X%-F-CQDs/P25的XRD图谱和局部放大图 Fig.3 XRD pattern and partial enlargement of P25 and X%-F-CQDs/P25 |
傅里叶变换红外光谱用于测定所制备样品中有机官能团的存在。图 4(a)是P25,F-CQDs和F-CQDs/P25复合光催化剂的红外光谱图,在P25图谱中,分别在3 445,1 608和6 67 cm-1处出现明显特征吸收峰,分别对应于P25表面吸附水的羟基(—OH)伸缩振动和弯曲振动以及Ti—O键的伸缩振动。F-CQD在3 437 cm-1处的特征峰归属为表面羟基(—OH)的伸缩振动,1 608 cm-1处的吸收峰来源于C=C的伸缩振动[20-21],1 385,1 271 cm-1的特征峰与C—O—H键,C—C键的伸缩振动有关。对于1%F-CQDs/P25复合催化剂的FT-IR光谱,可以发现其在3 437 cm-1处的特征吸收峰相比P25向低波数移动,667 cm-1处的特征吸收峰相比F-CQDs向低波数移动且吸收峰强度也明显不同,这是F-CQDs负载于P25上产生了相互作用引起的,而在1 639 cm-1处,其FT-IR光谱向高波数方向偏移,这是由C=C键伸缩振动与—OH的弯曲振动共同耦合作用引起。

|
图 4 P25, F-CQDs和1% F-CQDs/P25的红外谱图和P25,1% F-CQDs/P25的紫外可见漫反射谱图 Fig.4 FT-IR spectra of pure P25, F-CQDs and 1% F-CQDs/P25 and UV-Vis diffuse reflectance spectra of P25 and 1% F-CQDs/P25 |
紫外可见漫反射光谱反映光催化材料的光学吸收性能。图 4b是样品P25与1.0% F-CQDs /P25的紫外可见漫反射光谱,相比未改性P25, 1.0%F-CQDs/P25复合光催化剂的紫外可见漫反射光谱明显红移,在400~700 nm的可见光区也有明显吸收,说明对可见光吸收能力得到进一步提升。
2.5 XPS分析表征为进一步研究样品的表面化学状态和化学组成进行XPS测试。图 5(a)是复合光催化剂1.0%F-CQDs/P25的XPS全谱图,图 5(b),5(c),5(d)分别是O1s,C1s和Ti2P的XPS谱图,说明复合光催化剂F-CQDs/P25是由Ti,C, O三种元素组成,进一步证明F-CQDs被成功负载于P25。从图 5(b)可以看出Ti2P3/2和Ti2P1/2的结合能分别是458.35 eV,464.0 eV,对应于复合物中的Ti—O键,说明在复合物中钛是以+4价存在[22];图 5(c)中C1s图谱在284.65eV,288.65eV的模拟峰应分别归属为C—C/C=C键与C=O键的结合能;图 5d中O1s在529.9eV,532.3eV的结合能是由P25的晶格氧(Ti—O)和复合光催化剂表面的羟基氧(—OH)所致,这结果与文献报道相符[23]。

|
图 5 F-CQDs/P25的XPS全谱图及C1s, O1s, Ti2p的放大谱图 Fig.5 XPS spectra of F-CQDs/P25 and magnification of C1s, O1s, and Ti2p peak |
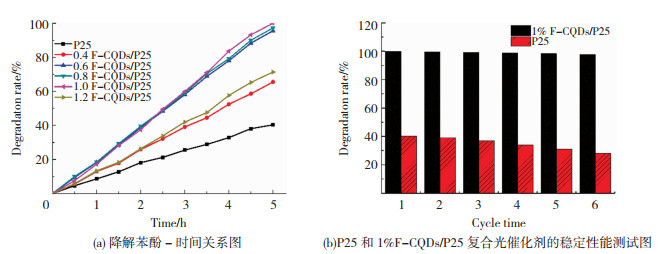
图 6(a)所示是P25和不同F-CQDs掺杂量的复合光催化剂在500 W氙灯(模拟太阳光)照射下光催化降解苯酚的降解率—时间关系图。相同照射时间5 h时,未改性P25对苯酚的去除率为40.3%,1.0%F-CQDs/P25则可将苯酚全部降解。随F-CQDs掺杂量从0.4%增加到1%,x%-F-CQDs/P25复合光催化剂对苯酚去除率从65.5%递增为100%,而当F-CQDs掺杂量为1.2%时,复合光催化剂对苯酚的去除效果反而降低为71.4%,这可能是由于随着F-CQDs的增加,其电荷转移能力增加,提高了复合光催化剂的电子空穴对分离效率,光催化性能增强,当进一步增加F-CQDs的负载量,由于F-CQDs自身发生团聚现象,覆盖了P25表面的活性位点,影响催化剂本体对太阳光的吸收利用,从而使其光催化性能降低。
|
图 6 不同光催化剂降解苯酚溶液的降解率—时间关系图以及P25和1%F-CQDs/P25复合光催化剂的稳定性能测试 Fig.6 Degradation rate-time relationship of phenol solution degraded by different photocatalysts and stability test of P25 and 1%F-CQDs/P25 composite photocatalyst |
为进一步研究复合光催化剂X%-F-CQDs/P25的稳定性能,将光催化效果最好的1%F-CQDs/P25与P25回收再利用,在相同的实验条件下重复试验6次,结果如图 6(b)所示。P25对苯酚的降解效果明显降低,相比第一次循环,6次循环后,其降解率下降了12%;而1% F-CQDs/P25在6个循环后,其对苯酚的去除率从100%下降到97.8%,仅下降了2.2%;这归因于碳量子点的表面自清洁能力,当二氧化钛被成功负载碳量子点时,其表面自清洁能力也随之增强,这充分证明F-CQDs/P25复合光催化剂具有优良的光催化稳定性。
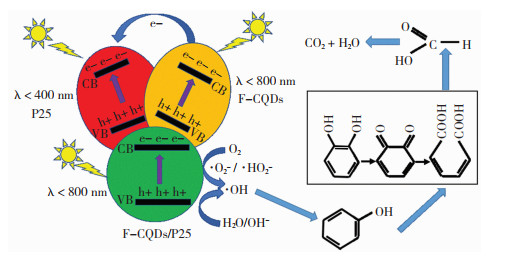
2.7 F-CQDs/P25光催化降解苯酚机理二氧化钛是一种金属半导体氧化物,因较宽的禁带宽度决定了其只能吸收利用小于388nm的太阳光。F-CQDs作为一种能发射黄蓝光的荧光量子点,除在紫外光区有强吸收外,在400-780 nm的可见光区也有明显吸收。当用F-CQDs敏化二氧化钛时,借助F-CQDs强的电子转移能力将电子转移至二氧化钛导带(conduction band, CB),在太阳光照下,当入射光能量大于或等于价带(Valentine band,VB)与导带之间的能量差时,价带上的电子受激发跃迁至导带,生成电子(e-)与空穴(h+)。这些电子捕获氧气分子(O2)并将其转化为超氧自由基(·O2-)和过氧化羟基自由基(HO2·)等,然后通过后续反应生成羟基自由基(·OH);另一方面,光生空穴也是羟基自由基(·OH)的主要来源,它能捕获二氧化钛表层的氢氧根(OH-)和水(H2O)中的电子,并将其转化为羟基自由基(·OH)[24]。羟基自由基(·OH)是降解苯酚的主要物质,其氧化能力(2.80 V)仅次于氟(2.87 V), 可无选择地直接氧化打开苯酚中的苯环生成CO2和H2O,而不会产生二次污染。图 7是F-CQDs/P25光催化降解苯酚机理与示意图。
|
图 7 F-CQDs/P25光催化降解苯酚机理示意图 Fig.7 Schematic diagram of photocatalytic degradation of phenol by F-CQDs/P25 |
| $ \begin{array}{c} \mathrm{F}-\mathrm{CQDs} / \mathrm{P} 25+h v \rightarrow \mathrm{F}-\mathrm{CQDs} / \mathrm{P} 25+\mathrm{h}^{+}+\mathrm{e}^{-} \\ \left(E_{\lambda}>E \mathrm{g}\right). \end{array} $ | (2) |
| $ \mathrm{h}^{+}+\mathrm{H}_{2} \mathrm{O} / \mathrm{OH}^{-} \rightarrow \cdot \mathrm{OH}+\mathrm{H}^{+}. $ | (3) |
| $ \mathrm{e}^{-}+\mathrm{O}_{2}+\mathrm{H}^{+} \rightarrow \cdot \mathrm{O}_{2-}+\mathrm{HO}_{2-} \rightarrow \cdot \mathrm{OH}. $ | (4) |
| $ \mathrm{C}_{6} \mathrm{H}_{6} \mathrm{O}+\cdot \mathrm{OH} \rightarrow \mathrm{CO}_{2}+\mathrm{H}_{2} \mathrm{O}. $ | (5) |
碳量子点改性二氧化钛可以缩短二氧化钛的禁带宽度,拓宽光吸收范围,提高对可见光的利用。利用混酸回流法制备了一种新型荧光碳量子点,然后将其用于二氧化钛改性。多种表征方法说明成功合成了复合光催化剂F-CQDs/P25,然后对其进行性能测试。以苯酚水溶液为模拟废水,500 W氙灯模拟太阳光,F-CQDs/P25作为光催化剂进行光催化实验,5 h,1%F-CQDs/P25可将苯酚水溶液全部降解,相比纯二氧化钛,苯酚降解率提高了60.0%,同时对复合光催化剂的稳定性进行测试,经过6次实验,F-CQDs/P25对苯酚的降解率几乎无明显差别,这是由F-CQDs/P25复合光催化剂中的F-CQDs的自清洁能力引起的。这说明经过碳量子点改性的二氧化钛具有优良的稳定性和光催化活性。本工作可为光催化处理含酚废水在工业中的应用提供理论指导。
| [1] |
XU Xueli, SONG Wei. Enhanced H2 production activity under solar irradiation over N-doped TiO2 prepared using pyridine as a precursor: a typical sample of N-doped TiO2 series[J]. Materials Technology, 2017, 32(1): 52-63. DOI:10.1080/10667857.2015.1118587 |
| [2] |
苗继娟, 汪李超, 河明玉, 等. Pt纳米颗粒负载SrTiO3/TiO2异质结结构制备及制氢性能[J]. 材料科学与工艺, 2018, 26(1): 16-23. MIAO Jijuan, WANG Lichao, HE Mingyu, et al. Preparation heterojunction structure of SrTiO3 /TiO2 nano-Pt loaded and photo-catalytic properties[J]. Materials Science and Technology, 2018, 26(1): 16-23. DOI:10.11951/j.issn.1005-0299.20170071 |
| [3] |
周亮, 张雪华, 林琳, 等. 无模板法水热合成CoTe及其可见光光催化还原CO2性能[J]. 物理化学学报, 2017, 33(9): 1884-1890. ZHOU Liang, ZHANG Xuehua, LIN Lin, et al. Visible-light photocatalytic reduction of CO2 by CoTe prepared via a template-free hydrothermal method[J]. Acta Physico Chimica Sinica, 2017, 33(9): 1884-1890. DOI:10.3866/PKU.WHXB201705084 |
| [4] |
XU Mingxi, WANG Yunhai, GENG Jiafeng, et al. Photodecomposition of NOx on Ag/TiO2 composite catalysts in a gas phase reactor[J]. Chemical Engineering Journal, 2017(307): 181-188. DOI:10.1016/j.cej.2016.08.080 |
| [5] |
王春来, 李钒, 杨焜, 等. 碳量子点-二氧化钛复合光催化剂的研究进展[J]. 材料导报, 2018, 32(19): 3348-3357. WANG Chunlai, LI Fan, YANG Kun, et al. Materials research progress on carbon quantum dots titanium dioxide composite photocatalysts[J]. Materials Review, 2018, 32(19): 3348-3357. DOI:10.11896/j.issn.1005-023X.2018.19.009 |
| [6] |
CHEN Xiaobo, SHEN Shaohua, GUO Lliejin, et al. Semiconductor-based photocatalytic hydrogen generation[J]. Chemical Reviews, 2010, 110(11): 6503-6570. DOI:10.1021/cr1001645 |
| [7] |
GEYS J, NEMMAR A, VERBEKEN E, et al. Acute toxicity and prothrombotic effects of quantum dots: impact of surface charge[J]. Environmental health perspectives, 2008, 116(12): 1607-1613. DOI:10.1289/ehp.11566 |
| [8] |
DU Jimin, WANG Huiming, CHEN Huijuan, et al. Synthesis and enhanced photocatalytic activity of black porous Zr-doped TiO2 monoliths[J]. Nano, 2016, 11(6): 1650068. DOI:10.1142/S1793292016500685 |
| [9] |
CHOI Y, KIM H I, MOON G H, et al. Boosting up the low catalytic activity of silver for H2 production on Ag/TiO2 photocatalyst: thiocyanate as a selective modifier[J]. Acs Catalysis, 2016, 6(2): 821-828. DOI:10.1021/acscatal.5b02376 |
| [10] |
YUN H J, PAIK T, DIROLL B, et al. Nanocrystal size-dependent efficiency of quantum dot sensitized solar cells in the strongly coupled CdSe nanocrystals/TiO2 system[J]. ACS Applied Materials & Interfaces, 2016, 8(23): 14692-14700. DOI:10.1021/acsami.6b05552 |
| [11] |
SUDHAKAR C, THANGASWAMY S, SELVAM K, et al. Flower mediated dye used as sensitizers for TiO2 based dye-sensitized solar Cells[J]. International Journal on Advanced Science, Engineering, 2016, 2(4): 209-213. DOI:10.1016/j.cej.2016.08.080 |
| [12] |
LI G S, WU L, LI F, et al. Photoelectrocatalytic degradation of organic pollutants via a CdS quantum dots enhanced TiO2 nanotube array electrode under visible light irradiation[J]. Nanoscale, 2013, 5(5): 2118-2125. DOI:10.1039/c3nr34253k: |
| [13] |
HARDMAN R. A toxicologic review of quantum dots: toxicity depends on physicochemical and environmental factors[J]. Environmental Health Perspectives, 2005, 114(2): 165-172. DOI:10.2307/3436504 |
| [14] |
YU C, LIU Z Q, CHEN Y W, et al. CoS nanosheets-coupled graphene quantum dots architectures as a binder-free counter electrode for high-performance DSSCs[J]. Science China Materials, 2016, 59(2): 104-111. DOI:10.1007/s40843-016-0121-2 |
| [15] |
LIM S Y, SHEN Wei, GAO Zhiqiang. Carbon quantum dots and their applications[J]. Chemical Society Reviews, 2015, 44(1): 362-381. DOI:10.1039/C4CS00269E |
| [16] |
LI Haitao, KANG Zhenhui, LIU Yang, et al. Carbon nanodots: synthesis, properties and applications[J]. Journal of materials chemistry, 2012, 22(46): 24230-24253. DOI:10.1039/C2JM34690G |
| [17] |
ZHANG Qinghong, SUN Xiaofei, RUAN Hong, et al. Production of yellow-emitting carbon quantum dots from fullerene carbon soot[J]. Science China Materials, 2017, 60(2): 141-150. DOI:10.1007/s40843-016-5160-9 |
| [18] |
FENG Zhibiao, LI Zeliang, ZHANG Xingwei, et al. Fluorescent carbon dots with two absorption bands: luminescence mechanism and ion detection[J]. Journal of materials science, 2018, 53(9): 6459-6470. DOI:10.1016/j.ijhydene.2014.02.020 |
| [19] |
LI X G, LIAO Y, HUANGM R, et al. Interfacial chemical oxidative synthesis of multifunctional polyfluoranthene[J]. Chemical Science, 2015, 6(3): 2087-2101. DOI:10.1039/C4SC03890H |
| [20] |
BIROJU R K, RAJENDER G, GIRI P. On the origin and tunability of blue and green photoluminescence from chemically derived graphene: hydrogenation and oxygenation studies[J]. Carbon, 2015, 95: 228-238. DOI:10.1016/j.carbon.2015.08.036 |
| [21] |
RAJENDER G, GIRI P. Formation mechanism of graphene quantum dots and their edge state conversion probed by photoluminescence and Raman spectroscopy[J]. Journal of Materials Chemistry C, 2016, 4(46): 10852-10865. DOI:10.1039/C6TC03469A |
| [22] |
SANTARA B, GIRI P, IMAKITA K, et al. Evidence of oxygen vacancy induced room temperature ferromagnetism in solvothermally synthesized undoped TiO2 nanoribbons[J]. Nanoscale, 2013, 5(12): 5476-5488. DOI:10.1039/C3NR00799E |
| [23] |
LI Fan, TIAN Feng, LIU Changjun, et al. One-step synthesis of nanohybrid carbon dots and TiO2 composites with enhanced ultraviolet light active photocatalysis[J]. RSC Advances, 2015, 5(11): 8389-8396. DOI:10.1039/C4RA14865G |
| [24] |
RAJENDER G, KUMAR J, GIRI P. Interfacial charge transfer in oxygen deficient TiO2-graphene quantum dot hybrid and its influence on the enhanced visible light photocatalysis[J]. Applied Catalysis B: Environmental, 2018, 224: 960-972. DOI:10.1016/j.apcatb.2017.11.042 |
 2020, Vol. 28
2020, Vol. 28


