2. 聚合物分子工程国家重点实验室(复旦大学),上海 200433
2. State Key Laboratory of Molecular Engineering of Polymers (Fudan University), Shanghai 200433, China
自1852年斯托克斯位移被发现以来,人们对光的研究开始广泛开展起来[1]。随着科技的发展,发光材料不仅在人们的日常生活中用于照明,也已逐渐广泛用于通信、医学诊断、航空航天、防伪标签等更高端的技术领域。
发光是指材料从外界吸收各种形式的能量后,通过原子结构内部的辐射跃迁等将这些能量转换并以光子的形式释放,目前最常见的发光材料是稀土荧光粉[2]。早在20世纪70年代,出现了稀土三基色荧光粉,主要应用在各类灯管。早期的灯用稀土荧光粉颗粒较大,且稳定性差。自2011年白光LED进入照明领域,灯用稀土三基色荧光粉的研究也逐渐萎缩。近年来,随着蓝紫光LED芯片技术的发展,稀土配合物用作近紫外激发有机荧光粉的研究得到了研究人员的重视。尽管国产稀土荧光粉所制成的白光LED器件的光效与国外产品相当,但产品制备工艺和质量稳定性与国外尚有差距[3-5]。
铕(Eu)作为一种典型的稀土元素,具有稀土离子的特征荧光,目前已广泛应用于发光材料载药、传感等领域[6-7]。铕元素的电子层结构为(Xe)(4f)7(6s)2,其特征价态是+3价,配位化学以+3价氧化态占主要地位[8]。李维[9]等采用2, 6-二(4-乙氧基苯甲酰基)吡啶(L)和1, 10-邻菲罗琳为配体,制备了新型的稀土铕离子三元配合物EuL(Phen)2,配合物具有很好的溶剂化效应。Hu[10]等采用化学共沉淀法制备了Ce3+掺杂的YAG稀土荧光粉。Wang[11]等合成了稀土铕与α-噻吩基三氟丙酮和三苯基氧化膦的配合物(Eu(TTA)3(TPPO)2),并与己二酸丁二醇酯和对苯二甲酸丁二醇酯的共聚物(PBAT)共混制备了可生物降解的光转换农用薄膜。Hao[12]等合成并研究了一系列Eu3+离子的稀土配合物,包括含有单配体乙烯-丙烯酸(EAA)的二元配合物和用1, 10-邻菲咯啉(phen),二苯甲酰甲烷(DBM)或噻吩甲酰三氟丙酮(TTA)作为第二配体的三元配合物。高分子配体相较于小分子配体、大分子配体等,不仅高分子链上可含有更多的配位官能团,且高分子金属配合物在催化剂、光材料等领域的研究也愈加广泛[13-14]。本文采用自主合成的高分子配体,聚合物含有羧酸、氨基等多种官能团,拥有较强的配位能力及多种配位方式,形成的配位聚合物结构稳定、无放射性物质、发光性能稳定、发射波长范围广、荧光寿命长,且兼具高分子优良的机械性能、热稳定性。
1 试验 1.1 试剂与仪器 1.1.1 试剂N-乙烯基甲酰胺(NVF):化学纯,梯希爱(上海)化成工业发展有限公司;丙烯酰胺(AM):化学纯,梯希爱(上海)化成工业发展有限公司;过硫酸钾(K2S2O8):分析纯,国药集团化学试剂有限公司;氢氧化钠(NaOH):分析纯,国药集团化学试剂有限公司;氧化铕(Eu2O3):分析纯,济宁市中凯新型材料有限公司;1, 10-邻菲咯啉(phen):分析纯,上海阿拉丁生化科技股份有限公司;盐酸(HCl):分析纯,国药集团化学试剂有限公司。
1.1.2 仪器赛默飞世尔科技有限公司的NICOLET is50型Fourier红外变换光谱仪;布鲁克科技有限公司的AVANCE III400型全数字化核磁共振波谱仪;日本尼康株式会社尼康TI-S型倒置荧光显微镜;布鲁克科技有限公司D2-PHASERA26-XI-AZEOBZAO型X射线衍射仪,测试条件为:2θ设置为5°~90°,检测速度为0.100 s/step;北京普析通用仪器有限责任公司TU-1901双光束紫外可见分光光度计;英国爱丁堡仪器公司FS5荧光光谱仪;浙大三色仪器有限公司PR-305荧光余辉亮度测试仪。
1.2 高分子配体的合成分别称取10 g的N-乙烯基甲酰胺(NVF)和6 g的丙烯酰胺(AM)于四口瓶中,按照单体总质量10wt.%加入溶剂去离子水,搅拌升温至80 ℃,将0.08 g的引发剂过硫酸钾(K2S2O8)溶于20 mL去离子水中,将溶液转移至恒压漏斗,开始缓慢滴加到四口瓶中,在氮气和冷凝回流保护下,保持体系在80 ℃、200 r/min条件下反应10 h,得到淡黄色粘稠状聚N-乙烯基甲酰胺(PNVF)。再将20 mL的NaOH溶液(8 mol/L)缓慢加入四口瓶,在氮气和冷凝回流保护下,保持体系在80 ℃、200 r/min条件下反应8 h,即可得到淡黄色粘稠状两性聚乙烯胺(PVAm)。
将反应后溶液装入分子量为8 000~14 000的透析袋(DM36),用去离子水透析纯化4 d,放入冷冻干燥机48 h后取出样品,经研磨得到粉末状的样品。
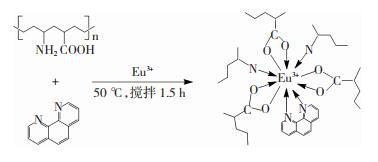
1.3 配位化合物的制备将1 mol的Eu2O3加入到6 mol的稀盐酸中,50 ℃下加热搅拌2.5 h至溶液澄清透明,制得EuCl3溶液,将合成的两性PVAm与phen按照物质的量比3: 1混合并加入到过量去离子水中,加热搅拌溶解均匀,待温度达到50 ℃时加入EuCl3溶液,开始缓慢出现絮状沉淀,搅拌1.5 h至沉淀完全,收集沉淀并反复洗涤后放入烘箱,80 ℃下恒温干燥,得到白色固体粉末即为稀土配合物Eu(PVAm)3phen荧光粉。稀土铕(Eu)离子与PVAm、phen的配位反应方程如图 1所示。
|
图 1 稀土铕(Eu)离子与PVAm、phen的配位反应方程图 Fig.1 Coordination reaction equation of rare earth Eu with PVAm and phen |
稀土元素拥有良好的光学性能,这源于稀土原子特殊的电子构型,即拥有未充满的4f5d电子组态,通常电子构型为(Xe) (4f)n (5s)2 (5p)6。随着原子序数逐渐增大,各稀土元素原子在内层的4f轨道中逐一填充电子,且该4f电子层被外层完全充满的(5s)2 (5p)6所屏蔽,从而为4f电子在不同能级的跃迁(f-f和f-d跃迁)创造了条件,使稀土元素在光学材料中获得了广泛的应用。
稀土铕配位化合物可受紫外光、X射线和阴极射线等照射后发光。这是由于在光线的激发下,稀土离子Eu3+被激发,从基态跃迁到激发态,然后再从激发态返回到能量较低的能态时,放出辐射能而产生荧光。稀土配合物发光的研究始于20世纪40年代,此后研究者们在积累了大量的实验结果后形成了相关的理论体系。Crosby、Sato[18-19]等在进行了系统研究后提出了配合物光致发光机理。目前,关于稀土配合物的发光机理通常有两种:一是能量转移机理;二是电荷转移机理。
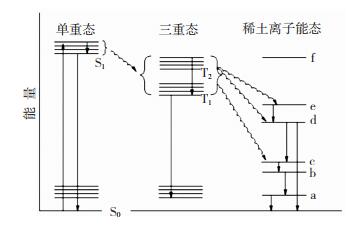
2.1 能量转移机理图 2是稀土配合物的能量转移过程示意图。
首先是配体的发色基团因吸收紫外激发光的辐射能,从单重态的基态S0跃迁至激发态S1, 然后激发能可以辐射方式回到基态S0,也可以非辐射方式转移到激发三重态T1或T2,三重态也可以辐射方式失去能量回到基态,也可以非辐射方式将能量转移到中心稀土离子的激发态,最后通过稀土离子较高能态的激发态到较低能态的基态辐射跃迁而产生荧光。
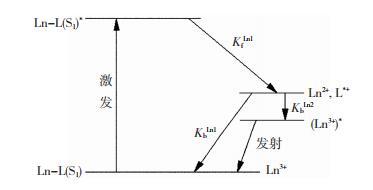
2.2 电荷转移机理图 3中Ln代表稀土镧系元素,L代表配体,带*表示处于激发态的物种,当稀土配合物Ln-L处于激发单重态时,配体L*与Ln3+间发生氧化还原反应,
| $ {\rm{Ln}} - {\rm{L}}{{\rm{n}}^*} \to {\rm{L}}{{\rm{n}}^{2 + }} + {\rm{ }}{{\rm{L}}^{* + }}. $ |
反应物的电荷发生了转移,反应体系的能量也将随之降低。此时的配合物体系中,配体正离子L*+具有强氧化性,而Ln2+具有还原性。在低于激发单重态的某一能级会再次发生氧化还原反应。
| $ {\rm{L}}{{\rm{n}}^{2 + }} + {{\rm{L}}^*} \to {({\rm{L}}{{\rm{n}}^{3 + }})^*} + {\rm{ L}}. $ |
此时反应过程伴随有能量转移,故出现(Ln3+)*物质在激发态的布居,中心离子随即发生辐射跃迁,进而发射出稀土离子的特征荧光。
|
图 3 稀土配位化合物发光的电荷转移机理图[15] Fig.3 Charge transfer mechanism of luminescence of rare earth coordination compounds[15] KfLn1,KbLn1分别代表Ln3+电荷正向和逆向转移率,KbLn2代表Ln2+→Ln3+电荷转移率 KfLn1 and KbLn1 represent the forward and reverse charge transfer rates of Ln3+, respectively; KbLn2 represents the charge transfer rates of Ln2+→Ln3+ |
对单体NVF、AM和经聚合水解后的产物PVAm分别做红外光谱测定。
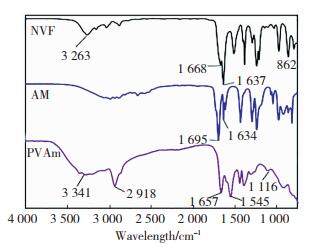
由图 4可知,对于NVF,3 263 cm-1处出现了由C-H不饱和氢键伸缩振动引起的吸收峰,1 668 cm-1处出现了由酰胺结构中C=O的伸缩振动引起的吸收峰,1 637 cm-1处则为C=C伸缩振所引起的吸收峰,此外750~1 000 cm-1处出现了较宽的吸收带,这是由N—H键面外弯曲振动所引起的吸收峰;对于AM,1 695 cm-1处出现酰胺结构中C=O的伸缩振动吸收峰,1 634 cm-1处出现C=C的伸缩振所吸收峰。
|
图 4 单体NVF,AM和聚合物PVAm的红外谱图 Fig.4 Infrared spectra of monomers NVF, AM, and polymer PVAm |
对于PVAm,在3 341 cm-1处出现了来自N—H的伸缩振动引发的特征峰,可能是酰胺在强碱性条件下水解生成了氨。2 918 cm-1处出现的是来自两性PVAm主链上C—H的伸缩振动引起的吸收峰,1 657 cm-1处则出现了由于酰胺结构中C=O的伸缩振动引发的吸收峰,此处是共聚物PNVF中的酰胺结构在高温及强碱性条件下水解生成羧酸盐并放出氨。
3.1.2 核磁共振谱图分析采用氘代水(D2O)为溶剂,对提纯后的配体两性PVAm进行核磁共振谱图检测。
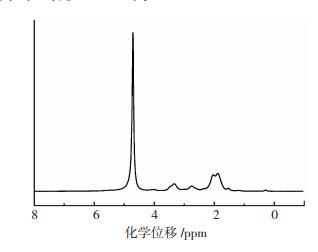
由图 5可知,两性PVAm的1H NMR谱图的峰位集中在1~5 ppm处,这是由于在两性PVAm中各单体间发生聚合、水解反应或氢键作用,因此, 化学位移1~4 ppm区域谱峰重叠现象较为严重,根据对酰胺类化合物合成共振研究,可将上述混合峰归类,1~2 ppm峰处主要是各种单体中CH3, CH2, NH2的重叠峰,2 ppm处主要是-N(CH2)2的三重峰和单峰的重叠峰,3~4 ppm处主要是各种碳水化合物的异头质子部分或-NHCHO中质子的谱峰,5 ppm处强核磁共振谱峰为氘代溶剂重水中氢键O-H峰。
|
图 5 PVAm的1H NMR谱图 Fig.5 1H NMR spectra of PVAm |
将提纯后的配合物Eu(PVAm)3phen样品粉末在荧光显微镜、并在手持式荧光剂紫外检测灯(365 nm)的照射下拍照观察配合物的发光现象。采用日本尼康株式会社尼康TI-S型倒置荧光显微镜进行观察。
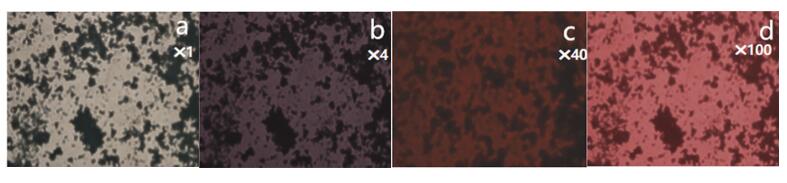
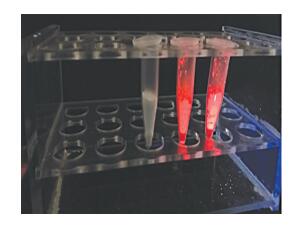
如图 6所示,配合物Eu(PVAm)3phen的粉末样品在荧光倒置显微镜下,样品在光源下放大不同倍数均显示出明显的红色荧光。图 7中,在荧光剂紫外检测灯(365 nm)照射下,样品也发出明显的红色荧光。这表明离子与配体配位反应后,内部结构发生电子跃迁,在光照条件下,Eu3+被激发,从基态跃迁到激发态,然后再从激发态返回到能量较低的能态时,放出辐射能而产生红色荧光,稀土离子的发光特性在配合物中得到充分发挥。
|
图 6 稀土配合物Eu(PVAm)3phen的荧光显微镜图 Fig.6 Fluorescence microscopy of rare earth complex Eu(PVAm)3phen |
|
图 7 紫外灯照射下稀土配合物Eu(PVAm)3phen图 Fig.7 Rare earth complex Eu(PVAm)3phen irradiated by ultraviolet lamp |
将提纯后的配合物Eu(PVAm)3phen样品粉末做XRD分析。图 8是配体两性PVAm(A)及配合物Eu(PVA)3phen(B)的粉末样品X射线衍射谱图。与配体相比,配合物Eu(PVAm)3phen出现更多的衍射峰且峰强度均有增强,多为尖锐的峰,说明配合物可能为定形结晶态结构。原配体的最大强度衍射峰在2θ=26°处,形成配合物时此位置偏移在2θ=32°处,且结晶强度更大,说明配体与Eu子空间上发生了大限度的配位,其配位共价键对X射线有反射作用,成晶态结构,配合物结构较为稳定。

|
图 8 配体PVAm(A)及稀土配合物Eu(PVAm)3phen(B)的XRD衍射谱图 Fig.8 XRD spectra of ligand PVAm(A) and rare earth complex Eu(PVAm)3phen(B) |
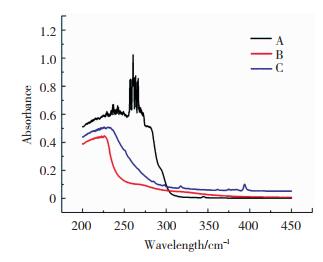
以丙酮为溶剂,对稀土配合物Eu(PVAm)3phen溶于丙酮后的溶液与配体在200~450 nm进行紫外-可见光光谱扫描。紫外吸收光谱如图 9所示。其中A代表第一配体PVAm,B代表第二配体phen,C代表配合物Eu(PVAm)3phen。配体与配合物在紫外光区均有较强的吸收,配体在215~235 nm形成了较强的吸收带,这是源于配体上羧酸上羰基的π→π*跃迁吸收峰,而配合物不仅在225~250 nm处有较强的吸收峰,在波长255~275 nm范围有很强的窄吸收峰,最大吸收峰在260 nm处,配合物中配体PVAm与中心离子Eu3+形成了稳定的螯合物,分子中引入助色基团,或由于溶剂的影响而发生红移,配合物在紫外-可见光等光源条件下具有优良的发光性能。
|
图 9 配体PVAm(A)、配体phen(B)以及稀土配合物Eu(PVAm)3phen(C)的紫外光谱 Fig.9 Ultraviolet spectra of ligands PVAm (A), phen (B), and rare earth complex Eu(PVAm)3phen(C) |
对稀土配合物Eu(PVAm)3phen样品粉末进行荧光光谱测定。以300 nm为激发波长(λex=300 nm),在400~700 nm进荧光发射光谱扫描。
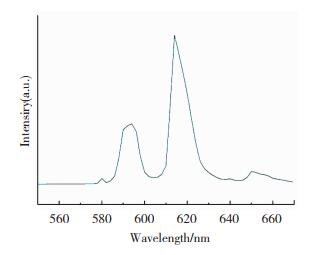
如图 10所示,稀土配合物Eu(PVAm)3phen在波长550~680 nm下有较强的荧光强度,Eu3+离子的发射谱主要存在位于580、593、614、650 nm的几个发射峰。分别对应Eu(Ⅲ)离子的5D0→7F0、5D0→7F1、5D0→7F2、5D0→7F3电子跃迁,其中以614 nm处的5D0→7F2发射峰强度最大且峰形最窄,与晶体场中Eu3+所处的位置有关。配合物在570~680 nm有明显的发射峰,此段波长范围位于橙红光区的波长,与稀土铕配合物作为红光材料基本吻合。
|
图 10 稀土配合物Eu(PVAm)3phen的荧光发射光谱 Fig.10 Fluorescence emission spectra of rare earth complex Eu(PVAm)3phen |
对稀土配合物Eu(PVAm)3phen样品粉末进行荧光余辉亮度测定。测试20 min内的荧光余辉亮度。
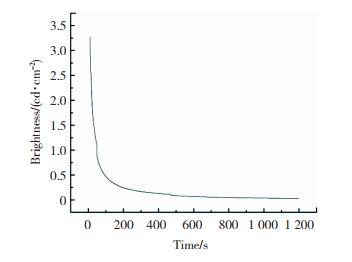
图 11是稀土配合物Eu(PVAm)3phen在马弗炉600 ℃高温煅烧后,在20 min内的荧光余辉亮度衰减曲线,激发时间为15 min。由图 11可知,在0~90 s时,荧光余辉亮度下降很快,在200 s时荧光余辉亮度在0.25 cd/m2,配合物此时还有优良的荧光释放。此后荧光余辉亮度逐渐缓慢衰减且衰减速度越来越慢,20 min时荧光余辉亮度为0.02 cd/m2,有肉眼可见的明显荧光,配合物热稳定性好且蓄光时间久,荧光寿命长。
|
图 11 稀土配合物Eu(PVAm)3phen在600 ℃处理下的荧光余辉亮度谱图 Fig.11 Fluorescence afterglow brightness spectra of rare earth complex Eu(PVAm)3phen treated at 600 ℃ |
1) 采用自由基溶液聚合法制备高分子化合物两性聚乙烯胺(PVAm),单体配比为NVF: AM= 5: 3,引发剂采用过硫酸钾(K2S2O8),用量为单体总质量的0.5%,在80 ℃、200 r/min下反应10 h,并在强碱性条件下水解制备出水溶性高分子聚合物两性聚乙烯胺(PVAm)。
2) 将两性聚乙烯胺(PVAm)作为第一配体,以1, 10-邻菲咯啉(phen)作为第二配体,稀土铕(Eu)作为中心离子,在50 ℃下搅拌反应,配位反应时先将两种配体充分混合均匀后再加入稀土元素,制备出Eu(PVAm)3phen稀土配位化合物。
3) 测试结果表明,配合物不仅具有优良的荧光性质,而且结构稳定、发光高效、蓄光时间长、高效节能、无放射性物质。
4) 本文所制备的稀土配合物不仅可作为荧光粉用于日常照明和夜光材料外,还可深入研究使其应用于半导体、防伪等更高端的技术领域。
| [1] |
杨晓林. 生物发光及化学发光研究及应用进展[J]. 继续医学教育, 2007, 21(26): 56-60. YANG Xiaolin. Progress in research and application of bioluminescence and chemiluminescence[J]. Continuing Medical Education, 2007, 21(26): 56-60. |
| [2] |
高银留, 张优灵, 尹荔松. 稀土荧光粉制备方法的研究进展[J]. 材料导报:纳米与新材料专辑, 2014, 28(1): 246-249. GAO Yinliu, ZHANG Youling, YIN Lisong. Research progress in preparation methods of rare earth phosphors[J]. Materials Review: Nano and New Materials, 2014, 28(1): 246-249. |
| [3] |
洪广言. 稀土发光材料的研究进展[J]. 人工晶体学报, 2015, 44(10): 2641-2651. Hong Guangyan. Research progress of rare earth luminescent materials[J]. Journal of Synthetic Crystals, 2015, 44(10): 2641-2651. |
| [4] |
刘斌, 段广彬, 刘宗明. 稀土有机配合物荧光材料的研究进展[J]. 中国粉体技术, 2018, 24(3): 6-10. LIU Bin, DUAN Guangbin, LIU Zongming. Research progress of rare earth organic complexes fluorescent materials[J]. China Powder Technology, 2018, 24(3): 6-10. |
| [5] |
胡静. ABO4型稀土荧光粉的制备及其发光性能研究[D].广州: 华南师范大学, 2015. HU Jing. Preparation and luminescent properties of ABO4 rare earth phosphors[D]. Guangzhou: South China Normal University, 2015. |
| [6] |
张杰强.稀土铕掺杂红色荧光粉的制备与性能研究[D].北京: 中国科学院大学, 2015. ZHANG Jieqiang. Preparation and properties of rare earth cerium doped red phosphors[D]. Beijing: University of Chinese Academy of Sciences, 2015. |
| [7] |
CHEN Fangfang, BIAN Zuqiang, HUANG Chunhui. Progresses in electroluminescence based on europium(Ⅲ) complexes[J]. Journal of Rare Earths, 2009, 27(3): 345-355. DOI:10.1016/S1002-0721(09)00003-9 |
| [8] |
储阳.稀土铕、铽丙烯酸酯基质的荧光材料的制备与性能研究[D].苏州: 苏州大学, 2017. CHU Yang. Preparation and properties of rare earth lanthanum and cerium acrylate matrix fluorescent materials[D]. Suzhou: Suzhou University, 2017. |
| [9] |
李维, 曾崇阳, 韩辉, 等. 一种新型稀土铕配合物的制备及荧光性能研究[J]. 化工新型材料, 2017, 45(1): 50-52. LI Wei, ZENG Chongyang, HAN Hui, et al. Preparation and fluorescence properties of a novel rare earth cerium complex[J]. New Chemical Materials, 2017, 45(1): 50-52. |
| [10] |
HU Yucai, LV Yimin, YU Xuehua, et a1. Synthesis and characterization of YAG: Ce3+ fluorescence powders by co-precipitation method[J]. Rare Earths, 2010, 28(S1): 303. |
| [11] |
WANG Dongmei, YU Yinlei, AI Xue, et al. Polylactide/poly(butylene adipate-co-terephthalate)/rare earth complexes as biodegradable light conversion agricultural films[J]. Polym Adv Technol, 2019, 30: 203-211. DOI:10.1002/pat.4459 |
| [12] |
H AO, Haixia, WU Qingyao, GAO Zihan, et a1. Preparation and luminescent properties of the novel polymer-rare earth complexes composed of Poly (ethylene-co-acrylic acid) and Europium ions[J]. Optical Materials, 2018(80). DOI:10.1016/j.optmat.2018.04.040 |
| [13] |
林玉辉.高分子配体及其金属络合物的研究[D].厦门: 厦门大学, 1990. LIN Yuhui. Research on polymer ligands and their metal complexes[D]. Xiamen: Xiamen University, 1990. |
| [14] |
王振华, 夏和生. 含金属-配体键高分子材料的研究进展[J]. 高分子材料科学与工程, 2014, 30(9): 170-176. WANG Zhenhua, XIA Hesheng. Research progress of metal-ligand bonded polymer materials[J]. Journal of Polymer Materials Science and Engineering, 2014, 30(9): 170-176. |
| [15] |
张洪杰, 牛春吉, 冯靖. 稀土有机-无机杂化发光材料[M]. 北京: 科学出版社, 2017. ZHANG Hongjie, NIU Chunji, FENG Jing. Rare earth organic-inorganic hybrid luminescent materials[M]. Beijing: Science Press, 2017. |
| [16] |
谢国亚, 张友. 稀土发光材料的发光机理及其应用[J]. 压电与声光, 2012, 34(1): 110-113, 117. XIE Guoya, ZHANG You. Luminescence mechanism of rare earth luminescent materials and application[J]. Piezoelectrics and Acoustooptics, 2012, 34(1): 110-113, 117. |
| [17] |
赵世华. 稀土发光材料的合成、发光机理及今后展望[J]. 化工新型料, 2015, 43(1): 213-215. ZHAO Shihua. Synthesis, luminescence mechanism and future prospect of rare earth luminescent materials[J]. New Chemical Materials, 2015, 43(1): 213-215. |
| [18] |
CROSBY G A, WHAN R E, ALIRE R M. Intramolecular energy transfer in rare earth chelates, role of the triplet states[J]. The Journal of Chemical Physics, 1961, 34: 743-748. DOI:10.1063/1.1731670 |
| [19] |
SATO S, WADA M. Relations between intramolecular energy transfer efficiencies and triplet state energies in rare earth β-diketone chelates[J]. Bulletin of the Chemical Society of Japan, 1970, 43: 1955-1962. DOI:10.1246/bcsj.43.1955 |
 2020, Vol. 28
2020, Vol. 28