2. 云南省新材料制备与加工重点实验室,昆明 650031
2. Key Laboratory of Advanced Materials of Precious-Nonferrous Metals of Yunnan Province, Kunming 650091, China
软磁铁氧体微粒以其高电阻、高化学稳定性、良好的电磁特性等优点,广泛应用于电子器件、催化、生物医学等领域[1-2]。Mn1-xZnxFe2O4(0≤x≤1)作为典型的尖晶石铁氧体,不仅在软磁领域占据较大份额,在微观领域,由于受表面效应和量子隧道效应以及独特形貌等影响,极大拓展了其应用,如吸附剂[3]、超级电容[4]、药物载体[5]等。
经过人们的广泛研究和探索,已发展出多种制备尖晶石铁氧体颗粒的方法,常用的有共沉淀法、溶胶凝胶法、水热/溶剂热法等,其中水热/溶剂热法通过改变溶剂的种类可用于制备特殊形貌的磁性颗粒。Wang等人[6]以乙二醇作为溶剂,合成由纳米颗粒自组装而成的直径在130~240 nm镍铁氧体微球; Tonto等人[7]分别使用1-丁醇,1-己醇,1-辛醇和1-癸醇作为反应介质得到不同长径比的ZnO纳米棒; Cao等人[8]在NaCl、H2O和乙醇的混合溶剂中,以聚乙烯吡咯烷酮(PVP)作为表面活性剂,在微波辅助下合成由纳米晶定向附着形成的单晶单分散α-Fe2O3介孔微球; Arumugam等人[9]分别使用N,N-二甲基甲酰胺(DMF)和乙二醇(EG)作为溶剂,通过溶剂热法合成正交结构的均匀Bi2S3纳米棒和纳米颗粒。
通常,在液相合成晶体过程中,单体聚集成核后便将经历生长过程,除借助经典的奥斯特瓦尔德熟化(OR)外,定向附着(OA)也是促使材料生长的非经典机制。OA是一种特殊的自组装形式,是以纳米级晶体作为生长基元,通过碰撞和旋转以特定晶面的原子键融合的生长过程[10],类似于烧结织构的形成,故在制备特殊形貌的纳米粉体方面引起人们极大的兴趣。本研究以乙二醇作为溶剂,采用溶剂热法制备纳米铁氧体微粒,并利用XRD、TEM、氮吸附和XPS进行表征,通过改变Zn2+含量,研究了粉末的物相、阳离子价态和形貌特征并探讨了微观颗粒生长机理。
1 实验 1.1 样品的制备采用溶剂热法制备Mn1-xZnxFe2O4(x=0、0.5、1),所有试剂均属于分析纯,制备流程如下:首先,按摩尔比分别称取FeCl3·6H2O、MnCl·4H2O、ZnCl2,其中Fe3+为6 mmol,在磁力搅拌器中搅拌直至完全溶于50 mL乙二醇,形成淡黄色透明溶液。然后,加入60 mmol NaAc和1 mL PEG-200,持续搅拌1 h后,将混合液倒入高压水热釜,加热至200 ℃并保温12 h。最后,在室温下冷却,将得到的黑色产物在离心机中用无水乙醇洗涤数次,沉淀产物放入60 ℃的恒温干燥箱中干燥并研磨。
1.2 样品的表征用中国通达TD-3500型X射线衍射仪(XRD),以Cu-Kα为辐射源,管电压为40 kV,管电流50 mA,扫描角度20°~75°,扫描速度为10 °/min,对经玛瑙研磨的实验样品的物相进行分析; 用美国赛默飞Escalab 250Xi型X射线光电子能谱仪(XPS)对实验样品的价态进行分析; 采用荷兰FEI公司的Tecnai G2 TF30 S-Twin型高分辨场发射透射电子显微镜(TEM)对试验样品的形貌和元素进行表征; 利用中国贝士德3H-2000A全自动氮吸附比表面仪对试样样品的比表面积进行表征。
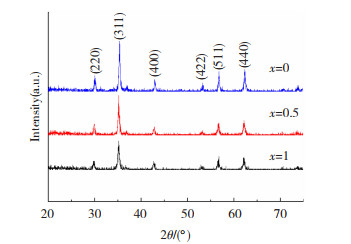
2 结果与讨论 2.1 XRD分析图 1为不同Zn2+含量溶剂热法制备的Mn1-xZnxFe2O4(x=0、0.5、1)的XRD谱图,可以看到,粉末主体相均为立方尖晶石结构,无明显杂质峰出现,衍射峰分别对应(220),(311),(400),(422),(511),(440)面。随着Zn2+的增加,(311)衍射峰角度2θ值向右偏移,分别为35.180°、35.229°和35.364°,而且,三者的衍射峰对比标准PDF卡片均有明显右移现象,这可能是由于乙二醇在高温反应中部分转变为乙醛,有较强的还原性。另外,原料中存在的结晶水及乙二醇中的微量水分使NaAc在高温下发生水解,造成的碱性还原环境将铁醇盐分离出的Fe3+还原为Fe2+,反应如下[11]。
| $ \begin{array}{c} 2 \mathrm{CH}_{3} \mathrm{CHO}+2 \mathrm{FE}^{3+}+2 \mathrm{OH}^{-} \rightarrow \mathrm{CH}_{3} \mathrm{COCOCH}_{3}+ \\ 2 \mathrm{Fe}^{2+}+2 \mathrm{H}_{2} \mathrm{O} \end{array} $ | (1) |
|
图 1 溶剂热合成Mn1-xZnxFe2O4的XRD谱图 Fig.1 XRD patterns of Mn1-xZnxFe2O4 prepared by solvothermal method |
为保证尖晶石铁氧体中金属阳离子与氧离子电荷平衡,Zn2+和Mn2+将被Fe2+部分取代,而Fe2+更加偏好占据B位(八面体),使部分Fe3+重新回到A位(四面体),使整体晶格常数偏向于Fe3O4,最终导致晶格常数变小而引起衍射峰偏移。Scherrer公式为
| $ D=0.89 \lambda / B \cos \theta $ | (2) |
式中: B为半峰宽度; λ为X射线波长; θ为衍射角。依据式(2),以(220)和(311)估算样品的晶粒直径分别为37.5、39.6和43.2 nm,说明Zn2+离子含量越高,晶粒度越大。
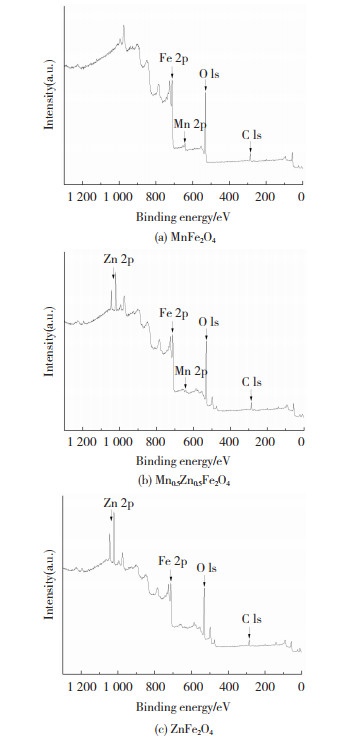
2.2 XPS分析图 2分别为Mn1-xZnxFe2O4(x=0、0.5、1)粉末的光电子全谱图。以285 eV处的碳C 1s峰作为电荷校正的参考值[12],碳主要来源于吸附颗粒表面乙酸根和乙二醇。由图 2可知,除C 1s外,样品的主要峰为Fe 2p、Mn 2p、Zn 2p和O 1s,对应的结合能峰值分别集中在715、641、1 030和530 eV处,其中x=0时,不存在Zn 2p,而x=0.1时,不存在Mn 2p,且随名义Zn含量的增加,相应Zn信号强度增加而Mn信号减弱至消失,与实际相符。
|
图 2 Mn1-xZnxFe2O4的XPS全谱 Fig.2 XPS full spectrum of Mn1-xZnxFe2O4 |
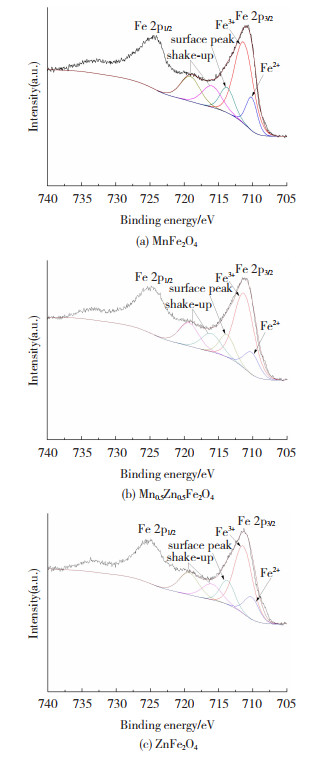
图 3分别为Mn1-xZnxFe2O4(x=0、0.5、1)粉末拟合后的Fe元素精细谱,可以看到,Fe 2p芯能级由相差约13 eV的Fe 2p3/2和Fe 2p1/2两个峰组成,均为非对称结构,其中Fe 2p3/2的结合能分别位于710.7、710.2和711.1 eV。根据拟合发现,Fe 2p3/2由表面峰、Fe3+峰和Fe2+峰组成,其中较高结合能的表面峰是由于颗粒表面阳离子配位数的减少,而被较低的电子密度所包围,需要更多的能量来产生光电子引起的[13],另外,在Fe3+和Fe2+峰高约8.0和6.0 eV处有各自的shake-up卫星峰[14],说明溶剂热合成的铁氧体中Fe离子具有类似于Fe3O4的混合价态,证明Fe2+的存在,但其峰值比Fe3O4中Fe2+在709.5 eV的结合能均高约0.6 eV,这可能是由于尖晶石中四面体A位和八面体B位相邻O-的间距不同导致,Fe3O4为反尖晶石结构,Fe2+处于B位,较A位而言,与O-的间距更长,结合能更低,少量Fe2+占据A位可能是导致结合能升高的原因[15]。根据拟合峰的面积比值,Fe3+与Fe2+的原子量比分别为80.2:19.8、81.7:18.3和79.2:20.8,均接近4:1,说明不同Zn含量对Fe2+的产生和占比几乎没有影响。
|
图 3 Mn1-xZnxFe2O4的Fe 2p芯能级图 Fig.3 Fe 2p core level spectra of Mn1-xZnxFe2O4 |
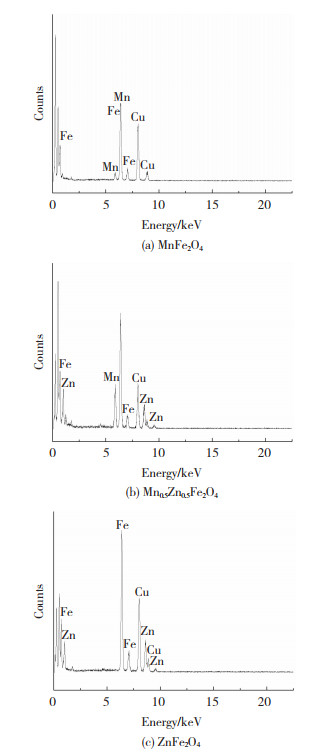
图 4分别为溶剂热合成的Mn1-xZnxFe2O4(x=0、0.5、1)粉末TEM照片,可以看到,3组粉末大部分为近球形微粒,这是由于EG作为非水溶剂,具有更大的黏度,更少的配位羟基,导致晶体成核和生长较慢[16]。另外,PEG-200也能防止晶体形核后生长,使其在热力学主导下,形成纳米晶。为达到表面能的最小化,纳米晶是通过原子间的相互作用,在较高黏度的溶剂中缓慢聚集,最后形成近球形的团聚颗粒,粒径分别约为95、90和82 nm。图 5分别为Mn1-xZnxFe2O4(x=0、0.5、1)粉末的能谱图,可以看到,样品中的金属元素与实际相符,无其他杂质元素出现,其中Cu产生于双联铜网。

|
图 4 Mn1-xZnxFe2O4的TEM形貌 Fig.4 TEM images of Mn1-xZnxFe2O4 |
|
图 5 Mn1-xZnxFe2O4的EDS能谱图 Fig.5 EDS of Mn1-xZnxFe2O4 |
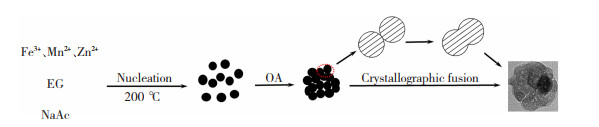
图 6(a)~(c)为相应图 4(a)~(c)颗粒边缘的高分辨TEM图以及衍射花样,可以看到,在包含不同聚集纳米晶的情况下,衍射花样依然为单晶性质。说明在缓慢的聚集过程中,纳米晶可通过充分的旋转取向完成OA,其结果即是产生取向一致与OR类似的单晶生长形式。由于纳米晶进行OA后,在未开始自我再结晶整合的情况下,纳米晶各自将无法消除聚集后产生的孔隙,从图 4(a)~(c)中选取的放大颗粒形貌可以清楚地看出存在的差异,并反应颗粒自我整合的程度。图 4(a)状态可以认为是OA后整合的初期,聚集颗粒表面不平整且纳米晶可大致分辨。图 4(b)状态为整合中期,表面趋于光滑但内部存在孔隙。图 4(c)状态为整合后期,孔隙减小或消失。说明提高Zn2+含量可促进整个OA生长阶段的进程,其原因可能是由于Zn2+—O2-(150.6 kJ/mol)的键能比Mn2+—O2-(946 kJ/mol)小[17-18],加快了晶粒表面悬挂键的连接。综合上述分析,发现在溶剂热环境下,通过单体沉积形核的初始纳米晶在经过OA过程的取向性团聚后,由于附着处的曲率半径为负,可通过缓慢的自我整合逐步消除界面[19],最终形成较致密的近球形颗粒,如图 7所示。

|
图 6 Mn1-xZnxFe2O4的高分辨TEM和衍射花样图 Fig.6 HRTEM and SADP patterns of Mn1-xZnxFe2O4 |
|
图 7 颗粒的定向附着生长示意图 Fig.7 Sketch of oriented attachment growth of particles |
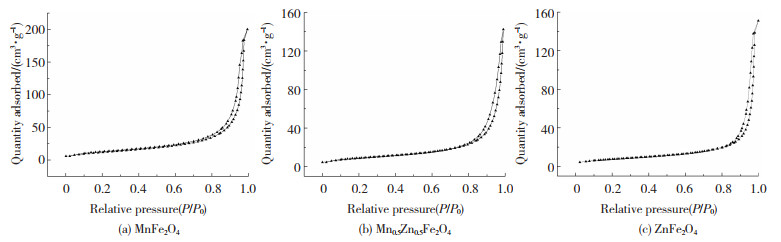
另外,根据图 8的Mn1-xZnxFe2O4(x=0、0.5、1)粉末氮吸附-脱附等温曲线所示,三者均为Ⅳ型等温线,具有H3回滞环特征,说明近球形颗粒存在由多个纳米晶聚集堆积而产生的孔隙。三者测得的BET比表面分别为45.14、32.54和27.84 m2/g,比表面积随Zn2+含量增加而减小,说明Zn2+的存在有利于颗粒体系的表面积最小化,侧面反应其具有加快颗粒生长的作用,与TEM图结果相符。
|
图 8 样品的N2吸附-脱附等温线 Fig.8 N2 adsorption-desorption isotherm of samples |
1) 采用溶剂热的方法合成尖晶石型Mn1-xZnxFe2O4(x=0、0.5、1)纳米颗粒, 其样品粉末均为尖晶石结构,晶粒度随Zn含量增加而增大,部分Fe3+还原为Fe2+,含量比约为4:1,导致衍射峰均向右偏移。
2) 尖晶石型Mn1-xZnxFe2O4(x=0、0.5、1)纳米颗粒形貌大部分为近球形,其依靠纳米晶之间的OA和自整合形成,并随着Zn2+的增加,促进了颗粒整个OA生长过程,导致比表面积减小。
| [1] |
KEFENI K K, MSAGATI T A M, MAMBA B B. Ferrite nanoparticles: Synthesis, characterisation and applications in electronic device[J]. Mater Sci Eng B, 2017, 215: 37-55. DOI:10.1016/j.mseb.2016.11.002 |
| [2] |
伍水生, 马博凯, 贾庆明, 等. 可磁分离的镍锌铁氧体-石墨烯复合材料的制备及其光催化性能[J]. 无机化学学报, 2016, 32(4): 561-566. WU Shuisheng, MA Bokai, JIA Qingming, et al. Synthesis and photocatalytic properties of magnetically separated Ni-Zn ferrite-graphene nanocomposite[J]. Chinese J Inorg Chem, 2016, 32(4): 561-566. DOI:10.11862/CJIC.2016.094 |
| [3] |
ADEOGUN A I, KAREEEM S O, ADEBAYO O S. Comparative adsorption of amylase, protease and lipase on ZnFe2O4 kinetics, Iisothermal and thermodynamics studies[J]. Biotech, 2017, 7(3): 198. DOI:10.1007/s13205-017-0859-6 |
| [4] |
ISMAIL F M, RAMADAN M, ABDELLAH A M, et al. Mesoporous spinel manganese zinc ferrite for high-performance supercapacitors[J]. J Electroanal Chem, 2018, 817: 111-117. DOI:10.1016/j.jelechem.2018.04.002 |
| [5] |
ENOCH I V M V, RAMASAMY S, MOHIYUDDIN S, et al. Cyclodextrin-PEG conjugate-wrapped magnetic ferrite nanoparticles for enhanced drug loading and release[J]. Appl Nanosci, 2018, 8: 273-284. DOI:10.1007/s13204-018-0798-5 |
| [6] |
WANG J, REN F, YI R, et al. Solvothermal synthesis and magnetic properties of size-controlled nickel ferrite nanoparticles[J]. J Alloy Compd, 2009, 479(1-2): 791-796. DOI:10.1016/j.jallcom.2009.01.059 |
| [7] |
TONTO P, MEKASUWANDUMRONG O, PHATANASRI S, et al. Preparation of ZnO nanorod by solvothermal reaction of zinc acetate in various alcohols[J]. Ceram Inter, 2008, 34(1): 57-62. DOI:10.1016/j.ceramint.2006.08.003 |
| [8] |
CAO S W, ZHU Y J. Monodisperse α-Fe2O3 mesoporous microspheres: one-step NaCl-assisted microwave-solvothermal preparation, size control and photocatalytic property[J]. Nanoscale Res Lett, 2011, 6: 1. DOI:10.1007/s11671-010-9742-7 |
| [9] |
ARUMUGAM J, RAJ A D, IRUDAYARAJ A A, et al. Solvothermal synthesis of Bi2S3 nanoparticles and nanorods towards solar cell application[J]. Mater Lett, 2018, 220: 28-31. DOI:10.1016/j.matlet.2018.02.123 |
| [10] |
ZENG C H. Synthesis and self-assembly of complex hollow materials[J]. J Mater Chem C, 2011, 21: 7511-7526. DOI:10.1039/C1JM10499C |
| [11] |
LI S, ZHANG T, TANG R, et al. Solvothermal synthesis and characterization of monodisperse superparamagnetic iron oxide nanoparticles[J]. J Magn Magn Mater, 2015, 379: 226-231. DOI:10.1016/j.jmmm.2014.12.054 |
| [12] |
YAMASHITA T, HAYES P. Analysis of XPS spectra of Fe2+ and Fe3+ ions in oxide materials[J]. Appl Surf Sci, 2008, 254(8): 2441-2449. DOI:10.1016/j.apsusc.2007.09.063 |
| [13] |
GROSVENOR A P, KOBE B A, BIESINGER M C, et al. Investigation of multiplet splitting of Fe 2p XPS spectra and bonding in iron compounds[J]. Surf Interface Anal, 2004, 36(12): 1564-1574. DOI:10.1002/sia.1984 |
| [14] |
ZHANG L, WU Y. Sol-Gel synthesized magnetic MnFe2O4 spinel ferrite nanoparticles as novel catalyst for oxidative degradation of methyl orange[J]. J Nanomater, 2013, 640940. DOI:10.1155/2013/640940 |
| [15] |
MITTAL V K, CHANDRAMOHAN P, BERA S, et al. Cation distribution in NixMg1-x-Fe2O4 studied by XPS and Mössbauer spectroscopy[J]. Solid State Communications, 2006, 137(1): 6-10. DOI:10.1016/j.ssc.2005.10.019 |
| [16] |
DUAN L, JIA S, ZHAO L. Study on morphologies of Co microcrystals produced by solvothermal method with different solvents[J]. Mater Res Bull, 2010, 45(4): 373-376. DOI:10.1016/j.materresbull.2010.01.002 |
| [17] |
WEI Y, KIM K B, CHEN G. Evolution of the local structure and electrochemical properties of spinel LiNixMn2-xO4 (0≤ x≤ 0.5)[J]. Electrochim Acta, 2006, 51(16): 3365-3373. DOI:10.1016/j.electacta.2005.09.035 |
| [18] |
INOUE T, HONMA T, DIMITROV V, et al. Approach to thermal properties and electronic polarizability from average single bond strength in ZnO-Bi2O3-B2O3 glasses[J]. J Solid State Chem, 2010, 183(12): 3078-3085. DOI:10.1016/j.jssc.2010.10.027 |
| [19] |
PAN Y, LYU W, NIU Y, et al. Initial-stage oriented-attachment one-dimensional assembly of nanocrystals: fundamental insight with a collision-recrystallization model[J]. Rsc Adv, 2015, 5(67): 54605-54612. DOI:10.1039/C5RA08796A |
 2020, Vol. 28
2020, Vol. 28


