石墨氮化碳(g-C3N4)作为一种不含金属的聚合物光催化纳米材料在光催化降解有机物、产氢、重金属离子处理以及CO2还原等方面有着潜在的应用价值[1]。但一些重要的限制因素,如低表面积、有限的光吸收和量子受限效应已成为其光催化性能进一步提高的重要障碍,为此人们引入了能带结构工程、掺杂、缺陷和异质结/复合材料等多样化的调制技术和方法,以拓宽其应用前景。
其中,通过元素掺杂进行的带隙工程被认为是调制其光学和电子特性的成功方法[2]。通过金属元素、非金属元素或共掺杂,可以很容易的设计带隙,以增强捕获光的能力和调整所需的光催化氧化还原反应的带边电位[3]。最近,元素掺杂的g-C3N4在光催化领域的光催化降解性能引起了研究人员的极大兴趣并取得了丰富的成果[3]。通过增加掺杂剂浓度或带隙中引入杂质能级,吸收边缘会发生红移并改变电子特性,以优化光吸收和电荷转移动力学。
相比金属元素掺杂,以P、S、O等元素为主的非金属元素更具优势。一方面,非金属元素掺杂g-C3N4基光催化剂的设计有大量可用的前驱体,没有任何二次污染。整个过程不仅简单且具有成本效益,而且需要相对较短的处理时间,因此,该方法具有大规模应用的可持续性;另一方面,非金属元素离子由于其高电负性和高电离能,通常可以通过从其他化合物获得电子而形成共价键,且掺杂后的g-C3N4仍然是无金属半导体化合物[3]。最近,人们开始关注B掺杂g-C3N4体系的光催化活性研究。B的缺电子特性有利于g-C3N4表面的电子和空穴对的分离,满足光氧化还原反应的基本要求。B的缺电子性质为电子离域化提供了空p轨道,加速了g-C3N4层中的电子通道化。赵大明等[4]通过在惰性气氛中煅烧g-C3N4与NaBH4成功制备了B-掺杂且含N-缺陷的g-C3N4材料,获得了高达561.2 μmol /(h ·g)的光催化产氧速率。Lu等[5]报道了用热缩聚法从硫脲和硼酸的混合物中制备掺B的g-C3N4以有效去除UO22+的研究成果。
可以看到,很多B掺杂的g-C3N4光催化剂,要么采用尿素或硫脲作为前驱体导致g-C3N4产量低[6],要么合成方法过于繁琐(两步法)[7]。煅烧三聚氰胺获得的g-C3N4产率高、成本低,可以大规模生产,缺点是所制备的g-C3N4较厚,导致比表面积小,而这种不足可以通过引入硼酸作为B源而得到部分解决。在热聚合过程中,由于硼酸的分解温度和H2O的挥发温度保持在相同的范围内,硼酸的引入有助于使材料形成多孔,这会增大比表面积。本文以三聚氰胺和硼酸为前驱体,采用煅烧法一步合成B掺杂g-C3N4光催化剂。对该光催化剂的结构、形貌和光学性能进行了表征,通过罗丹明B(RhB)和四环素(TC)的降解实验对光催化剂的光催化降解性能进行研究,本工作可提供一种在可见光下具有良好稳定性的有机物降解光催化剂。
1 实验 1.1 制备方法 1.1.1 纯g-C3N4(CN)制备将10 g三聚氰胺加入到100 mL去离子水中,搅拌1 h后,放入干燥箱中,60 ℃下干燥24 h。将干燥后的物体进行充分研磨,放入马弗炉中,以2 ℃/min的速率加热到500 ℃,保温4 h。随炉冷却到室温,研磨产物,得到淡黄色的g-C3N4粉末。
1.1.2 B掺杂g-C3N4(BCN)制备将0.05 g硼酸(H3BO3)加入到100 mL去离子水中,再加入10 g三聚氰胺,先超声30 min,再整体搅拌30 min。放入干燥箱中,60 ℃下干燥24 h。随后步骤与g-C3N4制备方法相同。最终得到黄色产物记为0.05BCN。为进行对照实验,同时制备了一系列不同硼酸比例的复合物,分别记为0.03BCN、0.1BCN、0.2BCN、0.3BCN和0.6BCN。
1.2 光催化降解实验光催化降解实验中采用300 W氙灯作为照射光源,配备光截止滤光片(λ>420 nm)模拟日光。将50 mg催化剂分别分散在60 mL,质量浓度都为10 mg/L的RhB和TC水溶液中。在照射前,溶液要在暗室中搅拌30 min以达到吸附-脱附平衡。每隔5 min,取出4 mL悬浮液。
光降解效率(E)由下式得到
| $ E=\left(1-\frac{c}{c_1}\right) \times 100 \%=\left(1-\frac{A}{A_1}\right) \times 100 \% $ | (1) |
动力学常数(k)由以下公式得到
| $ -\ln \left(\frac{c}{c_0}\right)=k t $ | (2) |
式中:c为RhB在不同时间的质量浓度;c1为RhB的初始质量浓度;c0为吸附平衡后的RhB的初始质量浓度;A和A1为对应的吸光度。
1.3 表征方法采用Cu Kα辐射(λ=0.154 06 nm) X射线衍射仪(XRD,Rigaku)对其晶体结构和物相组成进行表征。利用X射线光电子能谱(XPS,Thermo ESCALAB 250Xi)分析催化剂的化学组成、界面键合和价态。利用傅里叶变换红外光谱(FT-IR, Nicolet 6700)分析分散在KBr中的样品,以确定催化剂中官能团的种类及其周围化学环境。利用高分辨透射电子显微镜(HTEM, JEM-2100HR)观察样品形貌和晶格条纹。利用紫外-可见漫反射光谱(UV-Vis DRS, 日本岛津UV-2600)分析样品光吸收特性,以标准BaSO4粉末为参比。
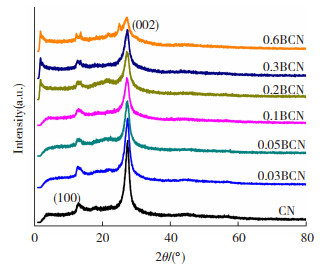
2 结果与讨论 2.1 结构、形貌和光学性能纯g-C3N4和不同掺杂量BCN样品的XRD谱图如图 1所示。由图 1可见,g-C3N4的XRD谱图有两个明显的衍射峰,27.4°的高角度(002)衍射峰,对应于芳香材料的层间堆积,而13.1°的低角度(100)衍射峰对应三嗪环结构面内堆积序。与纯g-C3N4相比,低掺杂下的BCN样品的晶面衍射峰基本与纯g-C3N4一致,说明B掺杂没有改变g-C3N4的晶体结构。随着掺杂量的增加,两个衍射峰强度逐渐减小,这是由于掺杂引起的无序度增加和结晶度降低所致[8]。基于衍射峰位置可以计算出,g-C3N4的层间距d=0.335 nm,0.05BCN的层间距d=0.376 nm,掺杂后的层间间距增加是由于B的掺杂半径大于N或C而对石墨层状结构的扰动造成的。当B掺杂量达到0.6 g时,可以观察到在24.9°左右存在明显的杂质峰,表明B掺杂只适合低掺杂浓度。
|
图 1 g-C3N4与BCN的XRD谱图 Fig.1 XRD patterns for g-C3N4 and BCN |
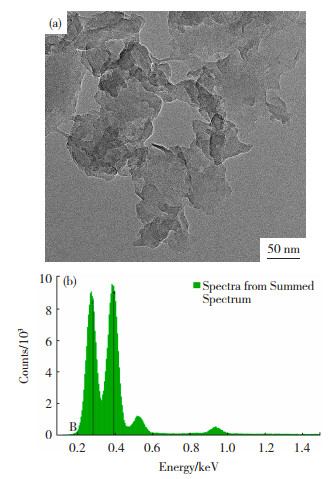
图 2(a)显示的是0.05BCN样品的TEM图,可以清楚的看到多层且不规则的絮状结构。絮状结构表明样品较薄,这种较薄纳米片结构有助于加速电荷的转移和分离。同时孔结构可以缩短光生电荷从体相到表面的扩散迁移距离,从而抑制内部光生电荷的重组。EDX能谱分析(图 2(b))显示了0.05BCN样品中存在C、N和O元素,而B元素的峰值较为微弱,这可能跟B的掺杂量太小有关。
|
图 2 0.05BCN样品的TEM图(a)和EDX图(b) Fig.2 TEM image(a) and EDX image(b)of 0.05BCN |
为了证实掺杂样品中B元素的存在,利用XPS对0.05BCN样品的化学组成和价态进行了鉴定。图 3(a)给出了0.05BCN光催化剂的XPS全谱图,清晰的显示掺杂样品中含有N、C、B和O 4种元素,其中O是样品暴露在空气中所致。

|
图 3 0.05BCN样品的元素分析全谱(a)、N1s(b)、C1s(c)和B1s(d) Fig.3 XPS spectra of survey spectra (a), N1s (b), C1s (c), and B1s (d) for 0.05BCN |
从图 3(b)可以看出,0.05BCN样品的N1s谱可分为398.4、399.4、400.6和404.3 eV 4个特征峰,分别对应于三嗪环的吡啶氮(C=N —C)、叔氮桥连的氮原子N-(C)3、氨基官能团中的氮原子(C—N—H)和π激发[9]。C1s谱(图 3(c))中的两个峰集中在284.6和288.1 eV处,分别归属于不定型碳(C—C/ C=C)和三-s-三嗪环中sp2杂化碳的特征峰(N— C=N)[10],其中288.1 eV处特征峰是BCN样品中的碳的主要特征峰。B1s高分辨谱图(图 3(d))中可以清晰的看到位于191.7 eV处的特征峰,源于B原子掺杂替代形成的N— B=N键[6],由此表明B原子在g-C3N4网状骨架上成功植入。
FT-IR测量进一步证实B在g-C3N4中的掺杂,如图 4(a)所示,并可观察到B掺杂对g-C3N4结构的影响。掺杂样品的化学骨架均与g-C3N4相似,1 200~1 700 cm-1范围内的强红外信号属于C—N和C=N杂环的典型拉伸振动[11],而808 cm-1和3 150~3 600 cm-1处的峰值分别与三嗪单元和N—H或C—OH的拉伸振动有关。掺杂样品在1 358 cm-1左右出现的一个吸收峰对应于BCN样品中形成的B—N键[12]。

|
图 4 g-C3N4和掺杂BCN样品的FT-IR图(a) 和图(a)阴影部位放大图(b) Fig.4 FT-IR spectra of g-C3N4 and BCN samples (a) and partial enlarged view of Fig.(a) (b) |
图 4(b)为图 4(a)中阴影部位的放大图,可以清楚的观察到1 358 cm-1处的峰发生了明显的偏移,当掺杂量达到0.3 g时,峰值为1 350 cm-1。由于其位置与g-C3N4的C—N杂环的拉伸振动有重叠,因此峰值变化较不明显,认为B—N键的形成是造成偏移的主要原因。还可发现B掺杂后,808 cm-1处的峰值变弱,表明三嗪重复单元的聚合度降低。此外,这些基团的氮元素含量也有所降低,表明在g-C3N4中成功实现了B掺杂。
图 5显示的是系列样品的光学吸收曲线。纯g-C3N4的吸收边约为464 nm,BCN的吸收边发生了明显的红移导致样品颜色略微加深,这是因为B掺杂引起价带边的上移导致带隙变窄。带隙测量发现(图 5中插图),0.05BCN样品的带隙为2.69 eV,0.3BCN样品的带隙只有2.62 eV,都明显小于纯g-C3N4的带隙2.74 eV。另外,掺杂样品吸收曲线的尾部隆起意味着可见光吸收的增强,这可能跟带隙中引入杂质能级有关。总之,掺杂样品相对于纯g-C3N4在400~800 nm之间的光吸收增强有利于更多光生载流子的产生。此外,BCN样品仍然呈现出弱吸收尾,Yan等[9]将此吸收尾归因于一些B原子掺杂到g-C3N4网络中而产生的结构缺陷。随着B含量的增加,BCN的吸收尾增强,其中0.3BCN样品的吸收尾最大,带隙最小,表明其结构缺陷量最大。

|
图 5 g-C3N4和BCN的UV-Vis曲线 Fig.5 UV-vis curves of g-C3N4 and BCN |
可见光照射下,将所制备的g-C3N4和不同掺杂量的BCN样品在相同条件下进行RhB光催化降解实验,降解曲线如图 6(a)所示。

|
图 6 g-C3N4和BCN样品的RhB降解曲线(a)和动力学常数分析(b) Fig.6 Degradation curves of RhB in the presence of BCN and g-C3N4 (a) and kinetic constant analysis(b) |
从图 6(a)可以看出,BCN样品的降解效率要明显优于g-C3N4,说明了B掺杂可以大大的提高材料在可见光下的光催化效率。g-C3N4、0.05BCN和0.3BCN在40 min下对RhB的降解效率分别为44.3%、100%和76.7%。其中,0.05BCN的降解效果最好,25 min降解达到90.8%,30 min降解即达到100%。
采用Langmiur-Hinshelwood模型,利用积分法将降解数据进行拟合处理,经一级拟合后的相关系数最好,结果如图 6(b)所示。ln(c/c0)随时间的变化呈线性关系,说明RhB溶液的降解符合一级反应动力学规律。根据公式(2),可得表观反应速率常数k[13]。0.05BCN样品的动力学常数k值为0.104 22 min-1,是纯g-C3N4(0.014 84 min-1)的7倍。掺杂后材料的光催化效率高于纯g-C3N4,说明掺杂材料的光催化性能优于单体g-C3N4。
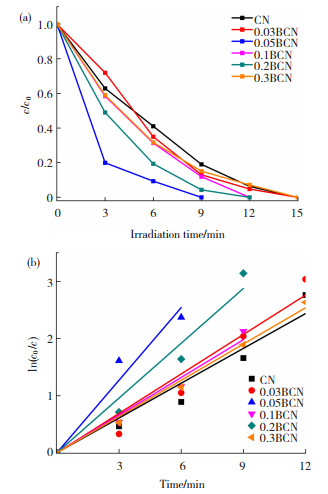
所制备光催化剂不仅对RhB降解较快,其另一个优点就是降解多样性。图 7(a)显示了所制备样品的TC光催化活性。可以清晰的看出,B掺杂后,样品的催化性能得到了显著的提升,其中最佳催化剂0.05BCN在9 min内对TC的降解效率达到了100%。
|
图 7 g-C3N4和BCN样品的TC降解曲线(a)和动力学常数分析(b) Fig.7 Degradation curves of TC in the presenceof BCN and g-C3N4(a) and kinetic constant analysis (b) |
由图 7(b)得出其动力学常数,经计算,0.05BCN样品的动力学常数k值(0.423 35 min-1)为g-C3N4(0.202 96 min-1)的2.09倍。由于RhB和TC是两种不同类型的物质,因此实验结果可表明所制备的0.05BCN光催化剂具有普遍的适用性。
BCN样品光催化性能的提升除了跟可见光吸收增加有关,还跟载流子动力学密切相关。为了深入研究BCN样品中电荷载流子转移和分离效率,进行了瞬态光电流响应和电化学阻抗谱(EIS)测试。如图 8(a)所示,BCN样品的光电流要高于g-C3N4,0.05BCN样品的光电流密度约为纯g-C3N4的1.3倍,表明B掺杂可以诱导有效的光致载流子分离。图 8(b)为纯g-C3N4和不同B掺杂样品的EIS曲线。0.05BCN样品的Nyquist半径明显小于g-C3N4以及其它掺杂样品的半径,表明其电导率增强,有望提高可见光照射下光诱导电子-空穴对的转移和分离效率,这一结果与光电流测量结果一致,证实了B的缺电子特性有利于g-C3N4表面的电子和空穴对的分离,富电子原子N被缺电子原子B取代,为电子离域化提供了空p轨道,加速了电荷的传输。

|
图 8 g-C3N4和BCN样品的光电流分析(a)和阻抗分析(b) Fig.8 Transient photocurrent responses(a) and Nyquist plots (b) of g-C3N4 and BCN |
半导体复合光催化剂的光催化性能增强的常见因素包括可见光吸收范围的增加、光生载流子复合的抑制以及比表面积提高导致活性位点的增加。为此,我们分别测量了CN、0.05BCN和0.3BCN样品的比表面积(SBET)的变化,如图 9所示。经测量CN、0.05BCN和0.3BCN的比表面积分别为4.35、4.21和1.69 m2/g。B掺杂并未导致比表面积的显著增加,甚至掺杂样品0.05BCN虽然表现出较高的光催化活性,但是比表面积比纯CN反而小了0.14 m2/g左右,表明比表面积并不是掺杂样品光催化活性增强的主要原因。

|
图 9 比表面积实验 Fig.9 Specific surface area experiment |
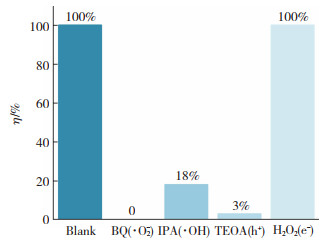
在自然光下,RhB降解发生,说明BCN样品对于RhB的降解是光催化作用,而不是染料的自敏化过程。通常,光催化反应会产生羟基自由基(·OH)和超氧离子(·O2-)两种活性基质[14],为了检测活性物质在光催化中的作用,在光催化反应体系中加入了不同的牺牲剂,测试了不同牺牲剂作为探针对0.05BCN样品降解RhB的去除率, 实验结果如图 10所示。
|
图 10 自由基捕获实验 Fig.10 Free radical trapping implementation |
采用过氧化氢(H2O2,10 mL)、三乙醇胺(TEOA,10 mL)、苯醌(BQ,10 mg)和异丙醇(IPA,10 mL)分别清除电子(e-)、空穴(h+)、超氧自由基(·O2-)和羟基自由基(·OH)[15]。如图 10所示,添加BQ、IPA和TEOA显著抑制RhB的降解,表明RhB降解的关键的降解活性物质为h+、·OH和·O2-,而e-不起作用。光降解实验表明,RhB光催化降解的主要原因是光照引成的空穴氧化和电子还原过程。与纯g-C3N4相比,BCN样品对RhB的降解活性提高。在0.05BCN样品中,B的掺杂使得g-C3N4的带隙从2.74 eV减小到2.69 eV,带隙减小和中间态杂质能级引入都可以增加光吸收,再加上B掺杂引起的电子通道效应,这些都有利于光降解反应的发生。
3 结论本文通过煅烧法制备了B掺杂g-C3N4材料,基于结构表征和光学性能测试,得出以下结论。
1) B掺杂的促进作用分别源于缺陷的产生和电子迁移能力的提高。
2) B掺杂后,g-C3N4的禁带宽度明显减小,扩大了材料的光谱响应范围,提高了光能利用率。且比表面积并不是掺杂样品光催化活性提高的主要因素。
3) 在可见光照射下,B掺杂g-C3N4相比纯g-C3N4光催化能力有明显提高,降解RhB和TC溶液的表观反应速率常数约是纯g-C3N4的7倍和2.09倍。
4) 经自由基捕获测试表明RhB关键的降解活性物质为h+、·OH和·O2-,而e-不起作用。
| [1] |
SEYED M S, AMANI-GHADIM A R, RASOULIFARD M H. Photocatalytic activity of g-C3N4: An empirical kinetic model, optimization by neuro-genetic approach and identification of intermediates[J]. Chemical Engineering Research and Design, 2017, 127: 113-125. DOI:10.1016/j.cherd.2017.09.012 |
| [2] |
董鹏玉, 奚新国. 可见光响应光催化材料[M]. 北京: 科学出版社, 2016: 116-118.
|
| [3] |
PATNAIK S, SAHOO D P, PARIDA K. Recent advances in anion doped g-C3N4 photocatalysts: A review[J]. Carbon, 2021, 172: 682-711. DOI:10.1016/j.carbon.2020.10.073 |
| [4] |
ZHAO Daming, DONG Chunglin, WANG Bin, et al. Synergy of dopants and defects in graphitic carbon nitride with exceptionally modulated band structures for efficient photocatalytic oxygen evolution[J]. Advanced Materials, 2019, 31: 1903545. DOI:10.1002/adma.201903545 |
| [5] |
LU Changhai, CHEN Rongyue, WU Xi. Boron doped g-C3N4 with enhanced photocatalytic UO22+ reduction performance[J]. Applied Surface Science, 2016, 360: 1016-1022. DOI:10.1016/j.apsusc.2015.11.112 |
| [6] |
QI Kezhen, CUI Nan, ZHANG Manjie. Ionic liquid-assisted synthesis of porous boron-doped graphitic carbon nitride for photocatalytic hydrogen production[J]. Chemosphere, 2021, 272: 129953. DOI:10.1016/j.chemosphere.2021.129953 |
| [7] |
ZHAO Daming, WANG Yiqing, DONG Chungli. Boron-doped nitrogen-deficient carbon nitride-based Z-scheme heterostructures for photocatalytic overall water splitting[J]. Nature Energy, 2021, 6(4): 388-397. DOI:10.1038/s41560-021-00795-9 |
| [8] |
CHEN Lin, WANG Yixuan, CHENG Shuai. Nitrogen defects/boron dopants engineered tubular carbon nitride for efficient tetracycline hydrochloride photodegradation and hydrogen evolution[J]. Applied Catalysis B: Environmental, 2022, 303: 120932. DOI:10.1016/j.apcatb.2021.120932 |
| [9] |
YAN S C, LI Z S, ZOU Z G. Photodegradation of rhodamine B and methyl orange over boron-doped g-C3N4 under visible light irradiation[J]. Langmuir, 2010, 26(6): 3894-3901. DOI:10.1021/la904023j |
| [10] |
SHE Xiaojie, LIU Liang, JI Haiyan. Template-free synthesis of 2D porous ultrathin nonmetal-doped g-C3N4 nanosheets with highly efficient photocatalytic H2 evolution from water under visible light[J]. Applied Catalysis B: Environmental, 2016, 187: 144-153. DOI:10.1016/j.apcatb.2015.12.046 |
| [11] |
ZHAO Jingli, LIU Yushan, WANG Yaping. Boron doped graphitic carbon nitride dots dispersed on graphitic carbon nitride/graphene hybrid nanosheets as high performance photocatalysts for hydrogen evolution reaction[J]. Applied Surface Science, 2019, 470: 923-932. DOI:10.1016/j.apsusc.2018.11.138 |
| [12] |
CHEN Pengfei, XING Pingxing, CHEN Zhiqiang. Rapid and energy-efficient preparation of boron doped g-C3N4 with excellent performance in photocatalytic H2-evolution[J]. International Journal of Hydrogen Energy, 2018, 43: 19984-19989. DOI:10.1016/j.ijhydene.2018.09.078 |
| [13] |
SALOMONE V N, MEICHTRY J M, ZAMPIERI G. New insights in the heterogeneous photocatalytic removal of U(Ⅵ) in aqueous solution in the presence of 2-propanol[J]. Chemical Engineering Journal, 2015, 261: 27-35. DOI:10.1016/j.cej.2014.06.001 |
| [14] |
YAN S C, LI Z S, ZOU Z G. Photodegradation performance of g-C3N4 fabricated by directly heating melamine[J]. Langmuir, 2009, 25(17): 10397-10401. DOI:10.1021/la900923z |
| [15] |
LI Yuanzhi, CHEN Changzhao, CHEN Xinxin. MoO3/g-C3N4 heterostructure for degradation of organic pollutants under visible light irradiation: High efficiency, general degradation and Z-scheme degradation mechanism[J]. Ceramics International, 2021, 47(23): 33697-33708. DOI:10.1016/j.ceramint.2021.08.279 |
 2023, Vol. 31
2023, Vol. 31


