2. 哈尔滨工业大学 化工与化学学院,哈尔滨 150001
2. School of Chemistry and Chemical Engineering, Harbin Institute of Technology, Harbin 150001, China
为应对能源危机同时实现可持续发展,开发和利用绿色能源正成为人类社会发展的理想选择。氢能作为一种可再生的绿色能源,具有高燃烧值、无污染、燃烧产物仅为水的特点,因而受到世界各国研究人员的广泛关注。传统的制氢方法包括电化学分解水、化石燃料气化、生物质热解和蒸汽重整等,存在高能耗和污染环境等缺点。相反,光催化制氢可以解决上述问题。Fujishima和Honda在1972年首次报道了TiO2在紫外光照射下可分解水产生氢气。然而,TiO2低的产氢效率及较大的禁带宽度限制了其广泛应用。因此,开发高效稳定的光催化剂用于光催化制氢一直是当代科学研究的热点之一。
近年来,由于纳米二氧化钛具有优异的光学和电学性质、强的氧化还原能力、无毒、低成本、抗光腐蚀和化学腐蚀的长期稳定性等优点,使得TiO2的制备、表征和改性一直是其光电化学和光催化研究过程的主要内容[1-3]。在设计高效TiO2半导体光催化剂的过程中,研究者采用了许多有效的方法[4-5],例如:在TiO2催化剂上负载Pt等贵金属用于提高其电子-空穴对的分离效率;利用催化剂的量子尺寸效应提高材料的量子产率;通过金属或非金属元素对TiO2催化剂进行改性或复合,以减小跃迁带隙或形成杂质能级等。同时,TiO2催化剂被设计成多层、多孔或核壳结构,以提高其比表面积或利用不同催化剂的协同效应。根据催化剂的结构,TiO2催化剂的发展趋势可以简单地划分为从纳米粉末分散于水中形成的悬浮液到固定化,即支撑或锚定在惰性载体(多孔玻璃、二氧化硅、沸石)和薄膜催化剂。
许多制备方法如溶胶-凝胶法、溶剂热法、火焰喷涂法、射频磁控溅射法等[6-9]被用于TiO2的制备。其中,等离子体电解氧化(PEO)是一种在电解液中通过微等离子体放电和电极表面烧结工艺在钛合金上制备TiO2薄膜催化剂的简便技术。2000年,李晓忠等[10]首次报道了在0.5M H2SO4溶液中阳极氧化Ti网制备Ti/TiO2网状电极,并研究了其在水溶液中光催化氧化和光电催化氧化罗丹明B。Meyer等[11]于有机混合溶液中在钛基体上制备了TiO2薄膜,但相应的催化实验未见报道。Sun等[12]和Bayati等[13]在不同电解液下制备了硫掺杂的TiO2/Ti薄膜,并对其光催化性能进行了评价。综上,此类薄膜催化剂具有催化活性高、表面积大、表面多孔结构等特点。但是,人们更多关注的是光催化氧化的效果。Yao等[14-15]曾通过PEO方法制备了掺杂Zn和掺杂Ni的TiO2/Ti薄膜催化剂,并探究了其光催化(PC)还原性能。
目前,尽管也有相同的证据表明V掺杂会导致相反的性能[16],但许多文献[17-20]普遍认为,钒掺杂或与V2O5复合是提高二氧化钛光活性的一种很有前景的策略。本文在磷酸盐溶液中,采用PEO法在TA1上制备了TiO2/V2O5复合薄膜光催化剂,并对其结构、光学性质以及在Na2S+Na2SO3溶液中催化分解产氢进行了讨论。
1 实验 1.1 膜层催化剂制备以钛片(纯度> 99.6%)作为工作电极,不锈钢电解槽作为对电极, 采用国产5 kW大功率脉冲单极PEO电源于不同电解液体系下反应10 min,实现钛片表面PEO膜层的制备。电解液体系中含有4.8 g/L (NaPO3)6、10 g/L Na2SO4和不同质量浓度的NH4VO3。工作频率为2 000 Hz,峰值电流密度为2 A/cm2。通过调节冷却水流量,将反应温度控制在30 ℃以下。反应结束后,将PEO膜层样品用水冲洗并在空气中干燥。本研究中使用的所有物质均为分析纯,无需进一步纯化即可使用。所有实验均使用去离子水。
1.2 膜层催化剂表征采用扫描电镜(SEM, JSM-6480A,日本)研究膜层催化剂形貌。利用能谱仪(EDS, JED-2200,日本)分析膜层催化剂中元素的相对含量。采用X射线衍射仪(XRD, D/max-rB, Ricoh, 日本)表征相组成。用X射线光电子能谱仪(XPS, XPhi5700 ESCA, 美国)分析膜层中表面元素组成和价态。利用紫外-可见分光光度计(UV-2400,Shimadzu,日本)记录样品的紫外-可见漫反射(DRS)光谱。
1.3 膜层催化剂的光催化产氢性能光催化实验在含有100 mL Na2S+Na2SO3水溶液的环形石英光化学反应器中进行。该反应器垂直放置,外部固定放置UV-A高压汞灯照射。Na2S和Na2SO3的初始浓度分别为0.1和0.02 mol/L。将膜催化剂(表面积为9 cm2)放置在反应器中间,灯与膜催化剂之间的距离为4 cm,光催化反应期间用磁力搅拌器连续搅拌溶液。在辐照前,对溶液进行氮气吹扫0.5 h,以保证催化剂表面达到充分的吸附平衡。通过气相色谱分析(SP2100A,北分仪器,中国)测量不同时间H2的量。
2 结果及分析 2.1 膜层催化剂的SEM及EDS分析不同NH4VO3浓度制备的膜催化剂呈现不同的颜色。未含NH4VO3所得膜呈蓝灰色,而在含NH4VO3的电解液中制得的膜呈黄褐色,随着NH4VO3浓度的增加,膜的颜色越来越深。图 1为膜催化剂的表面SEM图,可以看出所有薄膜均呈多孔结构,表面分布着许多微孔。当向电解液中加入1 g/L NH4VO3时所得薄膜催化剂膜表面微孔尺寸及数量均增加,而进一步增加NH4VO3质量浓度,膜表面微孔的尺寸进一步增大但数量减少。薄膜颜色的变化说明薄膜的组成和结构也发生了相应的变化。对膜进行EDS能谱分析,EDS能谱分析对应的SEM面扫描位置及结果分别如图 2及表 1所示,可以看出,膜主要由O、Ti和P组成,随着NH4VO3质量浓度的增加,膜中的V元素逐渐增加。

|
图 1 不同质量浓度NH4VO3制备的膜催化剂SEM图 Fig.1 SEM images of film catalysts prepared with different NH4VO3 content: (a) 0 g/L; (b) 1 g/L; (c) 3 g/L; (d) 5 g/L |

|
图 2 EDS能谱分析对应的SEM面扫描位置 Fig.2 EDS spectra analysis corresponding to SEM map scanning position: (a) 0 g/L; (b) 1 g/L; (c) 3 g/L; (d) 5 g/L |
| 表 1 不同质量浓度NH4VO3制备的膜催化剂元素组成(原子分数/%) Table 1 EDS analysis of film catalysts prepared without and with different dosages of NH4VO3 (at.%) |
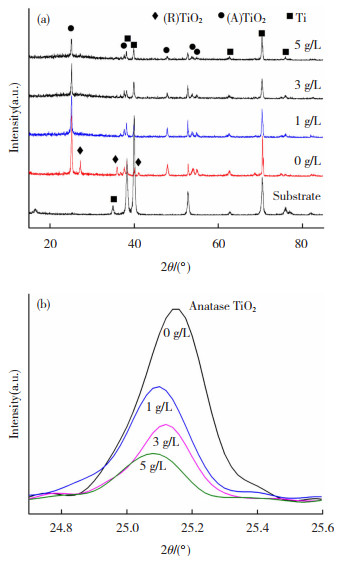
图 3为薄膜催化剂的XRD谱图。从图 3(a)可以看出,在未添加NH4VO3制备的薄膜中,TiO2主要以锐钛矿和金红石两种晶型存在。由于薄膜的多孔性和较薄的厚度,在薄膜中出现了与衬底对应的衍射峰。随着电解液中NH4VO3质量浓度的增加,根据特征峰的相对强度,锐钛矿的数量逐渐减少,而对应于金红石的衍射峰消失。这可以证实,V掺杂对TiO2的结晶度以及锐钛矿到金红石的相变过程有很强的抑制作用。根据Scherrer公式[21],通过相应X射线谱峰的展宽可以确定晶粒尺寸,结果表明,当NH4VO3质量浓度为0、1、3、5 g/L时,所制备薄膜的晶粒尺寸分别为32.72、30.60、33.53和30.96 nm。
|
图 3 不同质量浓度NH4VO3制备的薄膜催化剂的XRD谱图(a)及其TiO2(101)晶面相应峰位置的局部放大图(b) Fig.3 XRD patterns of film catalysts prepared under different concentrations of NH4VO3 (a) and enlarged images of the peak positions correponding to anatase TiO2(101) (b) |
与EDS能谱的结果相反,XRD分析并没有显示出与含有V物质对应的衍射峰,而且上述膜样品在500 ℃下退火处理后的XRD分析中也未找到这些衍射峰,因此只有极少量的V以无定形形式存在于膜中。尽管如此,V的存在影响了薄膜中TiO2的晶面间距,如图 3 (b)所示。随着NH4VO3用量的增加,衍射角2θ向低角区偏移。由布拉格方程2dsinθ=λ可知,晶面间距d的值随着入射X射线与晶面夹角(θ)的减小而增大,表明随着NH4VO3质量浓度的增加,晶面间距增大。从这个角度来看,这意味着TiO2与V元素之间应该存在很强的相互作用,特别是当电解液中NH4VO3质量浓度为1 g/L时。
2.3 膜层催化剂XPS分析图 4为薄膜催化剂的XPS谱图。
|
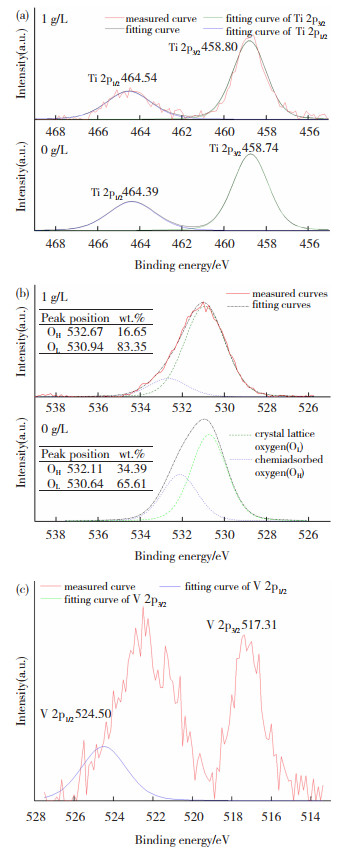
图 4 在质量浓度分别为0和1.0 g/L NH4VO3电解液中制得的膜催化剂的XPS谱图 Fig.4 XPS analyses of film catalysts without and with 1 g/L of NH4VO3: (a) Ti 2p; (b) O 1s; (c) V 2p |
图 4 (a)显示Ti 2p1/2和Ti 2p3/2的XPS峰是对称的,两者的XPS峰位置分别位于458.6和464.4 eV附近,说明样品中Ti的主要化学态为+4价态。O 1s的XPS谱图特征峰较宽且不对称,根据谱峰位于结合能526~536 eV的范围,表明至少存在两种化学态,包括低结合能处的晶格氧(OL)和高结合能处的化学吸附氧(OH)[22]。因此,O 1s的XPS谱图,根据高斯规则拟合可得到两种O化学态,如图 4(b)所示。OL XPS谱图主要归因于TiO2晶格中Ti—O的贡献,OH与主要由化学吸附水产生的羟基氧密切相关[23]。根据拟合结果可以发现,V元素掺杂可显著增加OL的量,同时降低OH的量,说明膜催化剂的表面氧空位(SOVs)由于膜中V元素的存在而减少。
有研究[24]表明,含有大量氧空位的TiO2通常呈现蓝色,因而,可以证明在未含NH4VO3的蓝灰色膜中存在相当数量的氧空位。在电解液中加入NH4VO3后,形成的TiO2在PEO过程中可以在阳极界面与VO3或多钒离子相互作用,导致TiO2中SOV降低。因此,膜的颜色发生了变化。随着NH4VO3质量浓度的增加,膜中钒离子或化合物的颜色越来越明显。通常认为,SOV往往在导带底部附近形成子带能级,容易捕获或束缚光生电子,这已被文献[16]所证实。由此可见,在含NH4VO3电解液中制备的薄膜催化剂对光生电子的利用效率要优于未含NH4VO3制备的催化剂。
图 4(c)显示了V 2p1/2和V 2p3/2的XPS特征峰。V 2p3/2的峰尖锐对称,但V 2p1/2的峰嵌入在O 1s Kα3, 4卫星峰中,V 2p1/2和V 2p3/2的XPS峰位置分别在524.50和517.31 eV附近,说明样品中V的主要化学态为+5价态。结合上述EDS、XRD和XPS分析,可以得出V主要以V2O5簇的形式存在,且分散在TiO2表面。
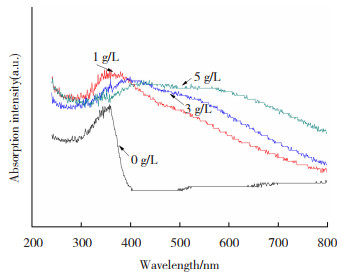
2.4 膜层催化剂UV-Vis-DRS光谱分析膜催化剂的UV-Vis-DRS光谱如图 5所示。根据TiO2的能带结构可知,在400 nm以下波长范围内的光吸收主要是由于电子从价带跃迁到导带(带到带跃迁,O 2p→Ti 3d)引起的。比较分析发现,当电解液中加入NH4VO3时,光学吸收光谱发生红移,吸收范围扩大。在波长范围内的吸收增加可能是V2O5团簇的吸收所带来的影响。然而,随着NH4VO3质量浓度的增加,V2O5团簇的形成越来越多,尺寸开始增大,从而在400~550 nm波长范围内出现另一个单独的光吸收,这是由于分散在薄膜催化剂上的V2O5团簇的电子跃迁造成的。
|
图 5 不同质量浓度NH4VO3制得的膜催化剂的UV-Vis-DRS光谱 Fig.5 V-Vis-DRS spectra of film catalysts under different concentrations of NH4VO3 |
在Na2S+Na2SO3溶液中评价了复合膜催化剂的光催化产氢活性,H2的析出速率如图 6所示。
|
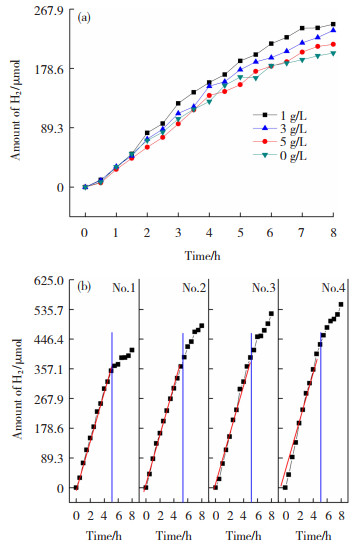
图 6 膜催化剂在Na2S+Na2SO3溶液中光催化产生H2的析出量:(a) H2析出量-时间曲线; (b) 连续光催化析氢曲线 Fig.6 Amount of H2 evolution in Na2S+Na2SO3 solution by photocatalytic process of film catalysts: (a) H2 evolution-time curve; (b) consecutive photocatalytic hydrogen evolution curve |
通常,H2的析出速率越大,催化剂的光催化还原活性越高。从图 6 (a)中可以看出,在含1 g/L NH4VO3电解液中采用PEO工艺制备的TiO2膜催化剂光催化还原活性最好。通常,光催化活性是由催化剂的用量及其结构决定的。综上分析可知,TiO2的量随着NH4VO3质量浓度的增加而减少,从而倾向于降低材料的光催化活性。另一方面,电解液中NH4VO3的加入导致TiO2与V2O5之间的强相互作用,影响了TiO2的晶面间距,使得薄膜催化剂中的SOV减小,DRS光谱的光吸收范围扩大,这势必会提高光催化活性;然而,假如V2O5的量进一步增加,其团簇会变大,从而导致TiO2与V2O5之间的协同作用减弱,此外正如文献[17]所报道的,V2O5团簇还可能成为光诱导产生e-和h+的复合中心。因此,样品中V2O5团簇含量过高会导致其光催化活性降低。另一方面,与未添加NH4VO3制备的膜相比,添加NH4VO3所得样品增加了膜表面孔洞的尺寸和数量,从而提高了样品的表面积,这也有利于光催化过程。这些因素的相互作用决定了当NH4VO3质量浓度为1 g/L时, 样品表现出最佳的光催化还原活性。图 6 (b)为电解液中含1 g/L NH4VO3所制备的薄膜催化剂在Na2S+Na2SO3溶液中的光催化析氢重复实验。每次测试在新鲜溶液中进行8 h,膜催化剂在每次光催化测试前用去离子水清洗并在空气中干燥。根据实验结果,每次实验H2的析出过程可分为2个阶段: 第1阶段为0~5 h,斜率不变,可估算出H2的析出速率约为2.09 μmol/(cm2·h); 第2阶段为5~8 h,由于Na2S + Na2SO3的过量消耗,曲线斜率减小。这说明薄膜催化剂具有高稳定性和恒定的光催化活性,优于表 2中所报道的催化剂。
| 表 2 TiO2/V2O5光催化制氢与文献报道光催化剂的性能比较[25-29] Table 2 Comparison of photocatalytic hydrogen production of TiO2/V2O5 with reported literatures[25-29] |
1) TiO2/V2O5复合薄膜催化剂由具有微孔结构的锐钛矿型TiO2和主要以无定形形式分散在TiO2表面的V2O5组成。V对TiO2的结晶有较强的抑制作用,TiO2与V2O5之间也存在较强的相互作用,使得膜催化剂的晶面间距增大,SOV减小。
2) 随着NH4VO3质量浓度的增加,复合膜的DRS光谱逐渐发生红移,光吸收范围逐渐扩大和发展,直到在400~550 nm波长范围内出现另一个独立的光吸收峰。NH4VO3可以提高催化剂在Na2S+Na2SO3溶液中光催化分解产H2的还原活性。此外,薄膜催化剂具有较高的稳定性和恒定的光催化活性。
| [1] |
LI Zhenzi, WANG Shijie, WU Jiaxing, et al. Recent progress in defective TiO2 photocatalysts for energy and environmental applications[J]. Renewable and Sustainable Energy Reviews, 2022, 156: 111980. DOI:10.1016/j.rser.2021.111980 |
| [2] |
ZHANG Kaimin, WANG Jinxin, NINAKANTI R, et al. Solvothermal synthesis of mesoporous TiO2 with tunable surface area, crystal size and surface hydroxylation for efficient photocatalytic acetaldehyde degradation[J]. Chemical Engineering Journal, 2023, 474: 145188. DOI:10.1016/j.cej.2023.145188 |
| [3] |
XIA Bingquan, HE Bowen, ZHANG Jianjun, et al. TiO2/FePS3 S-scheme heterojunction for greatly raised photocatalytic hydrogen evolution[J]. Advanced Energy Materials, 2022, 12(46): 2201449. DOI:10.1002/aenm.202201449 |
| [4] |
ARORA I, CHAWLA H, CHANDRA A, et al. Advances in the strategies for enhancing the photocatalytic activity of TiO2: Conversion from UV-light active to visible-light active photocatalyst[J]. Inorganic Chemistry Communications, 2022, 143: 109700. DOI:10.1016/j.inoche.2022.109700 |
| [5] |
XIA Changlei, NGUYEN Thihongchuong, NGUYEN Xuancuong, et al. Emerging cocatalysts in TiO2-based photocatalysts for light-driven catalytic hydrogen evolution: Progress and perspectives[J]. Fuel, 2022, 307: 121745. DOI:10.1016/j.fuel.2021.121745 |
| [6] |
CHEN Zuoyan, REN Xuechang, YANG Linhai, et al. Self-templating synthesis and photocatalytic activity of hollow TiO2 microspheres prepared by the sol-gel+solvothermal method[J]. Applied Surface Science, 2023, 619: 156731. DOI:10.1016/j.apsusc.2023.156731 |
| [7] |
ELSER M J, NEIGE E, BERGER T, et al. On the importance of nanoparticle necks and carbon impurities for charge trapping in TiO2[J]. The Journal of Physical Chemistry C, 2023, 127(18): 8778-8787. DOI:10.1021/acs.jpcc.3c00430 |
| [8] |
HAO Baofei, GUO Jinpeng, ZHANG Lan, et al. Magnetron sputtered TiO2/CuO heterojunction thin films for efficient photocatalysis of Rhodamine B[J]. Journal of Alloys and Compounds, 2022, 903: 163851. DOI:10.1016/j.jallcom.2022.163851 |
| [9] |
MUGUNDAN S, PRAVEEN P, SRIDHAR S, et al. Sol-gel synthesized barium doped TiO2 nanoparticles for solar photocatalytic application[J]. Inorganic Chemistry Communications, 2022, 139: 109340. DOI:10.1016/j.inoche.2022.109340 |
| [10] |
LI X Z, LIU H L, YUE P T, et al. Photoelectrocatalytic oxidation of rose bengal in aqueous solution using a Ti/TiO2 mesh electrode[J]. Environmental Science & Technology, 2000, 34(20): 4401-4406. DOI:10.1021/es000939k |
| [11] |
MEYER S, GORGES R, KREISEL G. Preparation and characterisation of titanium dioxide films for catalytic applications generated by anodic spark deposition[J]. Thin Solid Films, 2004, 450(2): 276-281. DOI:10.1016/j.tsf.2003.11.168 |
| [12] |
SUN Haijian, LIU Huiling, MA Jun, et al. Preparation and characterization of sulfur-doped TiO2/Ti photoelectrodes and their photoelectrocatalytic performance[J]. Journal of Hazardous Materials, 2008, 156(1): 552-559. DOI:10.1016/j.jhazmat.2007.12.087 |
| [13] |
BAYATI M R, MOSHFEGH A Z, GOLESTANI-FARD F. On the photocatalytic activity of the sulfur doped titania nano-porous films derived via micro-arc oxidation[J]. Applied Catalysis A: General, 2010, 389(1): 60-67. DOI:10.1016/j.apcata.2010.09.003 |
| [14] |
YAO Zhongping, JIA Fangzhou, JIANG Yanli, et al. Photocatalytic reduction of potassium chromate by Zn-doped TiO2/Ti film catalyst[J]. Applied Surface Science, 2010, 256(6): 1793-1797. DOI:10.1016/j.apsusc.2009.10.005 |
| [15] |
YAO Zhongping, JIA Fangzhou, TIAN Shujun, et al. Microporous Ni-doped TiO2 film photocatalyst by plasma electrolytic oxidation[J]. ACS Applied Materials & Interfaces, 2010, 2(9): 2617-2622. DOI:10.1021/am100450h |
| [16] |
MARTIN S T, MORRISON C L, HOFFMANN M R. Photochemical mechanism of size-quantized vanadium-doped TiO2 particles[J]. The Journal of Physical Chemistry, 1994, 98(51): 13695-13704. DOI:10.1021/j100102a041 |
| [17] |
WU Jeffrey C S, CHEN Chihhsien. A visible-light response vanadium-doped titania nanocatalyst by sol-gel method[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2004, 163(3): 509-515. DOI:10.1016/j.jphotochem.2004.02.007 |
| [18] |
LIU Baoshun, WANG Xuelai, GAI Guofa, et al. Low temperature fabrication of V-doped TiO2 nanoparticles, structure and photocatalytic studies[J]. Journal of Hazardous Materials, 2009, 169(1): 1112-1118. DOI:10.1016/j.jhazmat.2009.04.068 |
| [19] |
WANG Haipeng, ZHANG Fei, JIN Mengmeng, et al. V-doped TiO2 nanobelt array for high-efficiency electrocatalytic nitrite reduction to ammonia[J]. Materials Today Physics, 2023, 30: 100944. DOI:10.1016/j.mtphys.2022.100944 |
| [20] |
WASEEM M, AHMAD A, SAGIR M, et al. Hydrothermal synthesis of V2O5/TiO2 decorated graphitic carbon nitride nanocomposite for biomolecule oxidation inhibition and dye degradation applications[J]. Environmental Research, 2023, 234: 116440. DOI:10.1016/j.envres.2023.116440 |
| [21] |
ZHANG Qinghong, GAO Lian, GUO Jingkun. Effects of calcination on the photocatalytic properties of nanosized TiO2 powders prepared by TiCl4 hydrolysis[J]. Applied Catalysis B: Environmental, 2000, 26(3): 207-215. DOI:10.1016/S0926-3373(00)00122-3 |
| [22] |
LIAO Gang, YAO Wu. Upcycling of waste concrete powder into a functionalized host for nano-TiO2 photocatalyst: Binding mechanism and enhanced photocatalytic efficiency[J]. Journal of Cleaner Production, 2022, 366: 132918. DOI:10.1016/j.jclepro.2022.132918 |
| [23] |
PAN Honghui, SUN Minghui, WANG Xiaoguang, et al. A novel electric-assisted photocatalytic technique using self-doped TiO2 nanotube films[J]. Applied Catalysis B: Environmental, 2022, 307: 121174. DOI:10.1016/j.apcatb.2022.121174 |
| [24] |
LEE Y J, PUTRI L K, NG B J, et al. Blue TiO2 with tunable oxygen-vacancy defects for enhanced photocatalytic diesel oil degradation[J]. Applied Surface Science, 2023, 611: 155716. DOI:10.1016/j.apsusc.2022.155716 |
| [25] |
CURE J, COCQ K, NICOLLET A, et al. A Beehive inspired hydrogen photocatalytic device integrating a carbo-benzene triptych material for efficient solar photo-reduction of seawater[J]. Advanced Sustainable Systems, 2020, 4(9): 2000121. DOI:10.1002/adsu.202000121 |
| [26] |
ZUO Quan, LIU Tingting, CHEN Chuanshuang, et al. Ultrathin metal-organic framework nanosheets with ultrahigh loading of single Pt atoms for efficient visible-light-driven photocatalytic H2 evolution[J]. Angewandte Chemie International Edition, 2019, 58(30): 10198-10203. DOI:10.1002/anie.201904058 |
| [27] |
SPANU D, RECCHIA S, MOHAJERNIA S, et al. Site-selective Pt dewetting on WO3-coated TiO2 nanotube arrays: An electron transfer cascade-based H2 evolution photocatalyst[J]. Applied Catalysis B: Environmental, 2018, 237: 198-205. DOI:10.1016/j.apcatb.2018.05.061 |
| [28] |
ZHU Yuxiang, WANG Yanfei, CHEN Zhi, et al. Visible light induced photocatalysis on CdS quantum dots decorated TiO2 nanotube arrays[J]. Applied Catalysis A: General, 2015, 498: 159-166. DOI:10.1016/j.apcata.2015.03.035 |
| [29] |
HU Yubo, LIU Yuxiang, WU Jun, et al. A Case study on a soluble dibenzothiophene-S, S-dioxide-based conjugated polyelectrolyte for photocatalytic hydrogen production: The film versus the bulk material[J]. ACS Applied Materials & Interfaces, 2021, 13(36): 42753-42762. DOI:10.1021/acsami.1c10748 |
 2024, Vol. 32
2024, Vol. 32


