聚偏氟乙烯(PVDF)因其优秀的机械性能、耐化学性以及良好的热稳定性,广泛应用于水处理过程中[1-2].但是由于PVDF的疏水性,PVDF膜容易受到水中有机物的污染,导致膜通量的衰减[3-4].水中溶解性有机物(DOM)是引起膜污染的主要原因,而蛋白质是水中溶解性有机物(DOM)的典型代表性物质[5-6].众所周知,蛋白质的污染行为是一个复杂的过程,其中还受多种因素的影响,包括污染物的质量浓度、温度、pH、离子强度以及膜本身的物理化学性质等[7-8].在膜制备过程中,添加一种或多种有机添加剂能够有效地改性膜表面的亲水性,并在一定程度上提高膜表面的抗污染性.聚乙烯吡咯烷酮(PVP)、聚乙烯醇(PVA)、聚乙二醇(PEG)等已经广泛应用于超滤膜的改性中[9],由于其所含的亲水性官能团不同,对膜的改性方式上也有一定程度的区别.仅靠亲水性的好坏判断膜抗污染能力强弱是不全面的,因此,进一步深入研究膜表面性质与BSA之间的相互作用对PVDF超滤膜的改性和抗污染性研究具有重要的意义.
耗散型石英单晶微天平(QCM-D)是近年发展起来的界面表征技术,不仅可以检测到吸附层质量和厚度等信息,通过测量耗散系数(dissipation,D)还能够得到更多表面上吸附层结构变化的信息,从而极大地丰富了薄膜的表面信息,为研究微观作用机理提供了一种强有力的手段.目前,国内已有学者将QCM-D技术应用于化学、材料[10]、生物[11]、医学[12]等多个领域.本文采用QCM-D研究了经PVP、PVA或PEG改性后的3种PVDF超滤膜在不同亲水性表面上的蛋白质吸附行为及蛋白吸附层黏弹性随时间的变化规律.
1 实验 1.1 试剂与仪器牛血清白蛋白(BSA,Mw=67 ku,美国Sigma公司),二甲基乙酰胺(DMAc,天津科密欧化学试剂有限公司,分析纯),聚偏氟乙烯(PVDF,6020,Solef©,Solvay),聚乙烯吡咯烷酮(PVP,K30,德国BASF),聚乙烯醇(PVA,AH-26,日本合成化学工业),聚乙二醇(PEG,Mw=20 ku,天津市科密欧化学试剂有限公司),超纯水,去离子水,十二烷基硫酸钠(SDS).
E1型石英晶体微天平(QCM-D,瑞士Q-Sense公司),晶片(QSX 303,SiO2,d=14 mm),原子力显微镜(AFM,美国Nanoscope公司),匀胶机(KW-4A,中国科学院微电子研究所),亲水角测定仪(SL200B,美国科诺工业有限公司).
1.2 铸膜液的配制与亲水角的测定分别将一定量的添加剂(PVP/PVA/PEG:PVDF=1/40~1/20)溶于49 g DMAc中,60℃下搅拌完全溶解后各加入1 g PVDF搅拌3 h,获得3种含不同添加剂的均一铸膜液.
分别取10 mL铸膜液,滴在干净的载玻片上,60℃条件下干燥15 min,使溶剂挥发完全,并固化成膜,待其冷却完全后,将样品浸泡在去离子水中20 min,取出干燥备用.室温下,每个样品平行测定3个点,然后取平均值.通过调节PVP、PVA、PEG的添加量使不同改性膜的亲水角分别维持在(65±2)°、(75±2)°、(85±2)°(PVDF/PVP、PVDF/PVA、PVDF/ PEG分别代表3种含不同改性剂的膜;PVP65/75/85、PVA65/75/85、PEG65/75/85分别代表不同亲水性膜).
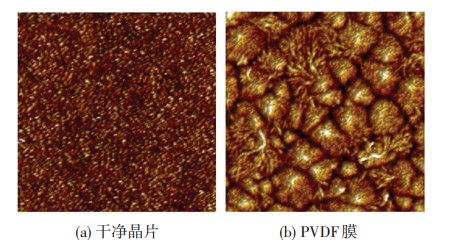
1.3 QCM-D样品的制备及表征采用旋转涂膜法制备QCM-D样品,先将晶片固定在匀胶机上,取配置好的铸膜液15μL滴在晶片中心,在低/高速(低速1 200 r/min,t1=10 s;快速6 000 r/min,t2=40 s)条件下通过离心作用分相,从而获得比较薄且均质的膜.将制好的成膜晶片用超纯水浸洗,N2吹干,最后置于真空干燥箱中备用.图 1为接触模式下晶片表面的AFM形貌图,可以看出,PVDF膜已均匀地涂覆在晶片上.
|
图 1 晶片的AFM表面形貌(5μm×5μm) Figure 1 AFM surface morphology of sensor (5μm×5μm) |
室温条件下,将一定量牛血清蛋白溶于去离子水中,配成质量浓度为100 mg/L的溶液.4℃条件下静置储藏备用,缓冲溶液为去离子水(DI),清洗液为质量分数2%SDS.将表面成膜后的晶片置于QCM-D流动池中,温度控制在(23±0.1)℃.先让样品在空气中检测,待基线平衡后再注入缓冲溶液直至曲线平衡,然后以0.1μL/min注入BSA溶液30 min,接着注入缓冲溶液.实验过程中记录3,5,7和9次倍频的频率(f)和耗散因子(D)随时间的变化曲线直至达到平衡,取相同倍频下不同改性膜的频率和耗散的变化数据,并作归一化处理,据此讨论膜表面吸附BSA的过程.取倍频n=5进行研究.
1.5 PVDF超滤膜污染研究以PVP75/PVA75/PEG75膜对应各聚合物的比例配置所需的铸膜液,通过添加可溶性较强的添加剂(如LiCl)作为制孔剂.以去离子水作为凝固浴,通过浸没凝胶相转化法制得PVDF平板超滤膜.用J/J0表征过滤过程中膜通量的衰减,J0、J分别指超滤膜的纯水通量以及污染实验过程中的水通量.膜过滤实验中,污染物BSA的质量浓度为20 mg/L.
2 结果与讨论 2.1 晶片表面形貌表征图 2为亲水角75°时不同膜晶片的AFM表面形貌.通过分析软件得到PVP75、PVA75以及PEG75的平均粗糙度分别为2.15、3.33、2.48 nm.由图 2可知,旋转涂膜法制成的不同改性膜表面整体较为均匀且平整.祝振鑫[13]认为影响亲水角测量的主要原因有固体表面性状及其亲/疏水性,由于晶体表面膜的粗糙度很小,可以忽略其对亲水角测量的影响.

|
图 2 不同改性膜晶片的AFM表面形貌(5μm×5μm) Figure 2 2-dimensional surface morphology of the sensors coated with different membranes (5μm×5μm) |
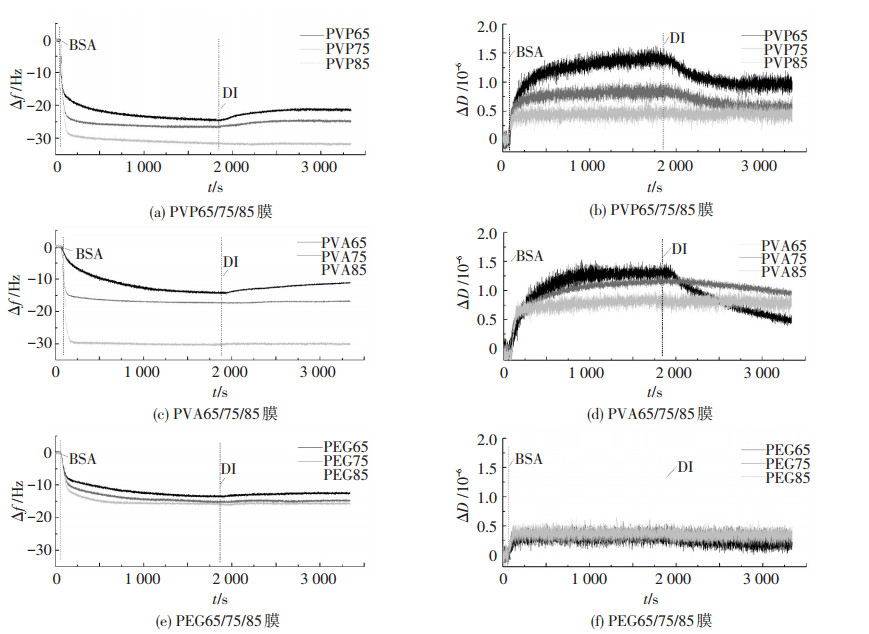
图 3是在不同亲水角条件下3种PVDF改性膜表面吸附BSA过程中QCM-D的频率和耗散的变化曲线.在吸附起始阶段(< 15 min)频率值(Δf)迅速下降,而后逐渐变缓直至平衡,说明膜在过滤初期受到的污染较严重.由图 3(a)、(c)、(e)可以看出,相同添加剂改性情况下,亲水角越小,频率变化越小.相比PVP85和PVA85膜,PEG85膜对BSA的吸附量最小,说明添加少量的PEG后能够有效地抑制BSA在膜表面的吸附,减小BSA在膜表面的吸附量,与Contreras等[14]研究结果一致.但是随着亲水角的减少,BSA的吸附量略微减小,用去离子水清洗后频率几乎没有发生变化,说明随着PEG含量的增加,膜的抗污染性能并没有显著提高.而对于PVP和PVA改性膜,随着亲水角的减少,初期吸附过程逐渐变缓并且吸附量出现减小,其中PVDF/PVA膜吸附量变化尤为明显.图 3(b)、(d)、(f)为BSA吸附到不同的表面上时耗散D的变化,对于吸附层厚度较薄并且致密度较高的薄膜,ΔD值几乎没有明显变化;相反,对于一些吸附层厚度较厚并且黏弹性较大的薄膜,ΔD值出现显著变化.由图 3(c)可以看出,当BSA吸附到不同亲水性PVDF/PEG膜表面上时,ΔD值非常小且无明显变化,表明BSA吸附到PVDF/PEG膜表面上时形成较为致密的污染层,并且不易受亲水角变化的影响.相反,当吸附到PVDF/PVP和PVDF/PVA膜上时,ΔD值相对较大,即吸附层黏弹性变大,清洗时频率与耗散也变化愈加明显,说明吸附层黏弹性变大后清洗时吸附层容易洗脱下来.由此可见,BSA的污染行为除了与膜表面亲疏水性有关,还与膜表面的化学性质密切相关.
|
图 3 不同亲水角下3种PVDF改性膜表面吸附BSA过程中QCM-D的频率(Δf)和耗散(ΔD)变化 Figure 3 QCM-D measurement of change in frequency(Δf) and change in dissipation(ΔD) versus time upon adsorption of BSA onto the sensors coated with different membranes |
实际上,膜污染主要由BSA与膜间的物理化学作用导致的,并非膜表面BSA之间的相互作用引起的.Huisman等[15]发现,聚醚砜超滤膜与BSA之间的疏水性作用是造成膜初期污染的主要原因,而后期污染主要是受BSA与BSA相互作用的影响.为了进一步了解BSA吸附过程中吸附层的构象信息,常用|-ΔD/Δf|值直接反映BSA吸附层流动性,进而获得BSA吸附层的黏弹性性质,即|-ΔD/Δf|值越大,吸附层流动性越强,黏弹性越好[16].图 4为不同亲水角下3种PVDF改性膜表面吸附BSA过程中|-ΔD/Δf|的变化曲线.可以看出,BSA吸附到PVDF/PVP膜过程主要分两个阶段,第一阶段是吸附初期蛋白分子迅速在膜表面附着,形成较为致密污染层,该过程主要受蛋白分子和膜材料之间相互作用的影响,实际上是多种力共同作用的结果,如范德华力、静电力、疏水作用等;第二阶段是蛋白分子在吸附层上进一步沉积,当膜表面的吸附量趋于平衡后,耗散仍会发生变化,即在吸附后期|-ΔD/Δf|值较第一阶段更大,说明BSA在PVDF/PVP膜表面吸附平衡后随时间发生了构象上的变化,黏弹性越来越大[17].随着亲水角的下降,两个阶段的|-ΔD/Δf|值均有明显提高,即随着PVP含量的升高,BSA在膜表面的吸附层逐渐变得疏松,黏弹性大.相对于PVDF/PVP膜,PVA的添加对BSA吸附层的影响更加明显.如图 4(d)所示,在亲水角75°时PVA75膜的|-ΔD/Δf|值比PVP75膜更大,形成的污染层更加疏松.这可能与膜表面的水合作用有关,随着BSA吸附过程的进行,由于受到膜表面化学改性的影响,越来越多的水分子逐渐进入吸附层内,使得膜表面吸附层的构象发生明显的变化.相反,随着PEG含量的升高(即亲水角变小),|-ΔD/Δf|值几乎无明显变化,污染层的结构受亲水角的影响并不明显,反而在吸附后期|-ΔD/Δf|有变小的趋势,表明吸附层更加倾向与膜表面结合,结构变得致密.因而控制膜表面第一阶段的污染对提高膜的抗污染性很有帮助.综上可知,在膜的改性过程中,有机亲水添加剂对吸附层影响的大小顺序为PVA>PVP>PEG.

|
图中S1、S2分别为|-ΔD/Δf|的两个变化阶段斜率 图 4 不同亲水角下3种PVDF改性膜表面BSA(100 mg/L)吸附过程中|-ΔD/Δf|的变化 Figure 4 Relation between dissipation shift(ΔD) versus frequency shift(Δf) induced by adsorption of BSA solution(100 mg/L) onto 3 kinds of PVDF modified membrane surface under different hydrophilic angle |
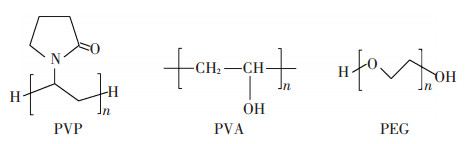
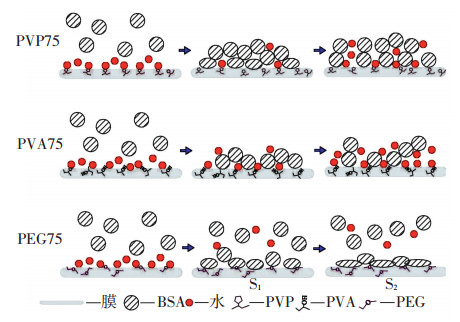
实验结果表明,随着亲水角的降低,不同改性膜所受亲水性的影响程度不一样,不同阶段下|-ΔD/Δf|值也呈现不同的变化趋势,因此,仅靠亲水角的变化考察BSA在膜表面的吸附行为是不全面的,其吸附行为还很大程度受膜表面化学性质的影响.图 5为3种添加剂(PVP、PVA和PEG)的化学结构式.从PEG(Mw=20 ku)的化学结构式看,除了含有羟基(—OH)外,还含有大量的醚基(—O—),由于其氧原子的电负性比碳强,具有微弱的极性,醚基中氧原子的孤电子对使其有可能与水分子形成氢键,因而表现出一定的亲水性[18-19].图 6为接触角为75°时不同膜表面上BSA的吸附过程示意图.当部分BSA分子在驱动力作用下通过破坏PEG膜表面的水合层吸附到膜上时,转而受到PVDF的强疏水化作用,水分子较难再进入吸附层内,致使所形成的污染层比较密实,后期吸附层几乎无明显的构象变化.由图 3(a)可知,BSA在PVDF/PEG膜表面的吸附量并不大,这可能是由于静电作用的影响,PEG的添加改变了吸附初期膜表面吸附层的电负性,通过影响吸附层的结构进而有效地阻碍了后期BSA的吸附.而PVA分子富含羟基,在水溶液中很容易与水分子结合,形成很强的氢键,膜面很容易再次吸附水分子,从而使吸附层变得越来越疏松,清洗时蛋白质层更容易被洗脱下来.随着PVA含量的升高,膜表面与水分子形成更紧密的水合层,从而有效地阻碍了吸附初期BSA分子与膜表面的吸附速度(见图 3(c)).PVP分子中存在大量的官能团—CON—,也具有较强的亲水性,但弱于羟基,因此,造成PVDF/PVP膜对BSA的吸附量有所增加,但随着添加剂含量的提高,吸附量和吸附层也逐渐发生明显变化.由此可见,通过添加有机亲水改性添加剂能够影响BSA在膜表面的吸附行为,并且通过选择含特殊官能团的添加剂可以有效地减少蛋白质的吸附量,而且能够改变了蛋白质吸附层的结构,提高膜的抗污染性.
|
图 5 PVP、PVA、PEG的化学结构式 Figure 5 Chemical structure formula of PVP, PVA and PEG |
|
S1、S2分别代表吸附层变化的不同阶段 图 6 接触角为75°时不同改性膜表面所含特殊官能团影响BSA吸附过程示意 Figure 6 Schematic diagram of the layer structure of BSA adsorbed onto three different modified membrane when the contact angle is 75 degrees |
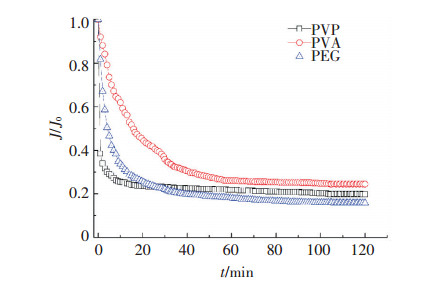
BSA的膜过滤实验中,膜表面污染层的形成以及膜孔的堵塞是造成膜通量下降的主要原因.图 7为不同改性膜的通量随过滤时间的变化,可以看出,在过滤前期,3种超滤膜的衰减速率大小顺序分别为PVP75>PEG75>PVA75,这与图 3(a)、(c)、(e)中频率f的变化过程相符;从污染曲线达到平衡所需的时间长短看,依次为PVA75>PEG75>PVP75,表明添加剂PVA能够有效地减缓膜过滤过程中的初期污染;当过滤曲线达到平衡时,3种膜通量衰减幅度大小为PEG75>PVP75>PVA75.由图 4可知,PVDF/PEG膜表面BSA吸附层更加致密,因而过滤时水力阻力变大,不利于水分子透过,这可能是造成该膜通量下降幅度增加的主要原因.将3种污染过的膜进行简单的表面冲洗后,发现PVP75、PVA75、PEG75膜的通量恢复率分别为45.7%、85%、66%.可以看出,PVP75的恢复率最低,这表明除了PVP75膜表面易形成污染层外,部分BSA分子还有可能进入到超滤膜内部,堵塞膜孔,不易清洗,恢复率偏低.在实际膜制备过程中,需要综合考查添加剂的改性作用和制孔作用,探索出一种合适的改性添加剂仍需进一步研究.
|
图 7 不同改性膜通量随BSA过滤时间的衰减曲线 Figure 7 Flux decline curve of the three modified membrane with BSA filtration |
1) 亲水性越好,BSA的吸附量就越少,结构也越疏松.随着亲水角的变化,不同改性膜表面对BSA表现出明显不同的吸附行为,即BSA的吸附行为除了受亲水性的影响,还受膜表面化学性质的影响.
2) 当亲水性较差时,PEG能够有效地抑制BSA在膜表面的吸附,减小BSA在膜表面的吸附量.随着亲水性的改善,PVDF/PVA与PVDF/PVP膜表面的吸附行为发生显著变化,吸附量逐渐降低,吸附层的结构逐渐由密实转变得疏松,黏弹性也越好,同时也便于清洗,而PEG膜表面对BSA的吸附行为几乎无明显变化,且形成的污染层均较为致密.
3) 不同化学官能团能够极大地影响膜表面对BSA吸附行为.在吸附BSA的实验中,PVDF/PEG膜易受到醚基的静电作用,使其吸附过程与亲水角的变化无明显的线性关系;而对于PVDF/PVA与PVDF/PVP膜,BSA的吸附行为极易受到亲水性的影响,但是不同改性膜表面吸附层的变化仍极大地取决于膜表面的化学性质.
4) 由膜过滤实验可以看出,相比PVP和PEG,添加剂PVA能够减缓过滤初期BSA在膜表面的堆积,而且能够在过滤后期仍然表现出较好的抗污染性,且易于清洗.
| [1] |
WANG Peng, TAN K L, KANG E T, et al. Synthesis, characterization and anti-foulingproperties of poly (ethylene glycol) grafted poly (vinylidenefluoride) copolymer membranes[J].
Journal of Materials Chemistry,2001, 11 (3) : 783-789.
( 0) 0)
|
| [2] |
CHANG Yung, SHIH Y J, RUAAN R C, et al. Preparation of poly (vinylidene fluoride) microfiltration membrane with uniform surface-copolymerized poly (ethylene glycol) methacrylate and improvement of blood compatibility[J].
Journal of Membrane Science,2008, 309 (1) : 165-174.
( 0) 0)
|
| [3] |
CAO Xiaochun, MA Jun, SHI Xuehua, et al. Effect of TiO2 nanoparticle size on the performance of PVDF membrane[J].
Applied Surface Science,2006, 253 (4) : 2003-2010.
( 0) 0)
|
| [4] |
王磊, 冯玲, 王旭东, 等. 二级出水残留有机物对PVDF超滤膜污染行为研究[J].
哈尔滨工业大学学报,2014, 46 (4) : 105-109.
WANG L, FENG L, WANG X D, et al. Fouling behavior of residual orianic matters of secondary effluent on PVDF UF membrane[J]. Journal of Harbin Institute of Technology,2014, 46 (4) : 105-109. (  0) 0)
|
| [5] |
YAMAMURA H, KIMURA K, WATANABE Y. Mechanism involved in the evolution of physically irreversible fouling in microfiltration and ultrafiltration membranes used for drinking water treatment[J].
Environmental Science & Technology,2007, 41 (19) : 6789-6794.
( 0) 0)
|
| [6] |
HER N, AMY G, PARK H R, et al. Characterizing algogenic organic matter (AOM) and evaluating associated NF membrane fouling[J].
Water Research,2004, 38 (6) : 1427-1438.
( 0) 0)
|
| [7] |
JONES K L, O'MELIA C R. Protein and humic acid adsorption onto hydrophilic membrane surfaces: effects of pH and ionic strength[J].
Journal of Membrane Science,2000, 165 (1) : 31-46.
( 0) 0)
|
| [8] |
MO H, TAY K G, NG H Y. Fouling of reverse osmosis membrane by protein (BSA): effects of pH, calcium, magnesium, ionic strength and temperature[J].
Journal of Membrane Science,2008, 315 (1/2) : 28-35.
( 0) 0)
|
| [9] |
RANA D, MATSUURA T. Surface modifications for antifouling membranes[J].
Chemical Reviews,2010, 110 (4) : 2448-2471.
( 0) 0)
|
| [10] |
张奕, 曾戎, 周长忍, 等. 基于QCM-D的天然多糖材料的蛋白吸附研究[J].
功能材料,2009, 40 (2) : 287-290.
ZHANG Y, ZENG R, ZHOU C R, et al. Quartz crystal microbalance study of protein adsorption on natural polysaccharides[J]. Journal of Functional Materials,2009, 40 (2) : 287-290. (  0) 0)
|
| [11] |
韦晓兰. 基于QCM-D技术的细菌生物膜研究[J].
重庆师范大学学报(自然科学版),2014, 4 : 027.
WEI X L. The improvement of the study on bacteria bio-film(BBF) by quartz crystal microbalance with dissipation(QCM-D)[J]. Journal of Chongqing Normal University(Natural Science),2014, 4 : 027. (  0) 0)
|
| [12] |
彭采宇.聚电解质微胶囊的药物缓释及其血液相容性研究[D].杭州:浙江大学, 2010.
PENG C N.Study on drug delivery and blood compatibility of polyelectrolyte microcapsules [D].Hangzhou:Zhejiang University, 2010. (  0) 0)
|
| [13] |
祝振鑫. 膜材料的亲水性、膜表面对水的湿润性和水接触角的关系[J].
膜科学与技术,2014, 34 (2) : 1-4.
ZHU Z X. Hydrophilicity, wettability and contact angle[J]. Journal of Membrane Science and Technology,2014, 34 (2) : 1-4. (  0) 0)
|
| [14] |
CONTRERAS A E, STEINER Z, MIAO Jing, et al. Studying the role of common membrane surface functionalities on adsorption and cleaning of organic foulants using QCM-D[J].
Environmental Science & Technology,2011, 45 (15) : 6309-6315.
( 0) 0)
|
| [15] |
HUISMAN I H, PRÁDANOS P, HERNÁNDEZ A. The effect of protein-protein and protein-membrane interactions on membrane fouling in ultrafiltration[J].
Journal of Membrane Science,2000, 179 (1/2) : 79-90.
( 0) 0)
|
| [16] |
PLUNKETT M A, CLAESSON P M, ERNSTSSON M, et al. Comparison of the adsorption of different charge density polyelectrolytes: a quartz crystal microbalance and X-ray photoelectron spectroscopy study[J].
Langmuir,2003, 19 (11) : 4673-4681.
( 0) 0)
|
| [17] |
康锴, 卢滇楠, 张敏莲, 等. 动态Monte Carlo模拟蛋白质与微滤膜相互作用及其对微滤过程的影响[J].
化工学报,2007, 58 (12) : 3011-3018.
KANG K, LU D N, ZHANG M L, et al. Dynamic Monte Carlo simulation of protein-membrane interaction and its implication on micro-filtration process[J]. Journal of Chemical Industry and Engineering(China),2007, 58 (12) : 3011-3018. (  0) 0)
|
| [18] |
WHITE G F, RUSSELL N J, TIDSWELL E C. Bacterial scission of ether bonds[J].
Microbiological Reviews,1996, 60 (1) : 216.
( 0) 0)
|
| [19] |
MENGER F M, CHLEBOWSKI M E. Is the ether group hydrophilic or hydrophobic[J].
Langmuir,2005, 21 (7) : 2689-2695.
( 0) 0)
|
 2016, Vol. 48
2016, Vol. 48


