纳滤膜应用领域[1-2]普遍存在的主要问题是膜污染造成的水通量下降及膜寿命的缩短[3-5],这也将影响膜的反冲洗频率和出水质量,加重运行维护负担.纳滤膜污染主要包括有机物污染、无机物污染、微生物污染和胶体污染4大类[6].自然水体中的天然有机物(NOM)是造成有机污染的主要原因[4, 7].腐殖质、多糖、蛋白质是构成NOM的主要物质,其物理化学特性(如结构、功能、电荷等)各不相同,故对纳滤膜造成不同程度的污染.无机污染主要指碳酸钙及钙、锶、钡的硫酸盐、硅酸盐等结垢物质对纳滤膜造成的污染[8].Lee等[9]的研究表明,与碳酸盐污染相比,硫酸盐污染更加难以去除,更需要早期发现与及时控制.难溶性无机盐除了在膜面形成垢体外,还可与水中的有机物作用对膜造成复合污染,对膜性能的影响更为复杂[10-11].Gouellec等[12]的研究表明,在有机污染物与无机盐共同存在的条件下,纳滤膜表面的无机污染行为发生改变.Farooque等[13]发现在实际运行过程中,有机污染先于无机污染形成.据此推测有机污染物会改变纳滤膜表面特性,进而会对垢体在纳滤膜表面的形成产生影响.
目前,关于有机物与高浓度无机离子结合对纳滤膜的综合污染方面只有少量的研究报道.然而在纳滤膜工程应用中,尤其是在海水/苦咸水淡化领域,由于自然水域含有丰富的Ca2+,原水中有机物和Ca2+对膜的污染作用无疑将严重降低纳滤膜工程应用的经济性.因此,选取具有代表性的聚酰胺复合纳滤膜为研究对象,针对现有研究的不足,探究在不同典型有机物改变膜表面特性的条件下,硫酸钙结垢对纳滤膜性能的影响,并结合扫描电镜、原子力显微镜等手段对污染机理进行深入研究,为纳滤膜污染的控制及性能恢复提供理论依据,并为纳滤系统的设计、运行提供方法.
1 实验 1.1 实验试剂聚砜(PSF),E6010,德国BASF;聚乙烯毗咯烷酮(PVPk30),分析纯,上海蓝季科技发展有限公司;N,N-二甲基乙酰胺(DMAc),分析纯,天津市科密欧化学试剂有限公司;聚乙二醇辛基苯基醚(TritonX-100),分析纯,国药化学试剂有限公司;聚乙二醇(PEG600),分析纯,天津市科密欧化学试剂有限公司;丙烯酸(AA),分析纯,天津市科密欧化学试剂有限公司;哌嗪(PIP,99%),aladdin;三乙胺(TEA,99 %),天津市福晨化学试剂厂;1,3,5-苯三甲酰氯(TMC,98 %),aladdin;正己烷,分析纯,广东光华科技股份有限公司;氯化钠、氯化钙、硫酸钠、硫酸镁均为分析纯,天津市天力化学试剂有限公司.
典型有机物:牛血清蛋白(Sigma-Aldrich,BSA)、腐殖酸(Sigma-Aldrich,HA)、海藻酸(Sigma-Aldrich,SA).
1.2 复合纳滤膜的制备 1.2.1 聚砜超滤膜的制备通过溶液相转化法制备聚砜超滤膜.首先进行铸膜液的配制:将PSF、PVP k30、PEG600、AA、Triton X-100按比例同时加入溶剂DMAc中,并于60℃条件下机械搅拌16 h,将搅拌好的铸膜液于60℃恒温静置脱泡3 h;在室温下将铸膜液均匀刮在无纺布上,制成溶液膜,并立即浸入以水为非溶剂的凝胶浴中,待相分离基本完成并成膜后,用去离子水反复冲洗多次以去除残留的有机物,最后将膜保存在去离子水中24 h以确保相分离完全完成.
1.2.2 复合纳滤膜的制备室温下,将PIP和TEA按一定比例配制成水溶液,TMC溶解于正己烷中配制成有机溶液.将制备好的聚砜超滤膜作为基膜浸渍在PIP的水溶液中,取出后用橡胶辊筒除去表面气泡与多余溶液,自然晾干,随后浸入TMC的正己烷有机溶液中反应一定时间,取出晾干,经过热处理即得到复合纳滤膜,反复漂洗后存放于去离子水中备用.制得的聚酰胺纳滤膜,测试压力0.6 MPa下纯水通量为(40±5)L·m-2·h-1,硫酸镁(2 g/L)截留率大于90%,截留分子质量为(400±50)u,接触角为(55±2) °,平均粗糙度为10.6 nm.
1.3 纳滤膜污染实验方法 1.3.1 实验装置及溶液配制选取HA、BSA、SA 3种典型有机物模拟水体中的腐殖质、蛋白质、多糖,其特性见表 1.3种有机物标准储备液(2 g/L)的配制方法:将SA、BSA的固体粉末(2 g)溶解于去离子水中并在室温下连续搅拌24 h以上;将HA粉末(2 g)溶解于0.1 mol/L NaOH溶液(100 mL)中并在室温下连续搅拌24 h以上,溶解完毕后定容至1 L.初步溶解后的SA、HA溶液需用0.45μm微滤膜(上海市新亚净化器件厂)过滤.最后,将3种溶液转移至无菌玻璃瓶中于4℃储存.制备CaCl2(2.3 mol/L)和Na2SO4(1.9 mol/L)的标准储备液用于硫酸钙(CaSO4·2H2O)结垢实验.
| 表 1 3种有机大分子的特性[14] Table 1 Properties of three kinds of organic macromolecules |
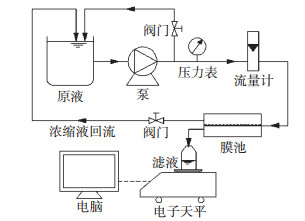
实验开始前,先将储备液稀释至所需浓度,分别作为基线、有机污染、硫酸钙结垢试验的原液.为了在整个污染试验中保持同样的溶液环境,污染液的总离子强度、pH保持相同.原液的化学组成列于表 2.其中,Ca2+和SO42-在原液中的溶度积略高于硫酸钙,其饱和指数为1.01,使结垢以适当的速度发生.实验装置如图 1所示.膜池采用错流过滤系统,纳滤膜为平板膜,膜片面积为4×12 cm2.
| 表 2 原液的化学组分 Table 2 Chemical composition of feed solutions |
|
图 1 实验装置 Figure 1 Experimental installation |
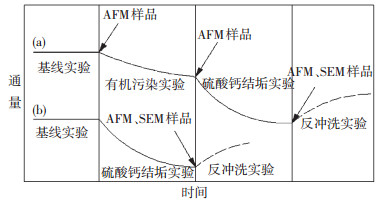
实验方案如图 2所示.(a) 每种有机污染/结垢实验按以下5个步骤进行:① 在膜池中装入新膜,选择层接触原液侧.② 用去离子水(DI)在0.8 MPa下预压膜2.5 h,使膜稳定,之后实时观察膜通量变化,如通量无变化则换为基线溶液.③ 在基线条件下测定初始膜通量.实时观察通量变化,待通量稳定后记录初始通量,进行下一步实验.④ 用新制备的有机物原液对膜面进行连续污染(24 h),以便在膜表面形成有机污染层.⑤ 将原液换成新制备的硫酸钙结垢实验溶液,立刻进行硫酸钙结垢实验(24 h).(b) 经过预压处理的新膜不进行有机污染实验(即(a)中步骤④ ),其余步骤同(a).污染实验条件保持一致:错流速度4.5 cm/s,原液pH为7,温度(20±1) ℃,压力0.6 MPa.硫酸钙结垢实验在不回流模式下进行,即滤液不回流至原液中.因此,随着过滤时间的增加,硫酸钙的饱和指数一直增加.
|
图 2 实验方案 Figure 2 Experimental plan |
硫酸钙结垢实验结束后,一部分膜进行反冲洗实验:用去离子水冲洗膜表面40 min (膜不透水),错流速度为9 cm/s,之后再次进行基线实验以确定通量恢复率.另一部分膜制成原子力显微镜(AFM)、扫描电镜(SEM)样品.
每组实验均重复进行3次以上,取相对误差小于5%的数据进行分析比较.
1.4 硫酸钙探针的制备及黏附力的测定 1.4.1 硫酸钙探针的制备在光学显微镜(奥林巴斯,TH4-200,日本)视野中实时监测制备过程.首先在微悬臂自由端黏附适量双组份环氧树脂胶(1:1,Epo Tek公司),然后将一直径为5~10μm、近似球形的硫酸钙微颗粒黏附于微悬臂自由端,在紫外灯照射下修复20 min,静置一周以上待用.
1.4.2 黏附力的测定将有机污染试验各阶段结束后的污染膜置于与污染试验相对应的污染物溶液中,待用.使用Multimode 8.0原子力显微镜(AFM,德国布鲁克)结合硫酸钙探针,测定新膜-硫酸钙、不同有机污染的膜-硫酸钙、硫酸钙-硫酸钙的黏附力.测试步骤:将污染膜置于液体池的底部,然后将液体池及探针安装于AFM上,设定相关参数后在液态“接触”模式下进行黏附力的测试.为了减小实验误差,在每个样品上选取至少6个不同的局域点进行作用力的测定,每个点进行10次重复测定.使用Nanoscope Analysis软件进行数据统计分析.
1.5 分析方法采用原子力显微镜扫描所制备膜的微观形貌并进行粗糙度测量,接触角测量仪(SL200 B,美国科诺工业有限公司)测定膜表面的接触角,扫描电镜(SEM,JSM-6510LV,日本JEOL)观察膜面结垢的表面、断面形态.
2 结果与讨论 2.1 有机污染实验首先进行基线实验,旨在消除盐离子对膜通量的影响.基线实验溶液不含有机物,其余溶液条件与有机污染实验相同,见表 2.
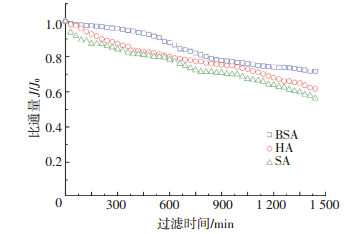
基线实验后进行聚酰胺纳滤膜的有机污染实验,将该过程中的膜通量随过滤时间衰减曲线绘制在同一张图中.以有机污染实验开始时膜的初始通量为标准通量,对每一时刻的通量进行标准化处理,结果如图 3所示.3种有机物对聚酰胺复合纳滤膜的污染程度顺序为SA > HA > BSA.
|
图 3 3种有机污染膜的比通量衰减曲线 Figure 3 Normalized flux decline curves of three organically conditioned membranes |
已有研究表明[15-16],在有Ca2+存在的情况下,有机污染主要受Ca2+和羧基作用影响.有机污染液中Ca2+ (1 mmol/L)可以使有机物分子聚合并且联接膜面(测试条件下主要是去质子化的羧基)和含羧基的有机物.因此,膜面的有机污染与有机物羧基含量有关.而上述3种有机物的羧基含量顺序为SA > HA > BSA[14],这与膜污染程度吻合.因此,随着膜面有机物浓度增高,膜污染越来越严重,并且膜面污染程度与有机物种类密切相关.
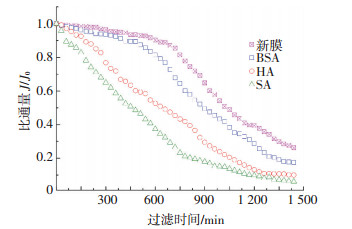
2.2 硫酸钙结垢实验有机污染试验后进行硫酸钙结垢污染实验,并将无有机污染的新膜作为对比,也进行硫酸钙结垢污染实验.以硫酸钙结垢污染实验开始时膜的初始通量为标准通量,对每一时刻的通量进行标准化处理.将4种硫酸钙结垢污染实验的膜通量随过滤时间衰减曲线绘制在同一张图中,结果如图 4所示.4种硫酸钙结垢膜通量衰减速率和衰减幅度为SA > HA > BSA >新膜,这与有机污染顺序一致.据此推测有机污染层生成以后,硫酸钙结垢行为与形成污染层的有机物的种类密切相关.
|
图 4 4种条件下硫酸钙结垢膜的比通量衰减曲线 Figure 4 Normalized flux decline curves of four gypsum scaling membranes |
硫酸钙结垢实验结束后,进行膜的反冲洗实验(膜不透水),之后再次进行基线实验以确定通量恢复率.以有机污染实验开始前,基线实验中的膜通量为标准通量,进行标准化处理.4种条件下的通量恢复率如图 5所示.

|
图 5 4种条件下膜的通量恢复率 Figure 5 Membrane flux recovery of four kinds of conditions |
在反冲洗后,膜通量恢复率为新膜> BSA > HA > SA.与硫酸钙结垢污染程度密切相关,说明在膜面已生成有机污染层的条件下生成的硫酸钙垢体更为稳定,难以去除.这是因为新膜与硫酸钙之间的作用力比有机物与新膜或有机物与硫酸钙之间的作用力小(具体将在2.5中阐述).
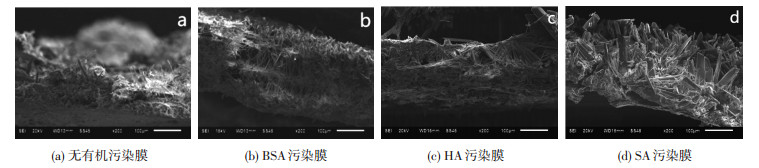
2.4 有机物对硫酸钙结垢的影响及结垢层形态为了更直观地理解有机污染层对硫酸钙结垢的影响,在硫酸钙结垢实验结束后,将膜取出并用SEM分析.硫酸钙结垢表面和断面图分别如图 6、7所示.可以看出,因有机污染物种类不同,硫酸钙晶体的大小、形状、密实度也不相同.无有机物污染的新膜表面硫酸钙晶体形状不规则(棒状、片状),并且尺寸相对较小,分布较分散(图 6(a));而BSA污染的膜表面硫酸钙晶体形状多为棒状,尺寸相对较小,结构较为松散(图 6(b));HA污染的膜表面硫酸钙晶体出现了一些尺寸较大的片状、块状结构(图 6(c));硫酸钙晶体在SA污染的膜表面为块状,尺寸最大,晶体沿中心向外侧生长(图 6(d)).从硫酸钙结垢的断面图(图 7)可知:在无有机物污染的膜表面,硫酸钙晶体层厚度非常薄,且排列不规则(图 7(a));在BSA污染的膜表面,硫酸钙晶体层厚度大,但结构松散(图 7(b));对于HA污染的膜,沿厚度方向有明显的硫酸钙晶体生长,结构也较为致密(图 7(c));硫酸钙晶体在SA污染的膜表面尺寸较大,在结垢层底部有薄且致密的污染层(图 7(d)).

|
图 6 不同膜条件下的硫酸钙晶体SEM表面图 Figure 6 SEM surface images of gypsum crystal of different fouling conditions |
|
图 7 不同膜条件下的硫酸钙晶体SEM断面图 Figure 7 SEM section images of gypsum crystal of different fouling conditions |
由此推测膜面形成的不同有机污染层对硫酸钙晶体生长的方式、速度和机理产生不同的影响.
2.5 AFM黏附力测定及硫酸钙结垢形成机理分子间黏附力与污染物在膜面的沉积密切相关,是预测及解析膜污染机理的有效手段[17].为更深入了解不同有机物对硫酸钙结垢的影响,采用AFM硫酸钙探针结合不同污染膜,测定不同膜面条件下膜-硫酸钙、硫酸钙-硫酸钙之间的黏附力并进行解析.AFM硫酸钙探针(图 8)所测定的黏附力与硫酸钙颗粒的半径成正比关系[18].为了避免不同硫酸钙探针的尺寸差异所致的黏附力大小差异,将所测定的黏附力除以探针上硫酸钙颗粒的半径(F/R).测力结果如图 9所示.

|
图 8 硫酸钙探针的SEM图 Figure 8 SEM image of the gypsum probe |

|
图 9 黏附力曲线图及相对应的频率分布 Figure 9 Representative adhesion force curves and frequency distributions of corresponding force |
图 9(a)、(c)为无有机污染的新膜和3种有机物污染膜与硫酸钙晶体之间的黏附力及其相应的黏附力概率分布.图 9(b)、(d)为4种纳滤膜面硫酸钙晶体之间的黏附力及其相应的黏附力概率分布.AFM所测黏附力平均值均为负值,代表作用力方向,与黏附力大小无关,故采用力的绝对值进行阐述.由图 9(a)可知,无有机污染的新膜、BSA污染、HA污染、SA污染膜与硫酸钙晶体之间的平均黏附力分别为0.220,0.218,0.254,0.308 mN/m;图 9(c)中上述4种黏附力所对应的最大概率分布区间与所测作用力的平均值相吻合.由图 9(b)可知,无有机污染、BSA污染、HA污染、SA污染条件下,硫酸钙晶体与硫酸钙晶体之间的平均黏附力分别为0.267,0.222,0.290,0.373 mN/m;图 9(d)中上述4种黏附力所对应的最大概率分布区间与所测作用力的平均值相吻合.
比较可知:1) 两种黏附力在3种有机污染的膜条件下,大小顺序均为SA > HA > BSA,与硫酸钙结垢污染实验膜通量衰减结果一致,进一步说明了硫酸钙结垢与有机物种类和性质密切相关.2) 膜-硫酸钙、硫酸钙-硫酸钙这两种黏附力均是无有机污染的新膜稍大于BSA污染膜,与硫酸钙结垢污染试验膜通量衰减结果不同.这是因为通量衰减是膜面化学和物理因素综合作用的结果.3) 4种条件下膜与硫酸钙晶体之间的黏附力均小于相应条件下硫酸钙晶体之间的黏附力.膜与硫酸钙晶体之间的黏附力较小,但是硫酸钙垢体在膜面的形成过程中,这种力必然会影响初期硫酸钙晶体的形成,进而对后期硫酸钙晶体之间的相互作用产生重要影响,因此,对硫酸钙垢体形成的程度和速率具有一定影响.
硫酸钙结垢有两种不同的机制[19]:1) 非均相或表面成核,晶体直接生长在膜表面.2) 均相成核,晶体形成在主体溶液中,然后沉积在膜表面.然而,先前的研究发现,膜材料表面性质的变化可能改变控制硫酸钙从均相到非均相结晶[11].同样,有机物可能会通过吸附改变膜表面性质,从而影响在膜表面的沉积.结合SEM所得硫酸钙晶体表面、断面图(图 6、7)证实:有机物大分子吸附在膜面改变了膜表面的性质,随后刺激非均相成核,晶核在过饱和溶液中继续生长成垢体[20].
有机物与硫酸钙之间的黏附力大小表明结垢开始时膜面不同有机物污染层对硫酸钙晶核的生成速率有不同的影响.因为SA是长链分子结构并具有大量的负电荷羧基官能团,羧基官能团有强烈的与Ca2+形成一个锯齿形结构而连接在一起的倾向,最终形成一个密集的海藻酸凝胶层,即多糖与二价阳离子形成的蛋盒(egg-box)结构凝胶污染层[21-22],所以,SA能迅速结合大量的Ca2+.由于静电作用的影响,这些Ca2+可以吸引大量的SO42-,使硫酸钙晶体开始在SA分子上生长,故SA可视作形成硫酸钙晶体的核[23].此外,由于SA作为晶核,晶体开始增长前成核所需的时间也会缩短,从而改变硫酸钙结晶的动力学,增大了形成的晶体尺寸,导致膜通量的迅速下降.同样,HA可以与Ca2+通过络合作用形成较大的络合物[10],分子间的架桥连接使得膜表面的结垢层更加致密,加速了膜通量的下降.然而,BSA在中性水溶液中具有一个心形结构[24],且只有少量羧基官能团,这种特殊的结构会干扰BSA分子与Ca2+之间的相互作用,一定程度上抑制了硫酸钙结垢的形成.
同时,滤饼增强浓差极化(CECP)理论[25]揭示了一个现象:随着过滤的进行,污染物会聚集在纳滤膜表面形成一个滤饼层,阻止盐离子反向扩散至体相溶液中,导致滤饼层附近盐离子浓度的增加.因此,在有机污染试验中,有机物在膜表面形成一个较薄的污染层,尽管这个污染层并没有严重地降低通量(图 3),但其在随后的硫酸钙结垢试验中可以增加Ca2+和SO42-在污染层(膜表面)的浓度.由于更高的离子浓度(更高的饱和指数),硫酸钙晶体形成速度加快.
由有机污染实验可知BSA污染条件下膜通量衰减最小(图 3),故可得出SA和HA污染层较BSA致密.而CECP与污染层结构有密切的关系,所以推得在硫酸钙结垢条件下SA和HA污染层引起的CECP作用较强,并且与Ca2+的结合能力较BSA污染层显著.而SA特殊的分子结构有利于大量结合Ca2+[26],这种特殊结构的凝胶层相对于HA与Ca2+所形成的污染层其密度和强度都比较大,导致凝胶层的水流阻力很大,因此受到水流剪切力的影响很小[27].所以,SA条件下的硫酸钙结垢污染导致的膜通量衰减均大于其他条件.
在原水预处理时,可以通过化学方法和物理方法结合达到分级处理的目的.如果可以有针对性的去除不同类型的天然有机大分子污染物,则可以有效降低硫酸钙结垢造成的纳滤膜污染,但具体的工程操作还需要进一步的探究.
3 结论1) BSA、HA、SA对膜的污染程度为SA > HA > BSA;4种膜面条件下膜的硫酸钙结垢污染程度为SA > HA > BSA >新膜.硫酸钙结垢污染后的通量恢复率为新膜> BSA > HA > SA.这说明SA污染条件下形成的硫酸钙结垢与膜面结合牢固,不易去除;也表明不同种类的有机物对纳滤膜的硫酸钙结垢有不同程度的影响.
2) SEM图像表明:3种有机物污染条件下生成的硫酸钙晶体在形态、厚度、紧密程度上各不相同,并且与无有机污染新膜的硫酸钙结垢有显著差异.
3) AFM测定了无有机污染的新膜-硫酸钙、3种有机物污染膜-硫酸钙之间的黏附力和上述4种膜面硫酸钙-硫酸钙之间的黏附力.两种黏附力在3种有机污染的膜条件下大小顺序均为SA > HA > BSA,与硫酸钙结垢污染实验结果一致;4种条件下的纳滤膜与硫酸钙晶体之间的黏附力小于硫酸钙晶体与硫酸钙晶体之间的黏附力.
4) SEM图像和黏附力测试结果说明:有机物大分子吸附在膜面改变了膜表面的性质,对硫酸钙晶体形成机理有显著影响.其中SA与Ca2+络合的蛋盒形结构和CECP作用是硫酸钙晶体成核时间缩短、晶体尺寸增大、纳滤膜通量迅速下降的主要原因.HA与Ca2+之间也存在相互作用,增大了结垢层的厚度与紧密程度.而BSA只有少量羧基官能团,并且特殊的分子结构干扰了有机物与Ca2+之间的结合,故硫酸钙结垢程度比其他有机污染条件稍轻.相比无有机污染的新膜,3种有机污染的膜面条件均加速了硫酸钙结垢.
5) 在原水预处理时,如果可以有针对性的去除不同类型的天然有机大分子污染物,则可以有效降低硫酸钙结垢造成的纳滤膜污染.但具体的工程操作还需要进一步的探究.
| [1] |
PETERSENR J. Composite reverse osmosis and nanofiltration membranes[J].
Journal of Membrane Science,1993, 83 (1) : 81-150.
( 0) 0)
|
| [2] |
MATSUURA T. Progress in membrane science and technology for seawater desalination:a review[J].
Desalination,2001, 134 (1) : 47-54.
( 0) 0)
|
| [3] |
韩璐, 王浩然, 王青林, 等. 天然有机物对纳滤膜污染的研究进展[J].
水资源与水工程学报,2012, 23 (2) : 48-53.
HAN Lu, WANG Haoran, WANG Qinglin, et al. Research of progress of natural organic to pollute nanofiltration membrane[J]. Journal of Water Resources & Water Engineering,2012, 23 (2) : 48-53. (  0) 0)
|
| [4] |
王磊, 福士宪一. 水中有机污染物的分子量分布特征对纳滤膜透水性能影响的试验研究[J].
给水排水,2003, 29 (7) : 35-37.
WANG Lei, FUKUSHI K. Experimental research on influences of nf performance by the apparent molecular weight distributions of organic pollutants in water[J]. Water & Wastewater Engineering,2003, 29 (7) : 35-37. (  0) 0)
|
| [5] |
FANE A G, WANG R, JIA Y.
Membrane technology:past, present and future[M]. Handbook of Environmental Engineering, 2011 : 1 -45.
( 0) 0)
|
| [6] |
刘家祺.
分离过程与技术[M]. 天津: 天津大学出版社, 2001 : 90 -92.
LIU Jiaqi. Separation process and technology[M]. Tianjin: Tianjin University Press, 2001 : 90 -92. (  0) 0)
|
| [7] |
CHOI J, FUKUSHI K, YAMAMOTO K. A study on the removal of organic acids from wastewaters using nanofiltration membranes[J].
Separation & Purification Technology,2008, 59 (1) : 17-25.
( 0) 0)
|
| [8] |
李晓明.海水纳滤软化过程中膜性能演变机制研究[D].青岛:中国海洋大学, 2008.
LI Xiaoming. Studies on membrane evolution mechanism of nanofiltration performance for seawater softening abstract[D]. Qingdao: Ocean University of China, 2008. (  0) 0)
|
| [9] |
LEE S, LEE C H. Effect of operating conditions on CaSO4 scale formation mechanism in nanofiltration for water softening[J].
Water Research,2000, 34 (15) : 3854-3866.
( 0) 0)
|
| [10] |
LEE S, CHOI J S, LEE C H. Behaviors of dissolved organic matter in membrane desalination[J].
Desalination,2009, 238 (1) : 109-116.
( 0) 0)
|
| [11] |
LIU Yaolin, MI Baoxia. Combined fouling of forward osmosis membranes: synergistic foulant interaction and direct observation of fouling layer formation[J].
Journal of Membrane Science,2012, 407/408 : 136-144.
( 0) 0)
|
| [12] |
GOUELLEC Y A L, ELIMELECH M. Calcium sulfate (gypsum) scaling in nanofiltration of agricultural drainage water[J].
Journal of Membrane Science,2002, 205 (1) : 279-291.
( 0) 0)
|
| [13] |
FAROOQUE A M, AL-AMOUDI A S, O'HARA J, et al. RO membrane failure: investigation of failure during preservation[J].
Filtration & Separation,2007, 44 (9) : 22-24.
( 0) 0)
|
| [14] |
LIU Yaolin, MI Baoxia. Effects of organic macromolecular conditioning on gypsum scaling of forward osmosis membranes[J].
Journal of Membrane Science,2014, 450 (2) : 153-161.
( 0) 0)
|
| [15] |
LEE S, CHO J, ELIMELECH M. Combined influence of natural organic matter (NOM) and colloidal particles on nanofiltration membrane fouling[J].
Journal of Membrane Science,2005, 262 : 27-41.
( 0) 0)
|
| [16] |
CORNELISSEN E R, SIEGERS W G, OGIER J, et al. Influence of calcium-NOM complexes on fouling of nanofiltration membranes in drinking water production[J].
Water Science & Technology Water Supply,2006, 6 (4) : 171-178.
( 0) 0)
|
| [17] |
WANG Lei, MIAO Rui, WANG Xudong, et al. Fouling behavior of typical organic foulants in polyvinylidene fluoride ultrafiltration membranes: characterization from microforces[J].
Environmental Science & Technology,2013, 47 (8) : 3708-3714.
( 0) 0)
|
| [18] |
COSTA A R, DE PINHO M N, ELIMELECHM. Mechanisms of colloidal natural organic matter fouling in ultrafiltration[J].
Journal of Membrane Science,2006, 281 (1/2) : 716-725.
( 0) 0)
|
| [19] |
MI B, ELIMELECH M. Gypsum scaling and cleaning in forward osmosis: measurements and mechanisms[J].
Environmental Science & Technology,2010, 44 (6) : 2022-2028.
( 0) 0)
|
| [20] |
周利民, 张士宾. 二水硫酸钙晶体生长及添加剂对它的影响(Ⅰ):二水硫酸钙成核及生长现象的研究[J].
海湖盐与化工,2001, 30 (2) : 15-17.
ZHOU Limin, ZHANG Shibin. The study of the phenomenon of nucleation and growth of calcium sulfate dihydrate (Ⅰ) :study on nucleation and growth of calcium sulfate in two water[J]. Sea-Lake Salt and Chemical Industry,2001, 30 (2) : 15-17. (  0) 0)
|
| [21] |
SIKORSKI P, MO F, SKJÅK-BRæK G, et al. Evidence for egg-box-compatible interactions in calcium-alginate gels from fiber X-ray diffraction[J].
Biomacromolecules,2007, 8 (7) : 2098-2103.
( 0) 0)
|
| [22] |
GRANT G T, MORRIS E R, REES D A, et al. Biological interactions between polysaccharides and divalent cations: the egg-box model[J].
Febs Letters,1973, 32 (1) : 195-198.
( 0) 0)
|
| [23] |
ANG W S, TIRAFERRI A, CHEN K L, et al. Fouling and cleaning of RO membranes fouled by mixtures of organic foulants simulating wastewater effluent[J].
Journal of Membrane Science,2011, 376 (1/2) : 196-206.
( 0) 0)
|
| [24] |
NG W S, ELIMELECH M. Protein (BSA) fouling of reverse osmosis membranes: implications for wastewater reclamation[J].
Journal of Membrane Science,2007, 296 (1/2) : 83-92.
( 0) 0)
|
| [25] |
HOEK E M V, ELIMELECH M. Cake-enhanced concentration polarization: a new fouling mechanism for salt-rejecting membranes[J].
Environmental Science & Technology,2003, 37 (24) : 5581-5588.
( 0) 0)
|
| [26] |
TONNESE H H, KARLSE J. Alginate in drug delivery systems[J].
Drug Development & Industrial Pharmacy,2002, 28 : 621-630.
( 0) 0)
|
| [27] |
李亚娟.反渗透膜有机污染的研究[D].上海:上海交通大学, 2010.
LI Yajuan. Research on organic fouling of reverse osmosis membrane[D].Shanghai: Shanghai Jiao Tong University, 2010. (  0) 0)
|
 2016, Vol. 48
2016, Vol. 48


