2. 城市水资源与水环境国家重点实验室(哈尔滨工业大学),哈尔滨 150090
2. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China
由于传统的硝化反硝化脱氮工艺在硝化阶段需要密集的曝气量,同时, 在反硝化阶段需要外加有机碳源,在处理低碳氮比废水时并不经济[1].全程自养脱氮工艺(CANON)是一种新型的脱氮工艺,污水中57%的NH4+-N在好氧氨氧化菌(AOB)作用下生成NO2--N, 生成的NO2--N与剩余的NH4+-N在厌氧氨氧化菌(AAOB)的作用下生成N2以及大约11%的NO3--N.CANON工艺不需要外加有机碳源,同时节约了63%的曝气量,被公认为是一种极为经济有效的脱氮方式[2-3].
目前,关于CANON工艺的研究取得了一定的进展,但是所用反应器形式大多为SBR[4-7].SBR反应器需要进水、反应、沉淀、排水、闲置等阶段,在反应期间基质质量浓度随时间不断下降,反应速率也会不断下降,相比之下在连续流反应器内,系统基质质量浓度不变,不会因基质质量浓度降低对反应速率产生影响.尤为重要的是,由于CANON工艺本身会产生大约11%的NO3--N,SBR在以一定比例的排水过程中会残留一部分硝氮,长此以往必将导致SBR反应器内硝氮质量浓度升高,影响出水水质.而连续流反应器采用连续进水的方式可以将反应器内的硝氮等物质及时排除,避免产生有害物质的积累, 影响反应器的脱氮性能[8].目前,黄鹏飞等[9]在UASB反应器内启动了厌氧氨氧化反应; 李德祥等[10]采用添加聚乙烯填料的方式在UASB反应器内成功实现了厌氧氨氧化污泥的颗粒化.然而,在连续流反应器内鲜有针对CANON颗粒污泥的研究, 对于大流量城市污水处理厂,针对连续进水的研究更具有现实意义.因此,本实验采用曝气上流式污泥床(aerated up-flow sludge blanket, AUSB)反应器,研究连续流CANON工艺的启动过程和脱氮性能.
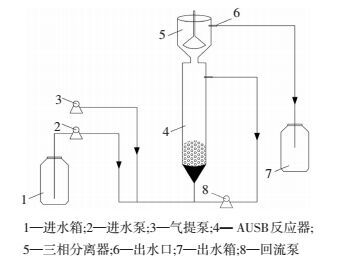
1 实验 1.1 实验装置与反应条件AUSB反应器内径8 cm,总容积为24 L,有效容积为16 L,具体结构如图 1所示.在反应器上方设置漏斗状的三相分离器,用以分离液体、污泥和反应过程中产生的气体.为了保持反应区恒温稳定在(28±1)℃,在反应器外部设有恒温水浴.为防止光能自养微生物繁殖,反应器外部采用黑布遮光.
|
图 1 实验装置示意 Figure 1 Experimental equipment schematic |
将SBR中稳定运行的亚硝化污泥接种至培养有厌氧氨氧化污泥的AUSB反应器内,接种后污泥质量浓度为4.36 g/L.在启动阶段的实验用水为人工配水,运行期间CANON工艺由于运行条件的不同经历了4个阶段,S1阶段进水NH4+-N质量浓度为95.19~107.16 mg/L,S2、S3、S4阶段进水NH4+-N质量浓度为160.19~176.73 mg/L, S1和S2阶段的水力停留时间为16 h,S3和S4阶段的水力停留时间分别为10和6 h,pH通过NaHCO3调节,本实验进水pH在7.8~8.2,出水pH在7.3~7.8,NaHCO3同时提供无机碳源,实验过程中没有人工排泥.
1.3 实验方法定期检测反应器内进出水NH4+-N、NO2--N、NO3--N(以下简称三氮)的质量浓度等参数, 通过WTW便携式测定仪监测DO、pH和水温等.水样分析中NH4+-N的测定采用纳氏试剂光度法, NO2--N采用N-(1-萘基)乙二胺光度法, NO3--N采用紫外分光光度法,颗粒粒径采用Mastersize2000型激光粒度仪进行检测,其余水质指标的分析方法均采用国标方法[11].
在系统运行的第28天、84天、125天从反应器中各取出1 L混合液,分别放入底部放置曝气环的1 L烧杯中,设置机械搅拌,分别测定CANON反应速率、Anammox反应速率及硝化反应速率, 用来表征AAOB和AOB的协同活性、厌氧氨氧化活性以及NOB的活性..烧杯内温度均为28 ℃, 碱度为进水总氮的10倍, pH为7.6左右, 每隔1 h取出水测定三氮, 待出水中三氮质量浓度不再发生变化时停止反应.测定CANON反应速率时, 进水只配氨氮(175 mg/L), 曝气量0.2 L/min.测定Anammox速率时, 进水配亚氮(95 mg/L)与氨氮(80 mg/L), 不曝气.测定硝化反应速率时, 进水只配亚氮(175 mg/L), 曝气量0.2 L/min.
总氮去除负荷、总氮去除率、氨氮氧化率、游离氨(FA)质量浓度以及CANON和Anammox反应速率的计算方法如下:
| $\begin{array}{*{20}{c}} {{\rho _{\rm{进水}}}\left( {{\rm{TN}}} \right) = {\rho _{\rm{进水}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right) + {\rho _{\rm{进水}}}\left( {{\rm{N}}{{\rm{O}}_2}^ - - {\rm{N}}} \right) + }\\ {{\rho _{\rm{进水}}}\left( {{\rm{N}}{{\rm{O}}_3}^ - - {\rm{N}}} \right),} \end{array}$ | (1) |
| $\begin{array}{*{20}{c}} {{\rho _{\rm{出水}}}\left( {{\rm{TN}}} \right) = {\rho _{\rm{出水}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right) + {\rho _{\rm{出水}}}\left( {{\rm{N}}{{\rm{O}}_2}^ - - {\rm{N}}} \right) + }\\ {{\rho _{\rm{出水}}}\left( {{\rm{N}}{{\rm{O}}_3}^ - - {\rm{N}}} \right),} \end{array}$ | (2) |
| $\Delta \rho \left( {{\rm{TN}}} \right) = {\rho _{\rm{进水}}}\left( {{\rm{TN}}} \right) - {\rho _{\rm{出水}}}\left( {{\rm{TN}}} \right),$ | (3) |
| ${\rm{总氮去除负荷}} = \frac{{\Delta \rho \left( {{\rm{TN}}} \right)}}{{{\rm{HRT}}}},$ | (4) |
| ${\rm{总氮去除率}} = \frac{{\Delta \rho \left( {{\rm{TN}}} \right)}}{{{\rho _{\rm{进水}}}\left( {{\rm{TN}}} \right)}} \times 100\% ,$ | (5) |
| ${\rm{氨氮氧化率}} = \frac{{{\rho _{\rm{进水}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right) - {\rho _{\rm{出水}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right)}}{{{\rho _{\rm{进水}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right)}} \times 100\% ,$ | (6) |
| $\rho \left( {{\rm{FA}}} \right) = \frac{{17 \times {\rho _{{\rm{in}}}}\left( {{\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}}} \right) \times {{10}^{{\rm{pH}}}}}}{{14 \times \left( {{{\rm{e}}^{6\;344/\left( {273 + T} \right)}} + {{10}^{{\rm{pH}}}}} \right)}},$ | (7) |
| ${v_{{\rm{CANON}},{\rm{Anammox}}}} = \frac{{{\rho _{\rm{始}}}\left( {{\rm{TN}}} \right) - {\rho _{\rm{末}}}\left( {{\rm{TN}}} \right)}}{{t \cdot {\rho _{{\rm{MLSS}}}}}},$ | (8) |
| ${v_{\rm{硝化}}} = \frac{{{\rho _{\rm{始}}}\left( {{\rm{N}}{{\rm{O}}_3}^ - - {\rm{N}}} \right) - {\rho _{\rm{末}}}\left( {{\rm{N}}{{\rm{O}}_3}^ - - {\rm{N}}} \right)}}{{t \cdot {\rho _{{\rm{MLSS}}}}}}.$ | (9) |
式中:ρ进水(NH4+-N)、ρ进水(NO2--N)、ρ进水(NO3--N)分别代表进水氨氮质量浓度、亚硝酸盐氮和硝酸盐氮质量浓度,ρ出水(NH4+-N)、ρ出水(NO2--N)、ρ出水(NO3--N)分别代表出水氨氮质量浓度、亚硝酸盐氮和硝酸盐氮质量浓度,ρin(NH4+-N)为反应器中氨氮质量浓度,t为水温.
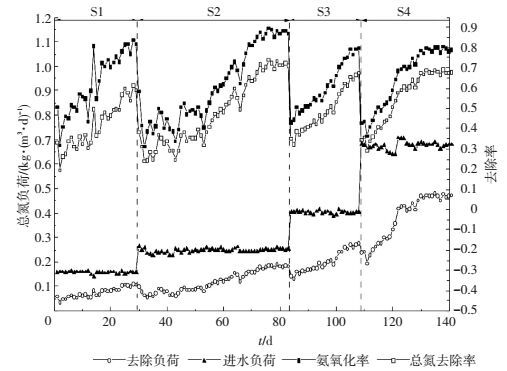
2 结果与讨论 2.1 反应器的脱氮效果 2.1.1 氨氮的转化和总氮的去除效果如图 2所示,不同进水条件下的总氮去除率和氨氧化率都经历了适应期和逐步增长期,并在各阶段的后期逐步趋向稳定.在整个运行期间,最高氨氧化率达到89%,总氮去除效果与氨氮氧化效果趋势大致相同,最高总氮去除率达到73%;在S4阶段后期,最高氨氧化率达到80%,最高总氮去除率达到了69%.国内外有关CANON工艺的报道中,总氮负荷在0.075~1.5 kg/(m3·d)[3, 12-13],Zhang Daijun等[14]的研究表明,在AUSB反应器内处理氨氮质量浓度在50~65 mg/L的废水时,CANON工艺的总氮负荷可以达到0.114 kg/(m3·d),并通过添加NO2的方式成功提升总氮负荷至0.234 kg/(m3·d).在本实验的运行过程中,总氮负荷会随着反应条件的改变在短时间内产生波动,总体上保持上升的趋势.在S4阶段的稳定期,最大总氮负荷达到了0.47 kg/(m3·d).
|
图 2 去除负荷、氨氧化率和总氮去除率变化 Figure 2 Variations of the total nitrogen removal load and ammonia oxidation rate and total nitrogen removal rate in influent and effluent |
由于自身的限制,CANON工艺的最高总氮去除率为88%.反应过程中的总氮去除率相对于氨氧化率偏小,根据张肖静等[7]的研究,分析原因主要是厌氧氨氧化过程产生一部分硝氮并且系统中NOB存在一定活性.为探究总氮去除率变化的影响因素,对系统出水氮元素进行了进一步的分析和讨论.
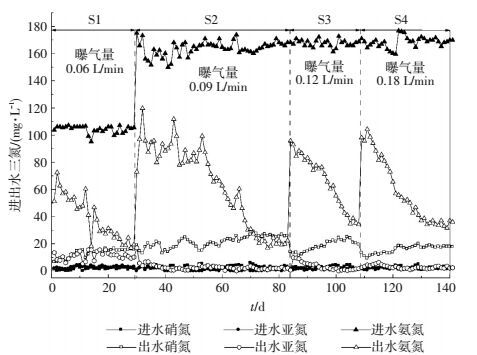
2.1.2 反应器运行条件和进出水氮元素变化如图 3所示,运行期间CANON工艺经历了4个阶段.实验的S1阶段(1~29 d)将来自于SBR反应器稳定运行的亚硝化污泥接种至富集有厌氧氨氧化菌的AUSB反应器内.在本实验中对于反应器曝气量的控制至关重要,如果在反应过程中氧气的供给量超出AOB所需,NO2--N就会在NOB的作用下转化为NO3--N[1].为了营造更适合CANON功能菌种的生存环境,控制反应器内DO为0.2 mg/L及以下,本实验S1阶段曝气量为0.06 L/min, 此阶段HRT为16 h.在接种初期,由于污泥的不适应性和污泥流失现象的存在,反应器的脱氮效果并不稳定.在经历了14 d的适应期后,脱氮效果得到稳定提升.
|
图 3 进、出水三氮质量浓度变化 Figure 3 Variations of ammonia nitrogen concentration and nitrite nitrogen concentration and nitrate concentration in influent and effluent |
在S2(30~84 d)阶段,增加进水氨氮质量浓度至170 mg/L, 此时反应器内FA质量浓度相应提高.在第30~50天内,总氮负荷并未得到明显提升.在全程自养脱氮工艺中,功能菌种生长缓慢.在氨饱和的情况下,氨氧化菌受供氧量的制约,厌氧氨氧化菌受亚硝酸盐量的制约.
因此,在本实验反应初期,氨氧化菌的活性和生长速度受到供氧量的限制.李冬等[7]的研究表明:在DO为0~0.40 mg/L内,提高曝气量可以提高全程自养脱氮工艺的总氮去除效率.因此,第50天开始,将曝气量从0.06 L /min增至0.09 L /min,此条件下检测出水溶解氧为0.2 mg/L.经过一段时间运行后,系统的出水NH4+-N开始降低,总氮去除率和氨氧化率得到逐步提升,在第85天分别上升至73%和89%,说明有限制地增加曝气量,可以提高AOB的活性以及生长速率,为厌氧氨氧化提供更多的反应基质,从而提高反应器的总氮去除效果.
在运行过程中,控制硝氮的产生极为重要,因为较多的硝氮生成势必影响实验的总氮去除率和出水水质.在全程自养脱氮过程中,硝氮的产生与转换一般存在两种路径[15]:首先在氧气供给充足的情况下,NOB可以利用NO2--N转换为NO3--N,另外由于细胞裂解等而存在有机碳源的情况下反硝化菌可以将NO3--N转换为N2.在本实验中,并不投加有机碳源,基本忽略反硝化作用的影响.根据Anthonisen等[16]的研究成果:FA对AOB和NOB都有抑制作用,对AOB的抑制质量浓度范围为13.34~73.6 mg/L,对NOB的抑制质量浓度范围为0.1~1.0 mg/L,若控制FA质量浓度在这二者之间,即可起到只抑制NOB而不抑制AOB的效果.在S2阶段计算得出反应器中的平均游离氨质量浓度为1.35 mg/L,介于NOB与AOB的抑制质量浓度范围之间,可以对NOB产生抑制作用.在此阶段后期,最大硝氮出水质量浓度达30 mg/L,说明在现有运行条件下,NOB活性并没有完全被抑制.
因此,为了缩短反应时间,将氨氮转为限制在亚硝氮的阶段,以达到限制NOB的目的[17],在S3(85~108 d)和S4(109~135 d)阶段分别降低HRT为10和6 h.S3和S4阶段反应器的曝气量分别为0.12和0.18 L/min.在改变HRT的初期反应器的脱氮性能下降,在运行环境稳定后反应器的脱氮性能逐步提升.在S4阶段,最大出水硝氮质量浓度为19.6 mg/L,Δρ(TN)/Δρ(NO3--N)接近于理论值8,说明采用增大进水负荷的方式促进了微生物的生长,构建出更适合CANON功能菌种的生长条件,NOB得到逐步淘汰.同时随着进水负荷的增大,反应器的实际脱氮能力也得到提高,在S4阶段最大总氮负荷达0.47 kg/(m3·d).在多种生物种群的共同作用下,本实验表现出了高效的去除效果,反应期间的最大总氮去除率和氨氧化率分别达到了73%和89%.通过竞争和与多种氮循环菌种的共同作用,AOB和厌氧氨氧化菌逐步成为优势菌种.
2.2 反应器脱氮性能提高原因 2.2.1 不同时间的污泥质量浓度比较在CANON工艺中,由于厌氧氨氧化菌较长的倍增时间(11 d)[18]致使基于其开发的工艺必须具有良好的污泥持留能力,避免功能菌种洗出系统.
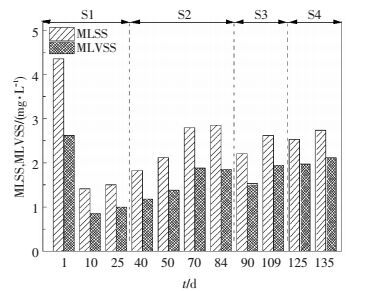
本实验考查了连续流反应器的污泥持留能力,图 4为反应器内污泥质量浓度随时间变化的示意.相比SBR反应器,污泥接种至AUSB反应器以后,要承受底部上升流速的影响,因此,沉降性能不好的松散污泥发生流失,在本实验前期反应器内污泥质量浓度不断下降.在反应器运行一段时间后,微生物对新环境不断适应,污泥质量浓度开始稳步提高,在第50天上升至2.14 g/L,此后污泥质量浓度上升趋势开始放缓,第84天反应器内污泥质量浓度为2.86 g/L.在S3和S4阶段,由于HRT的改变,上升流速变大,污泥流失现象再次出现.随着时间的推移,在反应器内水流剪切力、上升气流剪切力和污泥之间碰撞的共同作用下,微生物之间的黏结作用增强,细小颗粒开始向一起聚拢.在S3和S4阶段初期,虽然仍有污泥流失现象的出现,但是并未出现S1阶段初期污泥质量浓度持续降低的现象,说明反应器内微生物逐渐适应了水流剪切力的存在,通过形成较大的颗粒来抵抗剪切力对微生物的冲击,以此适应环境的变化.在本实验运行期间,污泥质量浓度体现出先降后升的趋势,在环境变化初期出现波动,反应后期的波动没有初期明显.
|
图 4 反应器内污泥质量浓度 Figure 4 Variations of the sludge concentration in the reactor |
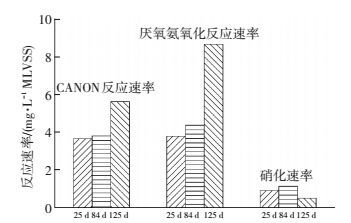
本实验测定了CANON反应速率、Anammox反应速率以及硝化反应速率,结果如图 5所示.可以看出,在较高氨氮质量浓度条件下的厌氧氨氧化菌和AOB活性较高,相比第25天,第84天的各项反应指标得到小幅提升.经过一段时间的培养,AOB和厌氧氨氧化菌的活性小幅提高,但此时反应器内的污泥质量浓度由第25天的1.52 g/L上升至2.86 g/L,总氮负荷由0.106 g/(L·d)上升至0.181 g/(L·d),因此,推测反应器的总氮负荷提高主要是由微生物浓度上升造成的.此阶段较大的HRT下,系统内进水流速和水流剪切力较小,此条件下有利于微生物的富集,这与冯骞等[19]的研究结果相似.
|
图 5 反应器不同时间段的反应速率比较 Figure 5 Comparison of reaction rate in different time periods in the reactor |
相比第84天,第125天的CANON反应速率和厌氧氨氧化反应速率均得到明显提高,同时在第60天,系统内出现可以肉眼观察到的颗粒.在连续流系统以较小的HRT运行的条件下,进水流量变大使得反应区内基质和污泥更充分地接触,进水负荷较高,在此条件下污泥生长较快.图 5显示第125天硝化速率下降,可以看出经过S3,S4阶段的培养,NOB活性得到抑制.此时反应器内微生物质量浓度由2.86 g/L变为2.73 g/L,并没有发生明显变化,总氮负荷上升至0.451 g/(L·d).一般认为,HRT越短,越容易导致污泥流失,不利于系统脱氮负荷的提高[20-22],然而对于连续流反应器,较小的HRT意味着较大的进水流速和水流剪切力,更有利于颗粒污泥的形成.国内外学者研究显示:在全程自养脱氮工艺中,在合适的条件下,污泥会形成外部好氧内部厌氧的颗粒,脱氮效率远远高于普通絮状污泥,从而保证了总氮去除效率[5, 23-24]. 图 6为反应器内不同时间CANON颗粒污泥粒径变化.本实验中,反应器的底部装有曝气头,在上升气流和水流共同产生的水流剪切力刺激下,颗粒污泥的粒径出现了持续增长.

|
图 6 颗粒污泥粒径变化 Figure 6 Variations of granular sludge particle size |
综合反应器内污泥质量浓度变化,分析认为前期反应器总氮负荷的上升,主要归因于污泥质量浓度的提高,而在改变系统的水力停留时间后,则是由于微生物活性明显提高,且微生物结构从松散状态形成更为紧实的结构.相比接种初期,反应器的污泥质量浓度和微生物活性都得到提高,在污泥质量浓度升高和微生物活性增强的共同作用下,系统的脱氮能力得以提升.
2.3 反应器中Δρ(TN)/Δρ(NO3--N)趋势变化在本实验中,对于系统出水硝氮的控制尤为重要.在不考虑存在硝化反应的情况下,根据CANON工艺的反应式,Δρ(TN)/Δρ(NO3--N)的理论值应为8,因此,将此值作为衡量本实验硝化反应进行程度的标准,分析NOB的被抑制程度.
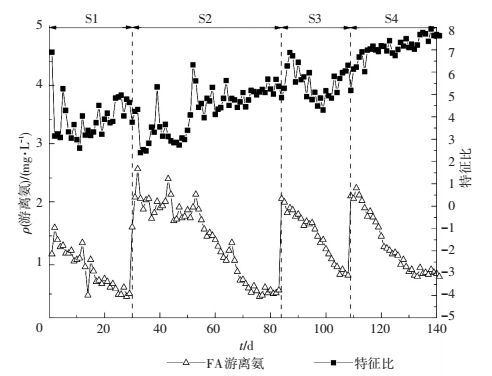
反应器运行期间游离氨和Δρ(TN)/Δρ(NO3--N)的比值如图 7所示,在反应初期由于HRT较长,且平均游离氨质量浓度较低,在S1和S2阶段特征值远低于理论值8,NOB仍保有一定活性.经历了S3和S4阶段后,特征比在S4阶段后期已经稳定在8左右,表明此时NOB已被淘洗,说明在本实验条件下,采用降低HRT的方式缩短反应时间,将反应停留在亚氮阶段,可以达到抑制NOB的目的.有研究表明,在25 ℃以上,AOB生长速率高于NOB[25-26],且AAOB活性随温度变化趋势较NOB明显[27];同时,Anthonisen等[16]的研究也指出,NOB比AOB对高FA质量浓度更敏感,因此,可以通过较高的FA质量浓度实现对NOB的抑制.反应期间反应器内平均FA为1.26 mg/L,在此条件下,AOB和AAOB保持着高于NOB的生长速率.在连续流反应器内,少量污泥会在上升气流和水流的作用下随出水排出,经过一段时间的培养,更有利于淘汰NOB.由于进水流速增大,上升气体与上升水流使反应器内气液充分混合,气液间传质效率也大幅提高,有利于微生物生长,保证了AAOB和AOB逐渐成为反应器内的主要功能菌种.在S4阶段后期,出水硝氮维持在较低水平,Δρ(TN)/Δρ(NO3--N)连续15 d在7以上,认为在连续流反应器内,CANON颗粒污泥启动成功.
|
图 7 游离氨质量浓度及Δρ(TN)/Δρ(NO3--N)变化 Figure 7 Variations of the free ammonia concentration and Δρ(TN)/Δρ(NO3--N) in the reactor |
1) 连续流反应器中,在限氧条件下采用增加进水和降低HRT的方式在135 d内实现了CANON颗粒污泥的启动.
2) 在启动期间,最高总氮去除率和去除负荷分别为73%和0.47 kg/(m3·d),最高氨氧化率达89%,氨氮和总氮去除效果较为理想.
3) 在反应运行的140 d内,污泥质量浓度总体上先降后升,而后趋于稳定.系统内AAOB和AOB活性均得到提高.在污泥质量浓度升高和微生物活性增强的共同作用下,系统的脱氮能力得到提升.
| [1] |
MULDER A, GRAAF A A V D, ROBERTSON L A, et al. Anaerobic ammonium oxidation discovered in a denitrifying fluidized bed reactor[J].
Fems Microbiology Ecology, 1995, 16(3): 177-183.
DOI: 10.1111/fem.1995.16.issue-3 |
| [2] |
SLIEKERS A O, DERWORT N, GOMEZ J C, et al. Completely autotrophic nitrogen removal over nitrite in one single reactor[J].
Water Research, 2002, 36(10): 2475-2482.
DOI: 10.1016/S0043-1354(01)00476-6 |
| [3] |
胡石, 甘一萍, 张树军, 等. 一体化全程自养脱氮(CANON)工艺的效能及污泥特性[J].
中国环境科学, 2014(1): 111-117.
HU Shi, GAN Yiping, ZHANG Shujun, et al. Performance and sludge characteristics of the CANON process[J]. China Environmental Science, 2014(1): 111-117. |
| [4] |
廖德祥, 李小明, 曾光明, 等. 单级SBR生物膜中全程自养脱氮的研究[J].
中国环境科学, 2005, 25(2): 222-225.
LIAO Dexiang, LI Xiaoming, ZENG Guangming, et al. Studies on deammonification process in single SBR biofilm[J]. China Environmental Science, 2005, 25(2): 222-225. |
| [5] |
肖洋, 廖德祥, 李小明, 等. 全程自养脱氮颗粒污泥培养及动力学研究[J].
环境科学, 2009, 30(9): 2667-2673.
XIAO Yang, LIAO Dexiang, LI xiaoming, et al. Enrichment and dynamic analysis of deammonification granules[J]. Environmental Science, 2009, 30(9): 2667-2673. |
| [6] |
唐林平, 廖德祥, 李小明, 等. 全程自养脱氮污泥颗粒化及其脱氮性能的研究[J].
环境科学, 2009, 30(2): 411-415.
TANG Linping, LIAO Dexiang, LI Xiaoming, et al. Cultivation and nitrogen removal characteristics of deammonifition granules[J]. Environmental Science, 2009, 30(2): 411-415. |
| [7] |
李冬, 崔少明, 梁瑜海, 等. 溶解氧对序批式全程自养脱氮工艺运行的影响[J].
中国环境科学, 2014, 34(5): 1131-1138.
LI Dong, CUI Shaoming, LIANG Yuhai, et al. The effect of dissolved oxygen on running canon process in sequencing batch reactor[J]. China Environmental Science, 2014, 34(5): 1131-1138. |
| [8] |
虢清伟. UASB的快速启动与改进型UASB对高质量浓度有机废水处理技术的研究[D]. 长沙: 湖南农业大学, 2003.
GUO Qingwei. Studies on rapid start-up of UASB reactor and wastewater treatment technology on high concentration organic materials by improved UASB reactor[D].Changsha:Hunan Agricultural University, 2003. |
| [9] |
黄鹏飞, 张锦耀, 秦玉洁, 等. 高流速启动ANAMMOX-UASB反应器及其脱氮特性[J].
中国给水排水, 2014(17): 9-13.
HUANG Pengfei, ZHANG Jinyao, QIN Yujie, et al. Start-up of anammox /uasbreactor with high rate and its nitrogen removal performance[J]. China Water and Wastewater, 2014(17): 9-13. |
| [10] |
李德祥, 李冬, 吴迪, 等. 改良型UASB厌氧氨氧化工艺研究[J].
中国给水排水, 2013, 29(21): 33-37.
LI Dexiang, LI Dong, WU Di, et al. Study on anaerobic ammonium oxidation in improved UASB reactor[J]. China Water and Wastewater, 2013, 29(21): 33-37. |
| [11] |
国家环境保护总局.
水和废水监测分析方法[M]. 北京: 中国环境出版社, 2013.
State Environmental Protection Administration of China. Methods for monitoring and analysis of water and wastewater[M]. Beijing: Chinese Environmental Science Press, 2013. |
| [12] |
左早荣, 付昆明, 仇付国, 等. CANON工艺的研究现状及面临困难分析[J].
水处理技术, 2013, 9: 4.
ZUO Zaorong, FU Kunming, QIU Fuguo, et al. Research status and difficulties analysis of CANON process[J]. Technology of Water Treatment, 2013, 9: 4. |
| [13] |
廖德祥. 全程自养脱氮及其颗粒化的研究[D]. 长沙: 湖南大学, 2005.
LIAO Dexiang. Granulation of deammonifieation mieorogranism in sbrreactor[D].Changsha:Hunan University, 2005. http://cdmd.cnki.com.cn/Article/CDMD-10532-2005125419.htm |
| [14] |
ZHANG Daijun, CAI Qing, CONG Liying. Enhancing completely autotrophic nitrogen removal over nitrite by trace NO2 addition to an AUSB reactor[J].
Journal of Chemical Technology and Biotechnology, 2010, 85(2): 204-208.
|
| [15] |
郑平.
新型生物脱氮理论与技术[M]. 北京: 科学出版社, 2004.
ZHENG Ping. New biological nitrogen removal theory and technology[M]. Beijing: Science Press, 2004. |
| [16] |
ANTHONISEN A C, LOEHR R C, PRAKASAM T B S, et al. Inhibition of nitrification by ammonia and nitrous acid[J].
Journal-Water Pollution Control Federation, 1976, 48(5): 835-852.
|
| [17] |
张肖静, 李冬, 梁瑜海, 等. MBR-CANON工艺处理生活污水的快速启动及群落变化[J].
哈尔滨工业大学学报, 2014, 46(4): 25-30.
ZHANG Xiaojing, LI Dong, LIANG Yuhai, et al. Rapid start-up of CANON treating domestic wastewater and the community dynamics in MBR[J]. Journal of Harbin Institute of Technology, 2014, 46(4): 25-30. DOI: 10.11918/j.issn.0367-6234.2014.04.005 |
| [18] |
STROUS M, HEIJNEN J J, KUENEN J G, et al. The sequencing batch reactor as a powerful tool for the study of slowly growing anaerobic ammonium-oxidizing microorganisms[J].
Applied Microbiology & Biotechnology, 1998, 50(5): 589-596.
|
| [19] |
冯骞, 薛朝霞, 汪翙, 等. 水流剪切力对活性污泥特性影响的实验研究[J].
河海大学学报(自然科学版), 2006, 34(4): 374-377.
FENG Qian, XUE Zhaoxia, WANG Hui, et al. Experimental study on the influence of flow shear force on activated sludge characteristics[J]. Journal of Hohai University(Natural Sciences), 2006, 34(4): 374-377. |
| [20] |
管锡君, 郑西来, 康艳. 现行的UASB反应器的设计问题及改良的可行性[J].
水处理信息报导, 2004, 22(2): 54-55.
GUAN Xijun, Zheng Xilai, KANG Yan. The design of UASB reactor and the feasibility of its improvement[J]. Water Treatment Information Coverage, 2004, 22(2): 54-55. |
| [21] |
胡勇, 尚连生, 刘永红, 等. 厌氧颗粒污泥床反应器污泥的流失与对策[J].
工业用水与废水, 2007, 38(4): 6-8.
HU Yong, SHANG Liansheng, LIU Yonghong, et al. Sludge wash-out from anaerobic granular sludge bed reactor and countermeasure there of[J]. Industrial Water and Wastewater, 2007, 38(4): 6-8. |
| [22] |
李红亮. EGSB反应器优化设计与性能研究[D]. 哈尔滨: 哈尔滨工业大学, 2007.
LI Hongliang.Optimization design and research of performance of EGSB[D]. Harbin:Harbin Institute of Technology, 2007. |
| [23] |
VLAEMINCK S E, CLOETENS L F, CARBALLA M, et al. Granular biomass capable of partial nitritation and anammox[J].
Water Science & Technology. A Journal of the International Association on Water Pollution Research, 2009, 59(3): 610-617.
|
| [24] |
LI X, XIAO Y, LIAO D, et al. Granulation of simultaneous partial nitrification and anammox biomass in one single SBR system[J].
Applied Biochemistry and Biotechnology, 2011, 163(8): 1053-1065.
DOI: 10.1007/s12010-010-9108-8 |
| [25] |
FUX C, BOEHLER M, HUBER P, et al. Biological treatment of ammonium-rich wastewater by partial nitritation and subsequent anaerobic ammonium oxidation (anammox) in a pilot plant[J].
Journal of Biotechnology, 2002, 99(3): 295-306.
DOI: 10.1016/S0168-1656(02)00220-1 |
| [26] |
HELLINGA C, SCHELLEN A A J C, MULDER J W, et al. The sharon process: An innovative method for nitrogen removal from ammonium-rich waste water[J].
Water Science & Technology, 1998, 37(9): 135-142.
|
| [27] |
张杰, 付昆明, 曹相生, 等. 序批式生物膜CANON工艺的运行与温度的影响[J].
中国环境科学, 2009, 29(8): 850-855.
ZHANG Jie, FU Kunming, CAO Xiangsheng, et al. Performance of CANON process in a sequencing batch biofilm reactor and influence of temperarure[J]. China Environmental Science, 2009, 29(8): 850-855. |
 2017, Vol. 49
2017, Vol. 49


