2. 城市水资源与水环境国家重点实验室(哈尔滨工业大学), 哈尔滨 150090
2. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China
亚硝化-厌氧氨氧化工艺因节省曝气、无需外加碳源、污泥产量低等优点成为目前已知最为节能、经济的脱氮途径[1-3], 而该工艺未能在生活污水中推广和应用的主要瓶颈在于,生活污水低NH4+-N且水质、水量波动较大的特点使亚硝化很难稳定运行. Ma等[4]指出亚硝化一旦失稳后很难恢复, 因此,对于失稳后的亚硝化“如何使其高效地恢复”是亚硝化工程应用上必须解决的难题.然而, 目前文献中提到的对亚硝化进行恢复的研究很少.如果采用与启动相似的高温[5]、高游离氨(FA)[6]、高游离亚硝酸(FNA)[7]的方式进行恢复, 常温低NH4+-N的实际生活污水在不投加药剂、不加热下很难达到.张功良等[8]在SBR中通过前置厌氧和降低溶解氧(DO)的方式实现了亚硝化的高效恢复, 这说明设置厌氧段能抑制NOB.但该研究存在以下两个问题, 一是采用模拟生活污水而非实际生活污水, 这对于实际工程的指导意义有限; 二是在SBR中运行, 而实际水厂均是连续运行.能否在连续流实际生活污水中进一步增加厌氧段的长度, 即先厌氧/厌氧后好氧/好氧运行, 或者一直采用厌氧/好氧运行来实现亚硝化的高效快速恢复, 还有待进一步研究.
为此, 采用两组两级CSTR (1#和2#), 1#采用厌氧/厌氧后好氧/好氧的运行方式, 2#一直采用厌氧/好氧运行, 对亚硝化恢复时间和恢复后稳定性进行比较, 以期为亚硝化的工程应用提供技术支持.
1 实验 1.1 实验装置和方法实验在北京某污水厂进行, 采用两组相同的两级CSTR (1#、2#), 如图 1所示.两级CSTR各级有效容积为7 L, 图中通气管的目的是使两级CSTR水流通畅, 每一级底部设置曝气沙盘, 通过可调式气泵为反应过程提供溶解氧, 由转子流量计控制气量.如表 1所示, 实验分为3个阶段, 在S1阶段1#采用厌氧/厌氧的运行方式, 厌氧段只搅拌不曝气, 不控制DO, 经检测DO在0~0.1 mg/L. 1#S1阶段的时间长度采用氨化率法, 即当氨氧化率连续5 d低于10%则进入S2阶段, 在S2阶段改变1#运行方式为好氧/好氧运行, 1#两级搅拌并曝气, 根据AOB氧饱和常数为0.2~0.4 mg/L, NOB氧饱和常数为1.2~1.5 mg/L[9], 控制两级DO分别为0.2~0.4和0.6~0.8 mg/L, 两级DO梯度是为了NO2--N更好地积累[10].2#在S1和S2阶段一直采用厌氧/好氧运行, 第一级只搅拌不曝气, 经检测DO在0~0.1 mg/L, 第二级搅拌并曝气, 控制DO在0.6~0.8 mg/L.

|
图 1 反应器装置示意 Figure 1 Schematic diagram of the experimental equipment |
| 表 1 各阶段反应器参数变化 Table 1 Parameter variations of reactors in each stage |
为比较恢复后亚硝化的稳定性, 进行S3阶段的研究.现有污水处理厂一般采用固定曝气的方式, 由于生活污水水质、水量波动较大的特点, 当进水NH4+-N质量浓度下降时必然会引起过度曝气, 在S3阶段分别提高1#和2#曝气量, 使二者两级DO均在1.0~1.2 mg/L, 这样比较恢复后亚硝化的稳定性更具有实际意义.
1.2 实验用水和接种污泥在整个实验过程中1#与2#进水水质相同, 均采用城市污水厂原污水经AO除磷后的出水为进水, 具体水质:NH4+-N质量浓度为35~43 mg/L, COD<50 mg/L (几乎全部是微生物难降解的物质), ρ(NOx--N)<2 mg/L. 1#和2#的接种污泥来自失稳的两级CSTR, 亚硝化率为25.2%, 氨氧化率为90.1%, MLSS为2 800 mg/L, MLVSS为2 100 mg/L, 污泥沉降性能良好, SVI为95 mL/g.
1.3 分析方法和计算方法定期检测反应器内混合液的MLSS、SV30及进出水NH4+-N、NO2--N、NO3--N质量浓度等参数, 通过WTW便携式测定仪测定DO、pH和水温等.水样分析中NH4+-N的测定采用纳氏试剂光度法, NO2--N采用N-(1-萘基)乙二胺光度法, NO3--N采用紫外分光光度法, COD采用快速测定仪.
氨氧化率(RA)、亚硝化率(RN)和游离氨(FA)和游离亚硝酸(FNA)按下式计算:
| $ {R_{\rm{A}}} = \frac{{\rho ({\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}})}}{{{\rho _{in}}({\rm{N}}{{\rm{H}}_4}^ + - {\rm{N}})}} \times 100\% . $ | (1) |
式中:ρin (NH4+-N)为进水NH4+-N质量浓度, mg/L; ρ(NH4+-N)为进出水NH4+-N质量浓度差, mg/L.
| $ {R_{\rm{N}}} = \frac{{\rho ({\rm{N}}{{\rm{O}}_2}^ - - {\rm{N}})}}{{\rho ({\rm{N}}{{\rm{O}}_2}^ - - {\rm{N}}) + \rho ({E_3}^ - - {\rm{N}})}} \times 100\% . $ | (2) |
式中:ρ(NO2--N)为进出水NO2--N的质量浓度差, mg/L; ρ(NO3--N)为进出水NO3--N的质量浓度差, mg/L.
| $ \rho \left( {{\rm{FA}}} \right) = {\frac{{17 \times {\rho _{{\rm{inner}}}}({\rm{N}}{{\rm{H}}_4}^ + {\rm{ - N}}) \times {{10}^{{\rm{pH}}}}}}{{14 \times ({{\rm{e}}^{6{\rm{ }}344/(273 + {\rm{T}})}} + {{10}^{{\rm{pH}}}})}}^{\left[ {11} \right]}}. $ | (3) |
式中:ρinner (NH4+-N)为反应器内NH4+-N质量浓度, mg/L; T为水温, K.
| $ \rho \left( {{\rm{FNA}}} \right) = {\frac{{47 \times {\rho _{{\rm{inner}}}}({\rm{N}}{{\rm{O}}_2}^ - {\rm{ - N}})}}{{14 \times ({{\rm{e}}^{ - 2{\rm{ }}300/(273 + {\rm{T}})}} \times {{10}^{{\rm{pH}}}} + 1)}}^{\left [ {11} \right]}}. $ | (4) |
式中:ρinner (NO2--N)为反应器内NO2--N质量浓度, mg/L; T为水温, K.
1.4 比氨氧化速率和比亚硝酸盐氧化速率的测定在实验过程中定期从1#和2#中取出100 mL活性污泥进行硝化细菌活性测试实验.首先将污泥利用各自反应器出水进行搅拌并清洗3遍, 去除上清液; 然后将污泥稀释到400 mL, 置于500 mL的广口瓶内, 同时采用0.1 mol/L HCl和0.1 mol/L NaOH将体系的pH控制在7.5±0.05内.实验过程中, 首先向体系中加入20 mg/L NO2--N测定NOB的底物降解速率, 曝气1 h后, 再次向体系中加入30 mg/L NH4+, AOB和NOB的活性分别以比氨氧化速率(specific ammonia oxidation rate, RSAO)和比亚硝酸盐氧化速率(specific nitrite oxidation rate, RSNO)表征[12].
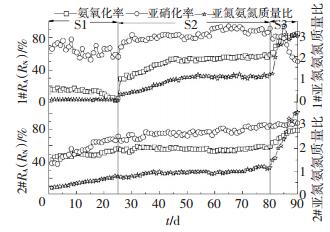
2 结果和讨论 2.1 S1阶段亚硝化效果比较在S1阶段1#采用厌氧/厌氧的运行方式.如图 2所示,氨氧化率由接种前的90.10%下降到第20天的10.29%, 且在第21~25天一直在10%以下.2#采用厌氧/好氧的运行方式, 氨氧化率由接种前的90.1%下降到第25天的57.18%.在整个S1阶段, 1#和2#氨氧化率的平均值分别为15.24%和50.17%, 均远低于接种时氨氧化率(90.1%), 同时亚硝化率平均值分别为64.38%和56.76%, 均比接种前的25.6%高.这说明两种厌氧运行均抑制了NOB, 有利于亚硝化的恢复, 同时氨氧化率的下降也说明两种运行方式抑制了AOB的活性.
|
图 2 1#和2#氨氧化率和亚硝化率变化 Figure 2 Variation of ammonia oxidation rate and nitrite accumulation rate in 1# and 2# |
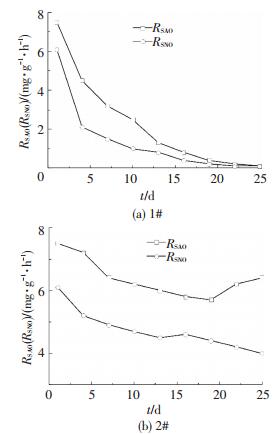
为了更深入地分析两种运行方式对亚硝化恢复的作用, 分别对1#和2#中的RSAO (比氨氧化速率)和RSNO (比亚硝酸盐氧化速率)进行测定.如图 3所示, 1# RSAO一直在下降, 由开始7.5 mg/(g·h)下降到0.1 mg/(g·h), RSNO由第1天的6.1 mg/(g·h)下降到第25天的0.1 mg/(g·h), 而2# RSAO下降较小, 仅由7.5 mg/(g·h)下降到6.4 mg/(g·h), 且在第22~25天回升, RSNO也下降较小, 由开始的6.1 mg/(g·h)下降到4 mg/(g·h).这说明与厌氧/好氧相比, 厌氧/厌氧对AOB和NOB的抑制作用更明显, 同时在厌氧/好氧条件下, RSAO在第22天出现回升.原因是AOB对供氧条件突变有个适应过程, 待适应条件后, 活性开始恢复.
|
图 3 S1阶段1#和2# RSAO和RSNO变化 Figure 3 Variation of RSAO and RSNO in 1# and 2# during S1 |
为使亚硝化快速恢复, 在S2阶段对1#全程采取好氧运行, 控制1#两级DO分别为0.2~0.4和0.6~0.8 mg/L.因为2#在第25天时亚硝化率仅为72.6%, 说明厌氧/好氧下, NOB活性没有被完全抑制, 故2#继续保持厌氧/好氧运行.
如图 2所示, 从S1过渡到S2阶段, 1#亚硝化率和氨氧化率均发生突跃, 氨氧化率由5.52%增加到29.33%, 亚硝化率由56.52%增加到68.93%, 到第59天时增加到91.26%, 且在第59~80天一直保持在85%以上, NO2--N和NH4+-N质量比在1~1.32, 平均值为1.11, 满足厌氧氨氧化进水要求, 而2#亚硝化率由第26天的66.67%上升到第71天的84.36%且在第71~80天期间保持在83%以上, NO2--N和NH4+-N质量比在1~1.32, 平均值为1.12, 也满足厌氧氨氧化进水要求, 这说明1#和2#亚硝化均得到恢复并成功过渡到半亚硝化.原因是二者采用的不同厌氧运行方式最终均抑制了NOB的活性, 使亚硝化得到恢复.然而2#曝气量比1#小, 而二者氨氧化率相当, 其主要原因可能是2#厌氧/好氧方式筛选出活性更高的AOB.如图 4所示, 2#亚硝化稳定期间RSAO平均值为9.4 mg/(g·h), 比1# 8.6 mg/(g·h)提高了9.30%, 这与高春娣等[13]指出的缺氧/好氧有利于筛选出RSAO较高的AOB结果相吻合.

|
图 4 S2和S3阶段1#和2# RSAO和RSNO变化 Figure 4 Variation of RSAO and RSNO in 1# and 2# during S2 and S3 |
对S2阶段RSAO和RSNO进行测定, 如图 4所示, 在S2阶段1#RSAO发生了一次突越, 由第25天的0.1 mg/(g·h)增加到第28天的4.5 mg/(g·h),且在第55天增加到8.8 mg/(g·h), 之后在8.8 mg/(g·h)左右波动. RSNO只略微增加, 在第26~59天由0.1 mg/(g·h)增加到0.9 mg/(g·h).这说明在好氧/好氧恢复过程中AOB活性得到快速恢复, 而NOB在短时间内不能恢复活性, 这与Kornaros等[14]和Bournazou等[15]研究结果相符合.而2# RSAO在第76天达到9.2 mg/(g·h), RSNO下降缓慢, 在第73天下降到1.0 mg/(g·h), 这进一步说明两种厌氧运行最终均有效抑制NOB活性, 同时说明厌氧/厌氧后好氧/好氧能更快地使亚硝化得到恢复.主要原因可能是厌氧/厌氧对NOB形成了较彻底的抑制, 在后续的好氧恢复过程中AOB能迅速地恢复活性, 而NOB不具备此特性.Gerards等[16]和Tappe[17]等指出当进入好氧环境后, 与NOB相比, AOB能更快地恢复活性, 这是因为二者不同能量需求以及恢复阶段的不同动力学效应所致, 以上结论均为本实验中厌氧运行后亚硝化得以恢复提供了有力支撑.
以上对亚硝化恢复方式的比较表明, 与厌氧/好氧相比, 先厌氧/厌氧后好氧/好氧运行可以使连续流实际生活污水亚硝化的恢复时间缩短12 d.
2.3 恢复后亚硝化稳定性的比较目前污水处理厂曝气控制一般采用固定曝气时间的方式, 这样在进水水质波动较大时必然会导致过度曝气, 因此, 在高曝气下比较恢复后亚硝化的稳定性更具有实际意义, 故进行S3阶段研究.在此阶段, 将1#和2#两级曝气量均提高至DO为1.0~1.2 mg/L, 在10 d的运行过程中1#亚硝化发生失稳, 亚硝化率由91.53%下降到50.66%, 2#氨氧化率上升到79.49%, 而亚硝化率一直保持在80%以上(包括80%), 这说明2#恢复后的亚硝化更稳定.同时如图 4所示, 在S3阶段1# RSNO由1.2 mg/(g·h)上升到5.8 mg/(g·h), 而2#中RSNO仅由1.2 mg/(g·h)上升到1.8 mg/(g·h), 这说明在高曝气下, 经过厌氧/厌氧后好氧/好氧的NOB已经恢复活性, 而厌氧/好氧运行下的NOB活性依然被抑制.原因是1#亚硝化恢复后, 一直保持好氧/好氧运行, 较充足的DO和亚氮的积累为NOB的增殖提供了有利条件.同时如图 2所示, 1#在第75~80天亚硝化率有下降的趋势, 也说明好氧/好氧长期运行可能导致亚硝化的失稳.与1#不同, 2#恢复后的亚硝化一直保持厌氧/好氧运行, 这对NOB形成了持续抑制, 因此,短时间内曝气量的增大并没有使亚硝化失稳.
以上对亚硝化稳定性的比较表明, 厌氧/好氧运行下的亚硝化更稳定.因此, 失稳后已经恢复的亚硝化应转变运行方式为厌氧/好氧, 这有助于亚硝化的长期稳定运行.
2.4 亚硝化恢复因素分析目前,影响亚硝化恢复的因素主要有温度、pH、基质质量浓度、游离氨(FA)、游离亚硝酸(FNA)等[17], 1#和2#温度均为(20±2)℃, 温度的波动是因为1 d内温差所致, 同时,温度高于25 ℃AOB和NOB的生长速度才有较大的差异,才有利于亚硝化的实现[18].而本实验的温度一直在(20±2) ℃, 可以排除温度原因使亚硝化恢复的可能.而亚硝化恢复前后pH较稳定, 且进水NH4+-N质量浓度一直在35~43 mg /L, 可以排除pH和基质质量浓度对亚硝化恢复的作用.在亚硝化恢复前后, 1#和2#FA一直在0.42~0.92 mg/L, 该值小于FA对NOB的抑制质量浓度(1~150 mg/L)[19].另外, 在孙洪伟等[20]的研究中, 在FA为5.3 mg/L时NO2--N的积累仍然很少, 相比之下, 本实验中的FA值很低, 不足以影响亚硝化的恢复, 因此,可以排除FA的作用使亚硝化得到恢复的可能.同时,1#和2#FNA最大值为0.001 6 mg/L, 远小于对NOB的抑制质量浓度(0.011~0.077 mg/L)[21], 因此,也可以排除FNA作用使亚硝化得到恢复的可能.
由此表明, 本实验中亚硝化快速恢复的原因是厌氧/厌氧后好氧/好氧和厌氧/好氧作用的结果, 而对比1#和2#的运行条件, 在整个实验过程中二者温度、pH基本相同, 而FA和FNA均没有达到对NOB的抑制质量浓度, 因此,可以排除温度、基质质量浓度、FA和FNA等使1#和2#亚硝化效果出现差异的可能, 故本实验亚硝化恢复效果的差异是不同厌氧运行方式所致.厌氧/厌氧后好氧/好氧运行更有利于亚硝化恢复的原因是开始阶段的厌氧/厌氧运行能更彻底地抑制NOB.
然而, 本实验中厌氧/厌氧运行的厌氧/好氧比相当于1:0, 厌氧/好氧运行的厌氧/好氧比为1:1, 那么是否存在一个厌氧/好氧比为0:1和1:1之间的数值, 使得此时有更好的亚硝化恢复效果仍有待进一步研究.
3 结论1) 与厌氧/好氧(DO分别为0~0.1和0.6~0.8 mg/L)相比, 厌氧/厌氧(DO均为0~0.1 mg/L)能够更彻底地抑制NOB.
2) 在连续流实际生活污水中, 与厌氧/好氧(DO分别为0~0.1和0.6~0.8 mg/L)相比, 厌氧/厌氧(DO均为0~0.1 mg/L)后好氧/好氧(DO分别为0.2~0.4和0.6~0.8 mg/L)运行的亚硝化恢复时间缩短了12 d.
3) 失稳后已经恢复的亚硝化运行方式转变为厌氧/好氧运行(DO分别为0~0.1和0.6~0.8 mg/L)有助于亚硝化长期稳定运行.
| [1] | TURK O, MAVINIC D S. Preliminary assessment of a shortcut in nitrogen removal from wastewater[J]. Canadian Journal of Civil Engineering, 1986, 13 (6) : 600-605. DOI: 10.1139/l86-094 |
| [2] | BARTROLI A, PEREZ J, CARRERA J. Applying ratio control in a continuous granular reactor to achieve full nitritation under stable operating conditions[J]. Environmental Science and Technology, 2010, 44 (23) : 8930-8935. DOI: 10.1021/es1019405 |
| [3] | STAR W, ABMA W R, DENNIS B, et al. Startup of reactors for anoxic ammonium oxidation: experiences from the first full-scale anammox reactor in Rotterdam[J]. Water Research, 2007, 41 (18) : 4149-4163. DOI: 10.1016/j.watres.2007.03.044 |
| [4] | MA B, ZHANG S, ZHANG L, et al. The feasibility of using a two-stage autotrophic nitrogen removal process to treat sewage[J]. Bioresource Technology, 2011, 102 (17) : 8331-8334. DOI: 10.1016/j.biortech.2011.06.017 |
| [5] | GABARRO J, GANIGUE R, GICH F, et al. Effect of temperature on AOB activity of a partial nitritation SBR treating landfill leachate with extremely high nitrogen concentration[J]. Bioresource Technology, 2012, 126 : 283-289. DOI: 10.1016/j.biortech.2012.09.011 |
| [6] | PENG Y, ZHANG S, ZENG W, et al. Organic removal by denitritation and methanogenesis and nitrogen removal by nitritation from landfill leachate[J]. Water Research, 2008, 42 (s 4/5) : 883-892. |
| [7] | GABARRO J, GANIGUE R, GICH F, et al. Effect of temperature on AOB activity of a partial nitritation SBR treating landfill leachate with extremely high nitrogen concentration[J]. Bioresource Technology, 2012, 126 (6) : 283-289. |
| [8] |
张功良, 李冬, 张肖静, 等. 延时曝气对常温低氨氮SBR亚硝化影响及恢复[J].
中国环境科学, 2014, 34 (8) : 1998-2002.
ZHANG G L, LI D, ZHANG X J, et al. Research on the recovery strategy for nitrosation at room temperature[J]. Zhongguo Huanjing Kexue/China Environmental Science, 2014, 34 (8) : 1998-2002. |
| [9] |
郭海娟, 马放, 沈耀良. DO和pH值在短程硝化中的作用[J].
环境污染治理技术与设备, 2006, 7 (1) : 37-40.
GUO Haijuan, MA Fang, SHEN Yaoliang. Effects of DO and pH on nitrosofication[J]. Techniques & Equipment for Environmental Pollution Control, 2006, 7 (1) : 37-40. |
| [10] |
张昭, 李冬, 邱文新, 等. 城市污水部分亚硝化的实现与稳定运行[J].
中南大学学报:自然科学版, 2013, 44 (7) : 3066-3071.
ZHANG Z, LI D, QIU W, et al. Achievement and stable operation of partial nitritation for municipal wastewater[J]. Zhongnan Daxue Xuebao, 2013, 44 (7) : 3066-3071. |
| [11] | ANTHONTHONISEN A C, LOEHR R C, PRAKASAM T B, et al. Inhibition of nitrification by ammonia and nitrous acid[J]. Journal-Water Pollution Control Federation, 1976, 48 (5) : 835-852. |
| [12] |
刘文龙, 彭永臻, 苗圆圆, 等. 好氧饥饿对膨胀污泥硝化性能及污泥特性的影响[J].
化工学报, 2015 (3) : 1142-1149.
LIU W L, PENG Y Z, MIAO Y Y, et al. Effects of aerobic starvation on nitrification performance and sludge characteristics of bulking sludge[J]. Huagong Xuebao, 2015 (3) : 1142-1149. |
| [13] |
高春娣, 王惟肖, 李浩, 等. SBR法交替缺氧好氧模式下短程硝化效率的优化[J].
中国环境科学, 2015, 35 (2) : 403-409.
GAO C D, WANG W X, LI H, et al. Optimization of efficiency on partial nitrification under the mode of alternating anoxic/oxic in sequencing batch reactor[J]. Zhongguo Huanjing Kexue/China Environmental Science, 2015, 35 (2) : 403-409. |
| [14] | KORNAROS M, DOKIANAKIS S N, LYBERATOS G. Partial nitrification/denitrification can be attributed to the slow response of nitrite oxidizing bacteria to periodic anoxic disturbances[J]. Environmental Science & Technology, 2010, 44 (19) : 7245-7253. |
| [15] | BOURNAZOU M, HOOSHIAR K, ARELLANO-GARCIA H, et al. Model based optimization of the intermittent aeration profile for SBRs under partial nitrification[J]. Water Research, 2013, 47 (10) : 3399-3410. DOI: 10.1016/j.watres.2013.03.044 |
| [16] | GERARDS S, DUYTS H, LAANBROEK H. Ammonium-induced inhibition of ammonium-starved Nitrosomonas europaea, cells in soil and sand slurries[J]. Fems Microbiology Ecology, 1998, 26 (4) : 269-280. DOI: 10.1111/fem.1998.26.issue-4 |
| [17] | TAPPE W, LAVERMAN A, BOHLAND M, et al. Maintenance energy demand and starvation recovery dynamics of Nitrosomonas europaea and Nitrobacter winogradskyi cultivated in a retentostat with complete biomass retention[J]. Applied & Environmental Microbiology, 1999, 65 (6) : 2471-2477. |
| [18] | PAREDES D, KUSCHK P, MBWETTE T S A, et al. New aspects of microbial nitrogen transformations in the context of wastewater treatment:A review[J]. Engineering in Life Sciences, 2007, 7 (1) : 13-25. DOI: 10.1002/(ISSN)1618-2863 |
| [19] |
张杰. 为我国水环境恢复而努力[J].
给水排水, 2003, 29 (4) : 1.
ZHANG J. Efforts to restore water environment in China[J]. Gei Shui Pai Shui/Water Supply and Drainage, 2003, 29 (4) : 1. |
| [20] |
孙洪伟, 尤永军, 赵华南, 等. 游离氨对硝化菌活性的抑制及可逆性影响[J].
中国环境科学, 2015, 35 (1) : 95-100.
SUN H W, YOSU Y J, ZHAO H N, et al. Inhibitory effect of free ammonia on the activity of nitrifying bacteria and recoverability[J]. Zhongguo Huanjing Kexue/China Environmental Science, 2015, 35 (1) : 95-100. |
 2017, Vol. 49
2017, Vol. 49


