2. 中国电建集团成都勘测设计研究院有限公司,成都610072;
3. 四川省环境保护科学研究院,成都610041;
4. 哈尔滨理工大学 设计研究院,哈尔滨 150080
2. Power China Chengdu Engineer Corporation, Chengdu 610072, China;
3. Sichuan Academy of Environmental Sciences, Chengdu 610041, China;
4. Design and Research Institute, Harbin University of Science and Technology, Harbin 150080, China
对挥发性有机污染物(VOCs) [1-2]的处理目前主要采用催化氧化[3]、气体膜分离[4]、生物滴滤[5]和吸附技术[6],以及其组合工艺[7].其中, 以活性炭为主的吸附技术因操作简单, 处理效率高而被广泛采用.但活性炭因制备温度高(一般1 100 ℃以上)、制备原料较单一及活化过程能耗高且易产生二次污染等问题, 限制了其大规模的应用.因而, 亟需寻求更为廉价的吸附剂或探索潜在的新型吸附剂材料.
生物质炭是一种低温(一般<700 ℃)热解生物质炭质形成的富含炭物质的多孔材料, 锯末、秸秆果壳等廉价而丰富的农业废弃物均可作为制备原材料, 制备成本十分低廉[8].大量研究表明,这种廉价的生物质炭可用于吸附水体和土壤中的有机污染物质, 如硝基甲苯、苯酚等[9-10].但是, 生物质炭对气体中有机污染物的吸附目前还鲜有研究.较多的研究结果表明,活性炭吸附废气中有机气体机理主要取决于活性炭孔隙结构的物理吸附, 但生物质炭不同于活性炭, 除含有较丰富的孔隙结构, 其表面还含有丰富的官能团, 这势必影响生物质炭对气体有机污染物的吸附行为.为此, 本研究主要探索生物质炭对气态有机污染物的吸附性能与作用机理.基于苯和甲苯巨大的危害和工业中的大量使用, 选取其作为典型的VOCs, 以核桃壳和椰子壳两种农业废弃物为原料, 不同热解温度(400、550和700 ℃)下, 制备一系列生物质炭材料.通过其理化性质分析和批量吸附实验, 探讨其吸附效果与机制.
1 实验 1.1 生物质炭制备椰子壳和核桃壳分别取自中国海南省海口市和四川省成都市.热解之前, 将其碎成2~4 mm颗粒, 并用去离子水清洗去除灰尘, 然后在100 ℃下烘干.将烘干后的核桃壳和椰子壳在管式热解炉(洛阳西格玛炉业有限公司)中热解.热解温度设定为400、550和700 ℃, 升温速率为10 ℃/min, 达到设定温度后继续热解2 h, 随后在炉体中冷却至室温, 全过程以氮气为保护气体, 流量为400 mL/min.
热解残渣即为生物质炭.研磨过筛后, 取0.125~0.150 mm粒径的生物质炭作为本研究用样品.对应热解温度下制得的核桃壳和椰壳生物质炭样品分别记为H400、H550、H700和Y400、Y550、Y700.
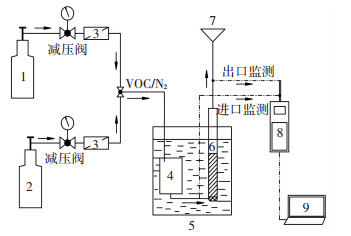
1.2 苯和甲苯吸附实验实验采用苯/N2标准气体和甲苯/N2标准气体, 通过高纯氮气和标准气体稀释控制所需VOCs的进气浓度, 苯和甲苯标准气体购于中国测试技术研究院, 实验装置见图 1.
|
1-高纯氮气;2-标准气体;3-气体质量流量计;4-气体缓冲瓶;5-温控水浴锅;6-生物炭吸附柱;7-尾气处理单元;8-便携式VOC在线监测仪;9-数据收集处理单元 图 1 实验装置示意 Figure 1 A schematic of adsorption apparatus |
实验装置主要由标准气体稀释单元、吸附柱单元和数据监测单元3部分组成.吸附柱为玻璃制品, 长25 cm, 直径1.5 cm, 吸附柱置于水浴锅内维持30 ℃吸附温度.进出口浓度检测采用ppbRAE3000便携式VOC在线监测仪(美国华瑞PGM7340型).每次吸附实验生物质炭质量为3.18 g, 进气量为300 mL/min.当出口浓度等于进口浓度时, 视为吸附饱和, 停止实验.
生物质炭对苯和甲苯的吸附量通过下式计算
| $ {{q}_{t}}=\frac{1}{m}\int\limits_{0}^{t}{v\left( {{\rho }_{0}}-{{\rho }_{t}} \right)\text{d}t}. $ | (1) |
式中:m为生物质炭质量, g; qt为t时刻VOCs吸附量, mg/g; ρ0和ρt分别为初始时刻进口处气体质量浓度和t时刻出口处气体质量浓度, mg/m3; v为进气量, m3/min.
1.3 分析方法样品C、H、N、O元素质量分数测定采用varioMACRO cube元素分析仪(德国ELEMENTAR Analysensysteme股份有限公司).表面含氧官能团和碱性基团质量摩尔浓度的测定采取Boehm滴定法[11].红外光谱(FTIR)采用IRAffinity-1红外光谱仪(日本岛津公司)测定, 扫描范围400~4 000 cm-1, 分辨率为4.0 cm-1.生物质炭BET比表面积和孔径分析采用BELSORP-max比表面积和孔隙率分析仪(日本BEL股份有限公司).
2 结果与讨论 2.1 生物质炭理化特征不同制备条件下生物质炭的元素组成和表面官能团质量摩尔浓度见表 1.可以看出, 随着热解温度的升高, 碳元素质量分数明显增加, 而氧和氢元素下降.氧碳摩尔比和氢碳摩尔比下降, 表明生物质炭的极性减小, 芳香性和疏水性增强[12], 这也与表面官能团变化一致.随着热解温度的升高, 生物质炭表面酸性官能团也逐渐减少, 这与许多研究结果类似[12-13].
| 表 1 生物质炭元素组成及表面官能团质量摩尔浓度 Table 1 Elemental compositions and surface functional groups of biochars at different pyrolysis temperatures |
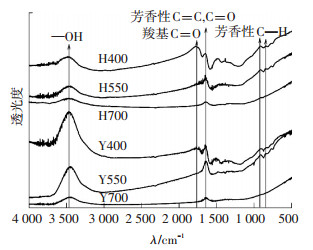
图 2为不同热解温度下制备的生物质炭的傅里叶红外光谱图.可以看出, 随着热解温度升高, 在1 700~1 760 cm-1处的羰基C=O振动峰逐渐消失, 在3 000~3 665 cm-1处的-OH振动峰也逐渐减弱[12-13].可以看出, 热解温度升高, 生物质炭表面含氧官能团逐渐减少, 甚至消失.结合表 1中酸性官能团质量摩尔浓度变化可以看出, 这些含氧官能团主要为羧基及羟基等, 而羧基和羟基具有强吸电子能力, 能与苯和甲苯通过C-H…O氢键作用力而结合在一起[14].因此, 随着热解温度的升高, 生物质炭表面含氧官能团与有机污染物之间的电子亲和力减弱.
|
图 2 生物质炭傅里叶红外光谱 Figure 2 FTIR spectra of biochars |
生物质炭的比表面积和孔隙结构也会对吸附性能产生一定的影响[15].生物质炭的BET比表面积(as)、外比表面积(ae)、微孔体积(V1)和介孔体积(V2)见表 2.可以看出, 生物质炭的比表面积和孔隙体积随着热解温度的升高而显著增加.意味着生物质炭的吸附性能可能会随热解温度升高而显著提升[16].
| 表 2 生物质炭比表面积和空隙体积 Table 2 Surface areas and pore volumes of biochars at various pyrolysis temperatures |
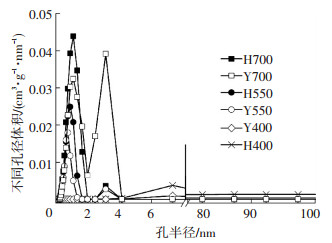
生物质炭孔径分布见图 3.可以看出, 低温下制备的生物质炭(400 ℃)孔隙结构十分贫瘠, 随着制备温度升高, 生物质炭孔隙显著增加, 以微孔为主, 且孔半径主要在5 nm以下.此外, Y700生物质炭2~4 nm的介孔显著高于H700生物质炭.
|
图 3 生物质炭孔径分布 Figure 3 Pore size distribution of biochars |
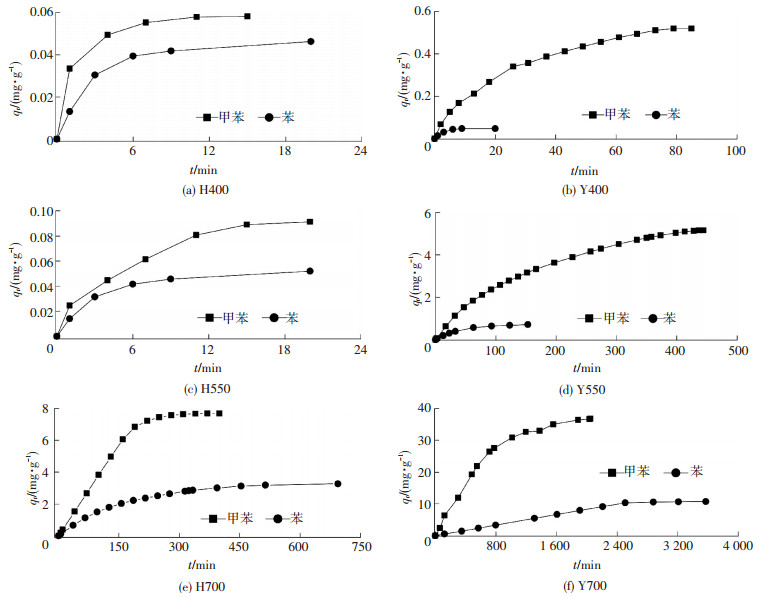
生物质炭对苯和甲苯的吸附动力学曲线见图 4.正如所料, 随着热解温度的升高, 两种材质的生物质炭对苯和甲苯的吸附性能均大大提高, 吸附饱和时间也极大延长.H400和H550生物质炭在20 min内对苯和甲苯的吸附即可达到吸附饱和, 而H700生物质炭的吸附饱和时间则大大增加, 甚至长达近700 min.同时, 对苯和甲苯的饱和吸附量也分别由0.05和0.06 mg/g提升至3.27和7.80 mg/g.这种趋势和不同温度下制备的椰壳生物质炭吸附规律一致, 这可能与高温制得生物质炭具有更加丰富的孔隙结构有关.
|
图 4 吸附时间对吸附量的影响 Figure 4 Effects of adsorption time on the total adsorption amount |
为了摸清生物质炭对苯和甲苯的吸附行为, 采取准一级动力学模型、准二级动力学和Elovich方程进行拟合, 其中准一级动力学模型主要描述吸附受扩散步骤控制[17];准二级动力学模型则认为吸附速率受化学吸附机理的控制, 涉及到吸附剂与吸附质之间的电子共用或转移[18];Elovich方程也通常用于描述气体物质在吸附剂上的化学吸附[19].
准一级动力学模型为
| $ \ln \left( {{q}_{\text{e}}}-{{q}_{t}} \right)=\ln {{q}_{\text{e}}}-{{k}_{1}}t, $ | (2) |
准二级动力学模型为
| $ t/{{q}_{t}}=1/\left( {{k}_{2}}q_{\text{e}}^{2} \right)+t/{{q}_{\text{e}}}, $ | (3) |
Elovich方程为
| $ {{q}_{t}}=\left( \frac{1}{b} \right)\left( \ln t+\ln ab \right). $ | (4) |
式中:k1(min-1)和k2(g·mg-1·min-1)为吸附速率常数, qe(mg/g)和qt(mg/g)分别表示在吸附平衡和反应t时刻的吸附量, a和b为Elovich方程常数.
将图 4结果代入式(2)、(3)和(4), 得到动力学参数见表 3.从相关系数R2可以看出, 低温下制备的生物质炭(如H400)对苯和甲苯的吸附更符合准二级动力学模型(0.997 1>0.965 0>0.948 6;0.999 7>0.987 0>0.968 3), 而高温下制备的生物质炭(如H700)对苯和甲苯的吸附过程更符合准一级动力学模型(0.990 6>0.988 2>0.946 4;0.934 4>0.883 6>0.861 7).这表明低温制备的生物质炭对苯和甲苯的吸附受化学机理控制, 高温下制备的生物质炭对苯和甲苯的吸附受物理扩散作用控制.可能是因为低温下制备的生物质炭表面含有更多的含氧官能团, 使得吸附速率受化学吸附机制控制[20];而随着制备温度升高, 生物质炭孔隙结构变得极为丰富, 且表面吸电子基团减少, 与苯和甲苯形成氢键的能力下降, 使得吸附过程主要受空隙内扩散机制控制.
| 表 3 生物质炭对苯和甲苯吸附动力学参数 Table 3 Adsorption kinetics parameters of benzene and toluene on biochars |
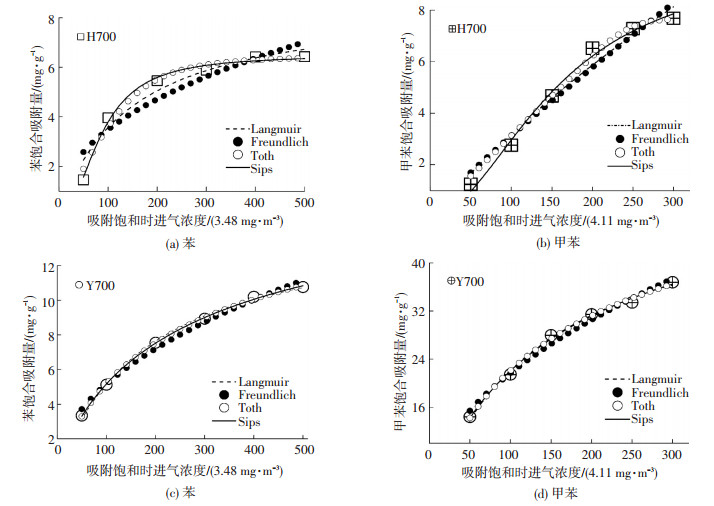
图 5分析了不同初始浓度下, H700和Y700两种吸附性能较好的生物质炭, 在吸附温度30 ℃时对苯和甲苯的等温吸附情况.可以看出, 初始浓度显著影响生物质炭的吸附量.初始浓度越高, 饱和吸附量越大.
|
图 5 H700和Y700生物质炭等温吸附曲线 Figure 5 Adsorption isotherms of benzene and toluene on H700 and Y700 biochars |
生物质炭对苯和甲苯平衡吸附通常采用Langmuir[21]、Freundlich[22]、Sips[23]和Toth[24]模型进行模拟.Langmuir模型主要认为吸附剂表面吸附点位均匀分布, 吸附过程主要为单分子层吸附;Freundlich模型描述的为非均匀体系的吸附;Sips模型和Toth模型为三参数模型, 也多用于描述非均匀体系的吸附.其方程式如下:
Langmuir模型为
| $ {{q}_{\text{e}}}=\frac{{{q}_{\text{m}}}\cdot {{k}_{\text{L}}}\cdot {{\rho }_{\text{e}}}}{\left( 1+{{k}_{\text{L}}}\cdot {{\rho }_{\text{e}}} \right)}, $ | (5) |
Freundlich模型为
| $ {{q}_{\text{e}}}=A\cdot \rho _{\text{e}}^{\frac{1}{n}}, $ | (6) |
Sips模型为
| $ {{q}_{\text{e}}}={{q}_{\text{m}}}\cdot \frac{{{\left( d{{\rho }_{\text{e}}} \right)}^{s}}}{1+{{\left( d{{\rho }_{\text{e}}} \right)}^{s}}}, $ | (7) |
Toth模型为
| $ {{q}_{\text{e}}}={{q}_{\text{m}}}b{{\rho }_{\text{e}}}/{{\left[1+{{\left( d{{\rho }_{\text{e}}} \right)}^{t}} \right]}^{\frac{1}{t}}}. $ | (8) |
式中:qe和ρe分别表示吸附平衡时吸附量(mg/g)和吸附平衡时进气质量浓度(mg/m3), qm(mg/g)表示理论最大吸附量, kL表示Langmuir吸附能量, A和n分别表示亲和系数和吸附强度, s和t均为不均匀能量参数.
为了检验以上4种模型拟合效果, 采用均方根差(RSMD)进行进一步检验[25],即
| $ \text{RSMD=}{{\left[1/n\sum{{{\left( {{q}_{\text{exp}}}-{{q}_{\text{p}}} \right)}^{2}}} \right]}^{1/2}}. $ | (9) |
式中:n为实验数据个数, qexp和qp分别表示实验测得值和理论计算值.
等温吸附模型拟合结果见表 4.可以看出, 对苯和甲苯的吸附更符合Toth模型, 表明其吸附为一个非均匀体系的吸附.
| 表 4 生物质炭对苯和甲苯等温吸附拟合参数 Table 4 Adsorption isotherm parameters of benzene and toluene on biochars |
由Toth模型计算得出吸附性能最佳的生物质炭Y700对苯和甲苯的吸附量分别为18.98和61.73 mg/g, 这与文献报道的活性炭最大吸附量有一定差距(见表 5),但生物质炭显然可以作为一种潜在的气体有机污染物吸附剂.
| 表 5 与文献报道的多孔炭材料最大吸附量比较 Table 5 Comparison of maximum adsorption capacity of benzene and toluene on different porous carbons |
生物质炭具有制备成本低廉、制备原材料广等优点, 同时可采取一些改性手段大大提升生物质炭的吸附性能, 改性后生物质炭的吸附性能甚至高于活性炭[26], 极大拓展了生物质炭在实际工程中的应用.其次,还为农、林废弃物如秸秆、果壳、锯末及市政污泥等提供了一种资源化利用途径.因此, 本研究具有极大的环境效应和生态效应.
2.4 生物质炭吸附机理分析| $ {{q}_{t}}={{k}_{i}}{{t}^{0.5}}+C. $ | (10) |
式中:ki(mg·g-1·min-0.5)表征颗粒内扩散速率, C(mg/g)表征边界层厚度.
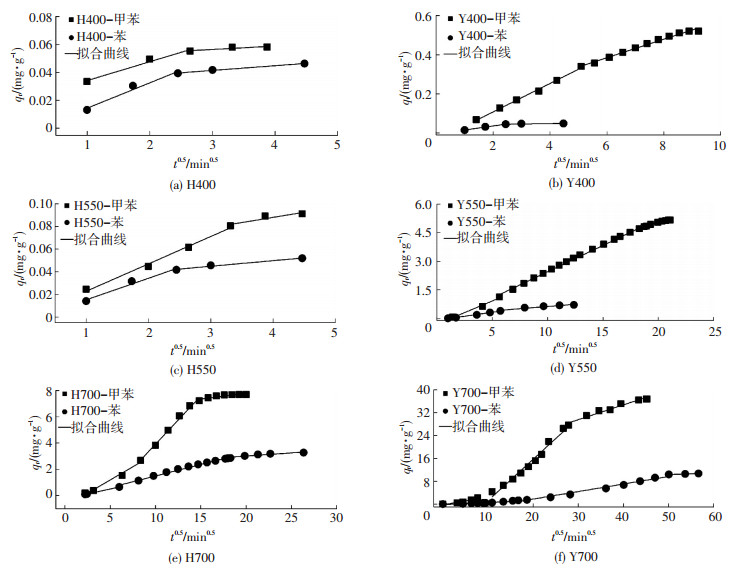
根据此模型, qt与t0.5若成线性, 表示吸附过程存在颗粒内扩散.若该直线过原点, 则表示该吸附速率受颗粒内扩散控制.拟合结果见图 6和表 6.qt与t0.5拟合呈折线, 表明颗粒内扩散不是速率主要控制步骤, 吸附过程呈现出2个或3个阶段的连续过程.低温下制得的生物质炭(400 ℃)主要为2个阶段, 第一阶段表示苯和甲苯扩散到生物质炭表面的表面扩散过程, 第二阶段为苯和甲苯进入生物质炭孔隙内部的颗粒内扩散过程, 且ki1>ki2;而高温制得的生物质炭(700 ℃)则呈现3个吸附阶段, 第3个阶段为吸附与脱附的最终平衡过程, 涉及在生物质炭微孔内的吸附[31], 这与高温制得生物质炭微孔结构被打开有关.
|
图 6 粒内扩散模型拟合 Figure 6 Test of the intraparticle diffusion kinetic model |
| 表 6 粒内扩散模型拟合参数 Table 6 Kinetic data obtained by the intraparticle diffusion model |
根据粒内扩散模型拟合结果, 得到不同作用过程对吸附量的贡献率, 见表 6.显然, 生物质炭对气态苯和甲苯的吸附包含表面扩散和粒内扩散等多种机制共同控制.其中, 低温制备的生物质炭以表面扩散吸附为主, 高温制得的生物质炭则受粒内扩散作用支配.
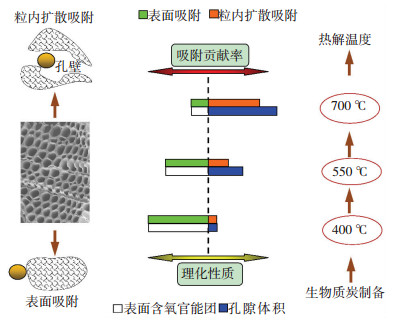
结合生物质炭理化特征和动力学模型分析结果可知, 生物质炭对气态苯和甲苯的表面扩散吸附主要是基于酸性官能团(如羧基)与苯环形成电子-电子复合物[32], 依靠含氧官能团间的C-H…O氢键作用力[14]将苯环束缚在生物质炭表面;而粒内扩散作用则是因为苯或甲苯在生物质炭内部孔壁上通过范德华力而被吸附, 甚至有机污染物分子可以在介孔中发生毛细管凝聚现象[31].吸附机理见图 7.
|
图 7 生物质炭吸附机理示意 Figure 7 Mechanism of VOCs adsorption on biochars |
1) 生物质炭可用于气态VOCs的吸附.不同材料制备的生物质炭, 其吸附性能差异显著.生物质炭对气态有机污染物的吸附性能低于活性炭的吸附性能.
2) 生物质炭的吸附过程与表面酸性官能团和孔隙结构有关, 低温制得的生物质炭表面酸性官能团丰富, 吸附过程以表面扩散吸附为主, 高温制得生物质炭表面官能团含量较少且孔隙结构更加丰富, 吸附过程以粒内扩散控制为主.
3) 为提升生物质炭吸附性能的改性研究提供了理论支撑.
| [1] | LI Yizhou, FAN Zeyun, SHI Jianwei, et al. Post plasma-catalysis for VOCs degradation over different phase structure MnO2 catalysts[J]. Chemical Engineering Journal, 2014, 241 (4) : 251-258. |
| [2] | WU Ye, WANG Renjie, ZHOU Yu, et al. On-road vehicle emission control in Beijing: Past, present, and future[J]. Environmental Science and Technology, 2011, 45 (1) : 147-153. DOI: 10.1021/es1014289 |
| [3] |
卜龙利, 杨力, 孙剑宇, 等. 双组分VOCs的催化氧化及动力学分析[J].
环境科学, 2014, 35 (9) : 3302-3308.
BO Longli, YANG Li, SUN Jianyu, et al. Catalytic oxidation of two-component VOCs and kinetic analysis[J]. Environmental Science, 2014, 35 (9) : 3302-3308. |
| [4] | MODELSKI S, KOŁTUNIEWICZ A, WITEK-KROWIAK A. Kinetics of VOC absorption using capillary membrane contactor[J]. Chemical Engineering Journal, 2011, 168 (3) : 1016-1023. DOI: 10.1016/j.cej.2011.01.075 |
| [5] | DETCHANAMURTHY S, GOSTOMSKI P A. Biofiltration for treating VOCs: An overview[J]. Reviews in Environmental Science and Bio/Technology, 2012, 11 (3) : 231-241. DOI: 10.1007/s11157-012-9288-5 |
| [6] | CHOU M S, CHIOU J H. Modeling effects of moisture on adsorption capacity of activated carbon for VOCs[J]. Journal of Environmental Engineering, 2015, 123 : 437-443. |
| [7] |
席劲瑛, 武俊良, 胡洪营, 等. 工业VOCs气体处理技术应用状况调查分析[J].
中国环境科学, 2013, 32 (11) : 1955-1960.
XI Jinying, WU Junliang, HU Hongying, et al. Application status of industrial VOCs gas treatment techniques[J]. China Environmental Science, 2013, 32 (11) : 1955-1960. |
| [8] | LUO Lei, XU Chang, CHEN Zien, et al. Properties of biomass-derived biochars: Combined effects of operating conditions and biomass types[J]. Bioresource Technology, 2015, 192 : 83-89. DOI: 10.1016/j.biortech.2015.05.054 |
| [9] |
陈宝梁, 周丹丹, 朱利中, 等. 生物碳质吸附剂对水中有机污染物的吸附作用及机理[J].
中国科学B辑:化学, 2008, 38 (6) : 530-537.
CHEN Baoliang, ZHOU Dandan, ZHU lizhong, et al. Adsorption and interaction mechanisms of organic contaminants in wastewater with biological carbon[J]. Science in China Series B: Chemistry, 2008, 38 (6) : 530-537. |
| [10] |
何秋香, 陈祖亮. 柚子皮制备生物炭吸附苯酚的特性和动力学[J].
环境工程学报, 2014 (9) : 3853-3859.
HE Qiuxiang, CHEN Zuliang. Characterization and kinetics of biochar prepared from pomelo peel for adsorption of phenol[J]. Chinese Journal of Environmental Engineering, 2014 (9) : 3853-3859. |
| [11] | BOEHM H P. Surface oxides on carbon and their analysis: A critical assessment[J]. Carbon, 2002, 40 (2) : 145-149. DOI: 10.1016/S0008-6223(01)00165-8 |
| [12] | CHEN Baoliang, ZHOU Dandan, ZHU Lizhong. Transitional adsorption and partition of nonpolar and polar aromatic contaminants by biochars of pine needles with different pyrolytic temperatures[J]. Environmental Science and Technology, 2008, 42 (14) : 5137-5143. DOI: 10.1021/es8002684 |
| [13] | MARCO K, NICO P S, JOHNSON M G, et al. Dynamic molecular structure of plant biomass-derived black carbon (biochar)[J]. Environmental Science and Technology, 2010, 44 (4) : 1247-1253. DOI: 10.1021/es9031419 |
| [14] | ISOGAI A, TSUMUKI T, MUROHASHI S, et al. (8-Benzoyl-2, 7-diethoxynaphthalen-1-yl)(phenyl) methanone[J]. Acta Crystallographica Section E, 2013, 69 (Pt1) : o71. |
| [15] |
简敏菲, 高凯芳, 余厚平, 等. 不同温度生物炭酸化前后的表面特性及镉溶液吸附能力比较[J].
生态环境学报, 2015, 24 (8) : 1375-1380.
JIAN Minfei, GAO Kaifang, YU Houping, et al. Comparison of surface characteristics and cadmium solution adsorption capacity of un-acidified or acidified bio-chars prepared from rice straw under different temperature[J]. Ecology and Environmnet, 2015, 24 (8) : 1375-1380. |
| [16] | WANG Gang, DOU Baojuan, ZHANG Zhongshen, et al. Adsorption of benzene, cyclohexane and hexane on ordered mesoporous carbon[J]. Journal of Environmental Sciences, 2015, 30 : 65-73. DOI: 10.1016/j.jes.2014.10.015 |
| [17] | DRAGAN E S, APOPEI D F. Synthesis and swelling behavior of pH-sensitive semi-interpenetrating polymer network composite hydrogels based on native and modified potatoes starch as potential sorbent for cationic dyes[J]. Chemical Engineering Journal, 2011, 178 (1) : 252-263. |
| [18] | ARSHADI M, FARAJI A R, AMIRI M J. Modification of aluminum-silicate nanoparticles by melamine-based dendrimer L-cysteine methyl esters for adsorptive characteristic of Hg (Ⅱ) ions from the synthetic and Persian Gulf water[J]. Chemical Engineering Journal, 2015, 266 : 345-355. DOI: 10.1016/j.cej.2014.12.109 |
| [19] | JUANG R S, CHEN M L. Application of the Elovich equation to the kinetics of metal sorption with solvent-impregnated resins[J]. Industrial & Engineering Chemistry Research, 1997, 36 (3) : 813-820. |
| [20] | MAKSIN D D, NASTASOVIĆA B, SURUČIĆ L T, et al. Equilibrium and kinetics study on hexavalent chromium adsorption onto diethylene triamine grafted glycidyl methacrylate based copolymers[J]. Journal of Hazardous Materials, 2012, 209/210 (4) : 99-110. |
| [21] | SONG Xiaolan, ZHANG Ying, YAN Chengyin, et al. The Langmuir monolayer adsorption model of organic matter into effective pores in activated carbon[J]. Journal of Colloid and Interface Science, 2013, 389 (1) : 213-219. DOI: 10.1016/j.jcis.2012.08.060 |
| [22] | PERUCHI L M, FOSTIER A H, RATH S. Sorption of norfloxacin in soils: Analytical method, kinetics and Freundlich isotherms[J]. Chemosphere, 2015, 119 : 310-317. DOI: 10.1016/j.chemosphere.2014.06.008 |
| [23] | EROL A, NUMAN H. Adsorption of bentazon and propanil from aqueous solutions at the high area activated carbon-cloth[J]. Chemosphere, 2004, 57 (8) : 755-762. DOI: 10.1016/j.chemosphere.2004.08.042 |
| [24] | TÓTH J. Uniform interpretation of gas/solid adsorption[J]. Journal of Colloid and Interface Science, 1995, 55 (1) : 1-239. |
| [25] | NASRI N S, HAMZA U D, ISMAIL S N, et al. Assessment of porous carbons derived from sustainable palm solid waste for carbon dioxide capture[J]. Journal of Cleaner Production, 2014, 71 (10) : 148-157. |
| [26] |
陈健康.紫外辐射改性碳材料对水中重金属的吸附研究[D].重庆:重庆大学, 2014.
CHEN Jiankang. The study of adsorption heavy metals from aqueous solution using ultraviolet radiation modified carbon materials[D]. Chongqing:Chongqing University, 2014. |
| [27] | WIBOWO N, SETYADHI L, WIBOWO D, et al. Adsorption of benzene and toluene from aqueous solutions onto activated carbon and its acid and heat treated forms: Influence of surface chemistry on adsorption[J]. Journal of Hazardous Materials, 2007, 146 (1/2) : 237-242. |
| [28] | SU F, LU C, HU S. Adsorption of benzene, toluene, ethylbenzene and p-xylene by NaOCl-oxidized carbon nanotubes[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2010, 353 (1) : 83-91. |
| [29] | MOHAMMED J, NASRI N S, ZAINI M A A, et al. Optimization of microwave irradiated-coconut shell activated carbon using response surface methodology for adsorption of benzene and toluene[J]. Desalination and Water Treatment, 2015, 57 (17) : 1-17. |
| [30] | WU F C, TSENG R L, JUANG R S. Initial behavior of intraparticle diffusion model used in the description of adsorption kinetics[J]. Chemical Engineering Journal, 2009, 153 (1/2/3) : 1-8. |
| [31] |
近藤精一, 石川达雄, 安部郁夫.
吸附科学[M]. 北京: 化学工业出版社, 2006 : 57 -105.
KONDO S, ISHIKAWA T, ABE I. Science of adsorption[M]. Beijing: Chemical Industry Press, 2006 : 57 -105. |
| [32] | YU Yang, WEI Zhongbo, ZHANG Xiaolong, et al. Biochar from Alternanthera philoxeroides could remove Pb (Ⅱ) efficiently[J]. Bioresource Technology, 2014, 171 (1) : 227-232. |
 2017, Vol. 49
2017, Vol. 49


