2. 城市水资源和水环境国家重点实验室(哈尔滨工业大学),哈尔滨150090
2. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China
煤制气废水含有大量有毒和难降解污染物,随意排放将带来严重的环境污染[1].传统的物化预处理组合生物工艺很难取得满意的去除效果,生化处理后出水仍具有较高质量浓度的污染物和极低的可生化性,属于典型的生物难降解工业废水[2].该类废水的处理已经成为煤制气产业发展的瓶颈,亟需寻找一种性能高效且低成本的深度处理技术解决此类难题,促进该废水最终“零排放”目标的实现.非均相催化臭氧氧化技术因对有毒和难降解物质高效的矿化能力受到关注[3].该技术利用固体催化剂促进臭氧产生羟基自由基,克服了单独臭氧选择性氧化效率低的缺陷,催化剂易于分离,适宜工程应用.其技术核心是高效、廉价催化剂的制备,研究最频繁的是活性炭,其是有效的催化剂也是性能良好的载体[4].围绕负载金属或金属氧化物对活性炭进行修饰强化催化剂活性的研究被广泛报道,例如,活性炭负载Fe、Mn、Ru、Ce、Co、Ni和其氧化物提高臭氧降解水中有机物的效能[5].但是,这些高效的催化剂制备工艺复杂,成本投入过高,不利于其实际应用.同时,废水生物处理工艺产生的污水污泥引起了广泛关注,其干污泥产生量可达1 500万t/a,数量还在逐年递增,如果不能妥善处理会造成严重的环境危害[6].事实上,污水污泥处置最好的方法是进行资源化回收而不是彻底去除,该污泥的本质是炭类物质,通过一些物理条件和化学试剂可以将其转换为类活性炭物质.近年,已有研究成功制备污泥基活性炭吸附染料和重金属等污染物[7-8],取得了良好的去除效果.同时,污泥基活性炭也具有作为臭氧催化剂载体的潜质,将其负载高效廉价的过渡金属氧化物制备臭氧催化剂,解决了催化剂的成本问题,更缓解了污水污泥类固体废弃物对环境的危害,实现了其高附加值的资源化利用.然而,该类催化剂的研制及其催化臭氧氧化深度处理煤制气废水的研究鲜有报道,更缺乏可以指导工业化应用的中试实验研究,限制了该技术进一步的应用.
本研究以废水生物处理工艺产生的污水污泥为原料制备污泥基活性炭(SBAC)作为臭氧催化剂载体,负载过渡金属锰和铁的氧化物研制臭氧催化剂,在中试实验条件下,考察了制备的催化剂(MnOx/SBAC和FeOx/SBAC)催化臭氧氧化煤制气废水生化出水的效能,分析了催化剂对臭氧利用率的影响,明确了其长期使用的稳定性并探讨了催化机理,为其实际应用夯实理论基础.
1 实验 1.1 实验材料中试实验采用的煤制气废水生化出水取自中煤鄂尔多斯能源化工有限公司煤制气废水生化组合工艺二沉池出水.该废水处理工艺主要包括酚氨回收预处理、外循环厌氧反应塔、生物增浓池、改良AO池、二沉池.水质参数为COD、TOC、总酚、氨氮和BOD5质量浓度分别约为150、50、30、30和9 mg/L,温度为25~30 ℃,pH为6.5~7.5.
1.2 催化剂的制备污泥基活性炭的制备采用Wen等[6]技术并进一步改良的方法.将污水污泥在自然条件下风干,然后在恒温烘干箱(105 ℃)烘焙至含水率为10 %以下,研磨筛选尺寸 < 0.1 mm的干污泥颗粒.室温下,取筛选后干污泥颗粒10 g浸渍在75 mL (3 mol/L)的活化剂ZnCl2溶液(m(干污泥):m (ZnCl2)=1:3)24 h,磁力搅拌器以50 r/min转速缓慢混匀(ZnCl2回收率约为70%).样品在恒温烘干箱烘焙24 h,然后在连续通入高纯氮气(流量300 mL/min)用以隔绝空气的马弗炉内进行高温热解,炉内温度按照18 ℃/s缓慢升高至600 ℃,恒温3 h,待热解完成后,使用HCl (3.0 mol/L)冲洗去除无机杂质和酸化金属,超纯水继续冲洗至出水pH不发生变化后在恒温烘干箱烘焙24 h,破碎至 < 0.1 mm得到最终粉末状的污泥基活性炭备用.
污泥基活性炭负载过渡金属氧化物的制备方法是在Faria等[4]方法基础上改良的一种简单的浸渍制备技术.按照实验设计取一定质量的污泥基活性炭浸渍至所需质量浓度的Mn和Fe硝酸溶液(m(污泥基活性炭):m(金属硝酸溶液)=1:1),在室温下利用搅拌器(150 r/min)搅拌一定时间以致完全混匀,回收上清液后沉淀在恒温烘干箱烘干(回收率约60%),样品在连续通入高纯氮气隔绝空气的马弗炉内600 ℃煅烧3 h后获得所需的催化剂.煅烧后的样品用HCl和超纯水清洗松散的杂质和金属离子,最后破碎至 < 0.1 mm烘干储存备用.
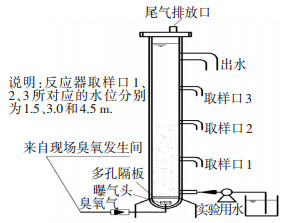
1.3 催化臭氧氧化中试实验中试实验在中煤鄂尔多斯能源化工有限公司废水处理现场进行,反应器装置如图 1所示.主体反应器是有机玻璃材料制成的高6 m的圆柱,有效体积200 L,底部设置微孔硅材料曝气头对臭氧进行均匀布气,利用微孔钛板筛网对催化剂进行阻隔.水样取样口置于反应器底部,中部和上部3处,排除水深带来的影响.顶部设置尾气出口和出水口,所使用臭氧气通过气体流量计对工程现场的臭氧发生器产生臭氧气进行分流得到,现场臭氧发生器类型为Ozonia 1M25101,产气量10 kg/h.间歇实验开始时,将制备的催化剂(原水吸附饱和)和废水按照所需质量和体积一次性投入,连续通入所需质量浓度的臭氧,在设定的时间间隔取样过滤进行测试.在连续流实验中,利用磁力水泵(MP-15R)连续进水,通过流量计(LZB-40)控制进水流速,取样等操作同间歇实验.反应条件为催化剂和臭氧投加量为1 g/L和18 g/h以及原水温度和pH.同时,选取普通工业水处理类型的活性炭与制备的污泥基活性炭进行比较实验.此外,羟基自由基检测是在催化臭氧氧化实验开始前,一次性投加捕获剂叔丁醇,投加质量浓度为100 mg/L,通过比较叔丁醇的投加对催化臭氧氧化矿化废水有机物的抑制性分析羟基自由基在反应过程中的作用.
|
图 1 催化臭氧氧化工艺中试实验装置 Figure 1 Schematic diagram of the pilot-scale catalytic ozonation process |
COD采用重铬酸钾消解比色法测定,总酚采用溴化滴定法测定,氨氮采用纳氏试剂分光光度法测定,臭氧质量浓度采用碘量法,总有机碳采用TOC分析仪(日本岛津,TOC-VCPN).催化剂的比表面积根据Brunauer-Emmet-Teller (BET)方法,采用ASAP-2020比表面积仪测定.催化剂主要元素的组成采用X射线荧光光谱仪分析(XRF,Axios PW4400).灰分采用高温灼烧方法.催化剂的晶型和物相采用粉末X射线衍射进行测定(XRD,RigakuD/max-2000),以Cu靶Kα作为辐射源(λ=0.154 18 nm),石墨单色器,管压45 kV,管流50 mA,步长0.02°,扫描范围10°~90°.根据《HJ557-2010固体废物浸出毒性浸出方法:水平振荡法》进行催化剂浸出毒性的鉴定,金属离子的溶出质量浓度通过全谱直读电感耦合等离子发射光谱仪测定(ICP-AES,Optima 5300DV).
2 结果与讨论 2.1 制备的催化剂特性表征制备的催化剂物理化学性质如表 1所示,污水污泥经过高温煅烧与活化剂ZnCl2发生强烈的蚀刻作用,导致污泥基活性炭(SBAC)形成了较高的比表面积(398.6 m2/g)[9],微孔和中大孔体积以及平均孔径分别为0.141, 0.221 cm3/g和3.725 nm,属于典型的介孔特征.
| 表 1 制备催化剂物理化学性质 Table 1 Physicochemical properties of the prepared catalysts |
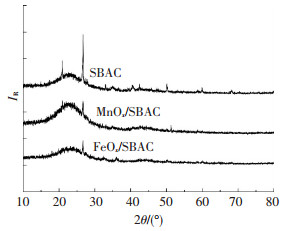
通过XRF对制备的催化剂金属负载量进行分析,Mn和Fe的氧化物在各自催化剂中所占比例为15.52%和7.45%,导致孔隙部分堵塞,轻微减少了其比表面积,MnOx/SBAC和FeOx/SBAC的比表面积分别为327.5和339.1 m2/g.SBAC的元素组成是以碳氧氮为主,这与污水污泥中含有较多生物处理工艺残余微生物和废水有机物的特性相吻合.同时,金属氧化物的负载并没有导致其他元素组成的显著改变.XRD图谱数据表明(图 2),制备的催化剂在23.5°具有较宽的峰,表明其具有类似活性炭的石墨结构,其中MnOx/SBAC的2θ在28.9°、36.1°、44.5°、50.8°和65.4°处均具有特征衍射峰出现,分别对应(112)、(211)、(220)、(105)、(400)晶面,与Mn3O4标准卡(JCPDS 80-0382)基本吻合.同时,FeOx/SBAC的2θ在30.5°、35.7°、44.2°、53.4°和62.3°具有特征衍射峰,相对应(220)、(313)、(400)、(511)、(440)晶面,与Fe3O4标准卡(JCPDS 88-0866)具有相似的衍射模式.因此,认为催化剂表面主要形成了多种价态的金属氧化物,分别为Mn3O4和Fe3O4.
|
图 2 污泥基活性炭和催化剂XRD图谱 Figure 2 XRD of SBAC and the prepared catalysts |
如表 2所示,6种主要重金属(Cr,Cu,Cd,Zn,As,Pb)质量浓度均远低于《危险废物鉴别标准-浸出毒性鉴别》(GB5085.3-2007)规定的允许浸出质量浓度,这表明制备的催化剂及载体在废水处理中不会产生二次污染,可以作为安全的催化剂长时间使用.相对于原污水污泥,高温活化导致重金属离子转化为难溶性金属氧化物被浓缩和包埋在污泥基活性炭内,与污泥基活性炭形成稳定的复合物.同时,对制备的产物通过盐酸彻底酸洗,可以有效去除不稳定的无机杂质和酸化态的金属,降低浸出液中金属质量浓度.添加活化剂ZnCl2导致催化剂的浸出液中Zn离子质量浓度出现小幅增加,但是该质量浓度仍为较低的重金属质量浓度,远低于国家的排放标准.
| 表 2 浸出液重金属质量浓度 Table 2 Result of extraction toxicity |
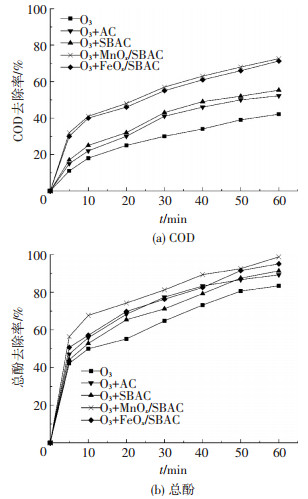
臭氧投加量为18 g/h,两种催化剂催化臭氧氧化煤制气废水生化出水的效能如图 3所示.单独臭氧氧化60 min后仅有42.1 %的COD被去除,这是由于该过程中有大量难以氧化的中间产物生成和积累,单纯依靠延长反应时间和增加臭氧投加量并不能大幅提高污染物的去除效果.制备催化剂的投入显著提高了臭氧氧化废水中COD去除效果,MnOx/SBAC,FeOx/SBAC和SBAC催化臭氧氧化对COD去除率分别达平均72.1(MnOx/SBAC和FeOx/SBAC)和52.2 %,较单独臭氧氧化提高了30%和10%.而且,SBAC与商业活性炭(AC)的催化活性相比没有明显差异,AC催化臭氧氧化对废水COD去除率为55.3%.相比而言,催化剂的吸附能力较弱,而且,在催化过程使用的催化剂均已在原水水质条件下吸附饱和后进行实验,以排除吸附的影响.因此,催化臭氧氧化对废水COD的高效去除归因于催化剂的催化活性而不是其吸附能力.同时,酚类化合物作为废水中主要的有毒和难降解物质与COD的去除趋势不完全相同[10].在单独和催化臭氧氧化过程,接近50%的总酚在反应10 min时被快速去除,反应结束时超过90%的总酚被去除,两种氧化体系并没有明显差异,这个结果与Martins和Quinta-Ferreira[11]使用商业催化剂Fe-Mn-O催化臭氧氧化酚类物质相吻合(反应60 min内接近90%的总酚被去除),这表明本研究制备的催化剂活性不低于商业催化剂Fe-Mn-O.
|
图 3 催化臭氧氧化去除废水污染物的效能 Figure 3 Performance of pollutants removal in catalytic ozonation |
如表 3所示,采用MnOx/SBAC和FeOx/SBAC催化臭氧氧化对废水COD、TOC、总酚和NH4+-N的去除率分别为71.3%~72.6%,60.0%~62.0%,97.1%~98.0%和82.0%~83.0%,相对应的出水质量浓度分别在41~43,19~20,0.6~0.9和4.3~4.5 mg/L,均达到城镇污水处理厂污染物排放一级标准的A标准(GB18918-2002),有利于该废水最终“零排放”目标的实现.综上,制备的催化剂显著提高了臭氧氧化煤制气废水生化出水的效能.
| 表 3 催化臭氧氧化对废水中污染物的去除效能 Table 3 Pollutants evolution in the raw and treated wastewater by ozonation without and with catalysts |
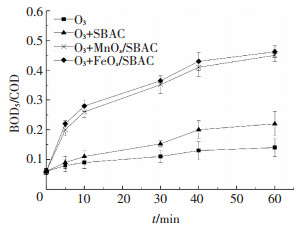
煤制气废水生化出水残留在COD中的物质大部分是难生物降解的有机物,例如酚类化合物、芳香烃和氮杂环类等,导致废水的BOD5/COD在0.1左右,难以进行有效的生物工艺处理[12].如图 4所示,随着臭氧氧化时间延长至60 min,BOD5/COD值逐渐增加至0.14(单独臭氧氧化),0.22(SBAC)和平均0.45(MnOx/SBAC和FeOx/SBAC).Esplugas等[13]认为,废水的BOD5/COD超过0.40即可认为其具有良好的可生物降解性能,显然,只有MnOx/SBAC和FeOx/SBAC催化臭氧氧化处理后的出水可以达到该标准,催化臭氧氧化过程产生的强氧化性自由基对废水中难降解有机物进行较为彻底的矿化或者生成易降解的小分子氧化产物例如低分子酸等,提高了废水的可生化性,不会对受纳水体产生二次污染.
|
图 4 催化臭氧氧化对废水可生化性的影响 Figure 4 Change of biodegradability during the catalytic ozonation process |
臭氧通入反应器后,会有相当一部分臭氧未参与氧化反应随气流排出,变成臭氧尾气,降低臭氧利用效率,影响其氧化能力和运行成本,催化剂的投加会对臭氧利用率产生显著的影响.由于两种催化剂的性能相近,在此不进行区分.
臭氧利用率公式为
| $ 臭氧利用率=\frac{进水\text{COD}-出水\text{COD}}{臭氧进气总量-残留臭氧量}. $ |
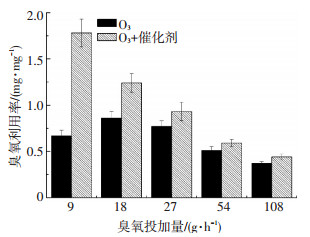
如图 5所示,单独臭氧氧化过程中,臭氧投加量为18 g/h时,臭氧利用率最高,达0.86 mg/mg (以COD计),随着臭氧投加量进一步增加其利用率逐步下降,最终108 g/h时利用率仅有0.37 mg/mg,这表明高臭氧投加量不能高效地去除废水中污染物.添加催化剂后,臭氧投加量为9 g/h时,其臭氧利用率达最高(1.78 mg/mg),随着臭氧投加量的增加其利用率也逐步下降,最终108 g/h时仅有0.44 mg/mg,这表明催化剂在低臭氧投加量具有更高的催化活性,过量的臭氧投加需要不断增加进气流量来实现,影响了催化剂与废水中污染物的有效接触,而且催化过程产生的羟基自由基会与过量的臭氧分子发生复合反应,产生自分解效应,降低了催化臭氧氧化的间接氧化性能,造成臭氧利用率偏低,成本增加与浪费严重.相比单独臭氧氧化系统,催化剂对臭氧利用率的增加分别为165%(9 g/h),45.2%(18 g/h),20.1%(27 g/h),15.7 %(54 g/h)和18.9%(108 g/h),催化剂的使用显著提高了臭氧利用率,降低了臭氧氧化过程的运行成本.同时,过低的臭氧投加量不足以对废水中污染物进行充分的氧化反应(臭氧投加量9 g/h时,其COD去除率仅为40%),因此,最佳的臭氧投加量为18 g/h,其臭氧利用率为1.24 mg/mg,较单独臭氧氧化提高了40%.
|
图 5 单独和催化臭氧氧化过程臭氧利用率的变化 Figure 5 Evolution of ozone utilization rate in catalytic ozonation |
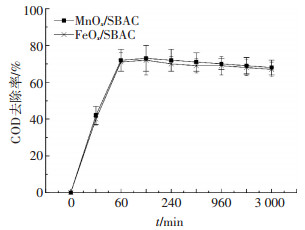
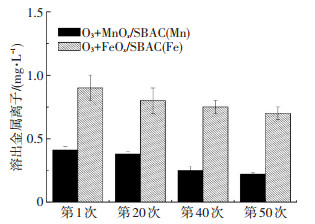
如图 6所示,相比新鲜的催化剂,连续50次的催化臭氧氧化运行(每次60 min),催化剂的催化活性并没有明显下降,MnOx/SBAC和FeOx/SBAC催化臭氧氧化对COD去除率平均下降5.2%,制备的催化剂具有长期的稳定性.污水污泥中的金属可分为酸溶态、可还原态、可氧化态和残渣态,其中,可氧化态和残渣态为稳定态.本研究中污泥基活性炭经过长时间的高温活化,含有的还原态金属较少,难以与Fe-Mn氧化物结合,进行解析和迁移.氧化态的金属与有机物和硫化物结合,通过部分有机物发生降解,进而析出金属元素,但是在较长时间的高温热解过程中(两次高温过程累计时间达6 h),大部分有机物和金属硫化物被氧化,无法引起大量的氧化态金属的析出,更多是以大分子的难溶性金属氧化物固定在碳矩阵内,以稳定的氧化态和残渣态存在.同时,催化剂制备的过程采用高质量浓度盐酸进行彻底酸洗,可以有效去除不稳定的无机杂质和酸化态的金属,降低金属析出质量浓度,增强污泥基活性炭的吸附性能.因此,制备的催化剂长期使用过程中,锰和铁金属的析出程度均较低,两种催化剂最大的溶出量分别为0.4 mg/L (Mn)和0.9 mg/L (Fe),仅为负载于SBAC的Mn和Fe总量的0.5%~1.0%,均低于国家城镇污水处理厂污染物排放标准(图 7),不会对环境产生二次污染,更保障了催化剂的长期活性.
|
图 6 连续催化臭氧氧化过程中催化剂的稳定性 Figure 6 Catalytic performance of catalysts in successive ozonation runs |
|
图 7 连续催化臭氧氧化过程中金属离子的溶出情况 Figure 7 Effect of successive ozonation runs on leached metal ions of catalysts |
催化剂制备过程使用的各化学试剂配置标准和用量及单价为:3 mol/L的ZnCl2,其与干污泥按照质量比3:1浸渍,回收率约为70 %,硝酸锰和铁溶液与污泥基活性炭浸渍比例为1:1,回收率约为60%.其中工业硝酸锰、硝酸铁和氯化锌市场售价约为5 000,2 500和6 000元/t,电费为0.6元/度,水费为2元/t.计算催化剂成本:SBAC的产率约为50.5 %,即2 t干污泥可以产生1 t的SBAC,消耗ZnCl2 1.3 t,酸洗的HCl使用量约为0.5 t/t (600元/t),耗电量约300度,费用180元,水费约为6元,污泥处理补偿费用为400元/t (按照进入焚烧炉焚烧处理计算),共计800元,计算后得出SBAC生产成本约为3 500元/t.进一步计算MnOx/SBA和FeOx/SBAC的制作成本约为5 500和4 500元/t,平均为5 000元/t,与普通工业级别活性炭价格相近.然而,制备的催化剂催化臭氧氧化煤制气废水生化出水的效能远高于工业级别的活性炭(图 3),相近的投资可以获得更优质的出水水质,达到国家规定的最高污水处理要求,有利于煤制气废水“零排放”目标的实现.同时,高附加值地利用固体废弃物污水污泥制备臭氧催化剂处理废水,实现了“以废治废”和可持续发展的目的.因此,本研究制备的催化剂催化臭氧氧化煤制气废水生化出水具有性能高效稳定、经济节约和可持续发展的技术优势和工业化应用的潜质.
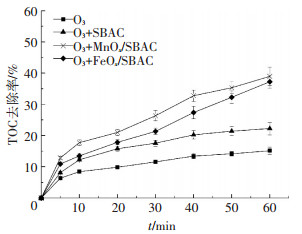
2.6 催化臭氧氧化煤制气废水生化出水机理探讨通过在催化臭氧氧化煤制气废水生化出水过程中添加羟基自由基捕获剂叔丁醇,分析该催化过程羟基自由基的作用.叔丁醇为常见的羟基自由基的捕获剂,能与羟基自由基快速反应生成惰性中间物质,终止臭氧的链式分解反应[14].由图 8可以看出,叔丁醇的投加负面影响了催化剂的催化活性,催化臭氧氧化对废水TOC的去除率从未投加叔丁醇的40.0%(SBAC)和平均61.1 %(MnOx/SBAC和FeOx/SBAC,表 2)分别减少到投加后的21.2%和平均37.1%(图 8),平均降低43.5%.该催化臭氧氧化过程可能的反应机理,基本属于羟基自由基间接氧化为主导,多种氧化反应协同作用[15].
|
图 8 投加羟基自由基捕获剂对催化臭氧氧化性能的影响 Figure 8 Effect of radical scavengers on the performance of catalytic ozonation |
1) 以污水污泥为原料制备了污泥基活性炭负载过渡金属锰和铁氧化物类型的臭氧催化剂,其比表面积分别为327.5和339.1 m2/g,负载的金属氧化物主要为Mn3O4和Fe3O4,负载量分别为15.52%和7.45%,均匀分布在载体表面和孔隙内.制备的催化剂浸出液重金属质量浓度均远低于国家环保规定的标准.
2) 制备的催化剂显著提高了臭氧氧化煤制气废水生化出水的效能,催化臭氧氧化出水COD、TOC、总酚和氨氮质量浓度分别为41~43,19~20,0.6~0.9和4.3~4.5 mg/L,均达到国家城镇污水处理厂污染物排放一级A标准.最佳的臭氧投加量18 g/h条件下,催化剂的使用将臭氧利用率提高40%,达1.24 mg/mg,降低了工艺的运行成本.
3) 相比于新鲜的催化剂,连续50次的催化臭氧氧化运行,COD去除率仅下降5.2%.催化剂具有良好的稳定性,催化剂制备成本平均仅为5 000元/t.
4) 添加叔丁醇严重抑制了催化剂活性的表达,该催化过程属于羟基自由基间接氧化反应为主导,多种氧化反应协同作用.
5) 本研究制备的催化剂催化臭氧氧化煤制气废水生化出水具有性能高效稳定、经济节约和可持续发展的技术优势,适宜工业化应用.
| [1] |
韩超, 叶杰旭, 孙德智. O3-MBR法深度处理煤气废水[J].
环境科学研究, 2010, 7 : 970-974.
HAN C, YE J X, SUN D Z. Advanced treatment of coal gasification wastewater by ozonation combined with membrane bioreactor process[J]. Research of Environmental Sciences, 2010, 7 : 970-974. |
| [2] | ZHAO W, SHEN Y, XIAO K, et al. Fouling characteristics in a membrane bioreactor coupled with anaerobic-anoxic-oxic process for coke wastewater treatment[J]. Bioresource Technology, 2010, 101 (11) : 3876-3883. DOI: 10.1016/j.biortech.2009.12.141 |
| [3] | KASPRZYK-HORDERN B, ZIOLEK M, NAWROCKI J. Catalytic ozonation and methods of enhancing molecular ozone reactions in water treatment[J]. Applied Catalysis B-Environmental, 2003, 46 (4) : 639-669. DOI: 10.1016/S0926-3373(03)00326-6 |
| [4] | FARIA P C C, ORFAO J J M, PEREIRA M F R. Ozonation of aniline promoted byactivated carbon[J]. Chemosphere, 2007, 67 (4) : 809-815. DOI: 10.1016/j.chemosphere.2006.10.020 |
| [5] |
赵雷, 孙志忠, 马军. 金属催化臭氧化应用在水处理中的机理研究进展[J].
现代化工, 2007 (S1) : 78-82.
ZHAO L, SUN Z Z, MA J. Research advances in mechanism of ozonation catalyzed by metal for application in water treatment[J]. Modern Chemical Industry, 2007 (S1) : 78-82. |
| [6] | WEN G, PAN Z, MA J, et al. Reuse of sewage sludge as a catalyst in ozonation:Efficiency for the removal of oxalic acid and the control of bromate formation[J]. Journal of Hazardous Materials, 2012, 239 : 381-388. |
| [7] |
游洋洋, 卢学强, 许丹宇, 等. 复合污泥基活性炭催化臭氧氧化降解水中罗丹明B[J].
工业水处理, 2015, 35 (1) : 56-59.
YOU Y Y, LU X Q, XU D Y, et al. The catalytic ozonation of sludge based composite activated carbon for the degradation of Rh B in aqueous solution[J]. Industrial Water Treatment, 2015, 35 (1) : 56-59. |
| [8] |
包汉峰, 杨维薇, 张立秋, 等. 污泥基活性炭去除水中重金属离子效能与动力学研究[J].
中国环境科学, 2013, 33 (1) : 69-74.
BAO H F, YANG W W, ZHANG L Q, et al. Efficiency and kinetics of heavy metal removal from water by sludge-based activated carbon[J]. China Environmental Science, 2013, 33 (1) : 69-74. |
| [9] | SMITH K M, FOWLER G D, PULLKET S, et al. Sewage sludge-based adsorbents: A review of their production, properties and use in water treatment applications[J]. Water Research, 2009, 43 (10) : 2569-2594. DOI: 10.1016/j.watres.2009.02.038 |
| [10] | SAEED M, IIYAS M. Oxidative removal of phenol from water catalyzed by nickel hydroxide[J]. Applied Catalysis B-Environmental, 2013, 129 : 247-254. DOI: 10.1016/j.apcatb.2012.09.028 |
| [11] | MARTINS R C, QUINTA-FERREIRA R M. Screening of ceria-based and commercial ceramic catalysts for catalytic ozonation of simulated olive mill wastewaters[J]. Industrial & Engineering Chemistry Research, 2009, 48 (3) : 1196-1202. |
| [12] | WANG W, HAN H J. Recovery strategies for tackling the impact of phenolic compounds in a UASB reactor treating coal gasification wastewater[J]. Bioresource Technology, 2012, 103 (1) : 95-100. DOI: 10.1016/j.biortech.2011.10.002 |
| [13] | ESPLUGAS S, CONTRERAS S, OllIS D. Screening of ceria-based and commercial ceramic catalysts for catalytic ozonation of simulated olive mill wastewaters[J]. Industrial & Engineering Chemistry Research, 2009, 48 (3) : 1196-1202. |
| [14] | MURUGANANDAM M, WU J J. Synthesis, characterization and catalytic activity of easily recyclable zinc oxide nanobundles[J]. Applied Catalysis B: Environmental, 2008, 80 (1/2) : 32-41. |
| [15] |
刘永泽, 江进, 马军, 等. 臭氧氧化过程中羟基自由基产率测定与分析[J].
哈尔滨工业大学学报, 2015, 47 (2) : 9-12.
LIU Y Z, JIANG J, MA J, et al. Determination of hydroxyl radical yields in the ozonereactions[J]. Journal of Harbin Institute of Technology, 2015, 47 (2) : 9-12. |
 2017, Vol. 49
2017, Vol. 49


