经典脱氮理论包括硝化和反硝化两个过程,分别需好氧和缺氧不同的环境条件;除磷则需要厌氧/好氧交替的环境条件,将磷酸盐合成聚磷后通过排泥的方式去除[1].有研究表明[2-3],硝化和反硝化可以在一个维持低溶解氧的反应器内同时进行,且聚磷菌可利用硝酸盐、亚硝酸盐或溶解氧作为电子受体氧化内源物质同时吸磷[4],控制厌氧/限氧条件获得脱氮除磷效果的这一过程称为同步脱氮除磷.其与传统控制厌氧/缺氧/好氧环境条件进行的脱氮除磷相比,具有节约溶解氧、有机碳源和反应器占地面积的优点.脱氮除磷的效果受系统中DO、pH、温度、C与N比等多种因素的影响[5-8],其中pH是反应器运行的重要参数,不仅对氨氧化、反硝化有影响,还对磷的释放和吸收有影响,但pH对同步脱氮除磷运行效果的影响尚鲜见报道.且有研究表明,同步脱氮除磷系统中最终主要产物并非N2,而是温室气体N2O[9],导致污染物由水相转移到气相,因此,考察pH对同步脱氮除磷系统中N2O的释放对控制温室气体具有重要意义.
本研究以模拟生活污水为研究对象,接种亚硝化活性污泥,在SBR中成功实现了同步脱氮除磷的启动及稳定运行.在此基础上, 对单周期C、N、P转化规律及不同进水pH对同步脱氮除磷效果及N2O释放特性进行研究,旨在为厌氧-限氧SBR同步脱氮除磷运行以及N2O减量化控制提供理论依据.
1 实验 1.1 实验装置与运行实验采用高径比34:15的圆柱形反应器,其有效容积为5 L.使用空气压缩机曝气,通过玻璃转子流量计控制曝气量约为280 mL/min,使好氧阶段DO质量浓度维持在0.3~0.8 mg/L.在曝气阶段同时进行搅拌,使泥水混合均匀.反应器在室温(18~22 ℃)下运行.
SBR启动期间反应器每天运行3个周期,每个周期8 h,其中进水2 min、厌氧搅拌180 min、曝气210 min、沉降50 min、排水10 min、闲置28 min.稳定运行后反应器每天运行4个周期,每个周期6 h,包括进水2 min、厌氧搅拌70 min、曝气210 min、沉降50 min、排水10 min、闲置18 min.排水比为0.5,HRT为12 h.利用微电脑时控开关实现SBR反应器的自动控制.
1.2 接种污泥与实验废水实验种泥取自实验室驯化好的亚硝化污泥,接种后反应器中初始污泥质量浓度(以MLSS计)约为2 000 mg/L.驯化阶段不排泥,稳定运行阶段每天在好氧末端排泥水混合液200 mL,使污泥平均停留时间SRT约为25 d.稳定后反应器内污泥质量浓度(MLSS)维持在5 000 mg/L左右.
实验采用人工配水,在启动期间配水成分为COD(以CH3COONa为碳源)200~400 mg/L、NH4+-N 40~100 mg/L、PO43--P 10~26 mg/L、MgSO4·7H2O 100 mg/L、CaCl2 60 mg/L、蛋白胨60 mg/L.微量元素的配比参见文献[10], 投加量为0.3 mL/L.系统稳定后配水成分为COD 400 mg/L、NH4+-N 40 mg/L、PO43--P 26 mg/L,其他元素投加量不变;稳定运行过程中进水pH约为7.5.
1.3 批式实验采用批式实验方法考察不同进水pH(6.0、7.0、8.0、9.0)对同步脱氮除磷系统的影响.批式实验采用内径6 cm、高50 cm的圆柱形玻璃反应器,有效容积为1.0 L.实验污泥均取自母反应器好氧末污泥0.6 L,用去离子水反复清洗直至清洗液中的NH4+-N、NO2--N、NO3--N和PO43--P质量浓度降至1 mg/L以下,弃去上清液后加入反应器内,同时加入与母反应器成分及质量浓度相同的基质至混合液的总体积为1 L,利用1 mol/L的盐酸或氢氧化钠调节初始pH分别为6.0、7.0、8.0、9.0.厌氧阶段采用高纯氮气曝气搅拌,曝气量约为500 mL/min;好氧阶段采用空气压缩机曝气,以多孔气泡石作为微孔曝气器,用玻璃转子流量计控制曝气量(约为15 mL/min),维持低氧环境(DO < 1.0 mg/L).为使污泥混合均匀,在好氧阶段同时曝氮气,使总曝气量维持在500 mL/min.批式反应器中污泥质量浓度(MLSS)约为3 400 mg/L.批式实验在室温环境下进行(20 ℃).
1.4 水质分析NH4+-N、NO2--N、NO3--N、PO43--P、MLSS、COD均按照国家环保总局颁布的标准方法进行测定[11],其中NH4+-N采用纳氏试剂分光光度法,NO2--N采用N-(1-萘基)-乙二胺光度法,NO3--N采用紫外分光光度法,PO43--P采用钼锑抗分光光度法,MLSS采用重量法;COD采用重铬酸钾法;pH用精密酸度仪(PHM210, HACH, US)测定;DO用哈希便携式溶解氧仪(HQ25d,HACH,US)测定.水样测定前先经0.45 μm滤膜过滤.
1.5 N2O分析及其释放速率和释放量的计算用气密性良好的气体采样针收集5 mL气样,采用PE 600气相色谱仪对气样中的N2O进行分析.所有气样均测定3次,取平均值.N2O的测定方法、释放速率和释放量的计算参考文献[12]的方法.
2 结果与讨论 2.1 SBR同步脱氮除磷系统的启动与维持图 1为厌氧-限氧SBR同步脱氮除磷启动及运行过程中氮、磷质量浓度随运行时间的转化情况.可以看出,第1~6天内,进水COD为100 mg/L, 进水NH4+-N质量浓度根据处理效果调整(18.3~49.5 mg/L),此时出水NO3--N质量浓度从10.8 mg/L上升到15.6 mg/L后下降到6.6 mg/L,NO2--N质量浓度从26.7 mg/L上升到44.9 mg/L后下降到13.5 mg/L,脱氮率在11.5%左右,表明系统中主要发生了(短程)硝化反应,脱氮效果差;此时间段内,进水磷质量浓度和出水磷质量浓度几乎相同,均在7.0 mg/L左右,无除磷效果.系统脱氮除磷效果差主要是因为接种污泥为自养型亚硝化菌.第7~15天,为了富集异养反硝化菌和聚磷菌,提高进水COD至150 mg/L,同时降低NH4+-N质量浓度至24.2 mg/L左右,出水NO2--N质量浓度从15.7 mg/L降至0.1 mg/L,NO3--N质量浓度在3.2 mg/L左右;进水磷质量浓度在8.3 mg/L左右,出水磷质量浓度从9.7 mg/L降到了0.3 mg/L.氮、磷的去除率分别达76.5%、96.8%,表明SBR中成功实现了同步脱氮除磷的启动.自第16~37天,为提高磷的去除效能,将进水COD和磷质量浓度分别提高至200和10 mg/L, 维持进水NH4+-N质量浓度在19.9 mg/L左右,出水NH4+-N质量浓度0.5 mg/L,出水NO2--N质量浓度从3.4 mg/L左右降低到0.8 mg/L,出水NO3--N质量浓度维持在0.9 mg/L左右,出水磷质量浓度维持在0.2 mg/L左右,氮和磷的去除率在87.7%和97.1%以上.第37天起,出水NO2--N有少量积累(4 mg/L左右),出水NO3--N质量浓度在1 mg/L左右,出水磷质量浓度小于1 mg/L,脱氮率和除磷率分别稳定在76.1%、98.4%左右,表明系统较为稳定运行.

|
图 1 SBR同步脱氮除磷系统启动及运行过程中氮、磷的转化 Figure 1 Concentration profiles of nitrogen and phosphorus in SBR during the start-up and running period of SNDPR system |
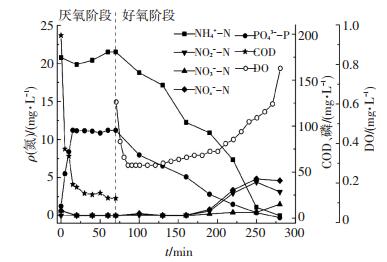
第55天研究了SBR单周期碳、氮和磷的转化特性,结果如图 2所示.可以看出,厌氧阶段,COD在前20 min内快速降低,由198.4 mg/L降至33.6 mg/L,之后只有少量COD被消耗,COD去除率达89.1%.相应地,磷质量浓度在前20 min内由12.9 mg/L升至94.9 mg/L,之后磷质量浓度几乎不变.进入好氧阶段后,磷质量浓度几乎呈直线下降,由95.4 mg/L降至0.5 mg/L,除磷率达99.5%,除磷效果良好.与此同时,NH4+-N质量浓度随时间不断降低,由21.5 mg/L降至0 mg/L,NOx--N质量浓度在前90 min(70~150 min)无积累,表明发生了同步硝化反硝化脱氮现象,90 min后开始有少量的积累,质量浓度由0.1 mg/L升至4.6 mg/L,TN去除率达78.6%.
|
图 2 SBR典型周期COD、氮素和磷的转化 Figure 2 Concentration profiles of COD, nitrogen and phosphorus during a typical cycle in parent reactor |
限氧条件下发生脱氮现象表明反应器中除了(短程)硝化外还发生了(短程)反硝化反应,单周期去除氮的量为16.9 mg/L,根据反硝化和短程反硝化的计量关系式计算得分别需消耗COD的量为48.3和29.1 mg/L,意味着脱氮过程至少需要29.1 mg/L的有机物;而厌氧结束后剩余COD的量仅为21.5 mg/L,因此,可以断定反硝化过程除消耗水中的COD外还消耗了内碳源,即系统中还发生了利用内碳源反硝化的过程,这也是同步脱氮除磷系统节省碳源的原因.此外,碳源不足是本研究单周期末NOx--N有少量积累的原因之一,另反应后期DO质量浓度的上升抑制了反硝化也是一个重要原因.
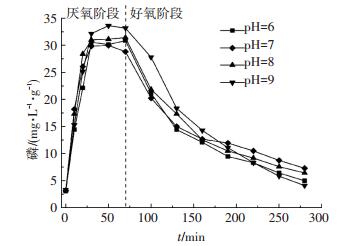
2.3 进水pH对释磷、吸磷的影响图 3为不同进水pH条件下磷质量浓度随时间的转化.可以看出,在不同的pH(6.0、7.0、8.0、9.0)条件下,厌氧前30 min溶液中磷质量浓度几乎均呈直线上升.厌氧后期,进水pH为6.0、7.0、8.0时磷质量浓度基本保持不变,而进水pH为9.0时反而缓慢释磷.随着pH由6.0升到9.0,单位MLSS厌氧释磷量分别达27.8、25.6、28.3、29.9 mg/(L·g),单位MLSS平均释磷速率分别达54.1、44.6、48.0、57.9 mg/(L·h·g).好氧阶段呈现良好的吸磷现象,尤其是前1 h内吸磷速度较快,进水pH为6.0、7.0、8.0、9.0时吸磷速率分别达16.4、12.9、12.1、14.9 mg/(L·h·g),整个好氧段单位MLSS平均吸磷量和吸磷速率分别达25.9、21.5、25.0、29.1 mg/(L·g)和6.6、4.7、5.6、8.3 mg/(L·h·g),可见厌氧段释磷量和释磷速率越大,好氧段吸磷量和吸磷速率越大.
|
图 3 不同进水pH下磷质量浓度随时间的转化 Figure 3 Concentration profiles of phosphorus under different influent pH conditions |
PAOs在厌氧条件下吸收VFA,需要消耗ATP,聚磷被酶水解产生的H+被排到细胞质膜的外面,使得膜内外形成电势差[13].因为乙酸的吸收速率保持不变,所以pH越高,需要更多的能量来实现主动运输[14],多聚磷酸盐分解速度越快,同时释放磷酸盐的速率也越大,这就造成pH为9.0和8.0时释磷量较大.但pH为6.0时的释磷量较pH为7.0时的要大,这是由于在厌氧条件下pH过低时会造成无效释磷而导致释磷量增大[15].
从本实验的结果看,进水pH为6.0、7.0、8.0、9.0时,除磷率分别为84.0%、74.7%、79.6%、87.7%,进水pH为9.0时除磷效果最好.
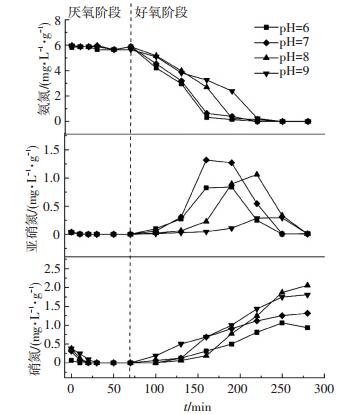
2.4 进水pH对脱氮的影响图 4为不同的进水pH条件下NH4+-N、NO2--N、NO3--N随时间的转化.
|
图 4 不同进水pH下氮随时间的转化 Figure 4 Concentration profiles of nitrogen under different influent pH conditions |
由图 4可以看出,进水pH为6.0、7.0、8.0、9.0时,氨氧化均在好氧阶段前150 min(整个反应过程中70~220 min)内完成,单位MLSS平均氨氧化速率分别为3.7、3.5、2.8、2.1 mg/(L·h·g).好氧30 min后NOx--N均有不同程度的积累,NO2--N质量浓度均呈现先上升后下降的趋势,出水质量浓度均低于0.03 mg/(L·g),NO3--N质量浓度是持续逐渐升高的趋势,pH为8.0时NO3--N质量浓度最高,为2.1 mg/(L·g).反应最终的脱氮效率分别为83.9%、77.5%、64.9%、67.8%.
综上,随着pH的下降,氨氧化速率和脱氮效率均呈上升的趋势,pH为6.0时,能获得较高的脱氮除磷效率,这为SNDPR工艺处理某些低碳氮比的市政污水提供了一定的理论依据,但同时要综合考虑传统脱氮除磷工艺补充碳源与此工艺加酸的经济合理性.
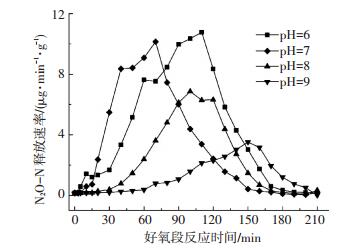
2.5 进水pH对氧化亚氮释放的影响图 5为好氧阶段不同进水pH(6.0、7.0、8.0、9.0)条件下氧化亚氮释放速率随时间的变化.可以看出,N2O的释放速率均呈现先升高后降低的趋势,释放速率的峰值随pH的升高呈降低的趋势,分别为10.8、10.1、6.9、3.5 μg/(min·g).经计算,进水pH为6.0、7.0、8.0、9.0时单周期N2O释放量分别为3.5、3.1、2.1、0.1 mg,释放量占去除氮的比例分别为21.4%、19.7%、14.8%、5.3%,因此,随着pH降低,N2O释放量增加.
|
图 5 好氧阶段不同进水pH下N2O-N释放速率随时间的变化 Figure 5 Profiles of N2O-N emission rate under different influent pH in aerobic stage |
在生物脱氮过程中,氨氧化和反硝化过程中都可能产生N2O,Meyer等[9]研究表明,反硝化是N2O释放的主要来源.值得关注的是,N2O的释放速率与NO2--N的质量浓度呈正相关关系,对比图 4、5可见,所有pH条件下,好氧前期随着NO2--N的积累,N2O释放速率随之增大;好氧后期随着NO2--N的减少,N2O释放速率也随之减小.具体原因是HNO2对N2O还原酶(Nos)产生抑制作用,使得N2O的生成速率大于还原速率,导致N2O的积累[10].而且,在相同NO2--N质量浓度下,pH越低,HNO2质量浓度越高,对Nos抑制作用越强,这也是本研究中N2O释放随pH降低而增加的原因.
3 结论1) 以含乙酸钠、氨氮、磷酸盐的人工配水为基质,通过控制厌氧-限氧(DO 0.3~0.8 mg/L)条件成功实现了SBR同步脱氮除磷,氮、磷的去除率分别达(76.1±5)%、(98.4±1)%.
2) pH由6.0升到9.0时, 除磷率分别为84.0%、74.7%、79.6%、87.7%,pH为9.0时除磷效果最好,其次为pH为6.0时.
3) pH由6.0升到9.0时,脱氮率分别为83.9%、77.5%、64.9%、67.8%,pH为6.0时脱氮率最好.
4) 随着pH升高,N2O释放量逐渐减少,pH为6.0时的释放量是pH为9.0时的3.5倍.
| [1] |
OEHMEN A, LEMOS P C, CARVALHO G, et al. Advances in enhanced biological phosphorus removal: From micro to macro scale[J].
Water Research, 2007, 41(11): 2271-2300.
DOI: 10.1016/j.watres.2007.02.030 |
| [2] |
GOGINA E, GULSHIN I. Simultaneous nitrification and denitrification with low dissolved oxygen level and C/N ratio[J].
Procedia Engineering, 2016, 153: 189-194.
DOI: 10.1016/j.proeng.2016.08.101 |
| [3] |
JIA Wenlin, LIANG Shuang, NGO H H, et al. Effect of phosphorus load on nutrients removal and N2O emission during low-oxygen simultaneous nitrification and denitri-fication process[J].
Bioresource Technology, 2013, 141(4): 123-130.
|
| [4] |
KAPAGIANNIDIS A G, ZAFIRIADIS I, AIVASIDIS A. Comparison between aerobic and anoxic metabolism of denitrifying-EBPR sludge: Effect of biomass poly-hydroxyalkanoates content[J].
New Biotechnology, 2013, 30(2): 227-237.
DOI: 10.1016/j.nbt.2012.05.022 |
| [5] |
LI Yongfeng, YANG Jianyu, ZHANG Guocai. Changes of pH in A2O process system and its impact on nitrogen and phosphorus removal[J].
Advanced Materials Research, 2012, 588: 55-58.
|
| [6] |
CHEN Hongbo, WANG Dongbo, LI Xiaoming, et al. Effect of dissolved oxygen on biological phosphorus removal induced by aerobic/extended-idle regime[J].
Biochemical Engineering Journal, 2014, 90(9): 27-35.
|
| [7] |
JIA Wenlin, WANG Qian, ZHANG Jian, et al. Nutrients removal and nitrous oxide emission during simultaneous nitrification, denitrification, and phosphorus removal process: impact of temperature[J].
Desalination and Water Treatment, 2016, 23(15): 15657-15664.
DOI: 10.1007/s11356-016-6758-2 |
| [8] |
WANG Xiaoxia, WANG Shuying, XUE Tonglai, et al. Treating low carbon/nitrogen (C/N) wastewater in simultaneous nitrification-endogenous denitrification and phosphorous removal (SNDPR) systems by strengthening anaerobic intracellular carbon storage[J].
Water Research, 2015, 77: 191-200.
DOI: 10.1016/j.watres.2015.03.019 |
| [9] |
MEYER R L, ZENG R J, GIUGLIANO V, et al. Challenges for simultaneous nitrification, denitrification, and phosphorus removal in microbial aggregates: Mass transfer limitation and nitrous oxide production[J].
FEMS Microbiology Ecology, 2005, 52(3): 329-338.
DOI: 10.1016/j.femsec.2004.11.011 |
| [10] |
ZENG R J, LEMAIRE R, YUAN Z, et al. Simultaneous nitrification, denitrification, and phosphorus removal in a lab-scale sequencing batch reactor[J].
Biotechnology and Bioengineering, 2003, 84(2): 170-178.
DOI: 10.1002/(ISSN)1097-0290 |
| [11] |
国家环境保护总局.
水和废水监测分析方法[M]. 北京: 中国环境科学出版社, 2002: 258-284.
State Environmental Protection Administration. Water and wastewater monitoring and analysis method[M]. Beijing: China Environmental Science Press, 2002: 258-284. |
| [12] |
吕永涛, 张雪玲, 王磊, 等. pH对高氨废水限氧半亚硝化过程中N2O释放的影响[J].
哈尔滨工业大学学报, 2015, 47(6): 88-93.
LÜ Yongtao, ZHANG Xueling, WANG Lei, et al. Effect of pH values on nitrous oxide emission during partial nitritation of high-ammonium wastewater under oxygen-limited condition[J]. Journal of Harbin Institute of Technology, 2015, 47(6): 88-93. DOI: 10.11918/j.issn.0367-6234.2015.06.016 |
| [13] |
苗志加. 强化生物除磷系统聚磷菌的富集与反硝化除磷特性[D]. 北京: 北京工业大学, 2013.
MIAO Zhijia. The study of PAO enrichment and performance of denitrifying phosphorus removal in EPBR system[D]. Beijing: Beijing University of Technology, 2013. |
| [14] |
SMOLDERS G J F, LOOSDRECHT M V, HEIJNEN J J. pH: Key factor in the biological phosphorus removal process[J].
Water Science & Technology, 1994, 29(7): 71-74.
|
| [15] |
郭琇, 孟昭辉, 董晶颢. 厌氧池中pH对生物除磷的影响[J].
哈尔滨商业大学学报(自然科学版), 2005, 21(3): 292-294.
GUO Xiu, MENG Zhaohui, DONG Jinghao. Study on pH value effect on removal of biological phosphorus in anaerobic pool[J]. Journal of Harbin University of Commerce (Natural Sciences Edition), 2005, 21(3): 292-294. |
 2018, Vol. 50
2018, Vol. 50


