纳滤(NF)膜表面通常荷电, 电荷作用和筛分作用[1]是决定溶质截留的主要机制.NF膜被广泛应用于饮用水深度处理、海水淡化及废水处理[2-4]等领域中.引起NF膜污染的主要污染物有难溶和微溶性无机盐、有机污染物、微生物及其代谢产物和胶体污染物[5-7].由于膜污染造成的水通量下降及膜寿命的缩短[8-9], 降低了其经济效益.
纳滤过程中, 有机污染通常先于无机污染形成[10-11].Liu等[12]研究正渗透膜表面吸附的不同有机污染物对随后硫酸钙结垢的影响时发现, 与新膜相比, 膜表面吸附牛血清蛋白后, 会明显阻碍随后硫酸钙结垢的生成; 然而当膜表面吸附腐殖酸和海藻酸(AA)后, 硫酸钙结垢的生成被显著加剧.据此推测NF膜表面特性很可能被其表面吸附的有机污染物改变[13-14], 进而影响随后NF膜表面的无机结垢.此外, 当水体中存在多种污染物时, 相比单一污染物的膜污染, 有机与无机污染物共存对NF膜的污染[15-16]更为显著.Higgin等[17]研究RO膜的硅酸盐结垢发现, AA与硅酸盐在溶液中共存时, 与硅酸盐共存的AA会降低RO膜的硅酸盐结垢程度.
多糖类有机物广泛存在于水体中, 是胞外聚合物的主要成分之一.本文选用典型多糖类有机物研究纳滤过程中AA的不同存在状态对聚酰胺复合纳滤膜硅酸盐结垢的影响.以新膜的硅酸盐结垢行为作对比, 考察AA与硅酸盐在溶液中共存时以及NF膜表面生成AA污染层时对随后硅酸盐结垢的影响.采用原子力显微镜及Zeta电位等手段揭示AA影响硅酸盐结垢的特点和机理, 从而为防治NF膜硅酸盐结垢提供更完善的理论依据.
1 实验 1.1 实验材料制膜试剂:N, N-二甲基乙酰胺(DMAc, 分析纯, 天津市福晨化学试剂厂); 聚乙二醇辛基苯(TritonX-100, 分析纯, 国药化学试剂有限公司); 聚乙二醇(PEG600, 分析纯, 天津市科密欧化学试剂有限公司); 丙烯酸(分析纯, 天津市福晨化学试剂厂); 聚乙烯吡咯烷酮(PVP k.30, 分析纯, 上海蓝季科技发展有限公司); 聚砜(PSF, E6010, 德国BASF); 无水哌嗪(PIP, 分析纯, aladdin); 三乙胺(TEA, 分析纯, aladdin); 均苯三甲酰氯(TMC, 98%, Sigma-Aldrich); 正己烷(分析纯, 广东光华科技股份有限公司).
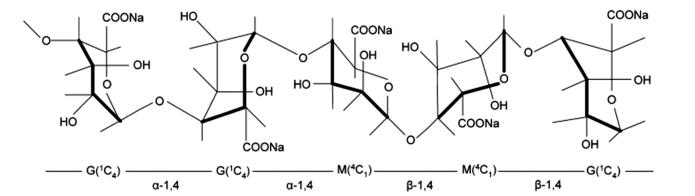
污染物试剂:偏硅酸钠五水合物(Na2SiO3·5H2O, 95%, 国药化学试剂有限公司); 海藻酸(AA, Sigma-Aldrich, St. Louis, Mo),其分子结构式如图 1所示[18].氯化钠(分析纯, 天津市巴斯夫化工有限公司); 硫酸镁及硫酸钠(分析纯, 天津市天力化学试剂有限公司).
1.2 聚酰胺复合纳滤膜制备 1.2.1 聚砜超滤膜制备采用溶液相转化法制备聚砜超滤膜.将TritonX-100、PEG600、丙烯酸、PVP k.30、PSF按照一定比例溶于溶剂DMAc中, 在60 ℃下恒温恒速搅拌16 h, 然后在恒温烘箱(DZ-2BC, 天津市泰斯特仪器有限公司)中60 ℃下静置脱泡, 得到均质的铸膜液.在室温下, 采用无纺布作为支撑层, 将铸膜液均匀涂覆在无纺布上, 随后立即浸入恒温凝胶浴中进行分相, 然后将分相完成后的膜用去离子水反复冲洗, 最后将聚砜超滤膜常温保存在去离子水中.
1.2.2 聚酰胺复合纳滤膜制备采用界面聚合法制备聚酰胺复合纳滤膜.室温下, 将PIP溶于去离子水中配制成水溶液, 将TMC溶于正己烷中配制成有机溶液.先将聚砜超滤膜浸泡在水溶液中一定时间, 用橡胶辊筒除去膜表面多余溶液与气泡, 然后再浸入有机溶液中反应一段时间, 随后置于烘箱中恒温热处理一段时间, 即得到聚酰胺复合纳滤膜, 将其存储于去离子水中备用.
聚酰胺复合纳滤膜基本性能如下:室温、压力为0.6 MPa条件下, 其纯水渗透通量为(35±5) L/(m2·h), 硫酸镁(2 g/L)截留率大于92%;平均粗糙度为7.71 nm, 用接触角仪(SL200B, 科诺, 美国)测定膜表面接触角为(53±2)°, 截留分子质量为(350±50) u.
1.3 膜污染过滤实验按照表 1所示组成配制各类污染液.制备AA(2 g/L)标准储备液.先将2 g的AA溶解在1 L的去离子水中, 再用0.45 μm微滤膜(密理博, 比勒利卡, MA)过滤得到储备液, 置于4 ℃的冰箱中进行保存.用1 mol/L的盐酸及氢氧化钠溶液调节所有原液的pH至7.5±0.1.在测试压力0.6 MPa、室温下进行实验.采用小型错流平板纳滤实验装置进行膜污染过滤实验, 装置见图 2.
| 表 1 原液的化学组分 Table 1 Chemical composition of the feed solutions |

|
图 2 小型错流平板纳滤测试装置示意 Figure 2 Schematic diagram of cross flow nanofiltration test device |
过滤实验分为3组:(a)新膜硅酸盐结垢实验; (b)AA与硅酸盐共存时(新膜)结垢实验; (c)AA污染膜硅酸盐结垢实验.
NF膜硅酸盐结垢实验具体步骤如下:1)利用去离子水预压膜1 h, 直至通量达到稳定状态.2)换用基线溶液继续平衡膜2 h, 待通量稳定后, 记录下初始膜通量J0(实验(a)和(b)).3)进行不同条件下的硅酸盐结垢实验.实验(a)组和(b)组, 分别利用硅酸盐溶液和AA与硅酸盐共存溶液进行结垢实验48 h; 实验(c)组中, 首先利用AA溶液对NF膜进行有机污染24 h, 在膜面生成有机污染层后, 记录下实验(c)的初始膜通量J0.再利用硅酸盐溶液对AA污染膜进行硅酸盐结垢试验48 h.实验结束后, 将过滤污染后的膜直接取出, 裁剪成两块, 一块利用原子力显微镜(AFM, Multimode 8.0, 布鲁克, 德国)测试污染膜表面微观形貌, 另一块晾干后采用扫描电子显微镜(SEM, JSM-6510LV, 日本JEOL)观察膜污染层结构.
1.4 污染液及膜的Zeta电位实验利用Zeta电位仪(ZS90Zeta, 马尔文, 英国)分别测定硅酸盐溶液及AA与硅酸盐共存溶液的Zeta电位.利用固体表面Zeta电位仪(SurPass, 安东帕, 奥地利)测定新膜和AA污染膜在相应溶液中的Zeta电位.
1.5 黏附力实验采用物理黏附法制备二氧化硅(SiO2)胶体探针[19].在光学显微镜(奥林巴斯, TH4-200, 日本)下, 利用微操作器在SiN无针尖探针(NP-010, 布鲁克, 德国)微悬臂自由端黏附少量环氧树脂胶, 接着黏附一个直径5 μm的SiO2微球.将制备好的SiO2胶体探针静置固化备用.SiO2胶体探针的SEM图见图 3.

|
图 3 SiO2胶体探针扫描电镜图 Figure 3 SEM image of SiO2 colloidal probe |
Mi等[20]利用SiO2胶体探针测定正渗透膜面的硅酸盐结垢界面作用力.利用AFM联合SiO2胶体探针测定硅酸盐结垢过程中的作用力.采用新膜和AA污染膜结合相应的结垢溶液测定膜-SiO2胶体探针及硅酸凝胶-膜之间的黏附力, 获得NF膜面硅酸盐结垢过程中的作用力特点.在液相接触模式下测定作用力, 为减小实验误差, 在膜表面选取6个不同的局域点, 每个点进行10次重复测定, 然后计算平均值进行分析.
1.6 其他分析方法采用接触角仪测定膜表面接触角; 用SEM检测结垢实验完成后所得膜面的污染层结构; 采用AFM扫描膜表面的微观形貌, 并且进行粗糙度的测量.
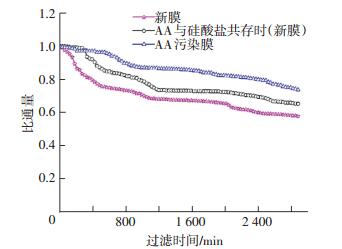
2 结果与讨论 2.1 AA不同存在状态对膜通量的影响图 4为不同条件下硅酸盐结垢的膜通量衰减曲线.不同条件下膜通量按照初始膜通量标准化(J/J0)处理.
|
图 4 不同条件下膜的硅酸盐结垢通量衰减曲线 Figure 4 Normalized flux decline curves obtained during silicate scaling on membranes of different conditions |
由图 4可以看出, 新膜、AA与硅酸盐共存时(新膜)及AA污染膜的硅酸盐结垢通量衰减率依次为42%、35%和26%, 故通量衰减率为:新膜>AA与硅酸盐共存时(新膜)>AA污染膜.在NF膜污染初期, 新膜硅酸盐结垢的通量衰减程度和速度稍强于AA与硅酸盐共存时(新膜); 在过滤实验中后期, 两者的污染特点非常近似.由于这两组新膜硅酸盐结垢实验, 除AA与硅酸盐共存溶液中含有AA外, 其他实验条件如温度、测试压力、pH及离子强度均一致, 且Mavredaki等[21]研究发现聚羧酸盐能促进硅酸盐结垢的溶解, 而AA具有多个解离羧基官能团(—COO-), 当AA与饱和硅酸盐在溶液中共存时, 很可能与无定形的硅酸盐发生反应, 可以一定程度上稳定溶液中的无定形硅酸盐, 进而延缓硅酸盐结垢进程.当膜表面预先生成AA有机污染层之后, 新膜硅酸盐结垢的通量衰减程度和速度明显大于AA污染膜, 故NF膜表面预先生成的AA有机污染层, 减缓了后续的硅酸盐结垢污染.说明污染层强化的浓差极化作用并未显著促进AA污染膜面的硅酸盐结垢.
2.2 污染膜表面研究 2.2.1 结垢层结构分析用SEM测试不同条件下膜表面硅酸盐结垢层特征.膜过滤过程中的结垢机理为非均相结晶和均相结晶[22].图 5(a)中, 新膜表面发生非均相结晶, 生成一层较厚的结垢层, 膜表面几乎被污染物完全覆盖;在结垢层上还附着密集的颗粒状硅酸盐结垢, 由结垢机理推测颗粒状结垢是由均相结晶产生的; 图 5(b)中, AA与硅酸盐共存时新膜表面散落着少量尺寸较大的硅酸盐结垢; 由图 5(c)可知, AA污染膜表面形成致密均匀的AA有机污染层, 且伴随一些尺寸很小的硅酸盐垢体.综合可知, AA不同存在状态对硅酸盐结垢的影响显著不同.与膜通量衰减曲线(图 4)相比, 新膜的通量衰减最为严重, 其SEM图的表面垢体最多且尺寸最大.AA污染膜的通量衰减最轻, 结合SEM图可知, AA在膜表面形成一层致密污染层, 基本完全覆盖了膜表面, 如果按照污染层强化的浓差极化作用分析, 在后续进行硅酸盐污染时, AA污染膜表面本应生成大量硅酸盐结垢, 但由图可知, 膜面并没有形成大量硅酸盐结垢, 有可能是AA污染层阻碍了溶解性硅酸盐在AA污染膜面的积累, 减轻了硅酸盐结垢程度.

|
图 5 不同条件下膜的硅酸盐结垢扫描电镜图 Figure 5 SEM images of membranes after silicate scaling in different conditions |
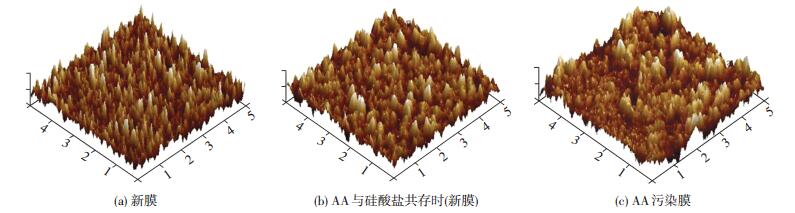
利用AFM测试膜表面结垢的微观形貌, 扫描范围为5 μm×5 μm.由图 6(a)可以看出, 污染层呈密集的竹笋状结构, 据此推测, 新膜表面的硅酸盐结垢致密.由图 6(b)可知, 图中峰高低略有差异, 据此推测AA与硅酸盐共存时新膜面生成的污染层较为致密.在图 6(c)中, AA污染膜的表面结垢层非常不均匀, 可以清晰看出峰的高度在两个区间, 且两个区间的峰高度差异较大.靠近膜面, 较低的峰数量多, 密度大, 且相互之间差异较小; 较高的峰数量较少, 分布不均匀.结合相应的实验条件, 推测较低的峰为AA污染层, 散落的较高的峰为硅酸盐结垢.3种条件下膜表面平均粗糙度分别为:新膜(图 5(a))19.6 nm, AA与硅酸盐共存时(新膜)(图 5(b))13.6 nm, AA污染膜(图 5(c))9.9 nm, 粗糙度大小为:新膜>AA与硅酸盐共存时(新膜)>AA污染膜.将SEM图、AFM形貌图以及膜通量衰减情况结合起来可以发现, 3种实验的分析结果是吻合的, 即结垢层越厚, 越致密, 结垢越严重, 则硅酸盐结垢实验中膜通量衰减越大.
|
扫描范围5 μm×5 μm 图 6 不同条件下膜的硅酸盐结垢的原子力表面形貌图 Figure 6 AFM images of membrane surface morphology of silicate scaling of different conditions |
分析污染液Zeta电位.由表 2可知, 硅酸盐溶液及AA与硅酸盐共存溶液的Zeta电位分别为-17.3和-15.66 mV, 则硅酸盐溶液中有AA共存时, 溶液Zeta电位降低, 说明AA在溶液中确实与溶解性硅酸盐发生了作用, 与过滤实验分析的原因相吻合.
| 表 2 污染物和膜的Zeta电位 Table 2 Zeta potentials of foulants and membranes |
不同条件下膜表面Zeta电位.新膜及AA污染膜的Zeta电位分别为-9.24和-17.36 mV.则新膜及AA污染膜与溶液中溶解性硅酸盐的静电排斥作用力大小为:新膜 < AA污染膜, 与膜通量衰减趋势相吻合, 故推测静电作用可能是新膜结垢与AA污染膜硅酸盐结垢过程中的主导作用.所以需要进一步进行微观作用力的测定.
2.4 黏附力结果分析由于分子间相互作用力比较复杂, 存在范德华力、静电力、氢键力等[23].由Costa等[24]的研究发现, 可以用黏附力综合表征范德华力、静电力、氢键力等复杂作用力的合力.探针与样品表面之间的黏附力计算公式为
| $ F{\rm{ = }}2\pi RW\left( \infty \right). $ |
式中:F为微球与膜表面之间黏附力, N; R为微球半径, m; W(∞)指将一无限接近于平面的微球移走时每单位面积需要的能量, J/m2.黏附力可以理解为污染物脱离膜表面或污染层所需要的能量.由公式可知, 所测定的黏附力与SiO2胶体颗粒的半径成正比关系.为避免因探针尺寸差异所导致的黏附力差异, 将所测定的黏附力标准化为(F/R).
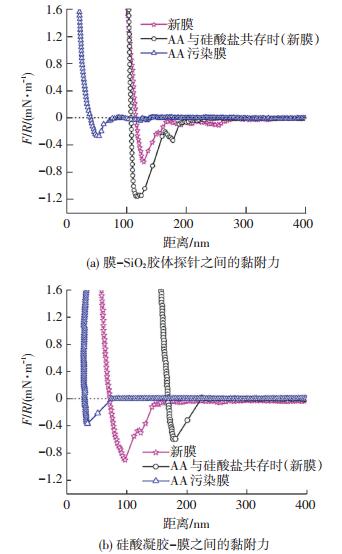
本实验研究了不同条件下的膜-SiO2胶体探针及硅酸凝胶-膜之间的黏附力.SiO2探针在测试溶液中表面含有羟基官能团(-OH), 硅酸盐在溶液中也含有-OH, 故用SiO2代替硅酸盐作为黏附力测定溶液中的硅酸盐污染物[20].由图 7(a)可知, 新膜、AA与硅酸盐共存时(新膜)及AA污染膜与SiO2胶体探针之间黏附力分别为0.65、1.16、0.28 mN/m.由图 7(b)可知, 新膜、AA与硅酸盐共存时(新膜)及AA污染膜的硅酸凝胶-膜之间的黏附力分别为0.90、0.59、0.37 mN/m.
|
图 7 不同条件下黏附力曲线 Figure 7 Representative normalized adhesive force curves at different conditions |
结合图 7(a)、(b)可知, 1)AA与硅酸盐共存时(新膜)不同结垢阶段的黏附力为:膜-SiO2胶体探针>硅酸凝胶-膜.2)对于AA污染膜, 硅酸凝胶-AA污染膜>AA污染膜-SiO2胶体探针.对比AA与硅酸盐共存时(新膜)与AA污染膜的作用力, 可以得出膜-SiO2胶体探针及硅酸凝胶-膜两系列作用力均为:AA与硅酸盐共存时(新膜)>AA污染膜, 与SEM、AFM及通量衰减结果吻合.3)膜-SiO2胶体探针作用力为:AA与硅酸盐共存时(新膜)>新膜, 而硅酸盐结垢通量衰减趋势为:AA与硅酸盐共存时(新膜)<新膜, 与黏附力大小相反.这可能是膜与溶解性硅酸盐间作用力只控制污染初期, 且污染初期通量衰减行为还受到膜面物理特性的影响, 而污染初期过后, 下一阶段硅酸凝胶-膜作用力是整体污染程度的控制因素.4)硅酸凝胶-膜作用力为:新膜>AA与硅酸盐共存时(新膜)>AA污染膜, 与整体通量衰减呈正相关, 说明硅酸凝胶-膜作用力是控制整体污染程度的主要作用.
3 结论1) 不同条件下硅酸盐结垢通量衰减率为:新膜(42%)>AA与硅酸盐共存时(新膜)(35%)>AA污染膜(26%).AA与硅酸盐共存可以较弱程度地减轻硅酸盐结垢; 当AA污染层预先在膜面生成后, 硅酸盐结垢程度明显减弱.
2) AA污染膜的表面Zeta电位显著高于新膜.因此, 在饱和硅酸盐结垢溶液中, 两种膜与溶解性硅酸盐离子间的静电排斥作用为:AA污染膜>新膜, 故AA污染膜表面的硅酸盐饱和度远低于新膜, 因此,AA污染膜表面的硅酸盐结垢程度和速率远低于新膜.与膜通量衰减速率和污染层的SEM和AFM分析结果相吻合.
3) 在AA不同存在状态下, 当AA与饱和硅酸盐在溶液中共存时, 膜-SiO2探针及硅酸凝胶-膜两系列的黏附力均为:AA污染膜 < AA与硅酸盐共存时(新膜), 与通量衰减趋势相一致.当膜面生成AA污染层后, 与新膜相比, 两系列作用力均为:AA污染膜 < 新膜, 与通量衰减结果吻合, 说明膜表面生成AA污染层后, 硅酸盐结垢会被减缓.结合Zeta电位可知, AA污染膜面和溶解性硅酸盐间的静电作用成为AA污染膜面硅酸盐结垢的主要影响因素.
| [1] |
任晓晶, 皇甫风云, 白云东. 芳香聚酰胺纳滤膜的制备及影响因素[J].
天津工业大学学报, 2007, 26(2): 18-20, 23.
REN Xiaojing, HUANGFU Fengyun, BAI Yundong. Preparation and influence factors of aromatic polyamide nanofiltration membrane[J]. Journal of Tianjin Polytechnic University, 2007, 26(2): 18-20, 23. DOI: 10.3969/j.issn.1671-024X.2007.02.005 |
| [2] |
SHON H K, VIGNESWARAN S. Influence of flocculation and adsorption as pretreatment on the fouling of ultrafiltration and nanofiltration membranes: Application with biologically treated sewage effluent[J].
Environmental Science and Technology, 2005, 39(10): 3864-3871.
DOI: 10.1021/es040105s |
| [3] |
王薇. 纳滤膜在水处理中的最新应用进展[J].
高分子通报, 2010(10): 24-29.
WANG Wei. Recent application progresses of nanofiltration membranes in water treatment[J]. Chinese Polymer Bulletin, 2010(10): 24-29. DOI: 10.14028/j.cnki.1003-3726.2009.10.009 |
| [4] |
DIAWARA C K. Nanofiltration process efficiency in water desalination[J].
Separation & Purification Reviews, 2008, 37(3): 302-324.
|
| [5] |
JERMANN D, PRONK W, BOLLER M. Mutual influences between natural organic matter and inorganic particles and their combined effect on ultrafiltration membrane fouling[J].
Environmental Science & Technology, 2008, 42(24): 9129-9136.
|
| [6] |
CONTRERAS A E, KIM A, LI Q. Combined fouling of nanofiltration membranes: Mechanisms and effect of organic matter[J].
Journal of Membrane Science, 2009, 327(1/2): 87-95.
|
| [7] |
LI Q, ELIMELECH M. Synergistic effects in combined fouling of a loose nanofiltration membrane by colloidal materials and natural organic matter[J].
Journal of Membrane Science, 2006, 278(1/2): 72-82.
|
| [8] |
FANE A G (Tony), WANG R, JIA Y. Membrane technology:Past, present and future[J].
Handbook of Environmental Engineering, 2011, 13: 1-45.
|
| [9] |
NATH K, PATEL T M. Mitigation of flux decline in the cross-flow nanofiltration of molasses wastewater under the effect of gas sparging[J].
Separation Science & Technology, 2014, 49(10): 1479-1489.
|
| [10] |
FAROOQUE A M, AL-AMOUDI A S, O'HARA J, et al. RO membrane failure: Investigation of failure during preservation[J].
Filtration & Separation, 2007, 44(9): 22-24.
|
| [11] |
LEE S, CHO J, ELIMELECH M. Combined influence of natural organic matter (NOM) and colloidal particles on nanofiltration membrane fouling[J].
Journal of Membrane Science, 2005, 262: 27-41.
DOI: 10.1016/j.memsci.2005.03.043 |
| [12] |
LIU Y, MI B. Effects of organic macromolecular conditioning on gypsum scaling of forward osmosis membranes[J].
Journal of Membrane Science, 2014, 450: 153-161.
DOI: 10.1016/j.memsci.2013.09.001 |
| [13] |
WANG J, WANG L, MIAO R, et al. Enhanced gypsum scaling by organic fouling layer on nanofiltration membrane: Characteristics and mechanisms[J].
Water Research, 2016, 91: 203-213.
DOI: 10.1016/j.watres.2016.01.019 |
| [14] |
张晓婷, 王磊, 杨若松, 等. 有机大分子对聚酰胺复合纳滤膜偏硅酸钠污染的影响[J].
中国环境科学, 2016, 36(2): 460-467.
ZHANG Xiaoting, WANG Lei, YANG Ruosong, et al. Effects of organic macromolecular on sodium metasilicate fouling behavior of polyamide composite nanofiltration membrane[J]. China Environmental Science, 2016, 36(2): 460-467. DOI: 10.3969/j.issn.1000-6923.2016.02.023 |
| [15] |
JARUSUTTHIRAK C, MATTARAJ S, JIRARATANANON R. Influence of inorganic scalants and natural organic matter on nanofiltration membrane fouling[J].
Journal of Membrane Science, 2007, 287(1): 138-145.
DOI: 10.1016/j.memsci.2006.10.034 |
| [16] |
AL-AMOUDI A S. Factors affecting natural organic matter (NOM) and scaling fouling in NF membranes: A review[J].
Desalination, 2010, 259(1/2/3): 1-10.
|
| [17] |
HIGGIN R, HOWE K J, MAYER T M. Synergistic behavior between silica and alginate: Novel approach for removing silica scale from RO membranes[J].
Water Resources Research, 2010, 250(1): 76-81.
|
| [18] |
KATSOUFIDOU K, YIANTSIOS S G, KARABELAS A J. Experimental study of ultrafiltration membrane fouling by sodium alginate and flux recovery by backwashing[J].
Journal of Membrane Science, 2007, 300(1/2): 137-146.
|
| [19] |
王磊, 苗瑞, 吕永涛, 等. AFM微颗粒探针及其在膜的有机物污染机制解析中的应用研究与展望[J].
材料导报, 2013, 27(13): 113-117.
WANG Lei, MIAO Rui, LU Yongtao, et al. Recent development of AFM microsphere probe and its application in analysis of membrane organic fouling[J]. Materials Review, 2013, 27(13): 113-117. DOI: 10.3969/j.issn.1005-023X.2013.13.024 |
| [20] |
MI B, ELIMELECH M. Silica scaling and scaling reversibility in forward osmosis[J].
Desalination, 2013, 312: 75-81.
DOI: 10.1016/j.desal.2012.08.034 |
| [21] |
MAVREDAKI E, ELEFTHERIA N A, DEMADIS K D. Inhibition and dissolution as dual mitigation approaches for colloidal silica fouling and deposition in process water systems: Functional synergies[J].
Industrial & Engineering Chemistry Research, 2005, 44(17): 7019-7026.
|
| [22] |
LEE S, LEE C H. Effect of operating conditions on CaSO4 scale formation mechanism in nanofiltration for water softening[J].
Water Research, 2000, 34(15): 3854-3866.
DOI: 10.1016/S0043-1354(00)00142-1 |
| [23] |
蔡元霸, 梁玉仓. 纳米材料的概述、制备及其结构表征[J].
结构化学, 2001, 20(6): 425-438.
CAI Yuanba, LIANG Yucang. Preparation and structure characterizations of nanosized materials[J]. Chinese Journal of Structural Chemistry, 2001, 20(6): 425-438. DOI: 10.3969/j.issn.0254-5861.2001.06.001 |
| [24] |
COSTA A R, PINHO M N D, ELIMELECH M. Mechanisms of colloidal natural organic matter fouling in ultrafiltration[J].
Journal of Membrane Science, 2006, 281(1/2): 716-725.
|
 2018, Vol. 50
2018, Vol. 50