随着高纯石墨日益成为现代科技与工业发展的重要原料[1],其需求量和生产量也将持续增长.出于经济性和实用性的考虑,目前高纯石墨的生产主要采用氢氟酸法[2],由此产生了大量酸性含氟废水.废水中排放过量氟会污染环境,危害农作物和牲畜的正常生长,更会严重影响人体健康[3],工业废水除氟研究变得尤为重要,其处理结果监测的准确性对控制该行业的环境冲击有着重要作用.
测定水中氟离子质量浓度常用的方法有氟离子选择电极法、氟试剂分光光度法、茜素锆比色法、离子色谱法、气相色谱法以及荧光法等[4].离子选择电极法具有电极结构简单牢固、灵敏度高、响应速度快、能克服色泽干扰、精度高等优点, 而且便于携带、操作简单,因而被作为标准方法广泛采用.在使用氟离子选择电极法测定石墨精制废水沉淀混凝法处理出水时,发现稀释后氟离子质量浓度偏高的现象.本文对这种现象的原因进行了研究,并探讨了石墨工业含氟废水处理出水氟离子质量浓度测量的影响因素及注意事项.
1 实验原理及方法 1.1 实验原理氟离子选择电极是一种均相晶体膜电极,电极管内有氯化钠和氟化钠混合液作为内参比溶液,其工作电极可表示为|Ag|AgCl,NaF, NaCl|LaF3单晶膜|.通常氟离子选择电极与甘汞参比电极联用,构成电池.两个电极之间的电位差即电动势(E)随氟离子活度变化而改变,其关系满足能斯特方程,当溶液的总离子强度值固定且有足够强度时,二者服从关系式
| $ E = K - \frac{{ 2.303RT}}{F}{\rm{lg}}{C_{{{\rm{F}}^ - }}}. $ | (1) |
式中:K为参比电极电位(固定值),R为气体常数(8.314 J/(mol·K)),F为法拉第常数,T为绝对温度,CF-为氟离子活度.通过测量标准溶液电极电位,将结果氟离子质量浓度负对数对应做出标准曲线,之后利用待测试样的电位值即可计算试样氟离子质量浓度.
1.2 试剂材料及实验装置实验中所用的试剂纯度均为分析纯,所用纯水均为去离子水.主要沉淀剂为氧化钙、氢氧化钙、碳酸钙,用于中和pH和去除氟离子.混凝剂分别为PAC(聚合氯化铝)和PAM(聚丙烯酰胺)等,用于进一步除氟并增强污泥的沉降性能.氟化钠用于配置氟离子标准溶液制作标准曲线,柠檬酸钠和硝酸钠为配置氟离子测定缓冲溶液的主要药品,碳酸钙和熟石灰为中和反应药剂.实验设备用到了沉淀混凝反应的相关设备如搅拌器、离心机以及测定用的pH计、氟离子选择电极、元素分析的ICP(等离子体发射光谱仪)、离子色谱等.此外还用到了塑料烧杯、玻璃烧杯、量筒、玻璃棒、pH试纸、移液管、定性滤纸、塑料薄膜、皮筋等常用实验用品.主要试剂和仪器如表 1、2所示.
| 表 1 实验药剂 Table 1 Experiment potion |
| 表 2 实验仪器 Table 2 Experiment instruments |
采用pH计和pH试纸进行pH测量.用pH试纸可快速测得大致范围,同时结果稳定可靠,pH计则更为精确.
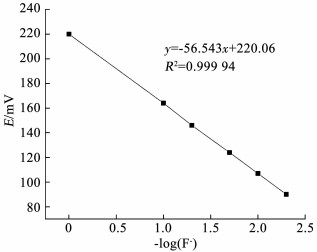
1.3.2 氟离子选择电极法测定氟离子氟离子测定严格按照GB7484—87中的操作规范进行.通过测定NaF标准溶液电动势测定氟离子标准曲线(图 1),再测定未知样的电位值即可根据标准曲线得到未知样的氟离子质量浓度.
|
图 1 氟离子质量浓度标准曲线 Figure 1 Standard curve of fluorine ion concentration |
离子强度缓冲液的配制:称取58.80 g二水柠檬酸钠和85.00 g硝酸钠,加水溶解,用盐酸调节pH至5~6,转入1 000 mL容量瓶中,稀释至标线,摇匀.
溶液中的氟离子质量浓度测量前需加入TISAB(离子强度剂),TISAB的体积占测量液的20%,调解pH,掩蔽铁、铝离子干扰.氟离子电极的测量范围为0.05~1 000 mg/L,溶液的氟离子质量浓度过高时需进行稀释.
1.3.3 离子色谱法测定氟离子水样经0.45 μm滤膜过滤除去不溶性物质后, 稀释至适宜的倍数,使用电感耦合等离子原子发射光谱仪ICP-6300型进行测定.
1.3.4 饱和氟化钙溶液的配制使用氟化钠和氯化钙溶液进行反应,加热搅拌促进反应进行,待反应液冷却后,静置沉淀24 h,使用0.45 μm膜过滤后得到饱和氟化钙溶液.
1.3.5 活性氧化铝吸附对稀释放大作用影响的对比实验对沉淀混凝处理后的出水进行吸附处理,采用活性氧化铝作为吸附剂,进行3组实验进行对比.第1组,沉淀混凝法处理含氟废水,出水用0.45 μm滤膜过滤,稀释后测量,测量时调节pH不加TISAB.第2组,沉淀混凝法处理含氟废水,出水用0.45 μm滤膜过滤,稀释后测量,测量时加TISAB.第3组,沉淀混凝法处理后的出水再进行吸附,吸附后对水样进行0.45 μm滤膜过滤,稀释并测量氟离子质量浓度.
2 结果与讨论 2.1 废水处理后出水不同稀释倍数下氟离子质量浓度的测量石墨工业酸性含氟废水呈强酸性,氟离子质量浓度很高,因此,采用沉淀混凝工艺处理以降低氟离子质量浓度.沉淀工艺通过投加氧化钙中和废水的pH,同时溶液中的钙离子和氟离子形成氟化钙沉淀,此工艺处理后出水可处理至pH中性,氟离子质量浓度大幅下降.混凝工艺通过投加PAC和PAM进一步混凝沉淀,降低溶液中氟离子质量浓度,增强污泥沉降性能.在一定的工艺参数下可以将氟离子质量浓度大于10 000 mg/L的废水处理至5 mg/L以下[5].对7组原废水经沉淀混凝工艺处理后的上清液进行不同倍数稀释,之后使用氟离子选择电极测量氟离子质量浓度,稀释样的测量结果乘以稀释倍数.结果发现将上清液按一定比例稀释后,测定溶液中的氟离子质量浓度并未按照稀释倍数等比例减小,相反,溶液中氟离子的质量浓度大于理论计算的质量浓度,结果相差很大.与原液相比,稀释液的氟离子质量浓度不符合稀释比例,质量浓度明显偏高,结果如表 3.
| 表 3 处理后出水水样及稀释样测量结果 Table 3 Measurements of diluted effluent |
这个现象不容小觑,如果结果属测量误差,应当分析误差原因,为生产实践、环境监测提供指导.如果测得结果为真值,则说明处理后的上清液稀释后会有氟离子溶出的现象,表明此含氟废水处理存在环境隐患,需要对此现象进行分析.
2.2 石墨精制生产废水的组分分析为了找到稀释液氟质量浓度偏高的原因,需要对原废水及处理后出水进行水质分析.通过对废水进行ICP测量以确定其组分测定结果,结果如表 4.可以看出,石墨精制废水中含有大量硅及铁、铝、硫、钙、镁、磷等元素.此外pH测量和离子色谱测量显示,原水的pH在1左右,氟离子质量浓度在10 000 mg/L以上.处理后出水的ICP测量结果如表 5.
| 表 4 石墨精制废水ICP测量结果 mg·L-1 Table 4 ICP measurements of graphite refining wastewater |
| 表 5 处理后出水ICP结果 Table 5 ICP measurements |
对处理后出水进行pH和氟离子质量浓度测量,结果出水pH为7左右,氟离子质量浓度降到5 mg/L以下,氟离子得到了有效的去除,各金属元素和硅的质量浓度大幅度下降,推测为生成各种硅酸盐、碳酸盐沉淀所致.因加入大量钙盐沉淀剂,钙离子质量浓度非常高,水中离子强度应很高.
2.3 稀释测量的误差分析 2.3.1 悬浮氟化钙微晶的溶解室温下饱和氟化钙溶液的氟离子质量浓度为8 mg/L左右,说明氟化钙具有较高的溶解度,而且反应中形成的氟化钙沉淀颗粒非常细小,其中粒径小于2 μm的约占60%[6].细小的氟化钙沉淀不易沉降,上清液中易存在较多氟化钙颗粒,在稀释后会再溶解使溶液中氟离子质量浓度上升.
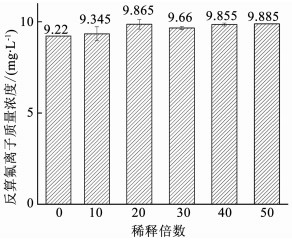
为了探究氟化钙微晶对上清液氟离子质量浓度测量的影响,对饱和氟化钙溶液进行离心和过膜处理,测量其稀释液的质量浓度.由于氟化钙沉淀细小,难以完全沉降,将氟化钙上清液直接稀释,会把悬浮在上清液中的氟化钙颗粒带入稀释液中,进而使氟离子质量浓度偏大.因此,应将氟化钙饱和溶液离心后,用0.45 μm的滤膜过滤,滤液稀释不同倍数,使用离子选择电极法测量稀释液和原液的氟离子质量浓度,将测得的质量浓度乘以稀释倍数可得到各组对应的测量值,以稀释倍数为横坐标,测量结果乘以稀释倍数得到的反算氟离子质量浓度为纵坐标,得出实验结果见图 2.可以看出,过膜后稀释液氟离子质量浓度与稀释比例基本符合.稀释倍数逐渐增大时,氟离子质量浓度略有逐渐偏高的现象.而对石墨精制废水处理后的出水进行离心过膜处理后,稀释样品依然存在质量浓度显著偏高的现象,见图 3.
|
图 2 饱和氟化钙溶液过滤后稀释测量结果 Figure 2 Measurements of filtered saturated calcium fluoride solution dilution |

|
图 3 废水处理出水过滤后稀释测量结果 Figure 3 Measurements of filtered effluent water dilution |
将稀释后样品的测量值乘以稀释倍数就得到反算氟离子质量浓度,原水处理后上清液稀释后氟离子的放大效应远远大于饱和氟化钙溶液稀释结果,这说明氟化钙微晶稀释溶出应该不是出水上清液氟离子测量稀释放大效应的主要原因.
2.3.2 离子强度的影响在稀溶液范围内,影响强电解质离子平均活度系数的决定因素是浓度和离子价数而不是离子的本性,并且离子价数的影响更大,因此引出离子强度的概念.离子强度是衡量溶液中存在离子所产生的电场强度的量度[7].溶液中离子的浓度越大,离子所带的电荷数目越多,粒子与其离子氛之间的作用也就越强,离子强度也越大[8],其定义公式如下
| $ I = \frac{1}{2}\sum\limits_{i = 1}^n {{C_i}Z_i^2} . $ | (2) |
式中:I为离子强度; Ci为离子的质量摩尔浓度(mol/kg),即某溶质的物质的量除以溶剂的质量; Zi为离子的价数.
在使用氟离子选择电极测量溶液中氟离子质量浓度时,氟电极电位与氟离子的活度符合Nernst方程,为使测量准确,需固定溶液的离子强度,使得活度系数成为常数,从而得到氟离子质量浓度负对数与电极电位线性的标准曲线[9].
对于普通的水样,TISAB的离子强度远远超过水样中离子强度,故可以保证测量时离子强度一致.而本文所研究的水样硬度很高,根据表 5中各元素的浓度近似计算,得到水中钙离子浓度为0.459 3 mol/L,硫酸根离子8.813×10-3 mol/L、硅酸根离子0.112 7 mol/L,溶液的阴离子主要是氯离子和硝酸根离子,使用离子色谱法测量二者浓度分别为5.354×10-2和0.557 0 mol/L.
进行离子强度的计算,体积分数20%的TISAB溶液离子强度记为I1,石墨精制废水处理出水的离子强度记为I2.
根据GB7484—87,选择TISAB配方1,即0.2 mol/L柠檬酸钠和1 mol/L硝酸钠.计算时近似认为溶液浓度约等于水的密度,则
| $ \begin{array}{l} {I_1} = \frac{1}{2}\left( {0.2 \times 3 \times {1^2} + 0.2 \times 1 \times {3^2} + 1 \times 1 \times } \right.\\ \left. {\;\;\;\;\;{1^2} + 1 \times 1 \times {1^2}} \right) \times 0.2 = 0.44\;{\rm{ mol/kg, }} \end{array} $ | (3) |
| $ \begin{array}{l} {I_2} = \frac{1}{2}\left( {0.459\;3 \times {2^2} + 0.011\;27 \times {4^2} + 0.053\;54 \times } \right.\\ \;\;\;\;\;\;\left. {{1^2} + 0.557\;0 \times {1^2}} \right) = 1.313\;7\;{\rm{mol/kg}}. \end{array} $ | (4) |
可见出水的离子强度远高于离子强度缓冲液的离子强度,因此,采用国标方法推荐20%体积分数的TISAB不能达到固定离子强度的效果,测定的结果会有误差.
因此,对于这种离子强度很高的水样,应根据其水质成分特点配置特殊的TISAB,如增加柠檬酸钠浓度,提高TISAB的体积分数等,或者对水样进行稀释后再测量.
2.3.3 难溶电解质溶解过程的复杂性氟化钙是难溶的强电解质,其溶解部分在水溶液中几乎完全解离成阴离子和阳离子,但由于离子间的静电作用,存在着一定数量的难溶电解质的“离子对”,这些“离子对”减少了溶液中水合离子的有效浓度,浓度越高,离子对越多,稀释倍数越高,离子对越少,相应的氟离子溶出[10].这很可能是稀释倍数越高,测定结果越高的原因之一.
氢氟酸是一种弱酸,在水溶液中会水解,因而会降低钙离子和氟离子的有效浓度,使氟化钙的溶解度增大.
在反应后的上清液中应该存在如下平衡[11]:
| $ \text{Ca}{{\text{F}}_{\text{2}}}\rightleftharpoons \text{C}{{\text{a}}^{\text{2+}}}\text{+2}{{\text{F}}^{-}}, $ | (5) |
| $ \text{HF}\rightleftharpoons {{\text{H}}^{\text{+}}}\text{+}{{\text{F}}^{-}}, $ | (6) |
| $ \text{HF}_{\text{2}}^{-}\rightleftharpoons \text{HF+}{{\text{F}}^{-}}, $ | (7) |
| $ \text{HF}_{\text{3}}^{\text{2}-}\rightleftharpoons \text{HF}_{\text{2}}^{-}\text{+}{{\text{F}}^{-}}\text{.} $ | (8) |
故不考虑氟的金属络合物的情况下,溶液中的总氟应表示为
| $ {{\left[ {{\text{F}}^{-}} \right]}_{\text{T}}}\text{=}\left[ {{\text{F}}^{-}} \right]\text{+}\left[ \text{HF} \right]\text{+}\left[ \text{HF}_{\text{2}}^{-} \right]\text{+}\left[ \text{HF}_{\text{3}}^{\text{2}-} \right]\text{.} $ | (9) |
因此在溶液稀释后,含氟物质发生电离,会使得溶液中氟离子质量浓度偏高.
2.3.4 掩蔽剂对氟离子的释放本实验氟离子测量采用国标规定的离子选择电极法,高浓度的Fe、Ca和Al等金属元素,会对测量产生干扰[12].使用ICP对反应后上清液中主要元素质量浓度见表 5,Al和Fe均可与氟离子反应形成络合物,干扰氟离子测定.加入TISAB(离子强度缓冲液)可掩蔽铁铝离子释放出络合物中的氟,国标7484—87中给出了3种掩蔽剂配方,以掩蔽剂配方1为例.配方1的主要成分是柠檬酸钠和硝酸钠,柠檬酸钠和铁铝离子的反应方程式[13]如下:
| $ \text{AlF}_{\text{6}}^{\text{3}-}\text{+}{{\text{C}}_{\text{6}}}{{\text{H}}_{\text{5}}}\text{O}_{\text{7}}^{\text{3}-}\to \text{6}{{\text{F}}^{-}}\text{+Al}{{\text{C}}_{\text{6}}}{{\text{H}}_{\text{5}}}{{\text{O}}_{\text{7}}}, $ | (10) |
| $ {\rm{AlF}}_{\rm{6}}^{{\rm{3}} - }{\rm{ + }}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{\rm{5}}}{\rm{O}}_{\rm{7}}^{{\rm{3}} - } \to {\rm{6}}{{\rm{F}}^ - }{\rm{ + Fe}}{{\rm{C}}_{\rm{6}}}{{\rm{H}}_{\rm{5}}}{{\rm{O}}_{\rm{7}}}, $ | (11) |
国标中TISAB溶液的加入量为待测液总体积的20%,国标7484—87指出,加入柠檬酸钠可以络合质量浓度5.0 mg/L的铝.由表 5可知,本文研究的石墨精制废水沉淀混凝工艺处理出水的铝质量浓度为48.8 mg/L,最多可络合206 mg/L的氟(以六氟合铝酸根离子计);铁的质量浓度为1.95 mg/L,最多可络合3.97 mg/L的氟(以六氟合铁酸根离子计).20%的TISAB加入量并不能完全释放上清液络合物中的氟离子,而随着溶液的稀释,TISAB相对过量,氟的络合物与掩蔽剂发生反应而使氟离子充分释放出来,因此稀释液的氟离子质量浓度测量值偏高.
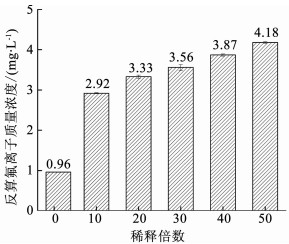
在调整合适的pH后,不加TISAB,过0.45 μm膜后对上清液及稀释液进行氟离子质量浓度测量,结果见图 4.
|
图 4 不加TISAB的氟离子测量结果 Figure 4 Measurement results of fluorine without adding TISAB |
图 4与图 3对比可见,在不加入TISAB的情况下,有随着稀释倍数增加上清液稀释液氟离子质量浓度偏高的现象不明显了,这说明过量的掩蔽剂TISAB将溶液中络合态的氟离子释放出来,是稀释后氟离子质量浓度偏高的主要原因.
2.3.5 氟离子选择电极法与离子色谱法测量结果对比氟铁络合物和氟铝络合物均是十分稳定的络合物,其具体的稳定常数见表 6[14].
| 表 6 含氟络合物的标准稳定常数 Table 6 Standard stability constant of fluorine complex |
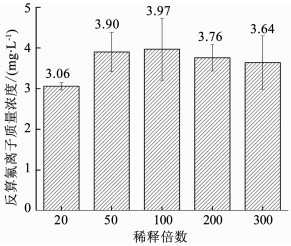
在水溶液中,氟铁络合物和氟铝络合物不会轻易分解,理论上单纯稀释不会释放出氟离子.使用氟离子选择电极法测量处理工业废水所得到的含氟上清液及其稀释液,进行验证,测定结果见图 5.
|
图 5 上清液稀释液离子色谱测量结果 Figure 5 Measurements of diluted supernatant fluid by ionchar-omatography |
原液的质量浓度测为3.48 mg/L,测得稀释液浓度反乘以稀释倍数后得到反算氟离子质量质量浓度,结果并未出现稀释液浓度偏高的现象.此结果与氟离子选择电极法测量结果不同,这是因为离子色谱法测量氟离子质量浓度是不加掩蔽剂的,测得的是溶液中的氟离子质量浓度,并非所有含氟物质中的氟.而离子选择电极法测量时加入掩蔽剂,可以将含氟络合物中的氟释放出来,测得的是总氟质量浓度.石墨精制废水含有较多铝元素和铁元素,处理后的出水中含有较多氟铝络合物和氟铁络合物.故离子色谱法与电极法测量结果会不一致.
《污水综合排放标准》中一级标准要求工业废水中氟化物的最高允许排放质量浓度小于10 mg/L[15].氟铝络合物和氟铁络合物属于氟化物的范畴,也应计算到总氟质量浓度中,故应该以离子选择电极法测量结果为准.
3 结论本文对氟离子选择电极法测定石墨精制废水沉淀处理出水时的浓度偏差现象及原因进行了分析.通过对比实验排除了氟化钙微晶稀释溶解的影响,分析了溶液离子强度、离子对、含氟弱电解质电离、铁、铝等共存离子等因素对测量结果的影响,通过水质分析与对比实验发现:出水中含有较多含氟络合物,稀释液中过量的掩蔽剂TISAB会将溶液中络合态的氟离子释放出来,从而导致氟离子选择电极法测定的结果随稀释倍数增加而增高.通过与离子色谱法的对比发现,使用离子色谱测量出水中氟离子质量浓度时,并未出现稀释液浓度偏高的现象,说明只是稀释处理的情况下,出水并不会释放氟离子,部分氟元素仍以含氟络合物形式存在.因此,若要测得总氟质量浓度,应以氟离子选择电极测量结果为准.对石墨精制废水处理出水中氟离子进行测定时应将水样稀释100倍后,使用氟离子选择电极按照国家标准方法进行操作.
| [1] |
陈婷芳. 石墨矿产市场分析[D]. 北京: 中国地质大学(北京), 2017. CHEN Tingfang. Market analysis of graphite mineral resources[D]. Beijing: China University of Geosciences (Beijing), 2017. http://cdmd.cnki.com.cn/Article/CDMD-11415-1016184320.htm |
| [2] |
罗立群, 谭旭升, 田金星. 石墨提纯工艺研究进展[J]. 化工进展, 2014(8): 2110-2116. LUO Liqun, TAN Xusheng, TIAN Jinxing. Research progress of graphite purification[J]. Chemical Industry and Engineering Progress, 2014(8): 2110-2116. |
| [3] |
张强国, 谢果. 氟危害及重庆氟污染的对策[J]. 重庆科技学院学报(自然科学版), 2005, 7(4): 17-19, 27. ZHANG Qiangguo, XIE Guo. Fluorine harm and the countermeasures of fluorine pollution in Chongqing[J]. Journal of Chongqing Institute of Technology (Natural Science Edition), 2005, 7(4): 17-19, 27. |
| [4] |
刘慧玲. 氟化钙及氟离子测定方法[J]. 广东建材, 2004(8): 80-82. LIU Huiling. Calcium fluoride and fluorine ion method[J]. Guangdong Building Materials, 2004(8): 80-82. |
| [5] |
任婷. 高纯石墨生产中含氟废水处理工艺研究[D]. 哈尔滨: 哈尔滨工业大学, 2016. REN Ting. The fluorine-containing wastewater treatment in the production of high-purity graphite[D]. Harbin: Harbin Institute of Technology, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10213-1016914904.htm |
| [6] |
李程文, 周康根, 姜科, 等. 晶种法处理含氟废水与氟化钙沉淀砂状化研究[J]. 环境科学与技术, 2011, 34(5): 157-160. LI Chengwen, ZHOU Kanggen, JIANG Ke, et al. Treatment of high-concentration fluoride wastewater by crystal seed process and granulation of calcium fluoride[J]. Environmental Science & Technology, 2011, 34(5): 157-160. |
| [7] |
万红友, 师会勤, 周生路, 等. 总离子强度缓冲剂对含氟溶液测定的影响[J]. 土壤通报, 2004, 35(3): 380-382. WAN Hongyou, SHI Huiqin, ZHOU Shenglu, et al. The impact of total ionic strength buffer on determination of fluoride solution[J]. Chinese Journal of Soil Science, 2004, 35(3): 380-382. |
| [8] |
肖衍繁, 李文斌. 物理化学[M]. 天津: 天津大学出版社, 2004: 288. XIAO Yanfan, LI Wenbin. Physical chemistry[M]. Tianjin: Tianjin University Press, 2004: 288. |
| [9] |
SRINIVASAN K. Activity measurements with a fluoride-selective membrane electrode[J]. Analytical Chemistry, 1968, 40(3): 8-16. DOI:10.1021/ac60259a706 |
| [10] |
大连理工大学无机化学教研室. 无机化学[M]. 北京: 高等教育出版社, 2006: 159. Dalian University of Technology of Inorganic Chemistry Teaching and Research Section. Inorganic chemistry[M]. Beijing: Higher Education Press, 2006: 159. |
| [11] |
NDÉ-TCHOUPÉ A. Technologies for decentralized fluoride removal: Testing metallic iron-based filters[J]. Water, 2015, 7(12): 6750-6774. DOI:10.3390/w7126657 |
| [12] |
中国环境监测总站. 水质氟化物的测定——离子选择电极法: GB7484—87[S]. 北京: 中国环境保护局规划标准处, 1987. China's Environmental Monitoring Station. Water quality determination of fluoride-ion selective electrode method: GB7484-87[S]. Beijing: China's Environmental Protection Bureau Planning Standards, 1987. |
| [13] |
严晔赓. 氟离子选择电极法测定废水中氟含量的试验研究[J]. 电力环境保护, 1987(1): 22-27. YAN Yegeng. Research on determination of fluorine content in waste water by Fluoride ion selective method[J]. Electric Power Environmental Protection, 1987(1): 22-27. |
| [14] |
GÁLVEZ J L, DUFOUR J, NEGRO C, et al. Determination of iron and chromium fluorides solubility for the treatment of wastes from stainless steel mills[J]. Chemical Engineering Journal, 2008, 136(2): 116-125. |
| [15] |
国家环境保护局. 污水综合排放标准: GB8978—1996[S]. 北京: 中国环境出版社, 1996. State Environmental Protection Agency. A standard of integrated wastewater discharge GB8978-1996)[S]. Beijing: China Environmental Press, 1996. |
 2018, Vol. 50
2018, Vol. 50


