2. 哈尔滨工业大学 环境学院, 哈尔滨150090;
3. 城市水资源与水环境国家重点实验室(哈尔滨工业大学), 哈尔滨150090;
4. 深圳职业技术学院 建筑与环境工程学院, 广东 深圳 518055
2. School of Environment, Harbin Institute of Technology, Harbin 150090, China;
3. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China;
4. School of Civil and Environmental Engineering, Shenzhen Polytechnic, Shenzhen 518055, Guangdong, China
四氯双酚A(4, 4’-亚异丙基双(2, 6-二氯酚), 简称TCBPA),是双酚A的氯代衍生物, 作为氯代阻燃剂被广泛用于建材、涂料、塑料制品、电路板中, 并用作聚合物、环氧树脂和聚碳酸酯树脂、耐冲性聚苯乙烯、酚醛树脂、黏合剂的添加剂[1, 2].由于TCBPA对化学纤维的优良阻燃性, 使其用途不断增加, 应用范围不断扩大.2005年全球年产量将近10 000 t[3], 大量的生产与使用导致其在水体中频繁检出, 对人体健康和生态环境造成危害[4].2011年8月— 2012年3月, 来自全国31个城市的37个饮用水样品检测结果显示,TCBPA的平均质量浓度为4.9 ng/L, 其中最高质量浓度达到7.7 ng/L[5].
目前对TCBPA的毒理研究尚不完善, 但已确定其具有雌激素性质, 是一种潜在的具有持久性生物累积性和毒性的化合物, 干扰生物的内分泌系统[6-7].因此, 需要利用有效的处理技术对水环境中TCBPA进行控制.有关TCBPA的氧化处理技术研究比较少, 研究较多的是溴代阻燃剂四溴双酚A(TBBPA)的氧化技术.Eriksson等[8]研究了光化学方法降解TBBPA的反应速率和氧化产物, pH=8(k=0.65×10-3 s-1)时TBBPA的分解速率是pH=6(k=0.12×10-3 s-1)时的6倍, 氧化产物主要是3个异丙基衍生物(4-isopropyl-2, 6-dibromophenol, 4-isopropylene-2, 6-dibromophenol和4-(2-hydroxyisopropyl)-2, 6-dibromophenol).Horikoshi等[4]在碱性条件下利用UV/TiO2氧化降解TCBPA和TBBPA, 2 h内可以完全被降解和脱卤, 5 h内矿化率能够达到45%~60%.Lin等[9]利用MnO2氧化降解TBBPA, 反应5 min内TBBPA降解了50%, 反应60 min去除率可以达到90%以上, 并给出了氧化产物及反应机理.本课题组在前期研究[10]中利用KMnO4氧化降解TBBPA, pH=5~10时二级反应速率为15~700 L/(mol·s), 质谱测得6个主要氧化产物(4-(2-羟基异丙基)-2, 6-二溴苯酚、4-异丙烯-2, 6-二溴苯酚、2, 6-二溴苯酚、2, 6-二溴-1, 4-苯醌和两个聚合产物).Voordeckers等[11]研究结果表明, TBBPA在产甲烷条件下, 55 d内完全降解, 并产生等化学当量的双酚A, 然后双酚A不再被进一步降解.而TCBPA在产甲烷条件下被完全降解需要112 d, 且产物主要为二氯双酚A和一氯双酚A, 未检测出双酚A.
综上, 化学氧化方法是降解TBBPA和TCBPA的有效处理技术, 到目前为止, 还没有KMnO4氧化降解TCBPA的相关报道.因此, 本文将利用绿色氧化剂KMnO4氧化降解阻燃剂TCBPA, 研究反应动力学、氧化产物及反应路径.
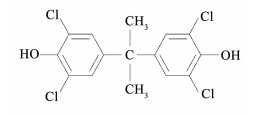
1 实验 1.1 化学试剂目标物四氯双酚A(TCBPA)为分析纯, 购买于Sigma-Aldrich中国公司, CAS号为79-95-8, 其分子结构式见图 1, 物理化学性质见表 1.甲醇、乙腈、甲酸为色谱醇, 购买于Merck中国公司.实验所用其他化学试剂均为分析纯, 购买于国药集团化学试剂有限公司.
|
图 1 四氯双酚A(TCBPA)的分子结构式 Figure 1 Molecular structure of tetrachlorobisphenol A |
| 表 1 四氯双酚A(TCBPA)的物理化学性质 Table 1 Main physicochemical properties of tetrachlorobisphenol A |
KMnO4氧化降解TCBPA的动力学实验在100 mL锥形瓶含50 mL pH缓冲溶液中进行, 反应温度为25 ℃, 加入0.3 μmol/L TCBPA, 摇匀, 加入不同浓度KMnO4起始反应, 不同反应时间取出样品, 用1 mol/L抗坏血酸终止, 样品中TCBPA浓度采用高效液相色谱(HPLC)测定.
KMnO4氧化降解TCBPA的产物测定实验在含10 μmol/L TCBPA、10%乙腈的10 mL反应液中, 分别加入0、5、10、15、20 μmol/L KMnO4起始反应, 待KMnO4完全消耗后, 用0.45 μm玻璃纤维膜对反应后样品进行过滤, 利用高效液相色谱-三重四级杆质谱联用仪(LC-MS/MS)对过滤后样品进行产物分析测定.
1.3 分析方法实验中采用高效液相色谱(Waters 1525)测定TCBPA浓度.色谱柱为Waters Symmetry反相C18柱(4.6×150 mm, 5 μm), 流速为1.0 mL/min, 进样量为100 μL, 流动相甲醇/水为90/10, 检测波长为230 nm, 柱温为35 ℃.
实验中采用三重四级杆串联线性离子阱质谱(AB SCIEX QTRAP 5500)与高效液相色谱(Agilent 1260)联用仪(LC-MS/MS)分析测定氧化产物.色谱柱为Waters XBridgeTM BEH C18(2.5 μm, 3.0×100 mm), 流动相为含0.1%甲酸的超纯水(A)和乙腈(B), 梯度为B先从5%开始, 保持10 min, 然后在50 min内从5%线性升至50%, 保持10 min, 然后在0.1 min内降至5%, 保持10 min, 流速为200 μL/min, 进样量为10 μL, 柱温为35 ℃.离子源采用电喷雾离子源负离子模式(ESI-), 检测模式为子找母扫描模式(Precursor Ion, 简称PIS), 在Q1设定质量数扫描范围为50~500 u, Q3设定子质量数为35或37 u, 扫描速度为1 000 u/s, 离子源电压和温度分别为-4 500 V和500 ℃, 氮气(N2)为气帘气, 流速为35 L/min, 去簇电压(DP)和入口电压(EP)分别为-70和-10 V, 碰撞电压(CE)为-30~-100 V.
2 结果与讨论 2.1 KMnO4氧化降解TCBPA的效果图 2给出了不同pH(5~10)条件下, KMnO4氧化降解TCBPA (0.3 μmol/L)的去除效果.从图 2中可以看出, 不同pH条件下, KMnO4氧化降解TCBPA的去除率都在95%以上.pH=5时, 60 μmol/L KMnO4氧化TCBPA, 反应20 min, TCBPA的去除率可以达到95以上;而在pH=8时, 18 μmol/L KMnO4氧化降解TCBPA, 反应2.5 min, TCBPA的去除率就可以达到95%.由此可见, KMnO4能够高效地氧化降解TCBPA.

|
图 2 KMnO4氧化降解TCBPA的去除效果 Figure 2 Removal of tetrachlorobisphenol A by potassium permanganate |
图 3给出了不同pH(5~10)条件下KMnO4氧化降解TCBPA的动力学规律([KMnO4]0≫[TCBPA]0).由图 3(a)可以看出, TCBPA的氧化降解符合假一级动力学规律, 直线的斜率即为该KMnO4浓度下的假一级速率常数Kobs (s-1).同时假一级速率常数随着KMnO4浓度的增加呈线性增加, 结果见图 3(b).

|
图 3 KMnO4氧化降解TCBPA的反应动力学 Figure 3 Oxidation kinetics of tetrachlorobisphenol A by potassium permanganate |
KMnO4与TCBPA的反应可以用反应式(1)进行描述, 即
| $ \begin{align} &-\frac{\text{d}\left[\text{TCBPA} \right]~}{\text{d}\mathit{t}}={{K}_{\text{obs}}}\left[\text{TCBPA} \right]= \\ &\ \ \ \ \ k\left[\text{Mn}(\text{VII}) \right]\left[\text{TCBPA} \right]. \\ \end{align} $ | (1) |
其中k为二级反应速率常数(L/(mol·s)), 能够通过KMnO4浓度与假一级速率常数Kobs (s-1)获得, 即图 3(b)中每条直线的斜率就是该pH下KMnO4氧化TCBPA的二级反应速率常数k, 见图 3(c).由图 3(c)可以看出, 二级反应速率常数k受pH影响较大, 为40.1~981.7 L/(mol·s), 随着pH的升高先增加而后降低, 在pH=8附近最大, 即二级反应速率常数越接近TCBPA的pKa(7.5/8.5)时越大.这一动力学规律与KMnO4氧化降解TBBPA的规律相一致[10].
KMnO4氧化TCBPA的反应机理与K2FeO4氧化降解酚类化合物的机理相似[12], 见反应式(2)~(5).首先, KMnO4(Mn(Ⅶ))与分子态的TCBPA反应形成氧化络合物Mn(Ⅶ)-TCBPA, 见反应式(4);产生的络合物Mn(Ⅶ)-TCBPA再氧化降解水中离子态的TCBPA, 见反应式(5).
| $\text{TCBP}{{\text{A}}_{总}}=\text{TCBPA}+\text{TCBP}{{\text{A}}^{-}}, $ | (2) |
| $ \text{TCBPA}\rightleftharpoons \text{TCBP}{{\text{A}}^{-}}+{{\text{H}}^{+}}. $ | (3) |
式中:TCBPA总表示反应中总有机物, TCBPA表示反应中分子态有机物, TCBPA-表示反应中离子态有机物.
| $\text{Mn}\left( \text{VII} \right)+\text{TCBPA}\rightleftharpoons \text{Mn}(\text{VII})-\text{TCBPA}~({{K}_{1}}), $ | (4) |
| $ \text{Mn}\left( \text{VII} \right)-\text{TCBPA}+\text{TCBP}{{\text{A}}^{-}}\xrightarrow{{{k}_{2}}}~氧化产物. $ | (5) |
根据反应式(5), TCBPA的氧化降解速率可以表示为
| $ -\frac{\text{d}\left[\text{TCBPA} \right]}{\text{d}\mathit{t}}={{k}_{2}}\left[\text{Mn}\left( \text{VII} \right)-\text{TCBPA} \right]\left[\text{TCBP}{{\text{A}}^{-}} \right]. $ | (6) |
由反应式(4), 反应式(6)可进一步表示为
| $ -\frac{\text{d}\left[\text{TCBPA} \right]}{\text{d}\mathit{t}}\text{ }={{k}_{2}}{{K}_{1}}\left[\text{Mn}(\text{VII}) \right]\left[\text{TCBPA} \right]\left[\text{TCBP}{{\text{A}}^{-}} \right]. $ | (7) |
设
| $ -\frac{\text{d}\left[\text{TCBPA} \right]}{\text{d}\mathit{t}}={{k}_{2}}{{K}_{1}}\left[\text{Mn}(\text{VII}) \right]{{\left[\text{TCBPA} \right]}_{总}}^{2}\cdot \\ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ \alpha \left( 1-\alpha \right). $ | (8) |
根据反应式(8), 当α=0.5, 反应中分子态与离子态TCBPA浓度相等, 即在TCBPA的pKa时, TCBPA的氧化速率最大.
因此, 低pH条件下, 产生的氧化络合物Mn(Ⅶ)-TCBPA多, 离子态TCBPA少, 导致反应中TCBPA的氧化降解速率慢;而高pH条件下, 形成的氧化络合物Mn(Ⅶ)-TCBPA少, 离子态TCBPA多, 导致TCBPA的氧化降解速率也慢;只有当pH在TCBPA的pKa附近时, 产生的氧化络合物Mn(Ⅶ)-TCBPA与离子态化合物TCBPA浓度相当, TCBPA的氧化降解速率才最快[12-14].
2.3 KMnO4氧化降解TCBPA的氧化产物天然环境中氯(Cl)的同位素主要有2个, 质量数为35和37(表示为Cl35和Cl37), 且峰度比为1:1/3.根据氯的这一同位素特性, 利用三重四级杆质谱可以选择性检测氯代有机物, 即子找母质谱扫描模式(LC-MS/MS-PIS)[10, 15-19].
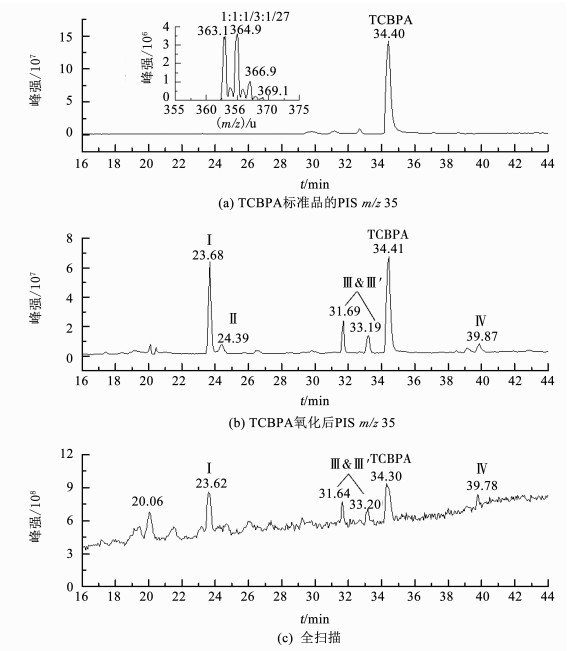
图 4给出了利用LC-MS/MS质谱方法测定KMnO4氧化降解TCBPA的色谱图, 图 4(a)是利用PIS m/z 35测定TCBPA标准样品的色谱图, 图 4(b)是利用PIS(m/z 35)测定KMnO4氧化TCBPA的色谱图, 图 4(c)是利用全扫描质谱模式(full scan)测定KMnO4氧化TCBPA的色谱图.通过对比可以清晰地看出, 全扫描色谱图中的色谱峰非常小, 而在子找母扫描色谱图中能够观察到响应值非常高的色谱峰.因此, 与全扫描质谱模式相比, 子找母质谱扫描模式对氯代有机物的测定更灵敏, 响应值更高.
|
图 4 LC-MS/MS测定KMnO4氧化降解TCBPA的色谱图 Figure 4 Chromatograms of the oxidation products of tetrachlorobisphenol A by potassium permanganate detected by LC-MS/MS |
图 4(b)中KMnO4氧化TCBPA的色谱图中除目标物TCBPA(34.41 min)还有4个主要产物, 分别标记为Ⅰ(23.68 min)、Ⅱ(24.39 min)、Ⅲ&Ⅲ′(31.69和33.19 min)、Ⅳ(39.87 min).利用PIS(m/z 35)子找母扫描模式测定TCBPA的质量数(m/z 35)为363/365/367/369, 且质谱峰的相对峰度比为1:1:1/3:1/27, 质谱图见图 4(a)中的嵌入质谱图.
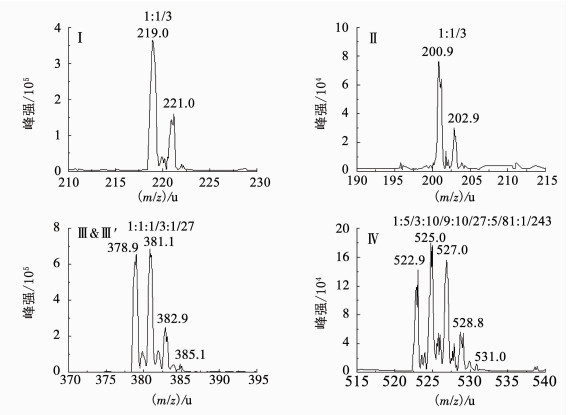
图 5给出了4个氧化产物的质谱图, 质量数PIS(m/z 35)分别为219/221(Ⅰ)、201/203(Ⅱ)、379/381/383/385(Ⅲ&Ⅲ′)、523/525/527/529/531/533(Ⅳ).从图 5可以看出, 产物Ⅰ的质量数(m/z 35)为219/221, 且质谱峰的相对峰度比为1:1/3, 推测结构中含有2个氯;产物Ⅱ的质量数(m/z 35)为201/203, 且质谱峰的相对峰度比为1:1/3, 推测结构中含有2个氯;产物Ⅲ&Ⅲ′的质量数(m/z 35)为379/ 381/383/385, 且质谱峰的相对峰度比为1:1:1/3:1/27, 推测结构中含有4个氯, 为聚合产物;产物Ⅳ的质量数(m/z 35)为523/525/527/529/531/533, 且质谱峰的相对峰度比为1:5/3:10/9:10/27:5/81:1/243, 推测结构中含有6个氯, 为聚合产物.
|
图 5 产物Ⅰ-Ⅳ的PIS(m/z 35)质谱图 Figure 5 Mass spectra of products Ⅰ-Ⅳ obtained by PIS (m/z 35) |
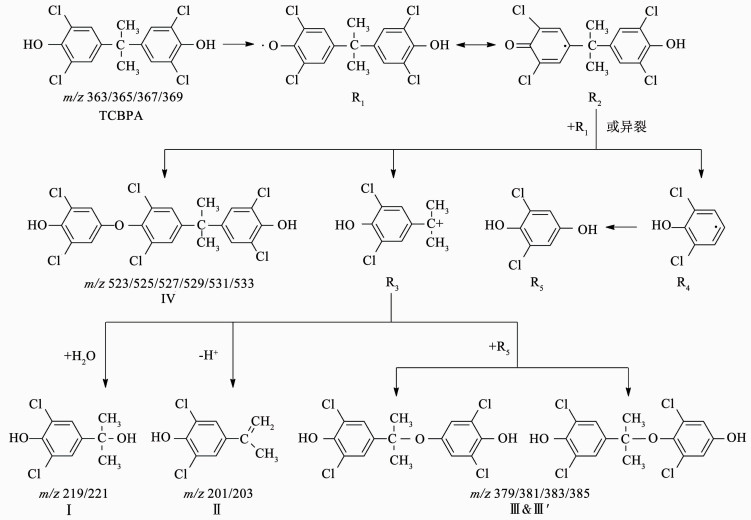
根据图 4、5中产物Ⅰ~Ⅳ的色谱和质谱信息, 推测LC-MS/MS-PIS测得KMnO4氧化降解TCBPA的4个产物的结构式及可能的反应路径见图 6.首先, TCBPA被KMnO4氧化后发生一电子反应形成酚氧自由基R1和R2;然后, 自由基R2经过β裂解为碳正离子R3和自由基R4, 也能够与自由基R1耦合形成产物Ⅳ(聚合产物);自由基R4进一步氧化形成2, 6-二氯-4-羟基苯酚R5;碳正离子R3与H2O反应形成产物Ⅰ(4-(2-羟基异丙基)-2, 6-二氯苯酚)或去掉一个H+形成产物Ⅱ(4-异丙烯-2, 6-二氯苯酚), 也可以与R5发生反应形成产物Ⅲ&Ⅲ′(聚合产物)[10, 20-21].
|
图 6 KMnO4氧化降解TCBPA的反应路径 Figure 6 Proposed reaction scheme for the oxidation of tetrachlorobisphenol A by potassium permanganate |
1) KMnO4氧化降解TCBPA的二级反应速率常数k受pH影响较大, 为40.1~981.7 L/(mol·s), 随着pH的升高先增加而后降低, 在pH=8附近最大, 即越接近TCBPA的pKa(7.5/8.5)时越大.
2) LC-MS/MS-PIS子找母质谱扫描方法测得KMnO4氧化降解TCBPA产生4个主要产物, 质量数(m/z 35)分别为219/221(Ⅰ)、201/203(Ⅱ)、379/381/383/385(Ⅲ&Ⅲ′)、523/525/527/529/531/533(Ⅳ).
3) KMnO4氧化降解TCBPA的反应路径为TCBPA首先发生一电子反应形成酚氧自由基, 并进一步断裂形成碳正离子中间体, 然后反应形成产物4-(2-羟基异丙基)-2, 6-二氯苯酚(Ⅰ)、4-异丙烯-2, 6-二氯苯酚(Ⅱ)和两个聚合产物(Ⅲ&Ⅲ′和Ⅳ).
| [1] |
Environmental Health Criteria, No. 172. Tetrabromobisphenol A andderivatives; International program on chemical safety[R]. Geneva, Switzerland: World Health Organization, 1995. http://www.inchem.org/documents/ehc/ehc/ehc172.htm (accessed August 2007).
|
| [2] |
何敬言, 宋晓红, 于白. 四氯双酚A的合成[J]. 化学工程师, 1990(1): 17-18. DOI:10.16247/j.cnki.23-1171/tq.1990.01.008 |
| [3] |
CHU S, HAFFNER G D, LETCHER R J. Simultaneous determination of tetrabromobisphenol A, tetrachlorobisphenol A, bisphenol A and other halogenated analogues in sediment and sludge by high performance liquid chromatography-electrospray tandem mass spectrometry[J]. J Chromatogr A, 2005, 1097(1/2): 25-32. |
| [4] |
HORIKOSHI S, MIURA T, KAJITANI M, et al. Photodegradation of tetrahalobisphenol-A (X=Cl, Br) flame retardants and delineation of factors affecting the process[J]. Appl Catal B: Environ, 2008, 84: 797-802. DOI:10.1016/j.apcatb.2008.06.023 |
| [5] |
FAN Z, HU J, AN W, et al. Detection and occurrence of chlorinated byproducts of bisphenol A, nonylphenol, and estrogens in drinking water of china: comparison to the parent compounds[J]. Environ Sci Technol, 2013, 47(19): 10841-10850. DOI:10.1021/es401504a |
| [6] |
KITAMURA S, JINNO N, OHTA S, et al. Thyroid hormonal activity of the flame retardants tetrabromobisphenol A and tetrachlorobisphenol A[J]. Biochem Biophys Res Commun, 2002, 293(1): 554-559. |
| [7] |
SUN H, SHEN O, WANG X, et al. Anti-thyroid hormone activity of bisphenol A, tetrabromobisphenol A and tetrachlorobisphenol A in an improved reporter gene assay[J]. Toxicology in Vitro, 2009, 23(5): 950-954. DOI:10.1016/j.tiv.2009.05.004 |
| [8] |
ERIKSSON J, RAHM S, GREEN N, et al. Photochemical transformations of tetrabromobisphenol A and related phenols in water[J]. Chemosphere, 2004, 54: 117-126. DOI:10.1016/S0045-6535(03)00704-5 |
| [9] |
VOORDECKERS J W, FENNELL D E, JONES K, et al. Anaerobic biotransformation of tetrabromobisphenol A, tetrachlorobisphenol A, and bisphenol A in estuarine sediments[J]. Environ Sci Technol, 2002, 36: 696-701. DOI:10.1021/es011081h |
| [10] |
PANG S Y, JIANG J, GAO Y, et al. Oxidation of flame retardant tetrabromobisphenol A by aqueous permanganate: Reaction kinetics, brominated products, and pathways[J]. Environ Sci Technol, 2014, 48: 615-623. DOI:10.1021/es4041094 |
| [11] |
LIN K, LIU W, GAN J. Reaction of tetrabromobisphenol A (TBBPA) with manganese dioxide: Kinetics, products, and pathways[J]. Environ Sci Technol, 2009, 43: 4480-4486. DOI:10.1021/es803622t |
| [12] |
LEE Y, YOON J, VON GUNTEN U. Kinetics of the oxidation of phenols and phenolic endocrine disruptors during water treatment with ferrate (Fe(Ⅵ))[J]. Environ Sci Technol, 2005, 39(22): 8978-8984. DOI:10.1021/es051198w |
| [13] |
庞素艳, 鲁雪婷, 江进, 等. KMnO4氧化降解雌酮反应动力学与氧化产物[J]. 哈尔滨工业大学学报, 2016, 48(2): 38-43. PANG Suyan, LU Xueting, JIANG Jin, et al. Oxidation of estrone by aqueous permanganate: Reaction kinetics and oxidation products[J]. Journal of Harbin Institute of Technology, 2016, 48(2): 38-43. DOI:10.11918/j.issn.0367-6234.2016.02.007 |
| [14] |
庞素艳, 王强, 鲁雪婷, 等. 中间价态锰强化KMnO4氧化降解三氯生[J]. 哈尔滨工业大学学报, 2015, 47(2): 87-91. PANG Suyan, WANG Qiang, LU Xueting, et al. Oxidative removal of triclosan by potassium permanganate enhanced with manganese intermediates[J]. Journal of Harbin Institute of Technology, 2015, 47(2): 87-91. DOI:10.11918/J.issn.0367-6234.2015.02.016 |
| [15] |
ZHANG X, TALLEY J W, BOGGESS B, et al. Fast selective detection of polar brominated disinfection byproducts in drinking water using precursor ion scans[J]. Environ Sci Technol, 2008, 42: 6598-6603. DOI:10.1021/es800855b |
| [16] |
ZHAI H, ZHANG X. Formation and decomposition of new and unknown polar brominated disinfection byproducts during chlorination[J]. Environ Sci Technol, 2011, 45: 2194-2201. DOI:10.1021/es800855b |
| [17] |
PAN Y, ZHANG X. Four groups of new aromatic halogenated disinfection byproducts: Effect of bromide concentration on their formation and speciation in chlorinated drinking water[J]. Environ Sci Technol, 2013, 47: 1265-1273. DOI:10.1021/es303729n |
| [18] |
XIAO F, ZHANG X, ZHAI H, et al. New halogenated disinfection byproducts in swimming pool water and their permeability across skin[J]. Environ Sci Technol, 2012, 46: 7112-7119. DOI:10.1021/es3010656 |
| [19] |
DING G, ZHANG X, YANG M, et al. Formation of new brominated disinfection byproducts during chlorination of saline sewage effluents[J]. Water Res, 2013, 47: 2710-2718. DOI:10.1016/j.watres.2013.02.036 |
| [20] |
LIN K, LIU W, GAN J. Reaction oftetrabromobisphenol A (TBBPA) with manganese dioxide: Kinetics, products, and pathways[J]. Environ Sci Technol, 2009, 43: 4480-4486. DOI:10.1021/es803622t |
| [21] |
FENG Y, COLOSI L M, GA OS, et al. Transformation and removal of tetrabromobisphenol A from water in the presence of natural organic matter via laccase-catalyzed reactions: Reaction rates, products, and pathways[J]. Environ Sci Technol, 2013, 47: 1001-1008. DOI:10.1021/es302680c |
 2018, Vol. 50
2018, Vol. 50


