2. 哈尔滨工业大学 燃烧工程研究所, 哈尔滨 150001;
3. 山东省特种设备检验研究院有限公司, 济南 250101
2. Research Institute of Combustion Engineering, Harbin Institute of Technology, Harbin 150001, China;
3. Shandong Special Equipment Inspection Institute Co., Ltd., Jinan 250101, China
氮氧化物(NOx)是燃煤锅炉和炉窑排放的主要大气污染物之一,它经过一系列的反应过程易形成酸雨、酸雾和光化学烟雾等[1-4]. “十三五”以来,NOx排放标准日益严格,实现NOx低排放愈加重要和急迫.再燃技术被认为是一种清洁高效、具有一定发展潜力的NOx控制技术[5-6].碳氢类(主要为CH4)再燃燃料因不含氮和高NOx还原率的优点,吸引了众多学者从化学反应动力学和工业应用层面对其进行深入研究,提出了许多碳氢类化合物反应机理并应用于NOx减排[7-9].然而,在常被作为再燃燃料的合成气、天然气和沼气中往往存在一种重要的“活跃”组分H2S[10].许多学者在H2S燃烧特性方面展开了实验和数值模拟研究. Chin等[11]实验表明在克劳斯炉中,温度在1 000~1 200 ℃H2S的氧化速率明显快于CH4;Song等[10]在流动反应器通过实验和数值计算提出适用于压力在3~10 MPa范围内CH4/H2S的氧化机理;Gersen等[12]探究了高压下在快速压缩机(RCM)中添加H2S对CH4着火和氧化的影响规律,结果表明添加H2S可加速CH4的氧化,缩短了点火延迟时间. Bongartz等[13]研究了富氧燃烧时,酸性天然气组分对点火延迟及燃烧速率的影响,结果表明H2S浓度的增加对火焰温度及层流燃烧速率影响相对较小,但可大幅度减少点火延迟时间.现有学者研究H2S对点火延迟均为高压条件下,同时在H2S对CH4还原NOx影响方面研究较少.而探究常压下H2S对CH4点火延迟及还原NOx的影响规律,对CH4/H2S在大量常压燃烧设备中的使用及NOx排放控制中具有实用价值.
本文采用化学动力学软件CHEMKIN-PRO中闭式均相0-D (closed homogeneous batch reactor)、柱塞流PFR (Plug Flow Reactor)反应器和leeds combined mechanisms动力学模型,探究H2S对CH4点火延迟及还原NOx的影响规律,结合敏感性和生成率分析揭示H2S影响CH4点火延迟时间及还原NO的深层机制,能够为高效清洁利用CH4/H2S燃料提供一定的参考.
1 数值模型和分析方法 1.1 数值计算模型0-D反应器模型排除了组分输运(对流、扩散)的影响,用于研究CH4/H2S/O2/N2预混气体在绝热定压条件下的点火延迟时间[14].其组分质量分数和温度的控制方程为
| $ \frac{{{\rm{d}}{Y_k}}}{{{\rm{d}}t}} = \frac{{{{\dot \omega }_k}{W_k}}}{\rho }, \quad \frac{{{\rm{d}}T}}{{{\rm{d}}t}} = - \frac{1}{{\rho {c_p}}}\sum\limits_{k = 1}^n {{h_k}} {\dot \omega _k}{W_k}. $ |
式中:ρ为密度,kg/m3;cp为定压比热容,J/(kg·K);hk为组分k的比焓,J/kg;
PFR反应器模型用于模拟绝热封闭系统下的化学反应,其主要控制方程为质量方程:
| $ \rho u \frac{\mathrm{d} A}{\mathrm{d} x}+\rho A \frac{\mathrm{d} u}{\mathrm{d} x}+u A \frac{\mathrm{d} \rho}{\mathrm{d} x}=0. $ |
动量方程:
| $ A \frac{\mathrm{d} p}{\mathrm{d} x}+\rho u A \frac{\mathrm{d} u}{\mathrm{d} x}+\frac{\mathrm{d} F}{\mathrm{d} x}=0. $ |
气体组分方程:
| $ \rho u \mathrm{d} Y_{k} / \mathrm{d} x=W_{k} \dot{\omega}_{k}. $ |
式中:u为气体轴向速度,m/s;A为反应器横截面积,m2;dF/dx=ai·ρu2f/2.
1.2 化学动力学机理CH4/H2S反应涉及碳氢类、含硫物质、含氮物质及中间自由基的相互作用.为准确描述该化学反应,本文采用利兹大学(University of Leeds)提出的Leeds综合机理(Leeds Combined Mechanism)[15],它包含的机理版本为Methane v1.5,NOx v2.0,SOx v5.1,该机理涉及5种元素:C、H、O、N和S,包含78种组分和892个不可逆基元反应;为排除H2S的热力和扩散因素对CH4点火火延迟的影响,在原机理基础上添加组分X,其热力学参数均与H2S相同,它不参与任何化学反应,故H2S和X引起着火延迟的差别只是源于H2S的化学影响[16].
1.3 分析方法敏感性分析(sensitivity analysis,SA)方法能够深入分析组分、基元反应、反应条件等因素对反应参数变化的敏感程度,能够计算出反应参数的变化对整体的影响[17].局部SA的正交表达式[18]如下:
| $ \tilde{S}=\frac{k_{j}}{c_{i}} \frac{\partial c_{i}}{\partial k_{j}}=\frac{\partial \ln c_{i}}{\partial \ln k_{j}}. $ |
式中:
生成率分析(rate of production analysis,ROP)可计算出某基元反应对某种组分的生成及消耗速率的贡献率,可通过追踪组分的连续变化得出所要研究组分的详细转化路径.
1.4 模拟工况过量空气系数λ、点火延迟时间τ和NO还原率ηNO定义为
| $ \begin{aligned} \lambda=\varphi_{0_{2}} /\left(2 \varphi_{\mathrm{CH}_{4}}+1.5 \varphi_{\mathrm{H}_{2} \mathrm{S}}\right) &, \tau=A p^{\alpha} \lambda^{\beta}\left[\mathrm{O}_{2}\right]^{\gamma} \mathrm{e}^{-\frac{E}{\mathrm{R} T}}, \\ \eta_{\mathrm{NO}}=\frac{\varphi_{\mathrm{NO}_{\mathrm{in}}}\varphi_{\mathrm{NO}_{\mathrm{out}}}}{\varphi_{\mathrm{NO}_{\mathrm{in}}}} . \end{aligned} $ |
式中:VX为组分X的体积分数,%;A为指前因子;α、β和γ为对应各项影响因子;φNOin和φNOout分别为反应器入口和出口NO体积分数,10-6.
采用0-D反应器进行预混气点火延迟研究,变量有H2S浓度、过量空气系数、压力和温度,其中H2S和X体积分数之和恒为0.20%.本文着火延迟时间定义为反应开始至OH自由基浓度峰值的时间间隔. 表 1所示为λ=1.0下模拟的工况.
| 表 1 0-D反应器模拟工况(λ=1.0) Tab. 1 Modeling conditions by 0-D reactor (λ=1.0) |
采用PFR反应器探究H2S对CH4/H2S还原NO的影响规律,其结构参数及组分CH4/NO初始浓度与Alzueta等[8]试验条件相同,Wang等[19]通过对比模拟与试验数据,验证了Leeds综合机理的可靠性.该模拟涉及的变量有H2S浓度、反应温度和过量空气系数,表 2所示为λ=0.7下模拟的工况.
| 表 2 PFR反应器模拟工况(λ=0.7) Tab. 2 Modeling conditions by PFR reactor (λ=0.7) |
保持CH4体积分数4.0%不变,选取H2S体积分数为0、0.05%、0.10%和0.20%进行对比,结果如图 1所示.
|
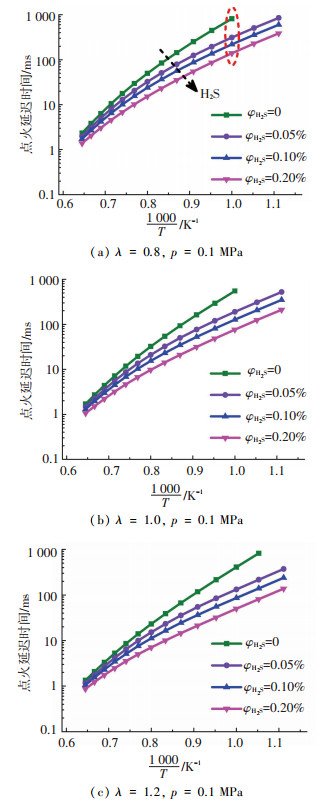
图 1 H2S对CH4/H2S/O2/X/N2预混气点火延迟的影响 Fig. 1 Effect of H2S on the ignition delay of CH4/H2S/O2/X/N2 premixed gas |
由图 1可知,在相同压力和过量空气系数下,随着H2S体积分数的增加,预混气点火延迟时间缩短,且低温下较高温下区别更加明显.以图 1(a)为例,反应初始温度为900和950 K工况下,未添加H2S的预混气未发生着火,而有H2S存在的预混气着火成功,这充分说明了H2S可显著降低预混气的着火温度.反应初始温度为1 000 K、H2S的体积分数为0、0.05%、0.10%和0.20%时,对应的点火延迟时间为550.33、189.52、127.31和76.52 ms;对比H2S=0的工况,对应点火延迟时间降低率为65.56%、76.87%和86.10%.反应初始温度为1 350 K时,对应的点火延迟时间降低率为25.87%、41.75%和60.42%.
在低温下(T=1 000 K)添加体积分数为0.05%的H2S,即可明显缩短点火延迟时间(降低率65.56%);继续增加H2S的浓度虽然可进一步缩短点火延迟时间,但是降幅减小(H2S体积分数为0.20%时,降低率86.10%).在高温下(T=1 350 K),H2S体积分数为0.05%和0.20%的工况,点火延迟时间降低率为25.87%、60.42%.因此,H2S对低温下预混气点火延迟影响作用更加显著;主要由于其他条件相同时,预混气温度越低,所需点火延迟时间越长.该结果与Bongartz等[13]在高压下的研究类似.
为从化学反应动力学机理层面揭示H2S对预混气点火延迟的影响机制,统计分析了H2S对主要活性基团的影响;并结合生成率和敏感性分析,从基团转化路径和敏感性方面进行阐述. 图 2所示为CH4/H2S/O2/X/N2预混气主要分子及基团浓度变化.

|
图 2 CH4/H2S/O2/X/N2预混气中主要分子及基团浓度变化(T=1 000 K, λ=1.0, p=0.1 MPa) Fig. 2 Concentration changes of main molecules and groups in CH4/H2S/O2/X/N2 premixed gas(T=1 000 K, λ=1.0, p=0.1 MPa) |
由图 2(a)可知,添加H2S可显著促进活性基团(H,O,OH,HO2,HO2和H2O2)的产生速率,且H2S迅速参与至反应中,即再次证明点火延迟时间的变化是由于H2S的作用引起的.以H2S体积分数为0.01%的工况为例,阐述H2S对点火延迟时间的影响机制.
基于生成率分析和不同基团反应的时间尺度,反应初期H2S的主要消耗反应为
| $ \mathrm{H}_{2} \mathrm{S}+\mathrm{H} \rightarrow \mathrm{SH}+\mathrm{H}_{2}, \quad(\mathrm{R} 673) $ |
| $ \mathrm{H}_{2} \mathrm{S}+\mathrm{CH}_{3} \rightarrow \mathrm{CH}_{4}+SH.\quad(R841) $ |
R673中R表示Reaction,673代表该反应在机理中的编号,下同.
H2S消耗反应主要生成SH基团,SH基团的主要消耗反应为
| $ \mathrm{SH}+\mathrm{O}_{2} \rightarrow \mathrm{SO}+\mathrm{OH}, \quad(\mathrm{R} 855) $ |
| $ \mathrm{SH}+\mathrm{O}_{2} \rightarrow \mathrm{HSO}+\mathrm{O} . \quad(\mathrm{R} 691) $ |
由图 2(b)可知,H2S反应速率峰值约在40.00 ms处,该工况下点火延迟时间为127.31 ms,而H2S该时刻下已基本反应完全.因此,H2S对点火延迟时间影响是由于其在反应体系中首先生成主要中间组分SH基团(H2S的主要消耗反应对应于SH基团的主要生成反应),该基团与其它分子反应生成了活性自由基OH、H,从而加速了链式反应的进行,缩短了预混气点火延迟时间.
对主控基元反应进行了温度敏感性分析,如图 3所示(注:正值表示促进,负值表示抑制,下同).
|
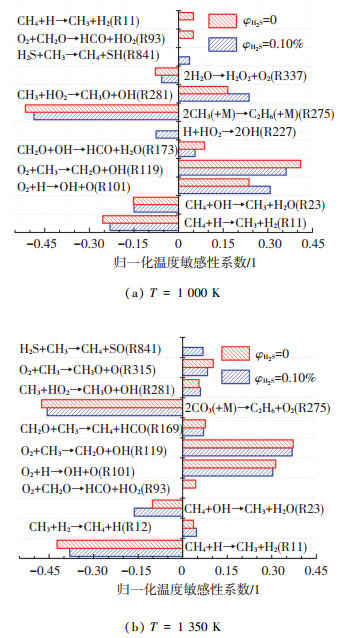
图 3 不同H2S体积分数下主控反应的温度敏感性系数(λ=1.0, p=0.1 MPa) Fig. 3 Temperature sensitivity coefficient of master reaction under different H2S volume fraction (λ=1.0, p=0.1 MPa) |
由图 3(a)可知,在低温下(T=1 000 K)对比未添加H2S工况,主要含硫基元反应R841促进了反应系统的温度上升,对着火具有促进作用;因H2S在点火时刻前基本反应完全,故温度主控反应中未直接体现H2S对系统温升的促进作用.
由3(b)图可知,在高温下(T=1 350 K)含硫组分参与直接促进系统温升的反应为R841.与低温下有所差别是由于反应初始温度的升高使系统能量增大,总体点火延迟时间缩短;同时相比低温工况,H2S消耗速率加快,系统能量的累积(温升)速率取决于H2S的消耗速率.
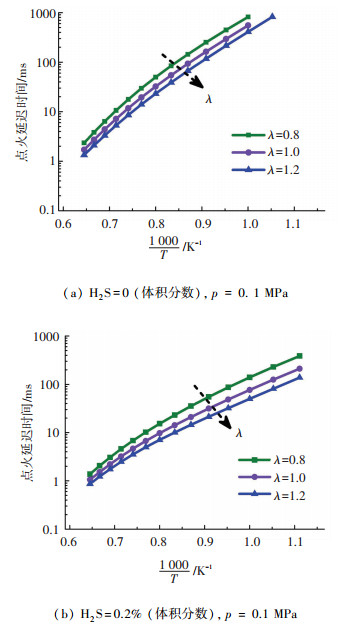
2.2 过量空气系数对预混气点火延迟的影响过量空气系数(λ)将影响预混气中氧气浓度值和含氧基团的变化,选取λ为0.8、1.0和1.2的工况进行对比分析,结果见图 4.由图 4可知,点火延迟时间随着λ增大而减少,H2S的存在进一步缩短点火延迟时间.未添加H2S时,在低温T=1 000 K工况下,λ=0.8、1.0和1.2时的点火延迟时间为818.84、550.33和408.68 ms;高温工况T=1 350 K下为17.68、11.74和8.54 ms.当H2S体积分数为0.20%时,低温T=1 000 K工况下相应点火延迟时间为139.35、76.52和49.96 ms;高温T=1 350 K工况下为6.82、4.64和3.52 ms,分析数据可知,低温工况下点火延迟时间的相对降低率大于高温工况.因此,H2S在低温下对点火延迟的影响较高温下更显著.
|
图 4 过量空气系数对CH4/H2S/O2/X/N2预混气点火延迟的影响 Fig. 4 Effect of excess air coefficient on the ignition delay of CH4/H2S/O2/X/N2 premixed gas |
为揭示λ对预混气点火延迟影响机制,选取H2S体积分数为0和0.10%工况,计算其主控反应的温度敏感性系数,结果如图 5所示.

|
图 5 不同过量空气系数下主控反应的温度敏感性系数(T=1 000 K, p=0.1 MPa) Fig. 5 Temperature sensitivity coefficient of master reaction under different excess air coefficients(T=1 000 K, p=0.1 MPa) |
由图 5(a)可知,反应O2+CH3→CH2O+OH(R119)和O2+H→OH+O(R101)对系统温度提升具有最为明显的促进作用,这两个反应均直接受O2浓度的影响,故λ的增大可提高该反应的速率,缩短点火延迟时间;同时对比不同λ下的反应可知,λ的增大可促进CH4向CH3的转化速率,而CH3直接参与的另一个反应CH3+HO2→CH3O+OH亦对温升有较大影响.由图 5(b)图可知,添加一定浓度的H2S后,促进温升的基元反应差别在H2S+CH3→CH4+SH(R841)上,这是因为H2S可在更低的温度下反应生成活性基团,可为链式反应进行提供链载体,从而促进了整体反应的速率提升,而λ的增加大对该反应具有促进作用.
2.3 压力对预混气点火延迟的影响反应系统压力增大会提高分子碰撞机率,进而提高反应速率.因本文研究压力为常压附近,故在压力对点火延迟时间的研究中取压力p=0.08、0.10和0.12 MPa工况作简单说明,结果如图 6所示.

|
图 6 压力对CH4/H2S/O2/X/N2预混气点火延迟的影响 Fig. 6 Effect of pressure on the ignition delay of CH4/H2S/O2/X/N2 premixed gas |
由图 6(a)可知,在研究压力范围内点火延迟时间差别不大,但预混气点火延迟时间仍呈现随压力的增大而缩短的趋势.尤其当初始温度为950 K时,仅当初始压力为0.12 MPa的工况点火成功.由图 6(b)可知,添加体积分数为0.20%的H2S后,点火延迟时间明显缩短,初始温度为900 K时,3种压力下的预混气均着火成功.在其他条件相同的提前下,添加H2S后不同压力下的点火延迟时间区别增大,而且低温下的点火延迟时间区别大于高温下.这是由于温度升高,反应系统的总能量能量增大,与点火状态所需能量差减少造成的.
2.4 H2S对CH4/H2S还原NO的影响在H2S对CH4/H2S还原NO的研究中,保持NO的体积分数920×10-6不变,对比H2S体积分数0、50×10-6、100×10-6和200×10-6下的反应器出口NO体积分数,结果如图 7所示.
|
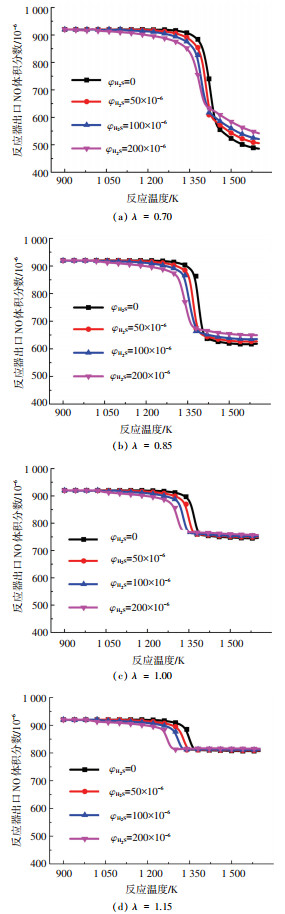
图 7 H2S对CH4/H2S还原NO的影响 Fig. 7 Effect of H2S on NO reduction by CH4/H2S |
由图 7可知,在贫氧(λ=0.70、0.85)至富氧(λ=1.15)气氛变化中,随着H2S浓度的增加,NO参与反应的温度点提前,即H2S降低了还原NO的温度;以反应器出口NO的体积分数降低至850×10-6为例,H2S体积分数为0、50×10-6、100×10-6和200×10-6下,对应的温度约为1 400、1380、1 360和1 340 K.但同时由图 7可知,随着H2S浓度增加,NO的还原率降低.以λ=0.70、反应温度为1 500 K的工况为例,H2S体积分数为0、50×10-6、100×10-6和200×10-6时,对应的NO还原率分别为43.2%、41.0%、39.1%和36.5%,H2S在贫氧气氛中对NO还原率影响较大;当λ=1.15时,相应的NO还原率为12.2%、12.0%、11.8%和11.3%,即在富氧环境中,H2S中对NO还原率影响较小.
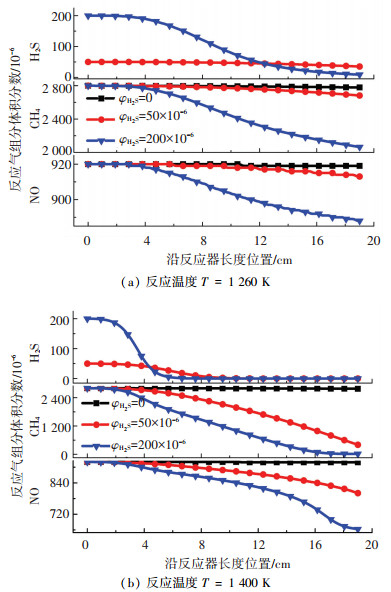
CH4/H2S还原NO实质在于反应中生成的CH3、CH2和CH等还原性基团对NO的还原作用,而CHi基团来源主要为CH4,因此CH4的起始反应温度和反应速率在一定程度上决定了CHi还原NO的起始温度和效率;而H2S降低了NO的还原温度,即可说明H2S可降低CH4反应温度.为验证该结论,统计分析了在工况λ=0.70,T=1 260 K和T=1 400 K下,主要组分CH4、H2S和NO沿反应器长度方向的浓度变化,如图 8所示.
|
图 8 反应气组分浓度沿反应器长度方向变化(λ=0.70) Fig. 8 Variation of concentration of reaction gas components along reactor length (λ = 0.70) |
由图 8可知,在温度T=1 260 K下,当H2S体积分数为0时,CH4几乎未反应,故NO浓度未发生变化;当H2S体积分数为50×10-6时,CH4浓度稍有降低,NO还原率不足1%;但当H2S体积分数提高至200×10-6时,CH4浓度在约4 cm处开始降低,这说明H2S的存在降低了还原NO所需的温度,此时NO的还原率约为3.5%.为进一步验证该结论,统计了温度为1 400 K下的数据.由图 8(b)图可知,温度的升高提高了总体反应速率,但未添加H2S时,CH4仍未参与反应;当H2S体积分数为50×10-6和200×10-6时,反应结束时CH4体积分数为403×10-6和11×10-6,对应NO的还原率为12.9%和27.9%,这说明由CH4生成的还原基团未完全与NO反应.综上可知,H2S可降低CH4的反应温度,进而降低其还原NO的温度,有利于实现低温下对NO的还原.
3 结论1) H2S可促进预混气活性基团的生成速率,促使链式反应的进行,缩短其点火延迟时间,且在低温下的影响作用更加明显;H2S主要消耗路径为H2S+H→SH+H2和H2S+CH3→CH4+SH,反应生成的SH基团主要消耗路径为SH+O2→HSO+O.
2) 预混气点火延迟时间随着过量空气系数的增大而减少;反应O2+CH3→CH2O+OH和O2+H→OH+O对系统温升具有较大的温度敏感性,过量空气系数促进上述反应以缩短点火延迟时间.压力增加亦有利于缩短点火延迟时间.
3) H2S可降低CH4/H2S还原NO的温度,主要由于H2S降低了CH4的反应温度,使还原性CHi基团在较低温度下产生;但同时H2S,在一定程度上降低了NO的还原效率,且在贫氧气氛中的影响更为显著.
| [1] |
LIU C, HUI S, ZHANG X, et al. Influence of type of burner on NO emissions for pulverized coal preheating method[J]. Applied Thermal Engineering, 2015, 85: 278. DOI:10.1016/j.applthermaleng.2015.03.081 |
| [2] |
LIU C, HUI S, PAN S, et al. The influence of air distribution on gas-fired coal preheating method for NO emissions reduction[J]. Fuel, 2015, 139: 206. DOI:10.1016/j.fuel.2014.08.068 |
| [3] |
SHU Yun, WANG Hongchang, ZHU Jinwei, et al. An experimental study of heterogeneous NO reduction by biomass reburning[J]. Fuel Processing Technology, 2015, 132: 111. DOI:10.1016/j.fuproc.2014.12.039 |
| [4] |
ZHAO Jie, WANG Qingcheng, YU Lihui, et al. Influence of the biogas reburning for reducing nitric oxide emissions in an alundum-tube reactor[J]. Atmospheric Environment, 2016, 132: 290. DOI:10.1016/j.atmosenv.2016.03.004 |
| [5] |
SU Sheng, XIANG Jun, SUN Lushi, et al. Application of gaseous fuel reburning for controlling nitric oxide emissions in boilers[J]. Fuel Processing Technology, 2009, 90(3): 396. DOI:10.1016/j.fuproc.2008.10.011 |
| [6] |
SMOOT L D, HILL S C, XU H. NOx control through reburning[J]. Progress in Energy and Combustion Science, 1998, 24(5): 385. DOI:10.1016/S0360-1285(97)00022-1 |
| [7] |
陈宝明, 张忠孝, 毕德贵, 等. 天然气再燃降低NOx排放的热态工业试验研究[J]. 热能动力工程, 2003, 23(1): 113. CHEN Baoming, ZHANG Zhongxiao, BI Degui, et al. Hot-state industrial experimental study of the reburning of natural gas to reduce NOx emissions[J]. Proceedings of the CSEE, 2003, 23(10): 204. DOI:10.16146/j.cnki.rndlgc.2015.01.030 |
| [8] |
ALZUETA M U, GLARBORG P, DAM-JOHANSEN K. Low temperature interactions between hydrocarbons and nitric oxide: an experimental study[J]. Combustion and Flame, 1997, 109(1/2): 25. DOI:10.1016/S0010-2180(96)00146-0 |
| [9] |
GLARBORG P, ALZUETA M U, DAM-JOHANSEN K, et al. Kinetic modeling of hydrocarbon/nitric oxide interactions in a flow reactor[J]. Combustion and Flame, 1998, 115(1/2): 1. DOI:10.1016/S0010-2180(97)00359-3 |
| [10] |
SONG Y, HASHEMI H, CHRISTENSEN J M, et al. An exploratory flow reactor study of H2S oxidation at 30-100 bar[J]. International Journal of Chemical Kinetics, 2017, 49(1): 37. DOI:10.1002/kin.21055 |
| [11] |
CHIN H S F, KARAN K, MEHROTRA A K, et al. The fate of methane in a claus plant reaction furnace[J]. Canadian Journal of Chemical Engineering, 2010, 79(4): 482. DOI:10.1002/cjce.5450790404 |
| [12] |
GERSEN S, ESSEN M V, DARMEVEIL H, et al. Experimental and modeling investigation of the effect of H2S addition to methane on the ignition and oxidation at high pressures[J]. Energy & Fuels, 2016, 31(3): 2175. DOI:10.1021/acs.energyfuels.6b02140 |
| [13] |
BONGARTZ D, GHONIEM A F. Impact of sour gas composition on ignition delay and burning velocity in air and oxy-fuel combustion[J]. Combustion and Flame, 2015, 162(7): 2749. DOI:10.1016/j.combustflame.2015.04.014 |
| [14] |
CHEN Z, JU Y. Theoretical analysis of the evolution from ignition kernel to flame ball and planar flame[J]. Combustion Theory and Modelling, 2007, 11(3): 427. DOI:10.1080/13647830600999850 |
| [15] |
PILL M J, TURANYI T, HUGHES K J. Combined mechanisms, Release 3[EB/OL]. (2004-10-18)[2018-9-21].http://respecth.hu/.html
|
| [16] |
TU Yaojie, SU Kai, LIU Hao, et al. Physical and chemical effects of CO2 addition on CH4/H2 flames on a Jet in hot coflow (JHC) burner[J]. Energy & Fuels, 2016, 30(2): 1390. DOI:10.1021/acs.energyfuels.5b02499 |
| [17] |
TURANY T, BERCES T, VAJDA S. Reaction rate analysis of complex kinetic systems[J]. International Journal of Chemical Kinetics, 1989, 21(2): 83. DOI:10.1002/kin.550210203 |
| [18] |
钱琳.煤气再燃还原氮氧化物化学反应动力学的研究[D].哈尔滨: 哈尔滨工业大学, 2007 QIAN Lin. Chemical kinetics of NOx reduction by reburning with coal-gas[D]. Harbin: Harbin Institute of Technology, 2007 http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D447774 |
| [19] |
WANG Xuebin, TAN Houzhang, NIU Yanqing, et al. Kinetic investigation of the SO2 influence on NO reduction processes during methane reburning[J]. Asia-Pacific Journal of Chemical Engineering, 2010, 5(6): 902. DOI:10.1002/apj.420 |
 2019, Vol. 51
2019, Vol. 51


