2. 哈尔滨供水集团有限责任公司,哈尔滨 150001
2. Harbin Water Supply Group Co., Ltd., Harbin 150001, China
目前,国内外净水厂普遍采用的常规净水工艺是混凝—沉淀—过滤—液氯消毒[1].液氯消毒不仅能够有效杀死水中存在的细菌、原生动物等微生物,同时在管网末端还能残存一定量的余氯,达到持续消毒的目的;但由于水厂中液氯消毒工艺的应用,导致其极易与水中的天然有机物,如腐殖酸、富里酸等生成具有“三致”毒性的消毒副产物(DBPs),严重危及人类的身体健康[2-4].而针对饮用水中DBPs的去除,主要有3种途径:从源头去除水中DBPs前体物;末端降解;更换新型消毒剂[5].
对于位于中国东北地区天然原始林区内的水库,由于水源地上游面积广阔,森林植被茂盛,使得这些水库水源中富含天然有机物,即含有大量DBPs前体物.因此,净水厂常规处理工艺,甚至强化混凝等新型工艺方法,并不能从根本上去除饮用水中的微量甚至痕量DBPs[6-7].末端处理方法,如高级氧化工艺中的UV-O3、UV-TiO2、微波等方法,能够产生大量具有强氧化作用的自由基,但会间接增加净水厂的运行能耗和成本,且目前只是处于实验室研究阶段[8-9].而更换新型消毒剂,如氯胺、ClO2、O3等[10-12],就目前国内外净水厂发展现状而言,是经济有效的措施手段.
针对中国北方寒冷地区含有较高天然有机物的湖库型水源水,在前期研究基础上[13],通过液氯生产性实验确定净水厂出水中检测到的DBPs分布情况,以此为依据,研究对比次氯酸钠消毒和氯胺消毒对饮用水中DBPs的控制情况,以期为富含天然有机物水源水净水厂消毒工艺的改造提供相关参考.
1 实验 1.1 主要试剂及仪器根据实验要求,包括检测、分析等需要使用的主要试剂、药品有:三氯乙醛标准品,百灵威科技有限公司;三氯甲烷标准品,百灵威科技有限公司;三氯乙酸标准品,百灵威科技有限公司;余氯试剂包标准品,哈希公司(美国);总氯试剂包标准品,哈希公司(美国);甲基叔丁基醚,色谱纯,上海安谱科学仪器有限公司;甲醇,色谱纯,上海安谱科学仪器有限公司.所有试剂均直接使用,未进一步做纯化处理.实验用水均由Millipore Milli-Q纯水系统制备(电阻率≥18.2 MΩ·cm).需要用到的玻璃器皿在使用前超声洗涤15 min,之后用自来水冲洗,并用超纯水清洗3次,随后在130 ℃烘干至少24 h.
实验中用到的主要仪器设备有超高效液相色谱,美国Waters;气相色谱(6890B),美国安捷伦;紫外分光光度计(UV-1800),SHIMADZU公司;余氯和总氯便携检测仪(PCII),美国HACH;数控超声波清洗器(KQ-500DB),昆山超声仪器有限公司;三维荧光光谱仪(FP-6500),日本JASCO公司等.
1.2 主要指标分析方法三氯甲烷:采用Agilent GC6890型气相色谱,色谱柱型号为DB-624,色谱柱尺寸为30 m×0.25 mm× 1.4 m.测试过程采用分流进样(10: 1).进样量为1 mL,进样口温度为200 ℃,检测器温度为250 ℃,空气流量控制在60.0 mL/min,氢气流量保持2.0 mL/min,以高纯氮气作为载气,流量为30.0 mL/min.方法检出限为0.3 μg/L,定量限为1 μg/L.
三氯乙酸:采用Agilent GC6890A型气相色谱,色谱柱型号为DB-1702,尺寸为30 m×0.25 mm×0.25 m毛细管柱.测试过程采用分流进样(5: 1).进样量为1 μL,检测器温度为300 ℃,空气流量控制在60.0 mL/min,氢气流量保持2.0 mL/min,以高纯氮气作为载气,尾吹流量为70.0 mL/min.方法检出限为1.08 μg/L,定量限为3.6 μg/L.
三氯乙醛:采用Agilent GC6890,色谱柱型号为HP-5,色谱柱尺寸为30 mm×0.32 mm×0.25 m毛细管柱.测试过程采用分流进样(5: 1).进样量为1 mL,检测器温度为300 ℃,以高纯氮气作为载气,尾吹流量为60.0 mL/min.方法检出限为1 μg/L,定量限为3.3 μg/L.
余氯:采用DPD分光光度法,吸取10 mL水样放置于10 mL比色皿当中,加入0.5 mL磷酸缓冲溶液和0.5 mL DPD溶液,在波长为515 nm条件下,以纯水作为参比,测得吸光度值.
总氯:采用DPD分光光度法,吸取10 mL水样放置于10 mL比色皿当中,加入0.5 mL磷酸缓冲溶液和0.5 mL DPD溶液,再加入0.1 mg KI晶体后,在波长为515 nm条件下,以纯水作为参比,测得吸光度值.
三维荧光光谱法:采用日本Jasco公司的FP-6500荧光分光光度计,设定温度为20 ℃.测试中,在分析样品前应使仪器手动归零,荧光激发光波长变化范围为220~450 nm,激发波长间隔为5 nm,同时,发射波长变化范围为220~600 nm,发射波长间隔为2 nm,设定仪器的扫描速率为2 000 nm/min.
1.3 实验方案采用东北寒冷地区水库型水源水,首先对净水厂水源水进行水质分析,根据液氯消毒后出厂水确定处理出水消毒副产物类别;采用净水厂滤池出水,进行次氯酸钠和氯胺消毒实验,并对比消毒效果.通过改变氯胺投加比例及投加次序,寻找最佳消毒方案,并对比分析3种消毒方式的出水效果.
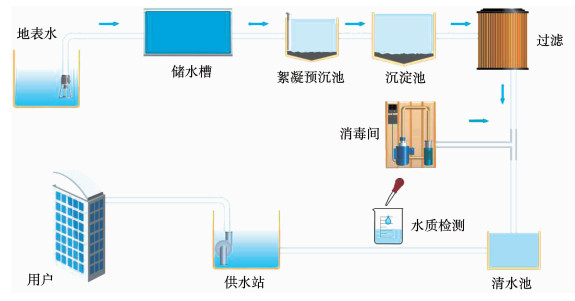
1.4 水厂概况水厂供水能力为90万t/d,采用常规净水处理工艺,如图 1所示.
|
图 1 常规净水处理工艺流程 Fig. 1 Flow chart of conventional water treatment process |
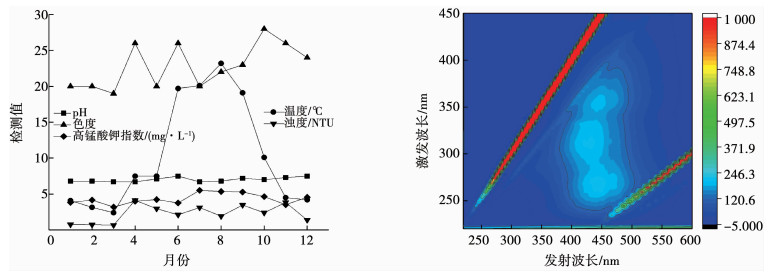
研究中监测了磨盘山水库2017年水源水的pH、温度、色度、浑浊度和高锰酸盐指数(CODMn)等水质指标,结果如图 2所示.可以看出,磨盘山水库水源水属于中性偏酸性,具有低温、低浊、高色度和高CODMn的特点,相比其他净水厂,增加了水源水的净化处理难度.经过图 1所示净化工艺(液氯消毒)处理后,水源水的pH、温度、色度、浑浊度和高锰酸盐指数均能达到《生活饮用水卫生标准》(GB5749—2006)规定的限值,但三氯乙醛水质指标明显超标,对居民饮水安全存在威胁,如表 1所示.为降低饮用水中消毒副产物质量浓度,保证饮用水安全,对比研究了次氯酸钠和氯胺消毒方法.
|
图 2 2017年水库原水水质及三维荧光图 Fig. 2 Original water quality and 3D fluorescence of the reservoir in 2017 |
| 表 1 典型滤后水水质 Tab. 1 Statistical list of typical water quality after filtration |
采用三维荧光光谱仪对磨盘山水库水源水进行检测分析.三维荧光光谱中的横纵坐标分别为激发波长和发射波长,图中等高线的峰值代表对应激发波长和发射波长下的荧光强度大小.有机物不同,其荧光基团种类也不同,在荧光光谱图的荧光峰中所对应的激发波长、发射波长以及应光强度也不同,检测结果如图 2所示.可以看出,磨盘山水库水源水的三维荧光光谱图中有3个明显的特征峰,A峰的激发波长(λex)/发射波长(λem)位于(240~260)/ (400~450)nm,B峰位于(300~330)/(400~440)nm,C峰位于(340~370)/(420~460) nm.A峰属于Region Ⅲ区域,为富里酸类物质,B、C峰属于RegionⅤ区域,为腐殖酸类物质,由此可说明富里酸和腐殖酸为磨盘山水库中天然有机物的主要组分[13].
此外,三维荧光光谱图中荧光强度的大小与有机物质量浓度的大小呈正相关关系.比较A、B和C峰可知,B和C峰的峰强大于A峰,由此可知磨盘山水库中的天然有机物组分主要是富里酸与大分子的腐殖酸,且腐殖酸所占的比重较大.
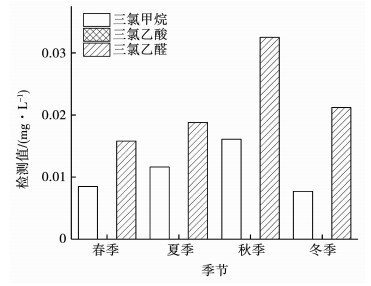
2.2 液氯消毒对消毒副产物生成的影响针对磨盘山水库原水,为保证管网末梢余氯满足>0.05 mg/L,采用2 mg/L液氯进行消毒,并按照《生活饮用水卫生标准》(GB5749—2006)的要求,定期对出厂水进行检测.卤代消毒副产物中,仅三氯乙醛有明显检出,且质量浓度逐年升高.水厂于2015年共计检测三氯乙醛25次,最大值为0.014 mg/L,最小值为0.004 mg/L,平均值为0.008 mg/L;2016年共计检测三氯乙醛49次,最大值为0.027 mg/L,最小值为0.008 mg/L,平均值为0.016 mg/L;2017年共计检测三氯乙醛45次,最大值为0.039 mg/L,最小值为0.009 mg/L,平均值为0.020 mg/L,其余消毒副产物及微生物学指标均符合国标要求.其中三氯甲烷、三氯乙醛和三氯乙酸统计情况如图 3所示.
|
图 3 出厂水中液氯消毒副产物生成情况 Fig. 3 Generation of disinfection by-products of liquid chlorine in finished water |
根据《生活饮用水卫生标准》(GB5749—2006),出厂水中三氯甲烷质量浓度<0.06 mg/L,三氯乙酸质量浓度<0.1 mg/L,三氯乙醛质量浓度<0.01 mg/L.通过图 3可以看出,三氯甲烷和三氯乙酸质量浓度均未超标,三氯乙醛质量浓度均超标,且在寒冷季节检测值明显较高.而其他消毒副产物及微生物学指标质量浓度均小于仪器设备检出限值.因此,将以上3种消毒副产物作为实验过程中的主要检测指标.
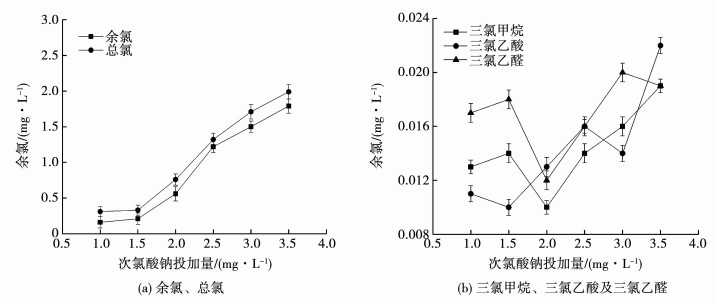
2.3 次氯酸钠消毒实验以净水厂滤后水为对象,在滤后水中依次投加质量浓度为1.0,1.5,2.0,2.5,3.0,3.5 mg/L的次氯酸钠,避光消毒0.5 h后,取样加入硫代硫酸钠保存并进行检测.检测指标为三氯甲烷、三氯乙醛、三氯乙酸、余氯和总氯,结果如图 4所示.可以看出,向净水厂滤后水中投加不同质量浓度的次氯酸钠,水中总氯和余氯随投加质量浓度增加而增加.当次氯酸钠投加质量浓度为2 mg/L时,出水余氯和总氯质量浓度能够达到标准要求,同时,在管网中也能起到一定程度的杀菌效果.此外,实验过程中,细菌总数和总大肠菌群指标均未检出,这也进一步说明次氯酸钠的杀菌效果明显.从图 4还可以看出,三氯甲烷、三氯乙醛和三氯乙酸的变化与液氯的消毒效果基本一致,其中检测出三氯乙醛均超标.当次氯酸钠投加量为2 mg/L时,3种消毒副产物的质量浓度均比较低,能够有效保证饮用水安全.
|
图 4 次氯酸钠消毒实验结果 Fig. 4 Results of disinfection test by sodium hypochlorite |
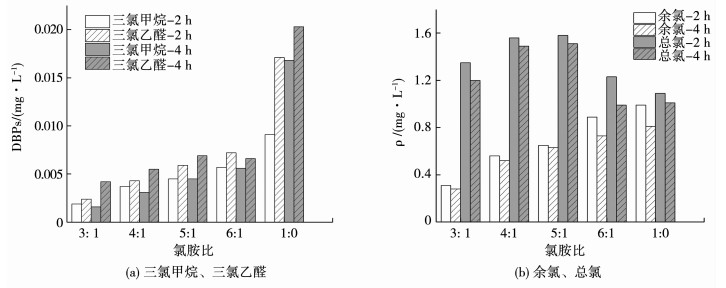
采用净水厂滤池出水,进行氯胺消毒实验,并分别研究3种氯胺投加顺序的消毒效果.分别为先投加硫酸铵后加次氯酸钠、同时投加次氯酸钠和硫酸铵以及先投加次氯酸钠后投加硫酸铵.根据待测水本底氨氮值调整氯胺投加量,使得次氯酸钠与硫酸铵投加比分别为1: 0(2 mg/L: 0)、6: 1(2 mg/L: 0.29 mg/L)、5: 1(2 mg/L: 0.36 mg/L)、4: 1(2 mg/L:0.46 mg/L)和3: 1(2 mg/L: 0.63 mg/L),然后分别调整不同氯胺投加顺序,同时设定消毒接触时间为2和4 h,并测定水样总氯、余氯和消毒副产物三氯甲烷、三氯乙醛、三氯乙酸的质量浓度.研究消毒剂随时间变化,对比氯胺消毒和氯消毒的剩余总氯随时间变化.其中先氨后氯消毒方式为:投氨点模拟在沉淀池出水后端,经过混合过滤,投氯点模拟在滤池出水后端.其中,氯的投加量为2 mg/L,沉淀池出水本底氨氮质量浓度为0.04 mg/L,实验通过调整氯胺比例来调整硫酸铵的投加量,测得结果如图 5所示.
|
图 5 先氨后氯消毒出水检测结果 Fig. 5 Results of disinfection test by ammonia and then chlorine |
氯胺消毒方式为:对滤池出水同时投加氯胺,氯的投加量为2 mg/L,通过调整氯胺比例调整氨投加量,检测结果如图 6所示.

|
图 6 同时氯胺消毒出水检测数据 Fig. 6 Results of disinfection test by chlorine and ammonia simultaneously |
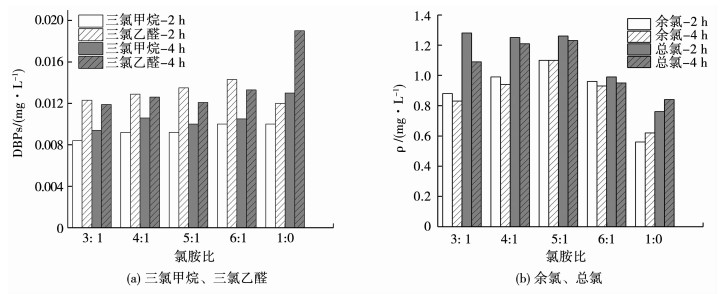
先氯后胺消毒方式:取磨盘山滤池出水进行先氯后氨消毒,投氯点模拟在沉淀池出水后端,经过混合过滤,投氨点模拟在滤池出水后端.氯的投加量为2 mg/L,磨盘山滤池出水氨氮质量浓度为0.03 mg/L,通过调整氯胺比例来调整氨投加量,检测结果如图 7所示.
|
图 7 先氯后胺消毒出水检测数据 Fig. 7 Results of disinfection test by chlorine and then ammonia |
通过以上实验分析,发现3种氯胺消毒方式出水中三氯乙酸均未检出.且三氯甲烷、三氯乙醛等各项消毒指标检测质量浓度值均低于《生活饮用水卫生标准》(GB5749—2006)规定的限值,相比单纯液氯和次氯酸钠消毒,氯胺消毒表现出良好的消毒效果,能够有效降低水中消毒副产物的质量浓度.
由图 5~7可以看出,氯胺消毒在满足国标的前提下,随着氯胺投加比例的增加,即氨质量浓度的不断降低,检测到出水中三氯乙醛、三氯甲烷和余氯的值均不断升高.这是由于在次氯酸钠投加量一定的情况下,氨质量浓度越低,表明水中游离氯越高,从而增加了三氯乙醛和三氯甲烷的生成风险.因而水中存在一定量的一氯胺能够有效减少游离氯离子与有机天然物质形成DBPs的可能性.此外,随着消毒时间的增加,也能有效降低消毒副产物的质量浓度.水中三氯甲烷的质量浓度在不断升高,而三氯乙醛、余氯和总氯则不断降低.说明适当延长消毒时间有助于降低水中三氯乙醛的质量浓度[14].
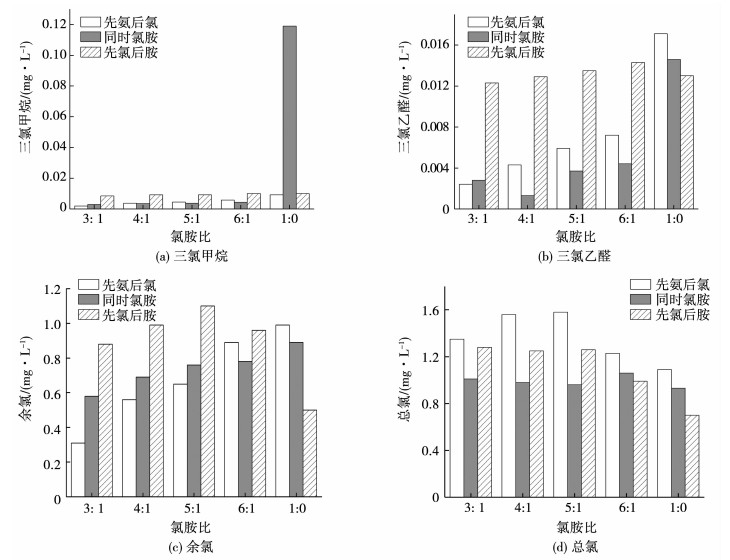
对比图 8 3种氯胺投加方式的消毒效果可知,同时投加次氯酸钠和硫酸铵的方式,出水中消毒副产物的质量浓度相对较低,且余氯质量浓度适当,更能够在管网末梢起到持续消毒的效果;纵观不同投加比例均衡考虑,投加比例为4: 1(2 mg/L: 0.46 mg/L)时,不仅能够有效降低出水中消毒副产物的质量浓度,使管网末端的余氯持续时间长;还能使水中保证一定比例的一氯胺,有效降低水中游离氯离子与天然有机物形成DBPs的可能性.
|
图 8 不同氯胺投加比对消毒指标的影响 Fig. 8 Effects of different dosages of chloramine on disinfection indexes |
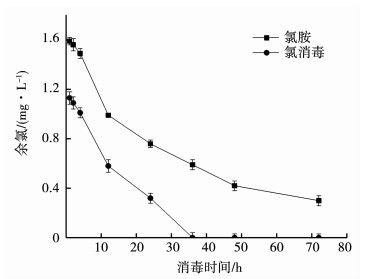
采用同时投加次氯酸钠和硫酸铵的方式进行氯胺消毒,氯胺比4: 1,氯投加量为2 mg/L,氨的投加量为0.46 mg/L.对比研究氯胺消毒与氯消毒方式中出厂水中余氯的变化,结果如图 9所示.可以看出,氯胺消毒后消毒剂余量在相同时间内明显高于氯消毒剂余量.液氯在消毒36 h后即降为0,而氯胺在消毒70 h后仍然保持较高的余氯质量浓度,且能达到国标的要求,消毒效果持续时间更长,相对更加稳定.综合消毒副产物质量浓度变化及出厂水中余氯的变化情况,可见氯胺消毒能够表现出更佳的消毒效果,有效保证净水厂的水质安全.
|
图 9 不同消毒方式余氯变化 Fig. 9 Changes of residual chlorine in different disinfection methods |
1) 常规水处理工艺下,液氯和次氯酸钠消毒导致以三氯乙醛为代表的DBPs超标.
2) 氯胺消毒方式可有效降低三氯乙醛的生成,且稳定达标.
3) 该水厂改用氯胺消毒时,即次氯酸钠和硫酸铵最佳投量比为4: 1(2 mg/L: 0.46 mg/L)时,消毒效果最佳,三氯乙醛、三氯乙酸、三氯甲烷均符合国标限值要求,尤其是三氯乙醛和三氯甲烷生成量明显降低.
| [1] |
AMBASHTA R D, SILLANPAA M. Water purification using magnetic assistance: A review[J]. Journal of Hazardous Materials, 2010, 180(1/2/3): 38. DOI:10.1016/j.jhazmat.2010.04.105 |
| [2] |
GAMAGE S M, SATHASIVAN A. A review: Potential and challenges of biologically activated carbon to remove natural organic matter in drinking water purification process[J]. Chemosphere, 2017, 167: 120. DOI:10.1016/j.chemosphere.2016.09.097 |
| [3] |
HOW Z T, KRISTIANA I, BUSETTI F, et al. Organic chloramines in chlorine-based disinfected water systems: A critical review[J]. Journal of Environmental Sciences, 2017, 58: 2. DOI:10.1016/j.jes.2017.05.025 |
| [4] |
ARMBRUSTER D, HAPPEL O, SCHEURER M, et al. Emerging nitrogenous disinfection byproducts: Transformation of the antidiabetic drug metformin during chlorine disinfection of water[J]. Water Research, 2015, 79: 104. DOI:10.1016/j.watres.2015.04.020 |
| [5] |
YANG Y, LU J, YU H, et al. Characteristics of disinfection by-products precursors removal from micro-polluted water by constructed wetlands[J]. Ecological Engineering, 2016, 93: 262. DOI:10.1016/j.ecoleng.2016.05.022 |
| [6] |
FU J, LEE W, COLEMAN C, et al. Removal of disinfection byproduct (DBP) precursors in water by two-stage biofiltration treatment[J]. Water Research, 2017, 123: 224. DOI:10.1016/j.watres.2017.06.073 |
| [7] |
牛志广, 孙媛媛, 张颖. 预氯化及常规工艺对消毒副产物的影响[J]. 环境工程学报, 2015, 9(11): 5142. NIU Zhiguang, SUN Yuanyuan, ZHANG Ying. Effects of pre-chlorination and conventional process on disinfection by-products[J]. Chinese Journal of Environmental Engineering, 2015, 9(11): 5142. |
| [8] |
SILLANPAA M, NCIBI M C, MATIAINEN A. Advanced oxidation processes for the removal of natural organic matter from drinking water sources: A comprehensive review[J]. Journal of Environmental Management, 2018, 208: 56. DOI:10.1016/j.jenvman.2017.12.009 |
| [9] |
LI M, XU B, LIUNGAI Z, et al. The removal of estrogenic activity with UV/chlorine technology and identification of novel estrogenic disinfection by-products[J]. Journal of Hazardous Materials, 2016, 307: 119. DOI:10.1016/j.jhazmat.2016.01.003 |
| [10] |
焦中志, 陈忠林, 陈杰, 等. 氯胺消毒对消毒副产物的控制研究[J]. 哈尔滨工业大学学报, 2005, 37(11): 1486. JIAO Zhongzhi, CHEN Zhonglin, CHEN Jie, et al. Control of disinfection by-products in drinking water by mono-chloramine disinfectant[J]. Journal of Harbin Institute of Technology, 2005, 37(11): 1486. DOI:10.3321/j.issn:0367-6234.2005.11.009 |
| [11] |
崔红军, 吴东升, 宋思怡, 等. 自来水厂采用次氯酸钠替代液氯消毒的可行性研究[J]. 中国给水排水, 2016, 32(19): 58. CUI Hongjun, WU Dongsheng, SONG Siyi, et al. Feasibility analysis of sodium hypochlorite instead of liquid chlorine in waterworks[J]. China Water & Wastewater, 2016, 32(19): 58. |
| [12] |
LIM M Y, KIM J, KO G. Disinfection kinetics of murine norovirus using chlorine and chlorine dioxide[J]. Water Research, 2010, 44(10): 3243. DOI:10.1016/j.watres.2010.03.003 |
| [13] |
XU T F, CUI C W, MA C. Color composition in a water reservoir and DBPs formation following coagulation and chlorination during its conventional water treatment in Northeast of China[J]. Desalination and Water Treatment, 2014, 54: 1375. DOI:10.1080/19443994.2014.914448 |
| [14] |
MCKAY G, SJELIN B, CHAGNON M, et al. Kinetic study of the reactions between chloramine disinfectants and hydrogen peroxide: Temperature dependence and reaction mechanism[J]. Chemosphere, 2013, 92(11): 1417. DOI:10.1016/j.chemosphere.2013.03.045 |
 2019, Vol. 51
2019, Vol. 51


