随着水污染和水资源短缺形势的加剧,分散式饮用水安全问题日益突出.受能耗、药耗、操作运维、规模化和长效评价机制的影响,常规水处理工艺难以应对复杂的分散式供水形势[1].超滤(Ultrafiltration)能够有效地截留水中的胶体、颗粒物和致病微生物(如细菌、病毒、“两虫”),且便于集成化和自动化管理,在分散式供水系统中具有得天独厚的应用优势[2].然而,常规超滤工艺频繁地采用反冲洗和化学清洗来控制膜污染,导致其在实际应用中存在运行能耗高、操作维护复杂、附属设备多等不足[1].因此,进一步降低超滤工艺的能耗、减少操作和运维、提升净水效能,是面向分散式供水超滤净水技术的重要改进方向.
研究人员围绕水质保障、节能降耗和简化运维等问题,研发了新型重力驱动膜过滤工艺(即GDM工艺),其长期运行通量可保持稳定,不需采用水力反冲洗、错流、曝气和化学清洗来控制膜污染,且所需的驱动压力较常规超滤工艺大幅降低[3-4].因此,GDM工艺具有无药剂、操作简单、低能耗、低维护、所需配套设备少等优点,可在无人值守条件下长期稳定运行[5].此外,GDM工艺长期运行其膜面形成的生物滤饼层对水中的污染物起到预过滤效应,既可有效地提高污染物去除效能,又能降低污染物在膜孔中的沉积风险,缓解膜污染[6].
本研究系统考察了GDM工艺在不同原水类型、膜组件及工艺条件下长期运行的通量稳定性,探究生物滤饼层强化除污染机制以及GDM工艺效能提升路径,解析GDM工艺通量稳定机制,为GDM技术在分散式供水系统中的推广应用提供理论和技术支撑.
1 实验 1.1 原水水质特性分析原水类型包括江水、河水、水库水和模拟配水,具体水质信息如表 1所示.
| 表 1 实验用原水水质信息 Tab. 1 Information of raw water quality |
GDM小试实验装置如图 1所示,其主要由原水箱、UF组件、集水瓶3部分组成,原水箱与UF组件通过硅胶管连接,原水在重力作用下流入UF组件中进行过滤处理(有效过滤膜面积均为0.005 65 m2),膜出水进入集水瓶中,通过测量单位时间内集水瓶中的产水量计算膜通量.GDM采用连续过滤模式,不采用反冲洗和化学清洗控制膜污染.为提高GDM过滤效能,研发了预处理+GDM联用工艺(如图 1(b)所示),即在原水箱和UF组件之间增加了预过滤装置,其余参数与GDM工艺一致.此外,为了探究不同参数对GDM通量稳定性的影响,构建了系列GDM工艺(表 2),膜材料信息如表 3所示.

|
图 1 GDM工艺流程图 Fig. 1 Flow chart of GDM process |
| 表 2 各GDM实验条件 Tab. 2 Summary of GDM process parameters |

|
图 2 不同条件下GDM长期运行的通量变化 Fig. 2 Flux variation of long-term GDM filtration under different conditions |
| 表 3 实验用超滤和微滤性质 Tab. 3 Information of ultrafiltration and microfiltration membranes |
实验中定期监测原水和出水水质,并分析膜面生物滤饼层的结构和生化组分.其中,生物滤饼层内的EPS采用超声-热提取法提取后,采用Excitation-emission matrix(EEM, F7000,日立,日本)和TOC检测仪(N/C2100S)检测EPS的种类和质量浓度; 滤饼层形貌:利用体式显微镜(Olympus C-7070,日本)观测;滤饼层内部结构:采用光学相干断层扫描技术(OCT,GAN610C1,Thorlabs GmbH,德国)观测;分子质量分布:水样经0.45 μm亲水性滤头预过滤后,采用凝胶色谱耦合有机碳联用仪(SEC-OCD,德国)检测;AOC:水样经3 d生化培养(37 ℃)后,采用流式细胞仪(Accuri C6,BD,美国)进行检测,并根据标准曲线计算AOC质量浓度;DOC:水样经0.45 μm滤膜预过滤后,采用TOC仪(N/C 2100S)检测;UV254:采用紫外可见分光光度计(波长为254 nm,T6, 普析,中国)检测;氨氮:采用纳氏试剂分光光度法检测;浊度:采用哈希浊度仪(2100N,美国)检测.
2 结果及讨论 2.1 通量稳定性研究考察了不同原水类型、驱动压力、膜组件、膜材质、膜孔径、温度、生物作用、间歇运行及缓速滤池预处理等工艺条件对GDM通量稳定性的影响.图 2(a)表明,GDM处理不同类型原水,长期运行中均观测到通量稳定现象,且稳定通量水平与原水水质显著相关.图 2(b)表明,尽管不同驱动压下GDM的初始通量差异显著,最终其通量均能达到稳定状态,且稳定通量相差不大,这是由于驱动压力增加会导致膜面滤饼层结构变得匀实致密,显著增加滤饼层阻力[3-4].因此,实际应用中难以通过增加驱动压力的方式来提高GDM的稳定通量.
图 2(c)表明,不同膜组件类型的GDM工艺长期运行其通量均可达到稳定状态,且平板膜组件的稳定通量略高于中空纤维膜组件;不同膜材质的GDM工艺长期运行其通量亦均可达到稳定,且稳定通量相差不大(PES膜通量略高,详见图 2(d)).图 2(e)表明,不同孔径的微滤膜和超滤膜构成的GDM工艺长期运行的通量变化规律基本一致,且均可达到稳定状态;然而,GDM(MF)的稳定通量显著高于GDM(UF),且UP150膜(截留分子质量150 ku)的稳定通量也略高于UP100膜(截留分子质量为100 ku),表明膜孔径会影响GDM的稳定通量水平.此外,图 2(f)表明在实验温度(5~30 ℃)内,GDM工艺长期运行通量均可达到稳定状态;但随着温度的降低,GDM通量达到稳定状态的时间显著延长,且稳定通量也随之大幅下降.
此外,间歇运行可显著地提高GDM的稳定通量,且不会影响GDM工艺长期运行的通量稳定性.图 2(g)表明,每个过滤周期内随着间歇运行时间的延长,GDM的稳定通量显著提高,这是由于间歇过程会促进膜面滤饼层内污染物反向扩散到膜池溶液中,导致滤饼层内污染物浓度降低,同时使滤饼层经历“压实-松弛”过程,有助于缓解滤饼层污染[7].实际运行中,为了保障每天膜总产水量,最佳间歇运行时间宜为6~12 h.图 2(k)表明,耦合缓速滤池预处理工艺后,GDM的稳定通量大幅提升(~100%),这是由于缓速滤池可有效地预去除水中的悬浮物、胶体、颗粒物、生物聚合物和腐殖质,缓解GDM膜污染[8].不同滤料对GDM稳定通量的提升效能相差较大,其中GAC效果最佳,陶粒次之.
然而,当向GDM系统中投加叠氮化钠抑制滤饼层内的微生物作用后,膜通量持续缓慢下降,难以达到稳定状态(图 2(h)),表明生物滤饼层内微生物作用是影响GDM通量稳定性的关键因素.当向GDM系统投加环己酰亚胺抑制原生/后生动物捕食作用后,GDM长期运行其通量虽可达到稳定状态,但较对照组显著下降,表明生物捕食作用是调控GDM稳定通量水平的重要因素.
以上分析表明,GDM工艺长期运行的通量稳定现象普遍存在,不受原水水质、膜组件类型和工艺条件的影响,该特性有助于推动其在分散式供水系统中的广泛应用.
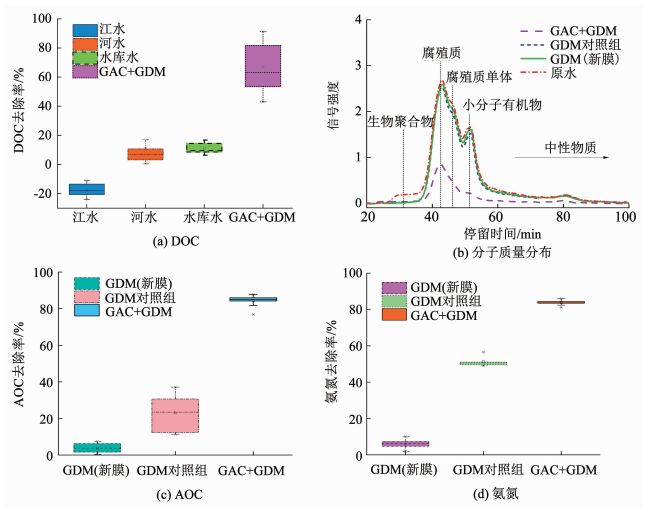
2.2 GDM净水效能研究实验中对比分析了GDM和常规超滤工艺对污染物去除效能的差异,结果如表 4和图 3所示.由表 4可知,常规超滤工艺出水中浊度为(0.09±0.01)NTU,而GDM工艺出水中浊度为(0.06±0.01) NTU,较常规超滤工艺有所下降,这可能是由于:1)常规超滤工艺操作压力大,容易导致部分胶体或颗粒性物质透过超滤膜;2)GDM膜面形成的生物滤饼层对水中的胶体和颗粒物起到了良好的预过滤效应[9].GDM出水中细菌总数与常规超滤工艺基本一致.可见,尽管GDM膜面生物滤饼层内滋生了大量微生物,但是其不会穿透超滤膜而进入出水中.有研究指出,GDM膜面生物滤饼层还可显著地提高对水中细菌和病毒的去除效能[10].
| 表 4 GDM工艺对浊度和微生物去除效能 Tab. 4 Removal performance of GDM process for turbidity and bacteria |
|
图 3 通量稳定后GDM工艺净水效能分析 Fig. 3 Removal performance of GDM process after flux stabilization |
图 3(a)表明,GDM在净化河水和水库水时,对DOC具有一定的去除作用,平均去除率约12%.然而,GDM在处理江水时,出水中DOC较进水中反而增加(~17%).部分研究也指出GDM出水中DOC高于进水,这可能是由于:1)GDM膜面生物滤饼层内藻类不断生长繁殖,利用光合作用合成了新的碳水化合物;2)GDM长期运行,水中的胶体/颗粒型有机物不断被截留在膜表面,并在微生物作用下被水解成小分子溶解性有机物而透过超滤膜,导致出水中DOC增加[11-12].本实验中GDM装置均采用了避光处理以抑制藻类生长;且对比江水、河水和水库水的原水水质发现,江水中的TOC明显高于后者,因此,胶体/颗粒型有机物的水解作用可能是导致GDM出水中DOC增加的主要原因.
实验中通过预过滤去除水中的胶体/颗粒型有机物后,出水中DOC显著降低,进一步证实了上述假设.此外,当缓速滤池预处理后,GAC+GDM联合工艺对DOC的去除效能显著提升(50% ~80%),可有效保障供水安全.
对比GDM(新膜)和GDM对照组对水中不同分子质量有机污染物的去除规律,发现GDM对照组和GDM(新膜)对生物聚合物均具有显著去除作用,但对腐殖酸类物质的去除效果较差(图 3(b));且相比GDM(新膜),GDM对照组对生物聚合物和腐殖质类物质的去除率增加了约8%和10%,表明膜面生物滤饼层起到了较好的预过滤作用[13-14].然而,GDM对照组对小分子有机物的去除效果低于GDM(新膜),这是生物滤饼层将截留在膜面的大分子有机物(如生物聚合物)水解成溶解性小分子有机物后透过超滤膜引起的.此外,采用GAC缓速滤池预处理后,出水中生物聚合物、腐殖酸类物质和小分子有机物浓度均显著下降.
可生物同化有机碳(AOC)是评估饮用水生物稳定性的重要指标.图 3(b)表明,超滤膜本身对AOC没有明显去除作用(< 5%),这是由于AOC通常是亲水性小分子有机物,其分子质量小于膜孔径而难以被截留去除.相比之下,GDM可有效削减水中的AOC((22.8±9)%),这是由于膜面生物滤饼层内滋生了大量的微生物,降解了水中的AOC[6, 15].此外,采用GAC+GDM耦合工艺可显著提高对AOC的去除效能(>80%),保障出水的生物稳定性.
常规超滤工艺对氨氮几乎没有去除作用[16].GDM长期运行,氨氮的去除率先逐渐增加,后趋于稳定,平均去除率高达50%(图 3(d)),这是由于水中的硝化细菌被截留在膜表面并在生物滤饼层内生长繁殖,促进了水中氨氮的去除[17].当采用GAC缓速滤池预处理后,GAC+GDM联用工艺对氨氮的去除效果进一步提升,平均去除率高达85%,这是由于GAC缓速滤池内滋生了大量的硝化细菌,使得联用工艺中的生物量远远高于GDM对照组.部分研究亦指出,GDM膜面生物滤饼层对氨氮具有较好的去除作用,且通过在膜面负载颗粒物(如粉末活性炭)可强化对氨氮的去除效能[12].
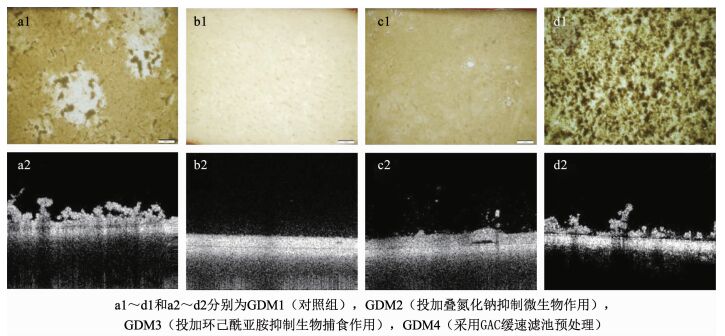
2.3 生物滤饼层特性及通量稳定机理 2.3.1 生物滤饼层结构特性研究为了揭示GDM工艺长期运行的通量稳定机理,观测了不同条件下生物滤饼层的形貌分布和内部微结构,结果如图 4所示.
|
图 4 生物滤饼层形貌和内部结构 Fig. 4 Morphologies and internal structures of bio-cake layer |
GDM对照组膜面生物滤饼层分布不均匀,可观测到显著的“团簇”和“膜裸露”结构,生物滤饼层内孔隙发达,且滤饼层的厚度随着过滤的进行先快速增加后趋于稳定.相比之下,当采用叠氮化钠抑制滤饼层内的生物作用后(图 4(b1-2)),生物滤饼层匀实致密,均匀分布,未观测到明显的“团簇”和“膜裸露”结构;OCT原位观测发现其生物滤饼层内部结构极为致密,厚度均一,未见“凹凸”及内部孔隙结构,表明生物作用是影响GDM膜面生物滤饼层粗糙多孔性结构形成的关键[3, 18].此外,抑制生物作用后滤饼层与超滤膜紧密贴合在一起,这可能是由于:1)抑制生物作用后,水中的污染物(如生物聚合物)因无法被水解去除而不断在膜面累积;2)叠氮化钠不利于微生物生长,刺激微生物分泌了大量的EPS,导致滤饼层的黏性显著增加.类似地,部分研究指出滤饼层内EPS质量浓度增加会显著地降低生物滤饼层的粗糙度和孔隙率,影响其微观结构[19].结合图 2通量变化规律可知,微生物作用调控的膜面生物滤饼层粗糙多孔性结构是导致GDM长期运行过程中通量达到稳定状态的关键因素.
图 4(c)表明,当投加环己酰亚胺抑制滤饼层内的生物捕食作用后,膜面生物滤饼层变得较为致密,仅观测到细微的“团簇”结构;生物滤饼层内局部观测到“隆起”结构及滤饼层从膜面分离的现象,表明生物捕食作用有助于提高GDM膜面生物滤饼层的粗糙度和多孔性.相比图 4(b),图 4(c)中生物滤饼层的形貌和结构均有所改善,这可能是抑制滤饼层内生物捕食作用后GDM3通量可达到稳定状态的主要原因.相比对照组,GDM3的稳定通量大幅下降,表明生物捕食作用会显著影响稳定通量水平[20].
当采用GAC缓速滤池预处理后,生物滤饼层在膜面分布尤为不均匀,“团簇”现象更为明显;生物滤饼层内部结构更为粗糙,孔隙结构更发达,并可观测到明显的生物滤饼层脱落现象(图 4(d)),这是由于GAC缓速滤池具有较好的预过滤效应,显著地降低了水中污染物(如生物聚合物和腐殖质等)在GDM膜表面的沉积,改善生物滤饼层结构特性.部分研究指出耦合GAC缓速滤池有助于提高生物滤饼层的粗糙度和多孔性,降低EPS质量浓度,提高GDM的稳定通量[21].
因此,GDM长期运行过程中,生物作用调控的膜面粗糙多孔性滤饼层结构是导致膜通量达到稳定状态的关键因素,而生物捕食作用和预处理工艺有助于提高GDM生物滤饼层的粗糙度和孔隙率,提升稳定通量水平.
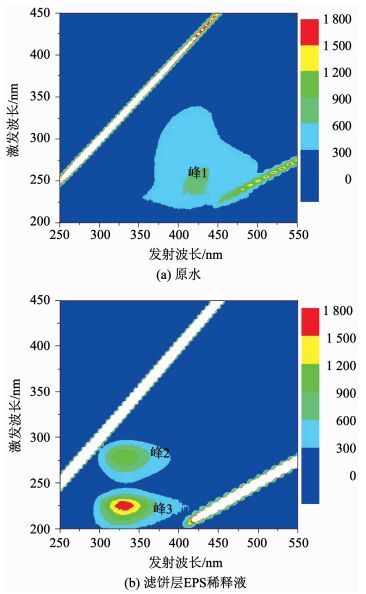
2.3.2 生物滤饼层生化组分特性研究实验中利用3DEEM指纹技术追踪了原水和滤饼层中EPS信息[22].图 5表明,原水和GDM膜面滤饼层内EPS的荧光峰截然不同,原水中的荧光性污染物(峰1)主要是腐殖质类物质,而GDM滤饼层内EPS主要是色氨酸类蛋白物质和芳香烃类蛋白物质,表明膜面滤饼层内的污染物可能是微生物代谢过程分泌的EPS.因此,调控GDM膜面微生物的代谢作用和EPS分泌,更有利于降低生物滤饼层内EPS质量浓度.采用缓速滤池预处理工艺,一方面可有效地预去除水中的污染物(如颗粒/胶体型有机物和生物聚合物),有效降低污染物在膜面生物滤饼层内的沉积量;另一方面缓速滤池内滋生的微生物将消耗掉大部分营养物,有助于降低GDM生物滤饼层内的生物量和EPS分泌量,缓解膜污染,提高稳定通量[8, 23].
|
图 5 原水和GDM膜面生物滤饼层内的荧光污染物 Fig. 5 Fluorescent foulants in raw water and bio-cake layer of GDM |
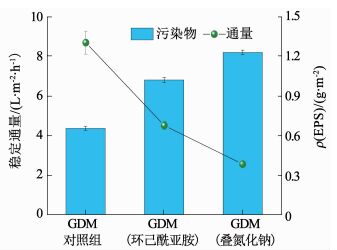
图 6表明,当投加叠氮化钠抑制生物作用后,膜面生物滤饼层内的EPS质量浓度显著增加,这可能是由于微生物在不利条件下分泌了大量的EPS,其通量大幅下降;当投加环己酰亚胺抑制滤饼层内的生物捕食作用后,膜面生物滤饼层内的EPS质量浓度较GDM对照组明显增加,通量亦有所下降,但高于GDM(叠氮化钠)的通量值,表明不同生物作用会显著影响滤饼层内EPS质量浓度,从而影响GDM的通量稳定性和稳定通量水平.因此,采取合理的措施调控生物滤饼层内微生物作用,可有效地降低EPS质量浓度,提高GDM的稳定通量.
|
图 6 滤饼层内EPS质量浓度与稳定通量的关联性分析 Fig. 6 Relation between stable flux level and EPS concentration of bio-cake layer |
结合上述分析可知,GDM的通量稳定性和稳定通量水平主要受膜面生物滤饼层的微观结构和EPS质量浓度影响.一方面污染物(如生物聚合物)不断被截留在膜表面,形成滤饼层污染,导致跨膜压差增加和膜通量下降;另一方面,在微生物作用下滤饼层的粗糙度和多孔性显著增加,渗透性随之提高,有助于提升膜通量[18].当二者的相互作用达到动态平衡时,GDM膜通量可达到稳定状态.可见,生物作用是影响GDM通量稳定性的关键因素.生物捕食和缓速滤池预处理措施可调控生物滤饼层内的微生物作用,改善生物滤饼层的粗糙多孔性和降低滤饼层内EPS质量浓度,显著提升GDM的稳定通量.
2.4 GDM工艺优势及应用前景相比常规超滤工艺,GDM有机地耦合了超滤膜和生物滤饼层的双重截留功效,能有效地强化超滤膜的截留作用,实现对水中颗粒物、胶体和病原微生物的深度脱除,保障出水的生物安全性;同时,对常规超滤工艺难以去除的氨氮和AOC等溶解性污染物也具有较好的去除作用,进一步强化超滤工艺对受氨氮污染水源水的适配性和提高出水的生物稳定性.此外,GDM工艺采用低压过滤模式(过滤压力约为常规超滤工艺的1/10),且不需要采用反冲洗和化学清洗措施控制膜污染,兼具无药剂、低能耗、低维护、配套设备少、净水效果稳定等优点,在分散式供水系统中拥有广阔的应用前景.
3 结论1) GDM工艺长期运行的通量稳定现象普遍存在,原水水质、驱动压力、膜组件类型、膜材质、膜孔径、温度、运行模式、预处理等工艺条件会影响GDM的稳定通量水平.
2) GDM膜面生物滤饼层具有预过滤效应,可强化对浊度、微生物和溶解性有机物的去除作用;还可提高对氨氮和AOC的去除效能,平均去除率分别为50%和23%,有助于保障出水的生物安全性和稳定性,提升超滤工艺对受氨氮污染水源水的适配性.
3) 微生物作用调控的生物滤饼层粗糙多孔性结构是导致GDM长期运行通量达到稳定状态的关键因素,生物滤饼层结构越粗糙、内部孔隙越发达、EPS质量浓度越低,GDM的稳定通量越高.
4) 缓速滤池预处理不但可有效地提高污染物的去除效能,保障供水水质;还可显著改善GDM膜面生物滤饼层的粗糙多孔性结构,降低滤饼层内EPS质量浓度,提高GDM稳定通量水平.
5) GDM工艺有机地耦合了生物滤饼层和超滤膜双重截留功效,兼具操作简单、低能耗、低维护、净水效果稳定等优点,有助于推动超滤技术在分散式供水系统中的广泛应用.
| [1] |
PETER-VARBANETS M, ZURBRVGG C, SWARTZ C, et al. Decentralized systems for potable water and the potential of membrane technology[J]. Water Research, 2009, 43: 245. DOI:10.1016/j.watres.2008.10.030 |
| [2] |
周丽英, 毛年英, 周莹莹. 浅淡超滤膜技术在徐泾自来水厂的应用[J]. 给水排水, 2013(S1): 54. ZHOU Liying, MAO Nianying, ZHOU Yingying. Application of ultrafiltration membrane technology in Xujing waterworks[J]. Water & Wastewater Engineering, 2013(S1): 54. DOI:10.13789/j.cnki.wwe1964.2013.s1.108 |
| [3] |
PETER-VARBANETS M, HAMMES F, VITAL M, et al. Stabilization of flux during dead-end ultra-low pressure ultrafiltration[J]. Water Research, 2010, 44(12): 3607. DOI:10.1016/j.watres.2010.04.020 |
| [4] |
TANG Xiaobin, DING An, QU Fangshu, et al. Effect of operation parameters on the flux stabilization of gravity-driven membrane (GDM) filtration system for decentralized water supply[J]. Environmental Science & Pollution Research, 2016, 23(16): 1. DOI:10.1007/s11356-016-6857-0 |
| [5] |
陈楠, 李星, 杨艳玲, 等. 低水头、低通量浸没式直接超滤工艺净水效能研究[J]. 中国给水排水, 2016(19): 53. CHEN Nan, LI Xing, YANG Yanling, et al. Water purification efficiency of submerged direct ultrafiltration process with low head and low flux[J]. China Water & Wastewater, 2016(19): 53. |
| [6] |
CHOMIAK A, TRABER J, MORGENROTH E, et al. Biofilm increases permeate quality by organic carbon degradation in low pressure ultrafiltration[J]. Water Research, 2015, 85: 512. DOI:10.1016/j.watres.2015.08.009 |
| [7] |
PETER-VARBANETS M, GUJER W, PRONK W. Intermittent operation of ultra-low pressure ultrafiltration for decentralized drinking water treatment[J]. Water Research, 2012, 46(10): 3272. DOI:10.1016/j.watres.2012.03.020 |
| [8] |
TANG Xiaobin, DING An, PRONK W, et al. Biological pre-treatments enhance gravity-driven membrane filtration for the decentralized water supply: Linking extracellular polymeric substances formation to flux stabilization[J]. Journal of Cleaner Production, 2018, 197: 721. DOI:10.1016/j.jclepro.2018.06.155 |
| [9] |
唐小斌, 梁恒, 瞿芳术, 等. 低压无清洗浸没式直接超滤工艺中试研究[J]. 中国给水排水, 2016, 17: 29. TANG Xiaobin, LIANG Heng, QU Fangshu, et al. Performance of gravity-driven low-pressure direct ultrafiltration system with submerged membrane[J]. China Water & Wastewater, 2016, 17: 29. |
| [10] |
PETER-VARBANETS M, JOHNSTON R, MEIERHOFER R, et al. Gravity driven membrane disinfection for household drinking water treatment[C]//Proceedings of 35th WEDC International Conference. Loughborough, UK: [s.n.], 2011 https://www.researchgate.net/publication/281290160_Gravity-driven_membrane_disinfection_for_household_drinking_water_treatment
|
| [11] |
AKHONDI E, WU Bing, SUN Shuyang, et al. Gravity-driven membrane filtration as pretreatment for seawater reverse osmosis: Linking biofouling layer morphology with flux stabilization[J]. Water Research, 2015, 70: 158. DOI:10.1016/j.watres.2014.12.001 |
| [12] |
SHAO Senlin, FENG Yijing, YU Huarong, et al. Presence of an adsorbent cake layer improves the performance of gravity-driven membrane (GDM) filtration system[J]. Water Research, 2016, 108: 240. DOI:10.1016/j.watres.2016.10.081 |
| [13] |
DING An, LIANG Heng, LI Guibai, et al. A low energy gravity-driven membrane bioreactor system for grey water treatment: Permeability and removal performance of organics[J]. Journal of Membrane Science, 2017, 542: 408. DOI:10.1016/j.memsci.2017.08.037 |
| [14] |
柳斌, 瞿芳术, 施周, 等. 低压重力驱动式超滤工艺处理引黄水库水中试研究[J]. 给水排水, 2018, 54(6): 40. LIU Bin, QU Fangshu, SHI Zhou, et al. Pilot-scale study of low-pressure gravity-driven ultrafiltration process for reservoir water derived from Yellow River[J]. Water & Wastewater Engineering, 2018, 54(6): 40. DOI:10.13789/j.cnki.wwe1964.2018.0162 |
| [15] |
DERLON N, MIMOSO J, KLEIN T, et al. Presence of biofilms on ultrafiltration membrane surfaces increases the quality of permeate produced during ultra-low pressure gravity-driven membrane filtration[J]. Water Research, 2014, 60: 164. DOI:10.1016/j.watres.2014.04.045 |
| [16] |
常海庆, 梁恒, 高伟, 等. 膜生物反应器与预处理联用净化微污染引黄水库水[J]. 哈尔滨工业大学学报, 2012, 44(12): 25. CHANG Haiqing, LIANG Heng, GAO Wei, et al. Purification of micro-polluted reservoir water from the Yellow River by membrane bioreactors combined with pretreatments[J]. Journal of Harbin Institute of Technology, 2012, 44(12): 25. DOI:10.11918/j.issn.0367-6234.2012.12.005 |
| [17] |
TANG Xiaobin, CHENG Xiaoxiang, ZHU Xuewu, et al. Ultra-low pressure membrane-based bio-purification process for decentralized drinking water supply: Improved permeability and removal performance[J]. Chemosphere, 2018, 211: 784. DOI:10.1016/j.chemosphere.2018.07.183 |
| [18] |
PETER-VARBANETS M, MARGOT J, TRABER J, et al. Mechanisms of membrane fouling during ultra-low pressure ultrafiltration[J]. Journal of Membrane Science, 2011, 377(1): 42. DOI:10.1016/j.memsci.2011.03.029 |
| [19] |
DESMOND P, BEST J P, MORGENROTH E, et al. Linking composition of extracellular polymeric substances (EPS) to the physical structure and hydraulic resistance of membrane biofilms[J]. Water Research, 2018, 132: 211. DOI:10.1016/j.watres.2017.12.058 |
| [20] |
DERLON N, PETER-VARBANETS M, SCHEIDEGGER A, et al. Predation influences the structure of biofilm developed on ultrafiltration membranes[J]. Water Research, 2012, 46(10): 3323. DOI:10.1016/j.watres.2012.03.031 |
| [21] |
TANG Xiaobin, PRONK W, DING An, et al. Coupling GAC to ultra-low-pressure filtration to modify the biofouling layer and bio-community: Flux enhancement and water quality improvement[J]. Chemical Engineering Journal, 2018, 333: 289. DOI:10.1016/j.cej.2017.09.111 |
| [22] |
吴梓坚, 余华荣, 梁恒. 应用前表面三维荧光表征有机膜污染物质的方法[J]. 哈尔滨工业大学学报, 2019, 51(2): 22. WU Zijian, YU Huarong, LIANG Heng. Characterization of organic membrane foulants with front-face fluorescence excitation-emission matrix[J]. Journal of Harbin Institute of Technology, 2019, 51(2): 22. DOI:10.11918/j.issn.0367-6234.201711139 |
| [23] |
LEE S, SUTTER M, BURKHARDT M, et al. Biocarriers facilitated gravity-driven membrane (GDM) reactor for wastewater reclamation: Effect of intermittent aeration cycle[J]. Science of the Total Environment, 2019, 694: 133719. DOI:10.1016/j.scitotenv.2019.133719 |
 2020, Vol. 52
2020, Vol. 52


