2. 北京城市排水集团有限责任公司,北京 100022;
3. 环境模拟与污染控制国家重点联合实验室(清华大学),北京 100084
2. Beijing Drainage Group Co., Ltd., Beijing 100022, China;
3. State Key Joint Laboratory of Environment Simulation and Pollution Control (Tsinghua University), Beijing 100084, China
污水再生利用愈发成为解决水资源短缺的有效途径,再生水的安全性也随之受到广泛关注,污水处理厂排放水质标准中对卫生学指标的限制,很好地保障了再生水的生物安全性。而由个人护理品、内分泌干扰物、全氟化合物等微量有机污染物可能引发的化学风险分析与管控较为复杂[1-4]。如何充分发挥再生水厂处理工艺的规模化效益,实现微量有机污染物在城市水循环关键节点的削减显得尤为重要。
再生水生产环节,除采用臭氧进行氧化脱色外,还具有一定的消毒效果[5],并且对微量有机污染物也有较高的转化效率[6]。但是有研究指出有机物经臭氧氧化后的中间产物可能比其前体物显现出更高的安全风险[7-8],需要考虑设置后续处理单元对臭氧氧化出水中的有机物进行强化去除。活性焦作为一种新型的低成本碳基吸附材料,中孔结构发达,可有效去除城镇污水处理厂二级出水中的有机物,且生物活性焦可以利用表面附着微生物的降解功能实现活性焦的动态吸附、再生[9]。但是新鲜的活性焦颗粒在向生物活性焦的演变过程中,其对有机物的去除率也在逐渐降低。因此,如何利用臭氧前处理单元,在缓解生物活性焦演变过程中有机物去除效果衰减的同时,借助生物活性焦后处理单元实现臭氧氧化中间产物的有效去除,以共同保证出水的安全性,具有重要的现实意义。
本文采用臭氧氧化与生物活性焦联用工艺处理城市污水处理厂二级出水,重点考察了该组合工艺对二级出水有机污染物、病原微生物的去除效果,并采用发光菌发光强度抑制率实验,考察了该工艺对出水生物安全性的影响,以期为臭氧氧化-生物活性焦技术在再生水深度处理领域的工程应用提供技术支撑。
1 实验 1.1 实验装置和原水水质臭氧氧化-活性焦过滤中试装置(O3-BACK)如图 1所示。某城镇污水处理厂二级出水经砂滤过滤后作为臭氧单元进水,主要水质参数见表 1。臭氧氧化接触柱为不锈钢材质,直径30 cm,有效水深3 m,超高0.6 m,上部进水错流式接触氧化。臭氧投加量为3 mg/L,水力停留时间为20 min,对应臭氧利用率约为98%。活性焦滤柱为有机玻璃材质,直径30 cm,高3.6 m,装填20~30目(0.55~0.83 mm)、厚度2 m的活性焦滤层,上向流过滤形式,空床停留时间(EBCT)为20 min,滤速为5.94 m/h。试验所用活性焦滤料购于杭州回水科技。活性焦总空隙体积为0.73 cm3/g,中孔与大孔体积占比59.73%,具体孔结构参数详见文献[9]。

|
图 1 臭氧氧化-活性焦过滤中试系统实物照片 Fig. 1 Picture of O3-BACK pilot-scale system |
| 表 1 某城镇污水处理厂二级出水(砂滤后)主要水质指标 Tab. 1 Main water quality parameters of secondary effluent (after sand filtration) in a municipal wastewater treatment plant |
CODCr和UV254测定采用DR6000型紫外分光光度计(HACH,USA),DOC测定采用multi N/C 3100总有机碳分析仪(Analytik Jena AG,Germany),浊度测定采用2100Q便携式浊度仪(HACH,USA),色度测定采用SD9012A水质色度仪(上海昕瑞,中国),利用RF-6000荧光分光光度计(Shimadzu,Japan)测定进出水三维荧光光谱。利用QuenchGone 21 Wastewater测试包测定滤料表面微生物ATP含量,大肠菌群、粪大肠菌群和大肠埃希氏菌依据固定酶底物法,使用科立得试剂盒(IDEXX,USA),总异养菌(HPC)采用SimPlate复合酶底物法测定。
1.2.2 有机微污染物与综合生物毒性测定试验选取具有代表性的11种微量有机物为目标污染物,以其在二级出水中的浓度本底值为O3-BACK系统进水初始值。其中,替米沙坦、厄贝沙坦、甲氧苄啶、磺胺甲恶唑、卡马西平、紫外吸收剂BP-4、双氯芬酸购自美国Sigma-Aldrich公司,全氟辛酸、全氟磺酸购自加拿大Wellington公司,雷尼替丁购自美国Alfa Aesar公司,苯并三唑购自上海源叶生物科技有限公司。所有标准品质量分数均大于98%。色谱纯的甲醇、乙酸铵、乙腈购自美国Thermo Fisher科技公司。
采用SUPELCO VISIPREP 24TM DL固相萃取装置和OASIS HLB固相萃取小柱对水样进行富集。富集后的萃取小柱真空干燥2 h,用甲醇溶液洗脱有机物,氮吹定容后使用超高效液相色谱串联四级杆质谱联用仪(Waters ACQUITY UPLCTM/ Waters XEVOTM, USA)对微量有机污染物进行检测分析。色谱柱为Waters ACQUITY UPLC BEH C18柱。进样量5 μL,正电模式(ESI+) 流动相为0.01 mol/L乙酸铵和乙腈(体积比为60∶ 40), 流速为0.2 mL/min;负电模式(ESI-)流动相为水和乙腈(体积比为50∶ 50),流速为0.3 mL/min。替米沙坦、厄贝沙坦、甲氧苄啶、磺胺甲恶唑、苯丙三唑、卡马西平、盐酸雷尼替丁7种物质采用ESI+检测模式,质谱条件为毛细管电压4.5 kV,干燥气温度300 ℃,干燥气流量12 L/min,雾化气压力345 kPa,定量离子对(m/z)分别为515.0>276.1、429.0>207.0、291.0>230.1、254.3>156.0、120.0>92.0、237.0>179.1、315.1>129.9。双氯芬酸、紫外吸收剂BP-4、全氟辛酸(PFOA)、全氟磺酸(PFOS)4种物质采用ESI-检测模式,质谱条件为毛细管电压-3.5 kV,干燥气温度300 ℃,干燥气流量12 L/min,雾化气体压力345 kPa,定量离子对(m/z)分别为250.1>178.0、307.0>210.0、412.8>368.8、298.9>80.0。
水样综合毒性以发光细菌(费氏弧菌)为指示生物,利用其对水中毒性物质的敏感性,测得加入待测水样后费氏弧菌发光强度较初始光强的抑制率,具体方法见文献[10]。
2 结果与讨论 2.1 常规水质指标变化在臭氧氧化-活性焦过滤中试系统正式启动后,近5个月的连续运行过程中,该组合工艺对二级出水中常规指标的去除情况见图 2。
|
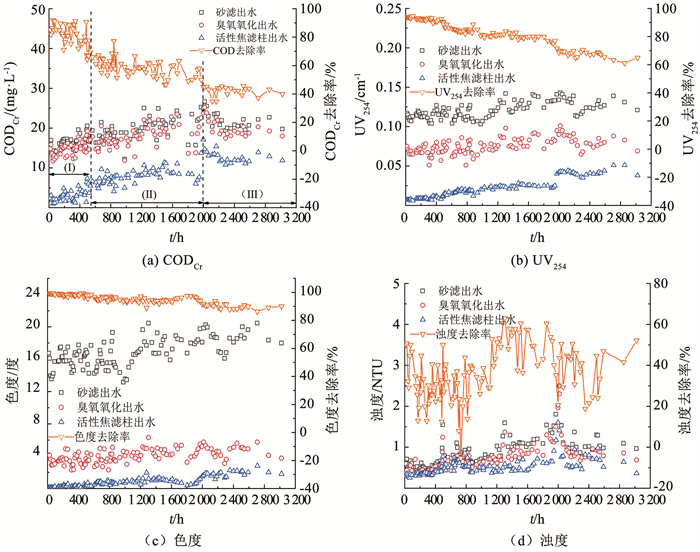
图 2 二级出水常规水质指标变化 Fig. 2 Variation of conventional water quality parameters in O3-BACK system |
臭氧对砂滤出水中CODCr、UV254、色度的平均去除率分别为8.5%、37.8%、76.2%。与前期研究中单独活性焦滤柱的发展过程相似[9],在设置臭氧前处理条件下,新鲜活性焦滤柱向生物活性焦滤柱的演变也可分为3个阶段:第Ⅰ阶段,持续23 d,以吸附作用为主,对臭氧出水CODCr的去除率维持在70%~90%,但衰减较快;第Ⅱ阶段,持续59 d,为吸附趋于饱和、生物降解作用逐渐增强阶段,对臭氧出水CODCr的去除率维持在45%~65%;第Ⅲ阶段,系统运行82 d后,进入稳定的生物吸附降解阶段,此时滤柱中部活性焦颗粒表面微生物ATP质量分数为578.5 ng/g,表明该阶段滤料表面有丰富的微生物附着。对臭氧出水CODCr的去除率维持在30%~40%,CODCr平均去除量与平均去除率分别为8.07 mg/L、36.49%。较稳定期单独生物活性焦滤柱对CODCr 6.68 mg/L的去除量与28.43%的去除率[9]分别提升了20.81%和28.35%。
尽管臭氧氧化单元对CODCr的直接去除率不高,但有机物的可生化性得到改善,被臭氧转化的这部分有机物更易被活性焦表面附着的微生物利用[11],而非占据滤料表面有限的吸附点位或者阻塞孔道。臭氧单元的引入,在强化后续活性滤柱生物降解作用的同时,有效地降低了活性焦颗粒的吸附负荷。生物活性焦滤柱稳定期出水CODCr、UV254、色度分别保持在12.74 mg/L,0.04 cm-1和2度左右。由于活性焦滤柱采用上向流形式,其出水浊度较易受上游来水浊度变化的影响,稳定期臭氧与生物活性焦滤柱出水浊度分别为1.0和0.75 NTU。
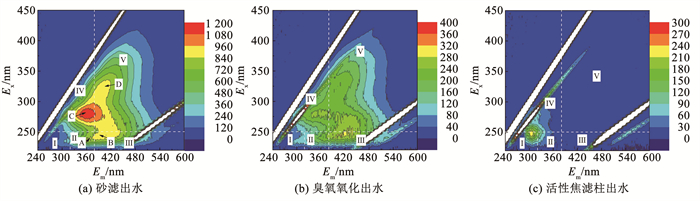
2.2 有机物荧光特性变化活性焦滤柱运行至第Ⅲ阶段稳定期时,对该组合工艺各处理单元出水进行三维荧光光谱(3DEEM)分析,按五区域(Ⅰ~Ⅴ)划分法,结果如图 3所示。二沉水经砂滤过滤后的出水在区域Ⅱ~Ⅳ内具有4个明显的荧光峰,分别为芳香族蛋白质峰A、类富里酸峰B、溶解性微生物代谢产物峰C、类腐殖酸峰D。砂滤出水经臭氧氧化后,峰A、B、C、D的荧光强度分别降低了约75.9%、79.1%、77.9%、75.1%。经活性焦滤柱进一步净化后,除区域Ⅳ的特征峰C外,其他3个特征峰均基本消失,说明臭氧氧化与活性焦过滤联用对二级出水中荧光特性类有机物有较好的去除效果。
|
图 3 各处理单元出水3DEEM光谱 Fig. 3 3DEEM fluorescence spectra of effluent samples in O3-BACK system |
结合上述3DEEM图谱,利用荧光区域积分方法[12],得到5个荧光区域对应的积分标准体积,如表 2所示。将各荧光区域标准体积所占比例与DOC相乘得到各区域对应的DOC质量浓度。可以看出,腐殖酸类物质和溶解性微生物代谢产物为砂滤出水的主要有机物组分,对应DOC质量浓度分别为1.73和1.46 mg/L,分别占荧光区域有机物总量的44.2%和37.2%。臭氧对不易被生物降解的腐殖酸、富里酸和芳香族蛋白质类物质去除率较高,这与Chen等[13]的研究结果一致。臭氧优先攻击腐殖酸类物质,并通过链引发反应生成羟基自由基(· OH),· OH进一步强化芳香族蛋白质等组分的去除。经活性焦滤柱净化后,各荧光区域的有机物含量进一步降低,但与单独生物活性焦过滤相比,出水有机物组分并未发生变化,溶解性微生物代谢产物、腐殖酸类物质仍为两大主要组分,分别约占DOC的60%和25%。
| 表 2 各单元出水3DEEM光谱区域积分标准体积 Tab. 2 Standard integration volumes for 3DEEM fluorescence spectra in O3-BACK system |
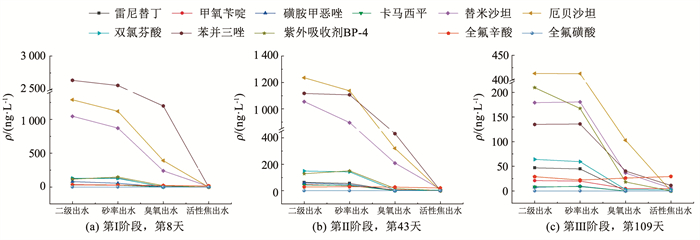
图 4为活性焦滤柱3阶段演变过程中11种微量有机污染物质量浓度变化。可以看出,二级出水中降压药替米沙坦、厄贝沙坦、抗腐蚀剂苯丙三唑质量浓度最高,分别在179.3~1 055.1、413.1~1 290.6、134.9~2 639.9 ng/L变化,其他化合物的质量浓度均在240 ng/L以下。
|
图 4 O3-BACK对微量有机污染物的去除 Fig. 4 Removal of trace organic pollutants in O3-BACK system |
砂滤对二级出水中有机微污染物去除效果并不明显。雷尼替丁、甲氧苄啶、磺胺甲恶唑、卡马西平、双氯芬酸、紫外吸收剂BP-4等均含有较高臭氧反应活性的富电子基团,如碳碳双键、酚类、胺或苯胺等[14-15],臭氧对其去除率均在80%以上。臭氧对降压药厄贝沙坦、替米沙坦和抗腐蚀剂苯并三唑的去除率在50%~80%。在厄贝沙坦的酰胺结构中,自由电子对容易被拉向吸电子的羰基基团,这降低了酰胺基与臭氧的反应速率[16];苯并三唑与臭氧反应速率常数较低,但臭氧与芳香族化合物的链反应生成的·OH,可一定程度强化此类低臭氧反应活性有机物的去除[17-18]。
二级出水中全氟辛酸(PFOA)的质量浓度约为28.7 ng/L,全氟辛烷磺酸(PFOS)的质量浓度低于检测限,< 2 ng/L。两者质量浓度之和低于美国环保署(US. EPA)关于饮用水中70 ng/L的最高限值[19]。全氟化合物有稳定的C—F键,且—COOH、—SO3H为吸电子基团,臭氧对PFOA的去除率较低[20]。由于PFOA具有较好的疏水性,正辛醇-水分配系数(log Kow)为6.28[21],活性焦滤柱启动初期,第8天,对PFOA有近30%的吸附去除效果。但是随着活性焦滤料吸附饱和以及生物膜的逐渐成熟,PFOA的去除率也随之降低,当活性焦滤柱运行至第Ⅲ阶段,第109天时,滤柱对PFOA无去除效果。
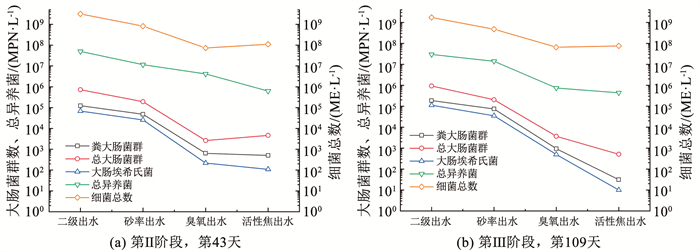
2.4 微生物指标变化活性焦丰富的中孔与大孔结构,在利于微生物附着生长的同时,为粪大肠菌群等致病菌提供了再生机会。在活性焦滤柱运行至生物作用增强的第Ⅱ和第Ⅲ阶段时,分别考察了该组合工艺各处理单元出水的微生物含量,结果见图 5。可以看出,二级出水中粪大肠菌群为105~106 MPN/L,砂滤后粪大肠菌群为104~105 MPN/L,臭氧氧化对粪大肠菌群有近两个log的灭活,臭氧对总大肠菌群、粪大肠菌群和细菌总数的去除率分别为98%、99%和88%。von Gunten等[22]研究表明,臭氧分子可直接攻击大肠杆菌的DNA导致其失活。经过生物活性焦滤柱处理后,尽管在第Ⅲ阶段,第54天,总大肠菌群有轻微再生,但是出水粪大肠菌群在31~504 MPN/L,仍满足GB/T 18921—2019《城市污水再生利用景观环境用水水质标准》中观赏性景观环境用水粪大肠菌群小于1 000 L-1的要求。
|
图 5 各单元出水微生物指标变化 Fig. 5 Variation of microbial concentrations in O3-BACK system |
再生水是多种物质组分协同或拮抗作用共存的混合体系,通过某些物化指标或特定化合物剂量效应关系难以客观有效地评价水样的安全性。利用发光菌体内敏感代谢机制对水质变化的及时响应,直观地衡量再生水水质的生物安全性是对理化分析的有力补充[23]。
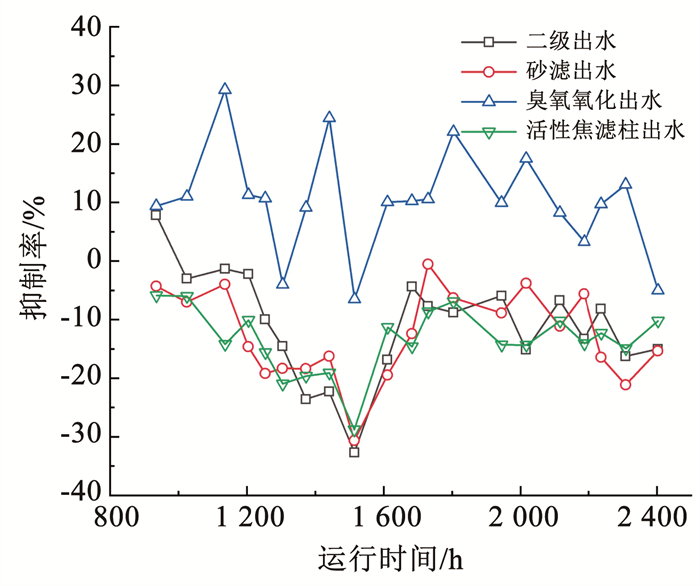
图 6为基于发光细菌发光强度抑制率实验得到的臭氧-生物活性焦中试系统各处理单元出水的生物毒性变化。可以看出,二级出水、砂滤出水、生物活性焦滤柱出水发光细菌光强抑制率为负值,均无生物毒性。砂滤出水经臭氧氧化后,出水对发光细菌毒性的平均抑制率为11%。由于水中残留臭氧质量浓度始终处于较低水平,<0.1 mg/L。推测部分有机物的臭氧氧化中间产物对发光菌有抑制作用[24]。而后续生物活性焦滤柱可有效去除此部分有抑制作用的氧化中间产物,最终活性焦滤柱出水无生物毒性。
|
图 6 各单元出水生物毒性变化 Fig. 6 Variation of biotoxicity of effluent samples in O3-BACK system |
1) 在臭氧氧化-生物活性焦过滤工艺(O3-BACK)中,活性焦滤柱由吸附饱和向生物活性焦发展的过程可分为3个阶段。第Ⅰ阶段,以活性焦滤料吸附作用为主,历时近22 d,对O3出水CODCr的去除率在90%~70%递减;第Ⅱ阶段,是由吸附趋于饱和向生物降解作用增强的过渡期,历时近60 d,对O3出水CODCr的去除率在65%~45%,以相对平缓的速率衰减;第Ⅲ阶段,为生物降解作用主导下的稳定期,活性焦颗粒表面微生物ATP质量分数为578.5 ng/g,生物活性焦可实现动态吸附、再生,对O3出水CODCr的去除率维持在30%~40%。
2) 较单独BACK过滤,3 mg/L臭氧投加量的预氧化过程,使后续BACK滤柱稳定期对CODCr的平均去除量与去除率分别提升了20.81%、28.35%。BACK滤柱出水CODCr、UV254、色度、浊度分别维持在12.74 mg/L、0.04 cm-1、2度、0.75 NTU附近。
3) O3单元对荧光特性有机物具有较好的氧化去除效果,难生物降解的腐殖酸、富里酸和色氨酸类芳香族蛋白质等组分的荧光区域积分标准体积分别减少了51.28%、75.73%和95.50%。O3-BACK进、出水中,微生物代谢产物、腐殖酸均为两主要组分,但两者所占比例此消彼长,分别由进水的37.34%、44.18%变为出水的59.73%、25.15%。O3单元对磺胺甲恶唑等11种目标微量有机污染物的去除率均大于65%;除全氟辛酸外,BACK出水中10种微量有机物质量浓度均降至10 ng/L以下。
4) O3单元对粪大肠菌群(FC)有近2log的灭活,BACK出水FC浓度为31~504 MPN/L,在无外加消毒剂的前提下,即可满足观赏性景观环境用水FC < 1 000 L-1的要求(GB/T 18921—2019)。二级出水经O3氧化后对发光细菌发光强度抑制率(IR)有所升高,平均抑制率为11%,经后续BACK过滤后,最终出水IR始终为负值,无生物毒性。
前期BACK单独过滤小试实验[9]与本次臭氧氧化-生物活性焦过滤组合工艺(O3-BACK)中试研究,为再生水水质安全性保障技术“O3-BACK”走向工程应用奠定了技术基础。
| [1] |
MICHAEL K I, MICHAEL C, DUAN X, et al. Dissolved effluent organic matter: characteristics and potential implications in wastewater treatment and reuse applications[J]. Water Research, 2015, 77: 213. DOI:10.1016/j.watres.2015.03.011 |
| [2] |
BUI X T, VO T P T, NGO H H, et al. Multicriteria assessment of advanced treatment technologies for micropollutants removal at large-scale applications[J]. Science of the Total Environment, 2016, 563/564: 1050. DOI:10.1016/j.scitotenv.2016.04.191 |
| [3] |
ABARGUES M R, GIMÉNEZ J B, FERRER J, et al. Endocrine disrupter compounds removal in wastewater using microalgae: degradation kinetics assessment[J]. Chemical Engineering Journal, 2017, 334: 313. DOI:10.1016/j.cej.2017.09.187 |
| [4] |
牙柳丁, 王文龙, 胡洪营, 等. 城市污水二级处理出水中不同种类PPCPs的臭氧氧化效果与机制研究[J]. 环境科学学报, 2020, 40(11): 3868. YA Liuding, WANG Wenlong, HU Hongying, et al. Comparative study on ozonation efficiency and mechanism of different types of PPCPs in secondary effluent from municipal wastewater[J]. Acta Scientiae Circumstantiae, 2020, 40(11): 3868. DOI:10.13671/j.hjkxxb.2020.0162 |
| [5] |
李魁晓, 时玉龙, 于丽昕, 等. 新冠肺炎疫情期间城镇再生水厂协同消毒工艺运行实践[J]. 给水排水, 2020, 46(4): 48. LI Kuixiao, SHI Yulong, YU Lixin, et al. Practice of synergistic disinfection process in water reclamation plants during COVID-19 epidemic[J]. Water & Wastewater Engineering, 2020, 46(4): 48. DOI:10.13789/j.cnki.wwe1964.2020.04.009 |
| [6] |
RIZZO L, MALATO S, ANTAKYALI D, et al. Consolidated vs new advanced treatment methods for the removal of contaminants of emerging concern from urban wastewater[J]. Science of the Total Environment, 2019, 655: 986. DOI:10.1016/j.scitotenv.2018.11.265 |
| [7] |
刘宝明, 王夕希, 张晓夏, 等. 臭氧对生物活性炭中微生物及出水消毒副产物的影响[J]. 环境科学, 2020, 41(1): 253. LIU Baoming, WANG Xixi, ZHANG Xiaoxia, et al. Effect of Ozonation on microorganism in the biological activated carbon and disinfection by-products in the effluent[J]. Environmental Science, 2020, 41(1): 253. DOI:10.13227/j.hjkx.201907102 |
| [8] |
SUNDARAM V, PAGILLA K, GUARIN T, et al. Extended field investigations of ozone-biofiltration advanced water treatment for potable reuse[J]. Water Research, 2020, 172: 115513. DOI:10.1016/j.watres.2020.115513 |
| [9] |
王赛, 时玉龙, 郑晓英, 等. 两种碳基材料对二级出水中有机物的去除特性[J]. 中国给水排水, 2021, 37(5): 43. WANG Sai, SHI Yulong, ZHENG Xiaoying, et al. Removal characteristics of organic matters from secondary effluent by two types of carbon based adsorbent[J]. China Water & Wastewater, 2021, 37(5): 43. DOI:10.19853/j.zgjsps.1000-4602.2021.05.007 |
| [10] |
李魁晓, 李鑫玮, 邢旭, 等. 混凝沉淀砂滤出水臭氧氧化研究[C]//全国排水委员会2012年年会论文集. 南宁: 中国土木工程学会, 2012: 152 LI Kuixiao, LI Xinwei, XING Xu, et al. Study on ozone oxidation of filtration water from coagulated sedimentation sand[C]//Proceedings of the 2012 Annual Meeting of the National Drainage Commission. Nanning: China Civil Engineering Society, 2012: 152 |
| [11] |
WANG Shutao, MA Ju, LIU Baicang, et al. Degradation characteristics of secondary effluent of domestic wastewater by combined process of ozonation and biofiltration[J]. Journal of Hazardous Materials, 2008, 150(1): 109. DOI:10.1016/j.jhazmat.2007.04.092 |
| [12] |
CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2015, 37(24): 5701. DOI:10.1021/es034354c |
| [13] |
CHEN Zhiqiang, LI Mo, WEN Qinxue, et al. Evolution of molecular weight and fluorescence of effluent organic matter (EfOM) during oxidation processes revealed by advanced spectrographic and chromatographic tools[J]. Water Research, 2017, 124: 566. DOI:10.1016/j.watres.2017.08.006 |
| [14] |
LEE C O, HOWE K J, THOMSON B M. Ozone and biofiltration as an alternative to reverse osmosis for removing PPCPs and micropollutants from treated wastewater[J]. Water Research, 2012, 46(4): 1005. DOI:10.1016/j.watres.2011.11.069 |
| [15] |
REUNGOAT J, ESCHER B I, MACOVA M, et al. Ozonation and biological activated carbon filtration of wastewater treatment plant effluents[J]. Water Research, 2012, 46(3): 863. DOI:10.1016/j.watres.2011.11.064 |
| [16] |
克莱门斯·冯·桑塔格, 乌尔斯·冯·贡滕. 水和污水处理的臭氧化学: 基本原理与应用[M]. 刘正乾, 译. 北京: 中国建筑工业出版社, 2016: 65 VON SONNTAG C, VON GUNTEN U. Chemistry of ozone in water and wastewater treatment: from basic principles to applications[M]. LIU Zhengqian, translate. Beijing: China Architecture & Building Press, 2016: 65 |
| [17] |
MARGOT J, KIENLE C, MAGNET A, et al. Treatment of micropollutants in municipal wastewater: ozone or powdered activated carbon?[J]. Science of the Total Environment, 2013, 461/462: 480. DOI:10.1016/j.scitotenv.2013.05.034 |
| [18] |
韩琦, 董文艺, 王宏杰, 等. 臭氧降解低浓度四溴双酚A及生物毒性控制[J]. 哈尔滨工业大学学报, 2019, 51(8): 54. HAN Qi, DONG Wenyi, WANG Hongjie, et al. Degradation of low concentration tetrabromobisphenol A and toxicity controlling by ozone[J]. Journal of Harbin Institute of Technology, 2019, 51(8): 54. DOI:10.11918/j.issn.0367-6234.201807193 |
| [19] |
SUN Y, ANGELOTTI B, BROOKS M, et al. A pilot-scale investigation of disinfection by-product precursors and trace organic removal mechanisms in ozone-biologically activated carbon treatment for potable reuse[J]. Chemosphere, 2018, 210: 539. DOI:10.1016/j.chemosphere.2018.06.162 |
| [20] |
RAHMAN M F, PELDSZUS S, ANDERSON W B. Behaviour and fate of perfluoroalkyl and polyfluoroalkyl substances (PFASs) in drinking water treatment: a review[J]. Water Research, 2014, 50: 318. DOI:10.1016/j.watres.2013.10.045 |
| [21] |
AHRENS L, TANIYASU S, YEUNG L, et al. Distribution of polyfluoroalkyl compounds in water, suspended particulate matter and sediment from Tokyo Bay, Japan[J]. Chemosphere, 2010, 79(3): 266. DOI:10.1016/j.chemosphere.2010.01.045 |
| [22] |
VON GUNTEN U. Ozonation of drinking water: Part Ⅱ.Disinfection and by-product formation in presence of bromide, iodide or chlorine[J]. Water Research, 2003, 37(7): 1469. DOI:10.1016/S0043-1354(02)00458-X |
| [23] |
NASUHOGLU D, ISAZADEH S, WESTLUND P, et al. Chemical, microbial and toxicological assessment of wastewater treatment plant effluents during disinfection by ozonation[J]. Chemical Engineering Journal, 2018, 346: 466. DOI:10.1016/j.cej.2018.04.037 |
| [24] |
JIA A, ESCHER B I, LEUSCH F D L, et al. In vitro bioassays to evaluate complex chemical mixtures in recycled water[J]. Water Research, 2015, 80: 1. DOI:10.1016/j.watres.2015.05.020 |
 2022, Vol. 54
2022, Vol. 54


