2. 城市水资源与水环境国家重点实验室(哈尔滨工业大学), 哈尔滨 150090
2. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China
由于自然作用和人类活动的影响, 溶解态氨、亚铁和锰广泛存在于地下水中[1-3], 天然有机物是自然水域的组成部分, 如河流、湖泊及地下水等[4-5]。地下水中过量的铁、锰离子会引发嗅味问题和输水过程中管道堵塞, 过量摄入还会引发一系列的健康问题[6]。氨氮与氯反应生成的氯胺有致癌性[7-8], 天然有机物本身虽毒性小, 却是水中色度和嗅味的主要来源, 影响水体中金属离子的代谢途径[9], 在常规水处理工艺中, 还会增加混凝剂的投量、加速滤池的堵塞和消毒副产物的生成等。生物过滤方法处理此类水有其独特优势, 因效果好、费用低且运行简单等优点已广泛用于含铁锰地下水的净化处理。
Albrektiene等[10]采用混凝、曝气和过滤相结合的方式处理实际地下水(TFe 5.6 mg/L, Mn(Ⅱ)0.25 mg/L, NH4+-N 1.6 mg/L, CODMn 6 mg/L),该工艺对铁、锰、氨氮和有机物的去除率分别为98%、87%、99%和80%;杨航等[11]采用人工配水和外加葡萄糖模拟地下水(TFe 6 mg/L, Mn(Ⅱ) 1 mg/L, NH4+-N 1.3 mg/L, CODMn 8 mg/L),研究表明生物滤池对铁锰、氨氮和有机物有良好的净化效果。天然水体中有机物的主要组成部分是腐殖质, 占水中总有机物的50%~90%,但关于此类物质对于滤池铁锰净化性能的影响鲜有报道。随着地下水水质的日益复杂化,天然有机物和氨氮对生物过滤的应用提出了挑战, 因此, 为明确氨氮和天然有机物对滤池铁锰净化性能的影响和同池净化的可行性, 进行了净化铁锰氨天然有机污染地下水工艺启动实验, 探究了氨氮和天然有机物对滤池铁锰净化能力和铁锰去除区位的影响, 以期拓展生物净化地下水工艺的应用水质范围,为实际滤池因变更水源地或水质恶化而造成除铁锰能力和净化所需滤层厚度的变化提供参考及为工程实践提供理论依据。
1 实验 1.1 实验装置一个实验室规模的有机玻璃柱(高度2.8 m,内径9 cm)作为实验生物滤柱, 如图 1所示, 滤料是粒径为0.6~1.2 mm的除铁锰成熟锰砂, 滤床高1.5 m, 生物滤柱底部填充鹅卵石作为承托层,承托层厚20 cm, 鹅卵石的粒径为1~3 cm, 水和滤料取样口的间隔分别为100和200 mm。

|
图 1 生物滤柱示意 Fig. 1 Diagram of the biofilter column |
地下水中有机物一般是天然有机物,其主要组成部分是腐殖质, 占水中总有机物的50%~90%(质量分数),土壤腐殖质中的低分子质量组分是天然水体中腐殖质的重要来源,如吉林省敦化地区土壤中腐殖质质量浓度较高,某水源地中腐殖酸质量浓度可高达4.76 mg/L,腐殖酸钠用腐殖酸经氢氧化钠溶液萃取而成,且腐殖酸钠的溶解性强于腐殖酸,因此,实验室内利用腐殖酸钠代替腐殖酸模拟天然有机物。进水混合方式如图 1所示,通过控制进水流量和加药浓度实现对进入滤柱内各污染物浓度的控制,进而模拟滤柱对于实际地下水的净化。
进水为硫酸亚铁、硫酸锰、氯化铵、腐殖酸钠和自来水混合模拟实际地下水, 向120 L储备溶液中加入12 mL浓硫酸, 以保持Fe(Ⅱ)处于还原状态, 从而确保进水水质的稳定。通过蠕动泵将储备溶液泵入进水混合器与自来水混合, 混合后通过跌水曝气进一步增加水中溶解氧(DO)。自来水水质指标如下:水温14~17 ℃, NO3--N 1.8~5.3 mg/L, NO2--N痕量, CODMn<1.5 mg/L, pH 6.9~7.2。混合后进水水质指标如表 1所示。
| 表 1 人工配水水质 Tab. 1 Water quality indexes of synthetic groundwater |
本实验所选用滤柱为成熟的除铁锰生物滤柱并且稳定运行超过100 d, 已经具备了良好的去除铁、锰的能力。本实验分为两个阶段, 阶段Ⅰ为培养滤柱去除氨氮的能力, 自来水中加入硫酸亚铁、硫酸锰、氯化铵, 以3 m/h的滤速进入滤柱, 将一定量的曝气池上清液与原进水混合进入滤柱, 出水回流入水箱进行循环接种, 2 d检测一次进、出水中总铁、Mn2+、NH4+质量浓度, 出水达标并稳定超过7 d时, 认为铁锰氨氮净化工艺启动成功[12-13]。阶段Ⅱ在阶段Ⅰ启动成功的基础上, 进水中加入腐殖酸钠, 理论进水腐殖酸质量浓度约5 mg/L(以TOC计), 2 d检测一次进出水中总铁、Mn2+、NH4+质量浓度,高锰酸盐指数(CODMn)和UV254, 出水能稳定达标后即视为有机物净化工艺启动成功, 在每个阶段的稳定期沿程取样测定。
1.4 检测方法Fe(Ⅱ):二氮杂菲分光光度法;Mn(Ⅱ):过硫酸铵分光光度法;NH4+-N:纳氏试剂比色法;NO2--N:N-(1-萘基)-乙二胺光度法;NO3--N:紫外分光光度法;UV254:用0.45 μm的水系滤膜过滤水样, 紫外分光光度计测定水样在254 nm处的吸光度值;化学需氧量:高锰酸盐指数(酸法);DO、pH、T:便携式测定仪(Qxi 315i-WTW)。
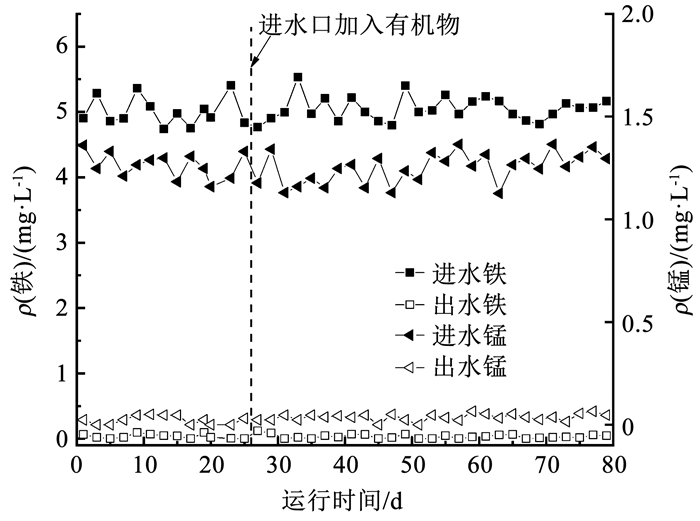
2 结果与讨论 2.1 铁锰氨天然有机污染地下水净化工艺启动 2.1.1 启动过程中铁锰净化能力启动过程中铁、锰的去除效果如图 2所示, 出水中总铁一直趋于痕量, 只有在有机物加入的当天, 出水铁质量浓度升高到0.12 mg/L, 但在2 d后, 出水铁质量浓度又恢复至痕量, 禹丽娥等[14]研究表明, 腐殖酸与Fe(Ⅱ)可形成络合物, 分析认为上述现象产生的原因为腐殖酸与Fe(Ⅱ)形成络合物沉淀在滤料上, 覆盖在Fe(Ⅱ)接触氧化触媒的表面, 影响了后续Fe(Ⅱ)的接触氧化, 但在2 d后铁氧化去除区间下移(详见2.2.2节), 下层滤料披覆了具有催化氧化能力的羟基氧化铁, 出水铁质量浓度又趋于痕量。因此, 氨氮和有机物的存在并没有影响总铁的去除效果, 其去除稳定性也得以证明。值得注意的是, 研究中天然有机物的存在会与Fe(Ⅱ)形成有机络合物, 部分异养菌可利用络合物中有机物部分, 而释放出的Fe(Ⅱ)又可经催化氧化而被去除[15], 因此,异养菌对于Fe(Ⅱ)的氧化可能有一定的协同作用。Mn(Ⅱ)的去除不同于Fe(Ⅱ), 氧气对于Mn(Ⅱ)的氧化在低于9的酸碱度下进行的非常缓慢, 大多数饮用水的pH为6~8, 在如此低的酸碱度情况下Mn(Ⅱ)不会被氧化, 因此,Mn(Ⅱ)不能通过简单的曝气和沉淀得到去除[16]。利用微生物氧化Mn(Ⅱ)在地下水处理中得到广泛应用[17],当滤层内以锰氧化菌(MnOB)为核心的生物群系增长并达到平衡时,在MnOB胞外酶的催化作用下,Mn(Ⅱ)被氧化成Mn(Ⅳ)沉积并黏附于滤料表面而得到去除。本研究所用生物滤柱为长期稳定运行的成熟生物除Mn(Ⅱ)滤柱, 因此,在开始即表现出了较强的去除Mn(Ⅱ)的能力, 氨氮和天然有机物的存在也并未造成出水Mn(Ⅱ)的超标。尽管有研究表明[18-19], 氨氮和有机物的存在会影响Mn(Ⅱ)的去除效果, 但本研究中氨氮和天然有机物的存在对滤柱的整体Mn(Ⅱ) 去除效果并无显著影响, 只是滤柱Mn(Ⅱ) 去除区位因天然有机物的存在出现了明显下移(详见2.2.2节), 在此进水Mn(Ⅱ)质量浓度下, 滤柱仍具备良好的Mn(Ⅱ) 去除能力, 并未受到氨氮和天然有机物存在的影响。
|
图 2 启动过程中铁、锰质量浓度变化 Fig. 2 Variation of iron and manganese concentrations during startup |
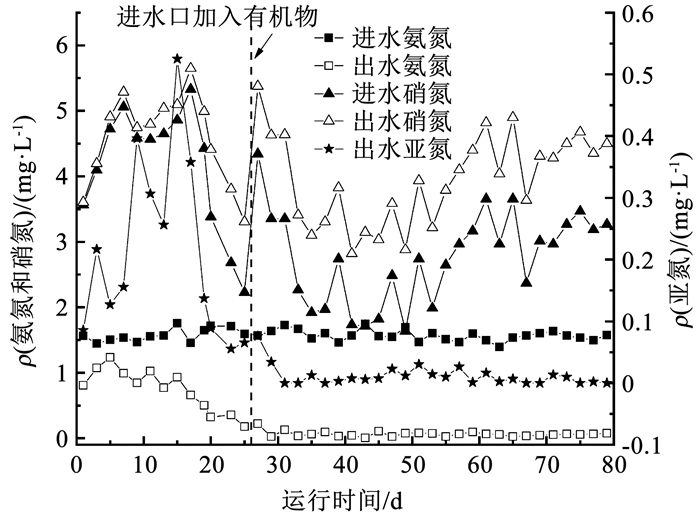
启动过程中氮素进出水的质量浓度变化见图 3。在滤柱启动之初氨氮便有去除, 但亚硝酸盐氮和硝酸盐氮的增加量小于氨氮去除量, 存在约0.5 mg/L的氮素损失, 而在2 d后出水氨氮质量浓度升高, 分析认为, 启动之初的氨氮去除是由于滤柱内滤料对氨氮的物理吸附作用[20], 而滤料的吸附位有限[21]和此时的生物硝化去除氨氮作用尚未成熟, 所以,2 d后出水氨氮质量浓度才又逐渐上升, 随着曝气池上清液的循环接种和培养时间的延长, 出水氨氮质量浓度不断降低, 硝酸盐氮的生成量也不断升高, 说明滤柱内硝化细菌逐渐发挥作用, 氨氮经氨氧化菌(AOB)转化成亚硝酸盐氮,亚硝酸盐氮经亚硝态氮氧化菌(NOB)转化成硝酸盐氮。随着培养的进行,生物硝化作用逐渐增强, 但由于AOB的适应性强于NOB, 且AOB繁殖速率高于NOB, 亚硝酸盐氮不能被及时充分硝化[22], 滤柱内出现了亚硝酸盐氮积累现象, 出水亚硝酸盐氮质量浓度最高达到0.52 mg/L。当出水氨氮质量浓度低于GB 5749—2006 《生活饮用水卫生标准》中对氨氮的限值要求0.5 mg/L时, 出水亚硝酸盐氮还居于标准线(0.1 mg/L)之上, 说明此时NOB的数量活性还不足以将由氨氮转化而成的亚硝酸盐氮充分氧化。随着滤柱的不断培养, 作为NOB繁殖基质的亚硝酸盐氮, 其出水质量浓度呈现降低趋势, 表明NOB不断繁殖和活性逐渐增强。随着NOB的不断富集, 当滤柱运行至第20天时, 出水亚硝酸盐氮降至0.08 mg/L, 出水氨氮质量浓度也降至0.3 mg/L, 去除氨氮生物滤层培养成功, 而且此后出水三氮质量浓度均在标准之下, 标志着生物硝化滤层的培养成熟[23]。在天然有机物加入后, 出水氨氮质量浓度并无升高迹象, 仍然位于0.1 mg/L以下, 可能是有机物浓度较低, 在传质充分的条件下, 能满足滤柱内硝化细菌和异养菌的最大需要, 它们之间不会产生明显的竞争, 所以,滤柱内氨氮的去除能够保持在相对稳定的状态, 并未因天然有机物的存在而出现出水氨氮质量浓度升高的现象。本实验表明, 在此有机物浓度下, 天然有机物的存在并不会造成氨氮去除效果的恶化。
|
图 3 启动过程中氮素质量浓度变化 Fig. 3 Variation of nitrogen concentration during startup |
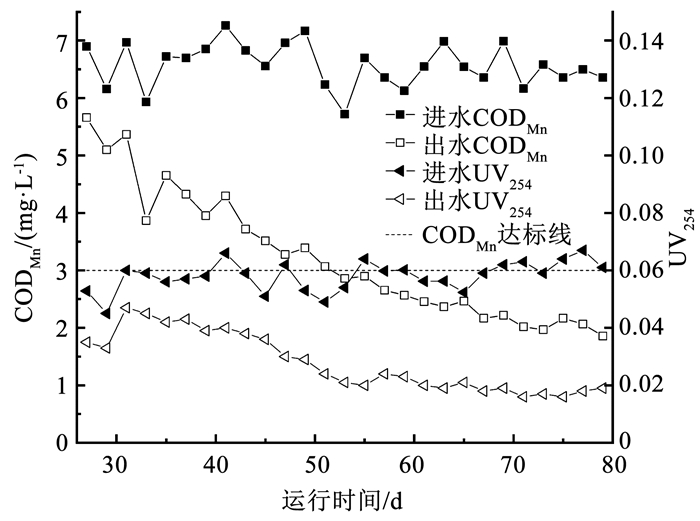
启动过程中滤柱对于CODMn、UV254的去除效果如图 4所示。杨晓敏等[24]研究表明, 在含有某种不饱和有机物单一组分的水体中, 能够通过UV254定量测定该有机物的浓度, 并且对于同一时期性质稳定的水体, 其中CODMn和UV254相关性较强, 本研究中去除CODMn和UV254的能力也是同步升高。在加入天然有机物的第1天,CODMn即有部分去除, 分析认为水中Fe(Ⅱ)和Mn(Ⅱ)被氧化、部分腐殖酸被络合和吸附共同造成了CODMn下降, 出水UV254的下降也证明了此时的确有天然有机物的去除, 但此时天然有机物应该不是经微生物分解去除, 因为滤柱之前进水中有机物极其微量, 滤柱内异养菌即便存在也是少量, 此时天然有机物应是滤柱通过络合、吸附等作用去除的。在进水中加入天然有机物15 d后, 即滤柱运行至第42天时,滤柱对CODMn的去除率已由最开始的20%升至40%, 出水CODMn略高于国家标准3 mg/L, UV254也有下降, 出水稳定在0.025左右波动, 分析认为这可能是异养菌对天然有机物分解的结果, 一部分铁锰氧化细菌能利用腐殖酸中的有机碳作为碳源来维持生命, 从而把腐殖酸降解成小分子物质, 又被分解成CO2和H2O。有研究表明[25], 在进水中有机物含量较低的情况下, 一种被称为贫养微生物的生物会在滤料上繁殖, 如芽孢杆菌、纤毛菌等, 因此, 滤柱对天然有机物会具备一定的去除能力, 在进水中加入天然有机物25 d后, 即滤柱运行至第52天时,滤柱对CODMn的去除能力又有进一步提高, 去除率达到51%, 出水CODMn约3 mg/L。并且在此后的24 d内, 出水CODMn并未超标, CODMn的去除率逐渐稳定在65%左右, 标志着滤层去除有机物能力培养成熟。滤柱对UV254的去除能力与对CODMn的去除能力同步提高, 此时UV254也一直稳定在0.015左右, 此部分天然有机物应该是微生物难以分解的较大分子有机物, 但是UV254的去除率也稳定在60%以上, 由此说明, 在本实验条件下铁、锰、氨氮和天然有机物可实现同池净化。
|
图 4 启动过程中CODMn和UV254的去除效果 Fig. 4 Removal effect of CODMn and UV254 during startup |
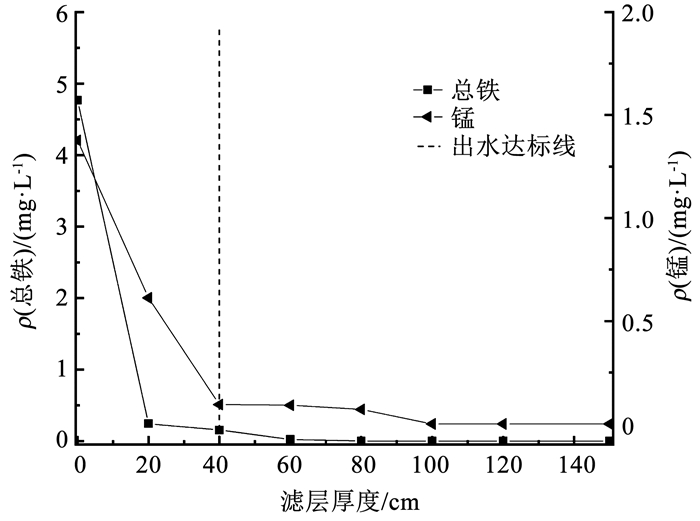
在阶段Ⅰ开始之前铁锰沿程变化如图 5所示, 当氨氮去除滤层培养成功后, 稳定期内铁、锰和三氮沿程变化如图 6所示。由于Fe(Ⅱ)的氧化还原电位低于Mn(Ⅱ)和氨氮[26], 滤柱内Fe(Ⅱ)主要是化学作用去除且化学接触速率较快, 铁优先被去除, 在滤柱内的前20 cm内即可去除绝大部分, 20 cm处出水已低于国家标准0.3 mg/L, 在40 cm处已降至痕量。由图 5和6可看出, Fe(Ⅱ)的氧化去除活性区间并未因氨氮的存在发生明显变化。
|
图 5 阶段Ⅰ开始前铁、锰沿程变化 Fig. 5 Variation of iron and manganese concentrations in the filter column before the beginning of stageⅠ |
|
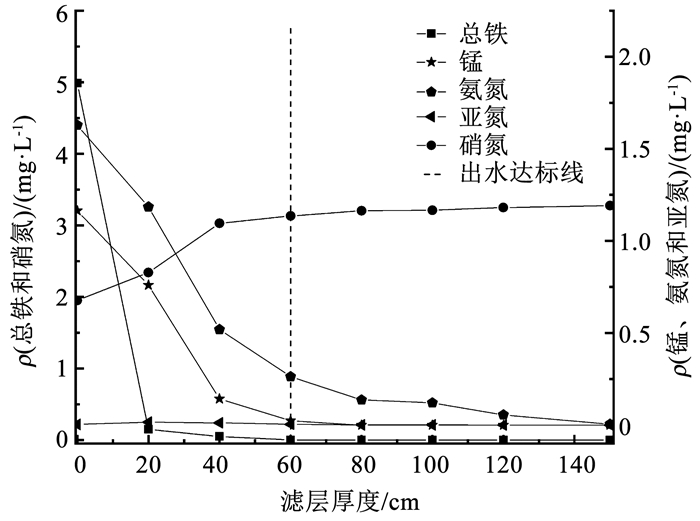
图 6 阶段Ⅰ稳定期内铁、锰和氮素沿程变化 Fig. 6 Variation of iron, manganese, and nitrogen concentrations in the filter column along the stable stageⅠ |
在进水中加入氨氮之前, 前20 cm约有0.7 mg/L的Mn(Ⅱ)去除, 在40 cm处Mn(Ⅱ)的去除率达到93%。而在氨氮存在后, 前20 cm内Mn(Ⅱ)的去除量下降至0.4 mg/L, 分析认为是氨氮对锰氧化细菌有一定的抑制作用[27]和前40 cm内的硝化细菌与锰氧化细菌竞争DO所致。值得注意的是, 本研究并未发现相关研究[28-29]中铁锰去除区间显著分级的现象, 可能因为其研究是低温启动和进水Fe(Ⅱ)质量浓度较高, 进水Fe(Ⅱ)质量浓度约为10 mg/L,明显高于本研究中进水Fe(Ⅱ)质量浓度5 mg/L, 其研究中前40 cm内Mn(Ⅱ)虽有去除, 但有更多Fe(Ⅱ)进入滤层,锰氧化物被还原, 低温(5~6 ℃)导致其滤柱内锰氧化细菌的活性低, 前40 cm内的锰氧化菌不足以将被还原出来的Mn(Ⅱ)氧化。而本研究中滤柱运行时间较久且在常温条件下, 滤柱内锰氧化细菌的活性和数量都能够满足Mn(Ⅱ)氧化去除需求, 进水中相对较低的Fe(Ⅱ)质量浓度在跌水曝气时部分即被氧化, 进入滤柱的Fe(Ⅱ)质量浓度进一步降低, 滤柱内锰氧化物被Fe(Ⅱ)还原的量较少, 被还原出来的Mn(Ⅱ)又被锰氧化细菌捕捉所氧化, 所以,结果表现为Mn(Ⅱ)在前20 cm也有部分去除。氨氮在前20 cm处的去除率为27%, 虽然其氧化困难程度要高于Fe(Ⅱ), 但是在DO充足的情况下(测得此时滤柱出水DO质量浓度约为3 mg/L), 氨氮的硝化过程和Fe(Ⅱ)的化学氧化过程是可以同时进行的, 由于在进水中氨氮和DO质量浓度都较高, 硝化细菌主要富集在滤柱的前半段, 氨氮的高效去除区间在前40 cm, 在40 cm处氨氮的去除率已经达到62%, 在60 cm处的氨氮质量浓度已符合国家标准。
由上述可知, 铁、锰和氨氮的高效去除区间重叠, 在DO充足的条件下, 铁、锰、氨氮三者的氧化顺序并不完全由其氧化还原电位决定, 一般认为, 三者的氧化顺序为Fe(Ⅱ)、氨氮、Mn(Ⅱ), 但本研究发现, 三者的氧化可同时进行, 其氧化顺序只是相对而言, 并不意味着只有前者全部氧化完成, 后者才会被氧化, 由此来看, 氨氮的存在不会造成净化所需滤层的显著增加。
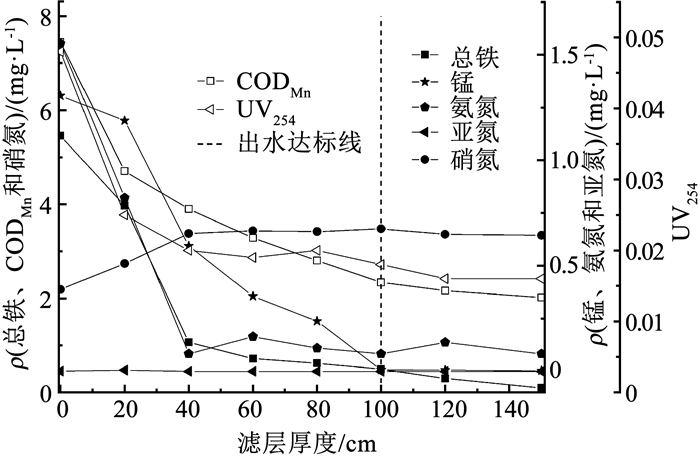
2.2.2 天然有机物对铁锰氨去除活性区位的影响阶段Ⅱ天然有机物去除滤层培养成功后, 稳定期内各污染物沿程变化如图 7所示。与未进水天然有机物时相比, Fe(Ⅱ)的去除效果和氧化速度都有明显下降, 由20 cm处总铁质量浓度可显著看出, 未加天然有机物时, 在20 cm处铁的去除率就可达到97%, 而此时20 cm处铁的去除率只有27%, 铁的高效去除区间明显下移, 在40 cm处去除率达到80%, 在滤层120 cm处Fe(Ⅱ)质量浓度方可满足国家标准, 由此可见, 天然有机物对于铁的去除影响较大。有研究表明[14], 水中天然有机物可与Fe(Ⅱ)形成络合物, 这种络合物中的Fe(Ⅱ)不易被氧气氧化, 分析认为, 由于有机络合物覆盖在滤料表面, 前20 cm内的羟基氧化铁触媒得不到再生, 阻碍了后续Fe(Ⅱ)被催化氧化, 造成前20 cm内的除铁能力严重下降, 有更多的Fe(Ⅱ)进入滤层20~40 cm内, 羟基氧化铁披覆在此滤层, 在滤层的20~40 cm内Fe(Ⅱ)去除量较大, 因此,表现为铁去除区间的下移。
|
图 7 阶段Ⅱ稳定期内铁、锰、氮素、CODMn和UV254沿程变化 Fig. 7 Variation of iron, manganese, nitrogen, CODMn, and UV254 in the filter column along the stable stageⅡ |
天然有机物的存在对于Mn(Ⅱ)去除的影响主要也是去除区间的下移, Mn(Ⅱ)的高效去除区间仍是前40 cm。未加有机物时, 前40 cm内的Mn(Ⅱ)去除率占总去除率的87%, 而此时前40 cm内的去除率占总去除率的54%, 下降了33%, 在滤层100 cm处Mn(Ⅱ)质量浓度才可满足国家标准。分析认为, 有机物的存在造成异养菌的增殖, 有文献表明[30], 有机物发生生物降解所需的氧化还原电位小于Mn(Ⅱ)氧化所需的氧化还原电位, 又经检测此时出水中DO质量浓度已经很低(约1 mg/L), 滤柱内氧分压较低,Mn(Ⅱ)氧化所需的氧化还原电位最高, 锰氧化细菌对Mn(Ⅱ)的网捕能力变差,前20 cm内Mn(Ⅱ)的氧化滞后于其他污染物的氧化, Mn(Ⅱ)随水流进入滤层下半段, 因而造成Mn(Ⅱ)去除区间的下移。
天然有机物对于氨氮去除的影响不同于对铁、锰的去除, 天然有机物的存在并未显示出负面作用, 出水氨氮质量浓度可能略高于未加有机物的滤层, 但也远远满足国家标准, 天然有机物的存在似乎加速了氨氮的去除。未加天然有机物时, 氨氮的高效去除区间在前40 cm内, 去除率为68%, 而进水中存在天然有机物后, 氨氮去除率增加明显, 前40 cm内的氨氮去除率达到95%, 硝酸盐氮在前40 cm内也大幅增加。注意到前40 cm内氨氮去除量与硝酸盐氮增加量的差值约0.2 mg/L, 相比进水中不含有机物时略有增大, 但考虑到微生物生长繁殖对氮素的消耗, 进水中有机物对氨氮的吸附作用基本可忽略不计, 氨氮经生物硝化作用转化成了硝酸盐氮, 整个滤层中亚硝酸盐氮一直处于痕量状态, 在40 cm处的出水氮素质量浓度即可满足国家标准, 此现象有悖于常规判断。一般认为, 有机物的存在会引起异养菌的增殖, 异养菌会与硝化细菌竞争空间, 造成氨氮的去除效果下降或者高效去除区间的下移。相关研究报道[25], 滤层内可能存在二级基质利用的现象, 根据其研究认为当初级基质, 如腐殖质类等物质(浓度远大于最小基质浓度)提供了微生物生长的基本碳源和能源后, 其他微量有机物即使未达到其最小基质浓度时也能被微生物利用, 滤层未进水有机物时, 硝化细菌产生的有机细胞物质堆积于滤层生物膜内, 代谢产物可能会影响硝化细菌的增殖和对氨氮的利用。而滤层内存在有机物造成异养菌的增殖, 此时硝化细菌产生的有机代谢产物可作为异养菌的电子供体而被利用, 间接地促进了硝化细菌的生长和提高了对氨氮的利用率, 在前40 cm内氨氮即可被快速且大量去除。滤层对于有机物的去除主要集中于前40 cm, 在前40 cm内CODMn的去除率占总去除率的65%, 这应该是由于滤层前半段有机物和DO质量浓度都较高, 异养菌得以快速繁殖, 部分腐殖酸也可与Fe(Ⅱ)形成络合物, 沉淀在滤料表面, 然后随反冲洗流出滤柱。前40 cm同样是UV254的高效去除区间, 去除率占总去除率的87%, 这应该与CODMn下降出于同样的原因。
由此可得, 天然有机物的存在对Fe(Ⅱ)和Mn(Ⅱ)去除区位影响最大, 在天然有机物存在之前, 出水中铁锰质量浓度达标所需滤层厚度为60 cm, 而在进水中含有天然有机物之后, 出水中铁锰质量浓度达标所需滤层厚度增至120 cm, 去除Fe(Ⅱ)和Mn(Ⅱ)所需滤层厚度显著增加。对氨氮去除区位影响最小, 对氨氮的去除表现出了一定的促进作用。
2.3 氨氮和天然有机物对反冲洗后滤柱净化性能的影响随着过滤的进行, 滤料间隙中的铁锰氧化物、微生物代谢产物和各种杂质必然越来越多, 水头损失越来越大, 运行到一定时间要对滤柱进行反冲洗, 以使滤柱恢复正常工作的能力。反冲洗过程中滤层会受到强力的水力冲刷, 滤柱反冲洗后初期,其滤层去除污染物的能力可能会有所下降[21], 因此, 对滤柱反冲洗后出水中各污染物进行分析以全面明确氨氮和天然有机物对滤层性能的影响。
在反冲洗强度为12 L/(m2 · s)和反冲洗时间为3~5 min时, 两阶段稳定期内滤柱在反冲洗后初期出水中各污染物逐时变化如图 8所示。铁锰净化滤柱在进水氨氮和天然有机物之前, 反冲洗后不需适应期出水即能达标, 去除氨氮和天然有机物滤层的培养也未对铁锰净化性能恢复造成显著影响, 出水铁锰质量浓度均能达标, 0.5 h后出水Mn(Ⅱ)在天然有机物存在后质量浓度虽有升高, 但也在0.1 mg/L以下,符合国家标准。出水氨氮质量浓度与前节分析一致, 氨氮在天然有机物存在后去除效果变好。在加入天然有机物前, 反冲洗后0.5 h出水氨氮质量浓度接近0.1 mg/L, 高于加入天然有机物后一直趋于痕量的出水氨氮质量浓度, 出水中UV254也一直处于0.015左右, 并无过高情况的出现。CODMn在反冲洗后0.5 h出水质量浓度为2.6 mg/L,高于稳定期出水, 但也在国家标准线3 mg/L以下。有研究表明,反冲洗水流和滤料颗粒的碰撞摩擦作用, 会使得滤柱内微生物随水流流出有一定的减少[31], 但本研究结果表明,随着培养的进行, 流出的微生物不足以破坏滤柱的净化性能, 因此,在反冲洗强度为12 L/(m2 · s)时,反冲洗对滤柱的各污染物去除能力并无显著影响, 当去除氨氮和天然有机物滤层培养成熟时, 适当的反冲洗对其净化性能的影响较小, 反冲洗后滤柱出水中各污染物仍不需要适应期即可达标。

|
图 8 滤柱反冲洗后初期出水中各污染物逐时变化 Fig. 8 Variation of each pollutant in initial effluent after filter column backwashing |
1) 在本实验条件下,生物同池净化铁锰氨天然有机污染(TFe 4.7~5.4 mg/L, Mn(Ⅱ) 1.1~1.3 mg/L, NH4+-N 1.4~1.8 mg/L, CODMn 5.9~7.4 mg/L)地下水工艺可实现启动并稳定运行。
2) 氨氮的存在会造成滤柱Mn(Ⅱ) 去除区间的下移, 对滤柱的铁锰去除能力无显著影响, 在DO充足的条件下, Fe(Ⅱ)、Mn(Ⅱ)和氨氮三者可同时被氧化去除。
3) 天然有机物的存在会降低滤层的铁锰去除能力,使得高效铁锰去除区间显著下移, 净化铁锰所需滤层厚度增加, 而对于氨氮的去除有一定的促进作用。
4) 适当的反冲洗不会对去除氨氮和天然有机物成熟滤层净化性能产生影响, 反冲洗后滤柱的净化性能不需要适应期。
| [1] |
冉海林, 梁伟. 环境监测中地表水监测现状分析[J]. 化工管理, 2021(8): 42. RAN Hailin, LIANG Wei. Analysis of surface water monitoring in environmental monitoring[J]. Chemical Engineering Management, 2021(8): 42. DOI:10.19900/j.cnki.ISSN1008-4800.2021.08.021 |
| [2] |
李冬, 刘孟浩, 张杰, 等. 低温地下水净化工艺中氨氮去除性能及机制[J]. 环境科学, 2021, 42(10): 1. LI Dong, LIU Menghao, ZHANG Jie, et al. Removal efficiency and mechanism of ammonia nitrogen in low temperature groundwater purification process[J]. Environmental Science, 2021, 42(10): 1. DOI:10.13227/j.hjkx.202102181 |
| [3] |
TEKERLEKOPOULOU A G, PAVLOU S, VAYENAS D V. Removal of ammonium, iron and manganese from potable water in biofiltration units: a review[J]. Journal of Chemical Technology & Biotechnology, 2013, 88(5): 751. DOI:10.1002/jctb.4031 |
| [4] |
孙群群, 屈婧祎, 童曼, 等. 地下水水化学组成对Fe(Ⅱ)氧化过程中锰氧化菌失活的影响[J]. 安全与环境工程, 2021, 28(3): 101. SUN Qunqun, QU Jingyi, TONG Man, et al. Effect of groundwater hydrochemical components on the inactivation of Mn-oxidizing bacteria upon Fe(Ⅱ) oxygenation[J]. Safety and Environmental Engineering, 2021, 28(3): 101. DOI:10.13578/j.cnki.issn.1671-1556.20201199 |
| [5] |
KOMLAN M A. 受氨氮和有机物复合污染的含铁锰地下水的处理研究[D]. 哈尔滨: 哈尔滨工业大学, 2018 KOMLAN M A. Research on treatment of groundwater containing iron and manganese contaminated by ammonia nitrogen and organic matter[D]. Harbin: Harbin Institute of Technology, 2018 |
| [6] |
HUANG B, LI Z, CHEN Z, et al. Study and health risk assessment of the occurrence of iron and manganese in groundwater at the terminal of the Xiangjiang River[J]. Environmental Science and Pollution Research, 2015, 22(24): 19912. DOI:10.1007/s11356-015-5230-z |
| [7] |
DU Xing, LIU Guangyang, QU Fangshu, et al. Removal of iron, manganese and ammonia from groundwater using a PAC-MBR system: the anti-pollution ability, microbial population and membrane fouling[J]. Desalination, 2017, 403: 97. DOI:10.1016/j.desal.2016.03.002 |
| [8] |
谈思颖. 胺类有机絮凝剂在氯胺消毒中生成亚硝胺类副产物研究[D]. 重庆: 重庆大学, 2019 TAN Siying. Study on N-nitrosamine formation from Amine-based organic flocculants during chloramintion[D]. Chongqing: Chongqing University, 2019 |
| [9] |
CHRISTENSEN J B, CHRLSTENSEN T H. The effect of pH on the complexation of Cd, Ni and Zn by dissolved organic carbon from leachate-polluted groundwater[J]. Water Research, 2000, 34(15): 3743. DOI:10.1016/S0043-1354(00)00127-5 |
| [10] |
ALBREKTIENE R, RIMEIKA M, TAMULAITIENE B, et al. Technology for treatment of groundwater simultaneously containing iron, manganese, ammonium and organic matter[J]. Journal of Water Supply: Research and Technology, 2017, 66(7/8): 665. DOI:10.2166/aqua.2017.017 |
| [11] |
杨航. 耦合自养脱氮生物滤池同步净化地下水中铁锰和氨氮技术研究[D]. 哈尔滨: 哈尔滨工业大学, 2019 YANG Hang. The study on simultaneous removal of iron, manganese and ammonia by biological filter coupling autotrophic nitrogen removal[D]. Harbin: Harbin Institute of Technology, 2019 |
| [12] |
李冬, 路健, 梁雨雯, 等. 低温生物除铁除锰工艺快速启动与滤速的探求[J]. 中国环境科学, 2016, 36(1): 82. LI Dong, LU Jian, LIANG Yuwen, et al. Quick start-up and filter speed searching of biological iron and manganese removal process[J]. China Environmental Science, 2016, 36(1): 82. DOI:10.3969/j.issn.1000-6923.2016.01.013 |
| [13] |
MANN A T, MENDOZA-ESPINOSA L, STEPHENSON T. Performance of floating and sunken media biological aerated filters under unsteady state conditions[J]. Water Research, 1999, 33(4): 1113. DOI:10.1016/S0043-1354(98)00301-7 |
| [14] |
禹丽娥. 天然有机物对饮用水生物氧化除铁的影响试验研究[D]. 长沙: 湖南大学, 2006 YU Li'e. The research on impact of natural organic matter on the biological removal of iron from drinking water[D]. Changsha: Hunan University, 2006 |
| [15] |
孙浩, 何雪英, 胡一超, 等. 铁锰氧化膜同步除微污染地表水铁锰氨氮研究进展[J]. 化工进展, 2021, 40(3): 1634. SUN Hao, HE Xueying, HU Yichao, et al. Research progress of iron-manganese oxide film simultaneous removal of iron manganese and ammonia nitrogen from micro-polluted surface water[J]. Chemical Industry and Engineering Progress, 2021, 40(3): 1634. DOI:10.16085/j.issn.1000-6613.2020-0836 |
| [16] |
VIESSMAN W, HAMMER M J. Water supply and pollution control[M]. Boston: Pearson, 1998.
|
| [17] |
张杰. 生物固锰除锰机理与工程技术[M]. 北京: 中国建筑工业出版社, 2005. ZHANG Jie. Mechanism and engineering technology of biological manganese fixation and removal[M]. Beijing: China Architecture & Building Press, 2005. |
| [18] |
W HO. Guidelines for drinking-water quality: health criteria and other supporting information[M]. Geneva: World Health Organization, 1996.
|
| [19] |
陈静. 生物除锰滤池的启动及腐殖酸对滤池稳定性的影响[D]. 哈尔滨: 哈尔滨工业大学, 2016 CHEN Jing. Set-up of biological manganese removal filters and the effects of humic acid on filters' stability[D]. Harbin: Harbin Institute of Technology, 2016 |
| [20] |
CAI Yan'an, LI Dong, LIANG Yuwen, et al. Effective start-up biofiltration method for Fe, Mn, and ammonia removal and bacterial community analysis[J]. Bioresource Technology, 2015, 176: 149. DOI:10.1016/j.biortech.2014.11.025 |
| [21] |
蔡言安. 含铁锰氨氮地下水生物净化试验研究[D]. 北京: 北京工业大学, 2015 CAI Yan'an. The research on biological purification of underground water containing ferromanganese ammonia nitrogen[D]. Beijing: Beijing University of Technology, 2015 |
| [22] |
李冬, 陶晓晓, 李占, 等. 常温SBR亚硝化快速启动及优化试验研究[J]. 环境科学, 2011, 32(6): 1653. LI Dong, TAO Xiaoxiao, LI Zhan, et al. Study on rapid start and optimization of room temperature SBR nitrification[J]. Environmental Science, 2011, 32(6): 1653. |
| [23] |
曾辉平. 含高浓度铁锰及氨氮的地下水生物净化效能与工程应用研究[D]. 哈尔滨: 哈尔滨工业大学, 2010 ZENG Huiping. Biological purification of iron, manganese and ammonia with high concentration in groundwater and engineering application[D]. Harbin: Harbin Institute of Technology, 2010 |
| [24] |
杨晓敏, 苏文洪, 黄旭冰, 等. 原水UV254与CODMn相关性研究[J]. 城镇供水, 2019(1): 34. YANG Xiaomin, SU Wenhong, HUANG Xubing, et al. Correlation study between raw water UV254 and CODMn[J]. City and Town Water Supply, 2019(1): 34. |
| [25] |
GOUZINIS A, KOSMIDIS N, VAYENAS D V, et al. Removal of Mn and simultaneous removal of NH3, Fe and Mn from potable water using a trickling filter[J]. Water Research, 1998, 32(8): 2442. DOI:10.1016/S0043-1354(97)00471-5 |
| [26] |
MOUCHET P. From conventional to biological removal of iron and manganese in France[J]. Journal AWWA, 1992, 84(4): 158. DOI:10.1002/j.1551-8833.1992.tb07342.x |
| [27] |
刘大为, 鄢姝恺, 顾雅婷. 饮用水检测中UV254替代耗氧量测定的可行性分析[J]. 供水技术, 2014, 8(6): 59. LIU Dawei, YAN Shukai, GU Yating. Feasibility analysis of UV254 replacing oxygen consumption measurement in drinking water testing[J]. Water Supply Technology, 2014, 8(6): 59. DOI:10.3969/j.issn.1673-9353.2014.06.014 |
| [28] |
李冬, 曹瑞华, 杨航, 等. 低温高铁锰氨氮地下水生物同池净化[J]. 环境科学, 2017, 38(12): 5097. LI Dong, CAO Ruihua, YANG Hang, et al. Removal of high concentration of iron, manganese and ammonia nitrogen from low temperature groundwater using single bio-filter[J]. Environmental Science, 2017, 38(12): 5097. DOI:10.13227/j.hjkx.201705096 |
| [29] |
王刘煜, 李冬, 曾辉平, 等. 生物滤池同步净化低温高铁锰氨氮地下水[J]. 中国环境科学, 2019, 39(8): 3300. WANG Liuyu, LI Dong, ZENG Huiping, et al. Simultaneous purification of low temperature and high iron, manganese and ammonia nitrogen groundwater by biological filter[J]. China Environmental Sciences, 2019, 39(8): 3300. |
| [30] |
高大文, 彭永臻, 王淑莹, 等. 利用ORP和pH控制豆制品废水的处理过程[J]. 哈尔滨工业大学学报, 2003, 35(6): 647. GAO Dawei, PENG Yongzhen, WANG Shuying, et al. Using ORP and pH to control the process of soybean wastewater treatment[J]. Journal of Harbin Institute of Technology, 2003, 35(6): 647. DOI:10.3321/j.issn:0367-6234.2003.06.003 |
| [31] |
余健. 生物过滤去除饮用水中有机物、铁和锰的特性与机理研究[D]. 长沙: 湖南大学, 2005 YU Jian. Study on the properties and mechanism of biofiltration to remove organic matter, iron and manganese from drinking water[D]. Changsha: Hunan University, 2005 |
 2023, Vol. 55
2023, Vol. 55


