2. 城市水资源与水环境国家重点实验室(哈尔滨工业大学),哈尔滨 150090
2. State Key Laboratory of Urban Water Resource and Environment (Harbin Institute of Technology), Harbin 150090, China
好氧颗粒污泥(aerboic granular sludge,AGS)因其良好的沉降性能、高生物量保持率等优势被认为是具有前景的污水处理技术之一[1],目前,有关好氧颗粒污泥的研究多在较高底物浓度的合成废水中进行,而中国生活污水普遍存在碳氮比较低的问题,进水碳源不足阻碍了其在低强度城市污水处理中的应用[2]。同步硝化内源反硝化除磷(simultaneous nitrification-endogenous denitrification and phosphorous removal,SNEDPR)工艺已被证明可节约能源、降低损耗[3],但将该工艺运用于处理实际生活污水时由于污水中难降解有机物占比高,导致有机物储存利用为聚羟基烷酸(poly-hydroxyalkanoate,PHA)过程受阻,造成长期运行过程中颗粒稳定性和脱氮除磷性能不佳[4-5]。
为了实现对有机物的水解,文献[6]提出单独设置水解酸化单元利用水解产酸菌将污水中大分子难降解有机物水解为小分子易降解有机物,但仍无法解决生活污水中COD低的问题。文献[7]表明, 初沉污泥中含有丰富的碳水化合物、蛋白质等均属于慢速可生物降解碳源,由于细菌细胞壁难以破坏,污泥中的这类碳源无法利用,若同时对生活污水和初沉污泥进行混合水解酸化,可提高进水有机物含量,为AGS提供充足挥发性脂肪酸(volatile fatty acids,VFA)促进PHA合成。文献[8]表明, 延长水解酸化工艺水力停留时间(hydraulic retention time,HRT)可以促进有机物与底物充分接触,也有研究[9]表明, HRT过长会造成水解酸化继续向产甲烷阶段运行,VFA被继续消耗,故合理调控水解酸化单元HRT有利于加强AGS厌氧PHA合成;此外,序批式反应器(sequencing batch reactor,SBR)排泥方式的不同会影响微生物菌群的相对活性和颗粒污泥稳定性,Winkler等[10]发现聚糖菌(glycogen accumulating organisms,GAOs)和亚硝酸盐氧化菌(nitrite-oxidizing bacteria,NOB)在颗粒粒径较小的污泥中占比较多,通过顶部排泥可以提升反硝化除磷性能,但文献[11]表明, 底部污泥龄过高,颗粒结构被破坏会影响系统运行长期稳定性,因此, 关于预处理单元HRT和SBR排泥方式还有待进一步研究。
实验采用SBR运行SNEDPR工艺,主要探究混合水解酸化预处理单元HRT和SBR排泥方式对AGS内碳源储存、反硝化聚磷菌(denitrifying polyphosphate accumulating organisms,DPAOs)等功能菌群活性和系统脱氮除磷特性的影响,以期为实际生活污水下同步硝化内源反硝化除磷工艺优选设计提供实验基础。
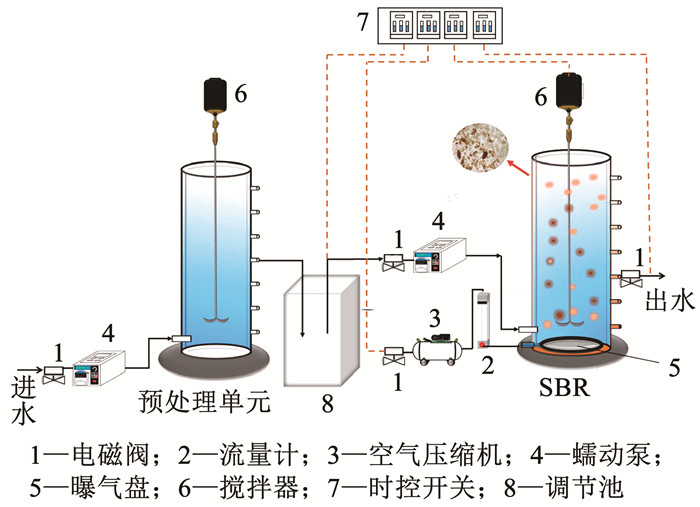
1 实验 1.1 实验装置与运行方法采用SBR反应器进行好氧颗粒污泥的培养,反应器由有机玻璃制成,高50 cm,内径14 cm,有效容积为6 L,换水比为60%。反应器壁垂直方向设置取样口,采用蠕动泵从底部进水,搅拌机进行混合,SBR底部设有曝气盘,采用鼓风曝气,反应器进料、搅拌、曝气和排水均采用时控开关自动控制。SBR前设置预处理单元,以生活污水和初沉污泥为底物(每4 d投加一次初沉污泥作为底物进料,污水与污泥体积比为10∶ 1)进行混合水解酸化,并将水解酸化液储存在调节池中作为SBR进水,控制SBR污泥龄为30 d,实验装置见图 1。SBR每天运行4个周期,以A/O/A模式运行,每周期运行6 h,包括进水5 min,沉淀3 min,排水3 min,其余时间闲置,其中好氧段曝气强度为0.8 L/min,具体运行情况如图 2。调整预处理单元HRT的实验分为3个阶段,具体参数见表 1。
|
图 1 反应器装置示意 Fig. 1 Schematic of reactor device |

|
图 2 SBR运行情况 Fig. 2 SBR operating parameters |
| 表 1 实验运行阶段及条件 Tab. 1 Experimental operation stage and conditions |
在上述实验基础上继续优化排泥方式,运行方式同上,预处理单元HRT设置为4 h,实验分为3个阶段,采取在SBR周期末沉降阶段结束后手动排泥。沉降过程中因沉降速度差异,颗粒在污泥床垂直方向不同位置发生分离,根据排除不同污泥床位置污泥设置排泥方式,其中, 阶段Ⅲ选择性排泥采取排除75%顶部和25%底部污泥方式运行,具体参数如表 2所示。
| 表 2 反应器运行工况 Tab. 2 Operational conditions of reactor |
预处理单元接种污泥取自实验室中试规模具有水解产酸性能的厌氧污泥,SBR反应器接种污泥是配水驯化的具有同步硝化反硝化除磷性能的颗粒污泥,污泥质量浓度为3 500 mg/L,实验用水为北京市某大学家属区化粪池实际生活污水,用NaHCO3和NaOH调节pH稳定,具体水质指标见表 3。
| 表 3 生活污水水质 Tab. 3 Water quality of domestic sewage |
采用国家规定的标准方法[12]对NH4+-N、NO2--N、NO3--N、MLSS、SVI和含水率等指标进行测定,DO和pH使用WTW多参数测定仪测定,颗粒粒径采用激光粒度仪(Mastersize 2000)测定。聚羟基烷酸(PHA)、糖原(Gly)分别采用有机溶剂萃取紫外分光光度法和蒽酮比色法测定[13]。VFA采用气相色谱法测定,EPS中蛋白质(PN)采用Lowry法测定,多糖(PS)采用蒽酮硫酸法测定[14]。
1.4 批次实验和计算公式在批次实验中,比氨氧化速率(specific ammonia nitrogen oxidation rate,RSAO)、比亚硝酸盐氧化速率(specific nitrite oxidation rate,RSNO)的测定方法参照文献[15],不同聚磷菌所占比例参照Hu等[16]研究方法测定,聚磷菌所占比例近似按以下公式计算:
| $ \left\{\begin{array}{l} \frac{P_{\mathrm{ONn}}}{P}=\frac{M_{\mathrm{ONn}}}{M_0} \times 100 \% \\ \frac{P_{\mathrm{ON}}}{P}=\frac{M_{\mathrm{ON}}-M_{\mathrm{ONn}}}{M_0} \times 100 \% \\ \frac{P_0}{P}=\frac{M_{\mathrm{O}}-M_{\mathrm{ON}}}{M_0} \times 100 \% \end{array}\right. $ | (1) |
式中:PONn为能利用O2、NO3-和NO2-作为电子受体的除磷菌数,PON为能利用O2和NO3-(不能利用NO2-) 作为电子受体的除磷菌数,PO为只能利用O2作为电子受体的除磷菌数,MO为单位VSS利用O2为电子受体在好氧段的吸磷量(mg/g), MON为单位VSS利用NO3-为电子受体在缺氧段的吸磷量(mg/g),MONn为单位VSS利用NO2-为电子受体的吸磷量(mg/g)。
污泥强度采用完整性系数(integrity coefficient,CI)表征,测定方法参照文献[17],计算公式为
| $ C_{\mathrm{I}}=\frac{m_1}{m_0} $ | (2) |
式中:CI为颗粒的完整性系数,用于表示污泥强度;m0和m1分别为总颗粒和经振荡后剩余完整颗粒的质量。
厌氧段被PAOs和GAOs储存为内碳源的COD量占总COD消耗量的比例CODin、PAOs在内碳源储存贡献比(PPAO)及SND效率[18](ESND)计算方法如下:
| $ \left\{\begin{array}{l} \mathrm{COD}_{\text {intra }}=\Delta \mathrm{COD}_{\mathrm{an}}-1.71 \Delta \rho\left(\mathrm{NO}_{2 \mathrm{an}}^{-}\right)-2.86 \Delta \rho\left(\mathrm{NO}_{3 \mathrm{an}}^{-}\right) \\ \mathrm{COD}_{\text {in }}=\frac{\mathrm{COD}_{\text {intra }}}{\Delta \mathrm{COD}_{\mathrm{an}}} \times 100 \% \end{array}\right. $ | (3) |
| $ 0.5 P_{\mathrm{PAO}}=\rho_{\mathrm{PRA}} / \mathrm{COD}_{\text {intra }} $ | (4) |
| $ E_{\mathrm{SND}}=\left[1-\frac{\Delta \rho\left(\mathrm{NO}_2^{-}\right)+\Delta \rho\left(\mathrm{NO}_3^{-}\right)}{\Delta \rho\left(\mathrm{NH}_4^{+}\right)}\right] \times 100 \% $ | (5) |
式中:CODintra为内碳源储存量;ΔCODan、Δρ(NO2an-)和Δρ(NO3an-)为厌氧段COD、NO2-和NO3-质量浓度变化,mg/L;1.71和2.86分别为异养菌反硝化单位NO2-和NO3-所消耗的COD量(以N与COD质量比计),mg/mg;ρPRA为厌氧段释磷量,mg/L;0.5为PAOs厌氧条件下吸收单位有机碳源释放的磷量,mol/mol;Δρ(NO2-)、Δρ(NO3-)、Δρ(NH4+) 分别为好氧段NO2-、NO3-和NH4+质量浓度变化,mg/L。
2 结果和讨论 2.1 预处理单元HRT优化 2.1.1 系统处理性能图 3为不同阶段系统COD、TN、TP去除情况,刚接种生活污水时由于微生物需要适应新的进水环境,SBR出水COD和TN、TP均有所增加,并在一周内恢复至正常。图 3(a)为运行过程中COD变化,整个运行过程中系统出水COD保持在50 mg/L以下,COD平均去除率为87.7%,出水符合国家污水排放一级A标准,说明预处理单元HRT的改变对系统COD的去除影响不大。

|
图 3 运行过程中COD、TN和TP变化 Fig. 3 Variation of COD, TN, and TP during operation |
在阶段Ⅰ,由于生活污水成分复杂,难降解有机物多,以较高HRT运行,保证了微生物与底物接触时间。由图 3(a)可以看出,水解酸化液中VFA约占60%,SBR内大部分COD在厌氧段被消耗,以PHA的形式储存到细胞内,平均内碳源储存率(CODin)达90.09%,证明水解酸化预处理可以有效提升生活污水的碳源利用率。但阶段Ⅰ的SBR进水COD低于生活污水水质,COD出现了较大损耗,主要是采用12 h的HRT,污水在反应器中的停留时间过长。Wang等[8]通过正交测试发现,HRT过长会造成底物继续向产甲烷阶段转化,VFA消耗速率大于产生速率是造成有机物损耗的主要原因,后续SBR厌氧PHA存储不足。阶段Ⅰ的VFA主要由乙酸、丙酸和异戊酸组成,以乙酸为主,对于较大分子质量VFA异戊酸,研究表明,细菌产生异戊酸的代谢途径复杂,所需的反应时间较长[19],阶段Ⅰ较长反应时间可能是异戊酸产生的原因。阶段Ⅱ将HRT调至8 h后,预处理单元COD损耗减小,VFA占比增加,VFA组分中异戊酸减少,同时出现正丁酸组分,说明调整HRT会引起水解酸化液组分的改变。阶段Ⅲ,VFA占比继续增加至77%左右,乙酸、丙酸和丁酸质量浓度增加,异戊酸占比降低,SBR厌氧CODin增加至96.5%左右。文献[10]指出,反硝化优先利用乙酸,其次为丁酸和丙酸,最后是戊酸; Chen等[20]指出适宜作为除磷碳源的两种有机酸为乙酸和丙酸。因而缩短HRT水解酸化液中组分的优化可能是脱氮除磷效果逐渐变好的原因,同时,混合VFA不同组分可为反硝化和除磷过程相关的各个细菌提供不同碳源,因而微生物对碳源利用率高,实现了SBR厌氧内碳源的高储存。
图 3(b)为运行过程中TN变化,水解酸化单元TN略有升高,主要是混合水解污泥释放氨氮的同时微生物生长需要消耗氨氮,造成质量浓度略有升高。生活污水氨氮质量浓度波动大,在阶段Ⅰ好氧颗粒污泥中部分氨氮未反应完全,造成TN去除效率低。随着反应进行,微生物逐渐适应生活污水水质,硝化性能得以恢复,但HRT过长导致的COD损失,造成出水TN仍未能达到污水排放一级A标准。到阶段Ⅲ缩短HRT后,预处理单元出水VFA大幅增加,且主要由乙、丙酸组成,好氧颗粒污泥反硝化性能提升,出水平均TN降至9.0 mg/L,出水TN达到污水一级A排放标准(15 mg/L)。
由图 3(c)可以看出,SBR厌氧磷释放量和CODin变化一致,阶段Ⅰ较长HRT使SBR进水COD偏低,厌氧内碳源存储不足,释磷量不足,影响PAOs和DPAOs的除磷效果,TP去除率仅为83%左右。阶段Ⅱ将HRT缩短后,预处理VFA增加,SBR进水基质中碳磷比增加,TP去除率逐渐恢复至90%,直至阶段Ⅲ去除率增加至92.5%,出水仍未稳定在0.5 mg/L以下,其原因可能是GAOs在厌氧阶段争夺碳源造成PAOs内碳源存储能力不佳。
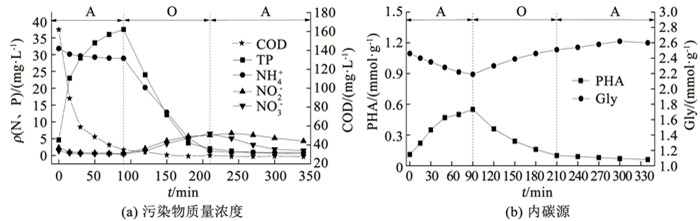
2.1.2 系统污染物去除机制由系统运行过程中污染物变化情况可以看出,反应器在S1-Ⅲ脱氮除磷效果提升。为进一步探究该阶段SBR污染物去除机制,在第60天分析了典型周期中COD、NH4+、NO2-、NO3-、TP和细胞内碳源变化,结果如图 4所示。在厌氧前30 min,反应器内NOx-变化明显,表明反硝化菌利用外碳源将残余的NOx-反硝化。厌氧末COD和GLy(单位VSS的C量)分别为34.8 mg/L、2.19 mmol/g,PO43-和PHA(单位VSS的C量)分别为37.5 mg/L、0.55 mmol/g,经计算,反应器厌氧段Δn(Gly)/Δn(PHA)为0.61,此值高于PAOs的理论模型值0.385[21],表明过多的Gly被利用但没有PHA的合成,这与GAOs增殖有关。厌氧段微生物将废水中的VFA吸收以PHA形式储存,造成COD下降并伴随磷的释放,根据式(3)计算得厌氧阶段CODintra为121.34 mg/L,约有高达95.4%的COD被PAOs和GAOs储存为内碳源,说明优化预处理单元HRT可以促进好氧颗粒污泥内碳源的贮存。
|
图 4 典型周期内污染物质量浓度和细胞内碳源变化 Fig. 4 Changes in pollutant concentrations and intracellular carbon source in typical cycles |
在好氧阶段刚开始时,PHA被氧化,PO43-质量浓度迅速降低,COD几乎未发生改变,表明脱氮和除磷过程都是通过消耗内碳源完成,由于GAOs在好氧阶段每消耗1 mol的PHA生成0.95 mol糖原,而PAOs每消耗1 mol的PHA只生成0.42 mol糖原[22],Δn(Gly)/Δn(PHA)(0.71)表明PAOs和GAOs共同参与了PHA的氧化。在整个好氧段约有27.60 mg/L的NH4+被氧化成NOx-(11.56 mg/L),NOx-质量浓度增加量小于NH4+质量浓度减小量,说明发生了同步硝化反硝化。经计算SND效率为58.1%,增强的SND主要是由于预处理单元提供了充足VFA供微生物贮存为内碳源用于反硝化NOx-,同时好氧段还存在NO2-的积累现象,推测可能发生了短程硝化反硝化反应。在缺氧阶段,PO43-质量浓度由2.01 mg/L降至0.52 mg/L,同时NOx-由12.50 mg/L下降至6.00 mg/L,表明此阶段发生了内源反硝化除磷作用。而由图 4可知,缺氧阶段NO2-质量浓度呈先升高后降低趋势,这是由于DGAOs对NO3-还原率高于NO2-,其优先利用NO3-作为电子受体进行反硝化脱氮,造成NO2-先上升,在缺氧段后期PHA几乎耗尽后观察到Gly有所下降,文献[23]表明,缺氧后反硝化可以由糖原驱动以改善氮的去除,因此,缺氧段反硝化可能是PHA和Gly共同驱动。
计算和实验结果表明,优化预处理单元HRT实现了PAOs和GAOs中细胞内碳源(PHA)的充足贮存,为SND、后置反硝化和P吸收提供充足碳源,加强内源性微生物反硝化和除磷。
2.2 排泥方式优化 2.2.1 颗粒物理特性变化不同排泥方式会对污泥物理特性产生影响,图 5为不同排泥方式下长期运行过程中反应器内搅拌混合均匀颗粒的粒径、沉降性能、含水率和污泥强度(以完整性系数表征)变化。

|
图 5 运行过程中颗粒粒径、SVI、完整性系数和含水率变化 Fig. 5 Changes in particle size, SVI, integrity coefficient, and moisture content during operation |
由图 5(a)粒径分布可以看出,阶段Ⅰ反应器内粒径在1 200 μm以上的颗粒占比明显降低,小于300 μm的颗粒占比增加。文献[24]表明,粒径的过度增长会造成基质传递受限,影响颗粒污泥的稳定性。阶段Ⅰ通过底部排泥将较大粒径的颗粒排除系统,新形成的小粒径颗粒积累,小颗粒与大颗粒共同竞争营养物质,控制了粒径的过度生长。但由图 5(b)SVI曲线可以看出,阶段Ⅰ系统SVI值上升,说明系统沉降性能变差,原因是底部排泥排出了大量沉降性能好的颗粒污泥,造成大颗粒的SRT过短,小颗粒污泥的SRT过长,沉降性能变差。
阶段Ⅱ通过将排泥方式转变为顶部排泥,颗粒粒径分布占比发生显著变化,其中,低于300 μm的小颗粒占比降低,1 200 μm以上的颗粒占比显著增加,污泥的沉降性能恢复。但此阶段颗粒强度降低到78.5%左右,文献[25]认为,CI低于0.80时表明颗粒污泥强度受到破坏,可见顶部排泥方式导致颗粒强度变差,这是由于反应器内存在大量成熟老化的颗粒污泥,Zhu等[26]认为颗粒粒径过大造成颗粒内部区域出现空腔,使颗粒结构的强度和内聚力降低,造成颗粒稳定性差。同时,阶段Ⅱ含水率逐渐下降,文献[27]指出,好氧颗粒的孔隙率随着颗粒粒径的增加而减少,阶段Ⅱ大粒径颗粒占比过高造成孔隙率低、含水率下降,导致基质无法传递到颗粒内部,影响反硝化性能。阶段Ⅲ在总SRT不变下,通过选择性排出底部老化颗粒污泥和顶部细小颗粒,观察到SBR内0.5~0.9 mm的粒径显著增加,约占总体积的40%以上,颗粒粒径分布集中。据报道[28],500~900 μm的颗粒具有更高的N去除能力,因为500~900 μm的颗粒可以提供厌氧、缺氧和好氧的微观环境,提高系统的硝化反硝化性能,这也是阶段Ⅲ污染物去除性能得到提升的主要原因。同时,阶段Ⅲ系统SVI平均值为33 mL/g,CI达90%以上,颗粒的沉降速度及强度均有所提升。因此,选择性排泥方式通过控制好氧颗粒粒径,形成结构密实、强度高的颗粒,保证工艺的稳定运行。
2.2.2 功能菌活性变化为进一步了解不同排泥方式对微生物菌群的影响,对3个阶段稳定期的污泥进行批次实验,分析不同排泥方式下污泥中聚磷菌活性、AOB和NOB活性以及不同电子受体聚磷菌所占比例。
由表 4可知,3个阶段的RSAO变化不大,说明排泥方式的改变对AOB活性影响不大。但RSNO变化较大,阶段Ⅰ的RSNO为2.34 mg/(g · h),而阶段Ⅱ和阶段Ⅲ的RSNO降低,说明NOB活性下降。Volcke等[29]认为NOB倾向生长在好氧区所占体积比例较高的小粒径颗粒中,而顶部污泥多为沉降性能较差的小粒径颗粒,因此,通过顶部排泥或选择性排出较大比例的顶部污泥可以选择性去除NOB,同时,文献[30]表明,水解酸化液中富里酸(HA)对NOB和AOB的不同限制导致了更多NO2-积累。因此,在水解酸化预处理下通过优化排泥方式可以进一步促进短程硝化的发生。
| 表 4 不同阶段SBR比氨氧化速率、比亚硝酸盐氧化速率、SND效率和Δρ(P)/ΔCOD Tab. 4 RSAO, RSNO, SND efficiency, and Δρ(P)/ΔCOD of SBR in different stages |
在厌氧条件下,VFA通过消耗多磷酸盐(poly-P)和糖原转化为PHA,PAOs的活性可由每摩尔厌氧P释放量与每摩尔COD吸收量之比(Δρ(P)/ΔCOD)反映,其中,PAOs的标准厌氧化学计量参数Δρ(P)/ΔCOD根据文献[31]显示为0.5,而GAOs的比率则为0[32]。由表 4可知,阶段Ⅰ在底部排泥方式下,Δρ(P)/ΔCOD为0.19,表明PAOs活性较差,阶段Ⅱ的Δρ(P)/ΔCOD为0.30,PAOs活性有所增加。Winkler等[10]认为PAO在大而致密的颗粒中占主导地位,而GAOs主要分布在污泥顶部,阶段Ⅱ顶部排泥更有利于富集PAOs, 但富集效果低于阶段Ⅲ。Zhang等[33]提出反应器中含有大量老化颗粒会造成颗粒稳定性差,尽管阶段Ⅲ去除部分底部污泥会损失一部分PAOs,但也促进了PAOs的新生长,可避免运行过程中除磷性能恶化,因此,采取选择性排泥的方式可抑制GAOs生长,促进PAOs富集,提高除磷性能。
表 4中SND效率为不同阶段的同步硝化反硝化效率,可以看出,阶段Ⅲ的SND效率最高。阶段Ⅰ的SND效率仅为52%,主要是由于反应器内小颗粒占比较多,颗粒内部缺氧区的缺乏造成反硝化效果不佳。而阶段Ⅱ颗粒强度稳定性变差、新生颗粒污泥的不足及好氧硝化体积分数较低造成SND效率低。阶段Ⅲ颗粒粒径分布均匀,颗粒的氧气和底物传质使细菌分层分布增强SND效果,避免了亚硝酸盐积累导致游离亚硝酸抑制养分去除过程,增强了系统同步硝化内源反硝化脱氮和除磷效果,系统TN去除率达86.38%,出水TN质量浓度降低至8.17 mg/L,达到GB 18918—2002《城镇污水处理厂污染物排放标准》的一级A标准。
为进一步探究不同类型聚磷菌占比情况,根据Hu等[16]的实验方法和计算公式进行了批次实验。如表 5所示,3个阶段不同类型聚磷菌占比发生明显变化,其中,阶段Ⅰ仅能利用O2的聚磷菌数(PO)占比较多(46.69%),主要是由于阶段Ⅰ反应器内粒径较小的颗粒占比增加,颗粒内部缺乏缺氧区,造成反硝化除磷性能差。阶段Ⅱ和阶段Ⅲ能利用O2、NO3-和NO2-的反硝化聚磷菌数(PONn)占比显著增加,主要是由于阶段Ⅱ和Ⅲ通过排出全部或部分顶部污泥将NOB淘洗,可以驯化出利用NO2-为电子受体的DPAOs(占比达40.5%),证明亚硝酸盐可以作为氧气或硝酸盐的替代电子受体,而以NO2-为电子受体的短程反硝化除磷可以进一步节省碳源,提高除磷效率,系统TP去除率达94.71%,出水TP质量浓度稳定在0.5 mg/L以下,达到GB 18918—2002《城镇污水处理厂污染物排放标准》的一级A标准。
| 表 5 不同阶段下反硝化聚磷菌占比变化 Tab. 5 Variation of content of denitrifying polyphosphate accumulating organisms in different stages |
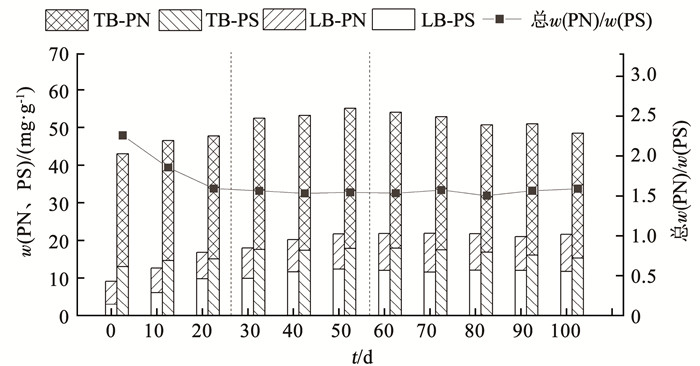
根据结构不同EPS可以进一步区分为松散附着EPS(LB-EPS)和紧密黏附EPS(TB-EPS),不同组分质量分数直接影响污泥的理化特性和颗粒稳定性的维持。如图 6所示,阶段Ⅰ LB-EPS显著增加,过量的LB-EPS会对生物絮凝和泥水分离产生不利影响[34],导致颗粒污泥较高的SVI值,与上述测量结果一致。阶段Ⅱ总EPS显著增加,这与该阶段反应器内较多大粒径的老化颗粒有关,当颗粒尺寸变大时,过量的EPS导致基质传递通道被阻塞,这可能是阶段Ⅱ孔隙率低、含水率不足的原因,同时会造成颗粒内部缺氧区反硝化性能变差。阶段Ⅲ的LB-EPS和TB-EPS都无显著变化,说明排出一定量的老化颗粒可以避免EPS的过量积累。在整个运行期间,PN质量分数变化很小,主要是PS质量分数发生改变,总PN与PS质量分数比从2.25下降到1.55左右,并趋于平缓。文献[35]表明,PS在维持颗粒结构完整性方面具有重要作用,可以增强细胞的内聚力和黏附力,PS的分泌保证反应器稳定运行。
|
图 6 运行过程中TB-PN、TB-PS、LB-PN、LB-PS及PN与PS质量分数比变化 Fig. 6 Variation of TB-PN, TB-PS, LB-PN, LB-PS, and PN/PS during operation |
1) 以生活污水(COD约250 mg/L、TN约50 mg/L、TP约5 mg/L) 和初沉污泥(每4 d投加一次污泥,污水与污泥体积比为10∶ 1)为底物进行混合水解酸化预处理,随着预处理单元HRT从12 h逐渐缩短至4 h,水解酸化液提供的乙、丙酸质量浓度和VFA占比提高,实现了AGS中PAOs和GAOs的PHA充足贮存,从而提高了SND和内源反硝化除磷效率,出水COD保持在50 mg/L以下,TN降至7.8 mg/L左右。
2) 以选择性排泥方式运行的系统内颗粒粒径集中在0.5~0.9 mm,颗粒结构密实、强度高,细菌的分层分布增强SND效果。批次实验表明,选择性排除顶部小粒径颗粒可以淘洗NOB和GAOs,系统中NO2-为电子受体的DPAOs占比提升,内源反硝化效率进一步提升。
3) 反应器以调整预处理单元HRT和选择性排泥促进了PHA的贮存和AOB、DPAOs等功能菌群的富集,颗粒强度高、沉降性能好,适量EPS的分泌维持了颗粒稳定性,出水TN和TP均达到GB 18918—2002《城镇污水处理厂污染物排放标准》的一级A标准。
| [1] |
ADAV S S, LEE D J, SHOW K Y, et al. Aerobic granular sludge: recent advances[J]. Biotechnology Advances, 2008, 26(5): 412. DOI:10.1016/j.biotechadv.2008.05.002 |
| [2] |
CAI Fangrui, LEI Lirong, LI Youming, et al. A review of aerobic granular sludge (AGS) treating recalcitrant wastewater: refractory organics removal mechanism, application and prospect[J]. Science of the Total Environment, 2021, 782: 146852. DOI:10.1016/j.scitotenv.2021.146852 |
| [3] |
ZENG R J, LEMAIRE R, YUAN Z, et al. Simultaneous nitrification, denitrification, and phosphorus removal in a lab-scale sequencing batch reactor[J]. Biotechnology and Bioengineering, 2003, 84(2): 172. DOI:10.1002/bit.10744 |
| [4] |
DERLON N, WAGNER J, DA COSTA R, et al. Formation of aerobic granules for the treatment of real and low-strength municipal wastewater using a sequencing batch reactor operated at constant volume[J]. Water Research, 2016, 105: 341. DOI:10.1016/j.watres.2016.09.007 |
| [5] |
WANG Hongyu, SONG Qun, WANG Jing, et al. Simultaneous nitrification, denitrification and phosphorus removal in an aerobic granular sludge sequencing batch reactor with high dissolved oxygen: effects of carbon to nitrogen ratios[J]. Science of the Total Environment, 2018, 642: 1146. DOI:10.1016/j.scitotenv.2018.06.081 |
| [6] |
YU Cheng, WANG Kaijun, TIAN Chen, et al. Aerobic granular sludge treating low-strength municipal wastewater: efficient carbon, nitrogen and phosphorus removal with hydrolysis-acidification pretreatment[J]. Science of the Total Environment, 2021, 792: 148297. DOI:10.1016/j.scitotenv.2021.148297 |
| [7] |
李晓玲, 彭永臻, 韩博涛, 等. 不同pH值下初沉污泥与二沉污泥厌氧发酵对比[J]. 中国给水排水, 2016, 32(3): 16. LI Xiaoling, PENG Yongzhen, HAN Botao, et al. Comparative study on primary sludge and secondary sludge in anaerobic fermentation at different pH values[J]. China Water & Wastewater, 2016, 32(3): 16. |
| [8] |
WANG Dong, WANG Guowei, XU Xiaochen, et al. Multiple factors influencing anaerobic acidogenic pretreatment in an up-flow non-woven biofilm reactor[J]. Chemical Engineering Journal, 2013, 221: 38. DOI:10.1016/j.cej.2013.01.104 |
| [9] |
ELEFSINIOTIS P, WAREHAM D G, SMITH M O. Use of volatile fatty acids from an acid-phase digester for denitrification[J]. Journal of Biotechnology, 2004, 114(3): 290. DOI:10.1016/j.jbiotec.2004.02.016 |
| [10] |
WINKLER M K H, BASSIN J P, KLEEREBEZEM R, et al. Selective sludge removal in a segregated aerobic granular biomass system as a strategy to control PAO-GAO competition at high temperatures[J]. Water Research, 2011, 45(11): 3293. DOI:10.1016/j.watres.2011.03.024 |
| [11] |
郑珍珍. 排泥方式及泥龄对好氧颗粒污泥脱氮除磷的影响[D]. 武汉: 华中科技大学, 2012 ZHENG Zhenzhen. Study on nitrogen and phosphorus removal by aerobic granular sludge with different sludge removal modes[D]. Wuhan: Huazhong University of Science and Technology, 2012 |
| [12] |
国家环境保护局. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002: 100. State Environmental Protection Administration. Monitoring and analysis methods of water and wastewater[M]. 4th ed.. Beijing: China Environmental Science Press, 2002: 100. |
| [13] |
李夕耀, 彭永臻, 王淑莹, 等. 聚磷菌胞内多聚物的分析检测方法[J]. 四川环境, 2009, 28(2): 107. LI Xiyao, PENG Yongzhen, WANG Shuying, et al. Analysis and detection method of intracellular polymer of phosphorus accumulating bacteria[J]. Sichuan Environment, 2009, 28(2): 107. |
| [14] |
FRLUND B, GRIEBE T, NIELSEN P H. Enzymatic activity in the activated-sludge floc matrix[J]. Applied Microbiology and Biotechnology, 2004, 43(4): 758. DOI:10.1007/BF00164784 |
| [15] |
李冬, 刘博, 王文琪, 等. 污泥龄对除磷亚硝化颗粒系统的影响[J]. 环境科学, 2019, 40(11): 5050. LI Dong, LIU Bo, WANG Wenqi, et al. Effect of solid retention time on phosphorus removal and nitrosation granules system[J]. Environmental Science, 2019, 40(11): 5050. |
| [16] |
HU J Y, ONG S L, NG W J, et al. A new method for characterizing denitrifying phosphorus removal bacteria by using three different types of electron acceptors[J]. Water Research, 2003, 37(14): 3463. DOI:10.1016/S0043-1354(03)00205-7 |
| [17] |
TAY J H, LIU Q S, LIU Y. Characteristics of aerobic granules grown on glucose and acetate in sequential aerobic sludge blanket reactors[J]. Environmental Technology, 2002, 23(8): 933. DOI:10.1080/09593332308618363 |
| [18] |
WANG Xiaoxia, WANG Shuying, XUE Tonglai, et al. Treating low carbon/nitrogen (C/N) wastewater in simultaneous nitrification-endogenous denitrification and phosphorous removal (SNDPR) systems by strengthening anaerobic intracellular carbon storage[J]. Water Research, 2015, 77: 195. DOI:10.1016/j.watres.2015.03.019 |
| [19] |
YAN Yuanyuan, FENG Leiyu, ZHANG Chaojie, et al. Ultrasonic enhancement of waste activated sludge hydrolysis and volatile fatty acids accumulation at pH 10.0[J]. Water Research, 2010, 44(11): 3332. DOI:10.1016/j.watres.2010.03.015 |
| [20] |
CHEN Yinguang, RANDALL A A, MCCUE T. The efficiency of enhanced biological phosphorus removal from real wastewater affected by different ratios of acetic to propionic acid[J]. Water Research, 2004, 38(1): 30. DOI:10.1016/j.watres.2003.08.025 |
| [21] |
COMA M, VERAWATY M, PIJUAN M, et al. Enhancing aerobic granulation for biological nutrient removal from domestic wastewater[J]. Bioresource Technology, 2012, 103(1): 102. DOI:10.1016/j.biortech.2011.10.014 |
| [22] |
ZENG R J, VAN LOOSDRECHT M C M, YUAN Z, et al. Metabolic model for glycogen-accumulating organisms in anaerobic/aerobic activated sludge systems[J]. Biotechnology and Bioengineering, 2003, 81(1): 92. DOI:10.1002/bit.10455 |
| [23] |
COATS E R, MOCKOS A, LOGE F J. Post-anoxic denitrification driven by PHA and glycogen within enhanced biological phosphorus removal[J]. Bioresource Technology, 2010, 102(2): 1020. DOI:10.1016/j.biortech.2010.09.104 |
| [24] |
ZHANG Cuiya, ZHANG Hanmin, YANG Fenglin. Diameter control and stability maintenance of aerobic granular sludge in an A/O/A SBR[J]. Separation and Purification Technology, 2015, 149: 362. DOI:10.1016/j.seppur.2015.06.010 |
| [25] |
GHANGREKAR M M, ASOLEKAR S R, JOSHI S G. Characteristics of sludge developed under different loading conditions during UASB reactor start-up and granulation[J]. Water Research, 2005, 39(6): 1126. DOI:10.1016/j.watres.2004.12.018 |
| [26] |
ZHU Liang, YU Yanwen, DAI Xin, et al. Optimization of selective sludge discharge mode for enhancing the stability of aerobic granular sludge process[J]. Chemical Engineering Journal, 2013, 217: 442. DOI:10.1016/j.cej.2012.11.132 |
| [27] |
LIU Yongqiang, TAY J H. Fast formation of aerobic granules by combining strong hydraulic selection pressure with overstressed organic loading rate[J]. Water Research, 2015, 80: 259. DOI:10.1016/j.watres.2015.05.015 |
| [28] |
WANG Lan, ZHENG Ping, XING Yajuan, et al. Effect of particle size on the performance of autotrophic nitrogen removal in the granular sludge bed reactor and microbiological mechanisms[J]. Bioresource Technology, 2014, 157: 242. DOI:10.1016/j.biortech.2014.01.116 |
| [29] |
VOLCKE E I P, PICIOREANU C, DE BAETS B, et al. Effect of granule size on autotrophic nitrogen removal in a granular sludge reactor[J]. Environmental Technology, 2010, 31(11): 1273. DOI:10.1080/09593331003702746 |
| [30] |
ZHANG Shaoyuan, WANG Jusi, JIANG Zhaochun, et al. Nitrite accumulation in an attapulgas clay biofilm reactor by fulvic acids[J]. Bioresource Technology, 2000, 73(1): 92. DOI:10.1016/S0960-8524(99)00133-9 |
| [31] |
LANHAM A B, OEHMEN A, SAUNDERS A M, et al. Metabolic modelling of full-scale enhanced biological phosphorus removal sludge[J]. Water Research, 2014, 66: 285. DOI:10.1016/j.watres.2014.08.036 |
| [32] |
BRDJANOVIC D, VAN LOOSDRECHT M C M, HOOIJMANS C M, et al. Temperature effects on physiology of biological phosphorus removal[J]. Journal of Environmental Engineering, 1997, 123(2): 146. DOI:10.1061/(ASCE)0733-9372(1997)123:2(144) |
| [33] |
ZHANG Hanmin, DONG Feng, JIANG Tao, et al. Aerobic granulation with low strength wastewater at low aeration rate in A/O/A SBR reactor[J]. Enzyme and Microbial Technology, 2011, 49(2): 217. DOI:10.1016/j.enzmictec.2011.05.006 |
| [34] |
LI X Y, YANG S F. Influence of loosely bound extracellular polymeric substances (EPS) on the flocculation, sedimentation and dewaterability of activated sludge[J]. Water Research, 2007, 41(5): 1024. DOI:10.1016/j.watres.2006.06.037 |
| [35] |
罗曦, 雷中方, 张振亚, 等. 好氧/厌氧污泥胞外聚合物(EPS)的提取方法研究[J]. 环境科学学报, 2005, 25(12): 1626. LUO Xi, LEI Zhongfang, ZHANG Zhenya, et al. Study on extraction method of extracellular polymer (EPS) from aerobic/anaerobic sludge[J]. Journal of Environmental Science, 2005, 25(12): 1626. |
 2023, Vol. 55
2023, Vol. 55


