2. 广东工业大学 土木与交通工程学院,广州 511400
2. School of Civil and Transportation Engineering, Guangdong University of Technology, Guangzhou 511400, China
当水体发生富营养化时,氮、磷等营养元素过度累积,导致大规模的蓝藻水华现象。尽管常规水处理工艺如气浮、混凝和过滤能有效去除藻细胞,但藻类代谢过程中释放的藻毒素、嗅味物质及胞外有机物(EOM)难以被这些工艺有效去除[1]。EOM是一种生物聚合物,富含多糖、蛋白质和脂肪等有机物,易与水中无机物结合形成有机胶体,严重干扰水处理工艺和出水水质[2]。例如,在高藻期原水中,EOM质量浓度较高,易与混凝剂发生络合反应,增加混凝剂需求量[3]。
EOM还是消毒副产物(DBPs)的主要前体物[4],滤池出水中富存的EOM会显著增加氯化消毒过程中DBPs的生成。相比天然有机物(NOM),EOM虽产生较少含碳消毒副产物(C-DBPs),因其含氮有机物质量浓度较高,更易生成高毒性的含氮消毒副产物(N-DBPs)及卤代醛[5]。尽管现有技术如混凝- 沉淀、过滤、吸附、氧化等可用于EOM去除[6],但实现其有效去除仍具挑战,对饮用水安全构成严重威胁。因此,开发高效的EOM处理工艺,实现有机质全面去除及DBPs控制,成为水处理领域亟待解决的难题。
近年来,基于硫酸根自由基(SO4· -,2.5~3.1 V) 的髙级氧化技术(AOPs)在去除难降解污染物领域得到了广泛研究。相比羟基自由基(HO· ,1.8~2.7 V),SO4· -表现出更广的pH适用范围、对目标物的选择性以及更长的半衰期等优势[7]。SO4· -可通过加热、紫外(UV)辐照、过渡金属催化、超声等方式活化过硫酸盐(S2O82-,PS)或过硫酸氢盐(HSO5-,PMS)生成[8],实现对目标污染物的有效降解。真空紫外(VUV,紫外光波段为100~200 nm)也应用于激发SO4· -和HO· ,其优势在于185 nm VUV辐照能够原位生成ROS(式(1)、(2))[9],具备高效、“绿色”等特点。VUV/PS技术可有效降解氰化物[10]、抗生素[11]以及全氟辛酸[12]等污染物,在真实工业废水[11]中也得到了有效运用,显示出在复杂水基质中去除有机污染物的巨大潜力。然而,目前将VUV/PS技术应用于含藻水特别是EOM的研究仍较为罕见。
| $ \mathrm{H}_2 \mathrm{O} \xrightarrow{185 \mathrm{~nm}} \mathrm{HO}^{\cdot}+\mathrm{H}^{\cdot}, \varPhi_{\mathrm{HO}^{\cdot}}=0.33 $ | (1) |
| $ \mathrm{H}_2 \mathrm{O} \xrightarrow{185 \mathrm{~nm}} \mathrm{HO}^{\cdot}+\mathrm{H}^{+}+\mathrm{e}_{\mathrm{eq}}^{-}, \varPhi_{\mathrm{HO}^{\cdot}}=0.045 $ | (2) |
本文利用VUV活化PS对水中EOM进行降解。首先,研究VUV/PS及其对照体系对EOM的去除效能以及特性,探讨不同PS投加量、溶液初始pH和共存阴离子对去除效果的影响;其次,对VUV/PS体系反应机制进行探讨,研究溶解氧质量浓度对EOM去除的影响;再次,探究EOM在后续加氯消毒过程中DBPs的形成;最后,将VUV/PS体系应用于对实际含藻水的处理。
1 实验 1.1 实验材料与试剂本实验使用铜绿微囊藻(中国科学院武汉水生生物研究所,编号:FACHB-905)提取EOM。采用BG11培养基培养铜绿微囊藻,恒温培养箱光暗比为12 h∶ 12 h,温度为25 ℃。根据文献[6]描述的方法,取处于稳定期(35 d)的铜绿微囊藻,将藻液以10 000 r/min离心15 min,上清液通过0.45 μm醋酸纤维素膜真空抽滤即得到EOM提取液。
过硫酸钠(PS)、氯化钠、硝酸钠、碳酸氢钠、香豆素(COU)、硫代硫酸钠和叔丁醇均为AR级,购自上海阿拉丁生化科技有限公司。抗坏血酸(AR级)、硝基苯(NB,HPLC级)、间甲基苯甲酸(mTA,HPLC级)和甲基叔丁基醚(GC级)购自上海麦克林生化科技有限公司。三氯甲烷(TCM)、一溴二氯甲烷(BDCM)、二溴一氯甲烷(DBCM)、二氯乙腈(DCAN)、三氯乙腈(TCAN)、二溴乙腈(DBAN)、二氯乙酸(DCAA)、三氯乙酸(TCAA)和一溴二氯乙酸(BDCAA)标准品购自坛墨质检。甲醇(HPLC级)、乙腈(HPLC级)和磷酸(AR级)购自重庆川东化工有限公司。
1.2 实验用水本实验采用的天然含藻水取自重庆市3个饮用水源(RW 1~3),取样于夏季水华爆发期,水质参数如表 1所示。
| 表 1 天然含藻水水质特征 Tab. 1 Water quality characteristics of natural algae-containing water |
无特殊说明,采用超纯水(UP,18.2 MΩ · cm)稀释EOM提取液及天然含藻水至溶解性有机物(DOC)质量浓度为(4.5±0.2) mg/L后使用。
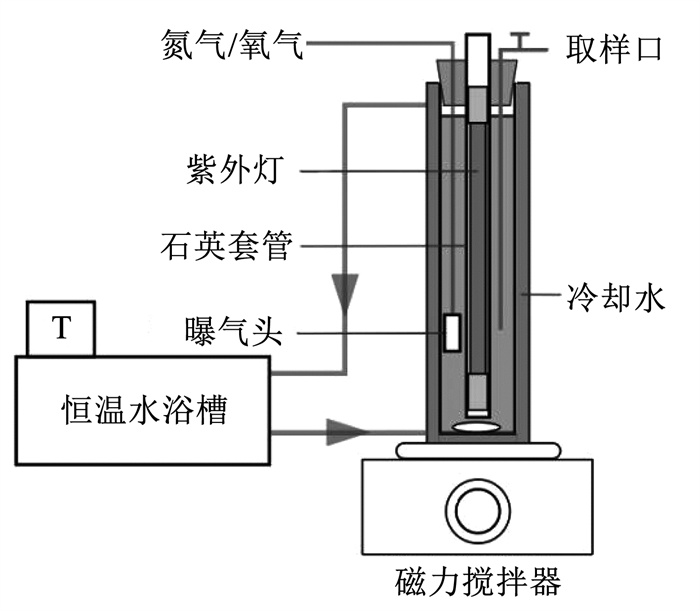
1.3 实验方法所有实验均在体积为900 mL的自制光化学反应器(图 1)中进行,并使用恒温水域槽(SCIENTZ DC-0515,中国)将其温度控制在(25±0.1) ℃。作为光源的UV灯(254 nm,北京航天宏达光电技术有限公司)在254 nm处的光子通量为5.93×10-6 E/s[13],VUV灯((254+185)nm,北京航天宏达光电技术有限公司)在185 nm处的光子通量为5.26×10-7 E/s[14]。
|
图 1 实验装置 Fig. 1 Experimental setup |
在EOM去除实验中,配置900 mL EOM溶液加入到反应器中,根据实验需求加入PS和阴离子,用0.1 mol/L H2SO4溶液和NaOH溶液调节初始pH,随后将预热15 min的VUV灯放入石英套管中触发反应。在曝气实验中,使用曝气头将气体(氮气/氧气)通入溶液中,气体流速为0.5 L/min。为保证溶解氧质量浓度稳定,实验开始前20 min及整个实验期间保持气体持续供应。在加氯消毒实验中,将处理后的溶液置于棕色玻璃瓶中,加入次氯酸钠(活性氯质量浓度20 mg/L),用聚四氟乙烯衬垫瓶盖密封,在25 ℃的黑暗环境下消毒24 h后,加入抗坏血酸终止反应。
1.4 分析方法UV254、DOC、三维激发- 发射矩阵(EEM)光谱分别通过紫外分光光度计(Shimadzu UV-2600,日本)、总有机碳分析仪(Shimadzu,日本)和荧光光谱仪(Hitachi F-4700,日本)进行测定。EOM的相对分子质量分布采用超滤膜分级的方法进行测定[15]。NB和mTA通过高效液相色谱仪(Thermo Fisher Scientific UltiMateTM 3000,美国)进行检测[16]。DBPs根据Chen等[15]描述的方法,三卤甲烷和卤乙腈采用MTBE进行液液萃取,卤乙酸用甲醇衍生化后采用MTBE进行液液萃取,萃取后DBPs采用气相色谱仪(GC/ECD, Agilent 7820,日本)测定。天然含藻水中,浊度通过台式浊度仪(哈希TL23,美国)测量,阴离子浓度使用离子色谱仪(ECO IC,瑞士)检测。
采用伪一级动力学模型拟合EOM的矿化,通过式(3)计算DOC降解速率常数kobs:
| $ \ln \frac{\rho_t}{\rho_0}=k_{\mathrm{obs}} t $ | (3) |
式中ρ0和ρt分别代表反应时间为0和t min时的DOC质量浓度。
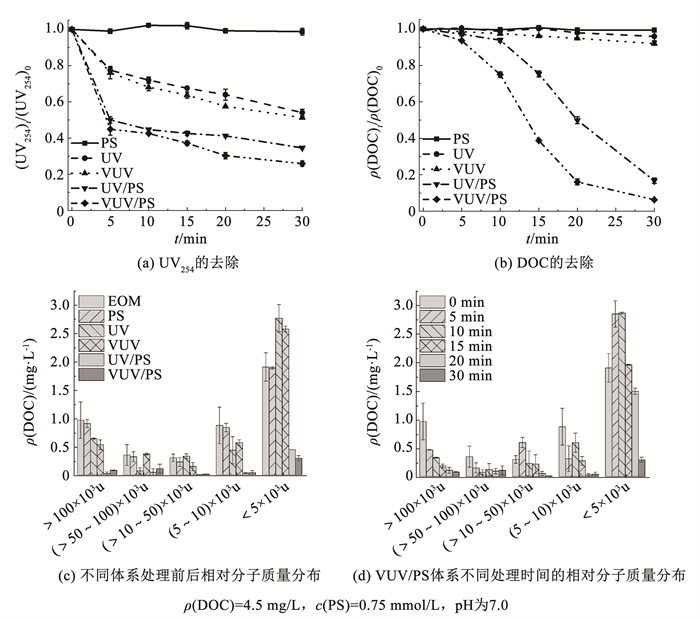
2 结果与讨论 2.1 VUV/PS体系对EOM的去除效能 2.1.1 DOC和UV254的去除DOC和UV254是表征EOM的典型指标。如图 2(a)所示,反应30 min后,PS、UV、VUV、UV/PS和VUV/PS体系中UV254的去除率分别为1.25%、46.0%、48.7%、65.4%、74.1%。可以看出,尽管PS是一种强氧化剂(E0S2O82-=2.01 V),但它无法去除EOM中的芳香性有机物。而EOM中的芳香发色基团与不饱和C C或C O可直接吸收UV和VUV辐射[17],故UV和VUV体系中UV254明显降低。VUV体系中UV254的去除率略高于UV体系,这与VUV光解H2O生成HO· 有关(式(1)、(2)),此外,185 nm VUV光子的直接光解也促进了EOM的降解。UV/PS和VUV/PS体系中生成了SO4· -(式(4)~(6))和HO· (式(7))[18],UV254的去除率得以提升。特别在VUV/PS体系中,185 nm VUV辐照可裂解H2O(式(1)、(2))和PS(式(5))产生更多ROS,故其对UV254的降解效果优于UV/PS体系。
| $ \mathrm{S}_2 \mathrm{O}_8^{2-} \xrightarrow{254 \mathrm{~nm}} 2 \mathrm{SO}_4^{·-}, \varPhi_{\mathrm{SO}_4^{·-}}=1.4 $ | (3) |
| $ \mathrm{S}_2 \mathrm{O}_8^{2-} \xrightarrow{185 \mathrm{~nm}} 2 \mathrm{SO}_4^{·-} $ | (5) |
| $ \mathrm{S}_2 \mathrm{O}_8^{2-}+\mathrm{e}_{\mathrm{aq}}^{-} \rightarrow \mathrm{SO}_4^{·-}+\mathrm{SO}_4^{2-} $ | (6) |
| $ \mathrm{SO}_4^{·-}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{SO}_4^{2-}+\mathrm{HO}^{·}+\mathrm{H}^{+}, k=200 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (7) |
|
图 2 VUV/PS及其对照体系中EOM的去除效果以及相对分子质量分布的变化 Fig. 2 Removal efficiency of EOM and changes in relative molecular weight distribution in VUV/PS and control systems |
如图 2(b)所示,DOC的去除率遵循VUV/PS(93.7%)>UV/PS(83.3%)>VUV(8.0%)>UV(4.1%)>PS(0.6%)。与UV254降解不同的是,UV和VUV辐照对EOM的矿化效果不佳,说明芳香性有机物容易被分解或转化,却难以矿化[19]。UV/PS和VUV/PS体系中DOC的去除率显著提升,表明EOM矿化主要归因于SO4· -和HO· 等ROS的氧化作用。此外,VUV、UV/PS和VUV/PS体系中EOM矿化的kobs分别为0.002 7、0.059 1和0.100 0 min-1,kobs,VUV/PS为kobs,UV/PS与kobs,VUV之和的1.62倍,表明VUV与PS存在协同作用,体现了185 nm VUV辐照在体系中的关键作用。
2.1.2 EOM相对分子质量的变化AOPs通常会改变有机物相对分子质量(MW)的大小及分布[19]。因此,考察了各体系反应30 min后,EOM的相对分子质量分布情况,结果如图 2(c)所示。原EOM溶液中MW>100×103u、(>50~100)×103u、(>10~50)×103u、(5~10)×103u和<5×103u的有机物分别占比22.0%、8.0%、6.9%、19.9%和43.3%,小分子有机物(MW<5×103u)占比最多。UV和VUV辐照后,大分子有机物(MW>100×103u)质量浓度不同程度减少,而小分子有机物(MW<5×103u)质量浓度从1.91 mg/L分别增加到2.77、2.58 mg/L。这一现象表明,EOM的高分子聚合结构被破坏,裂解成小分子有机物及少量无机物,进一步证实了EOM中的芳香性有机物易转化却难矿化。在UV/PS和VUV/PS体系中,不同相对分子质量的有机物质量浓度均显著下降,小分子有机物(MW<5×103u)质量浓度仍占主体地位。
如图 2(d)所示,进一步探究了VUV/PS体系中不同反应时间EOM相对分子质量的分布情况。反应5 min后,MW>50×103u的有机物质量浓度从1.31 mg/L降至0.62 mg/L,而MW<5×103u的有机物质量浓度从1.91 mg/L增加到2.85 mg/L;随反应时间增加,不同相对分子质量的有机物均被降解。这一现象表明,VUV/PS体系中ROS优先将高相对分子质量物质转化为小分子有机物,之后再将其矿化[20]。
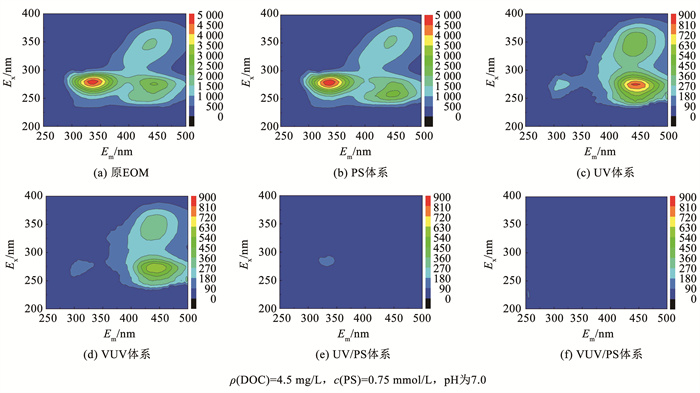
2.1.3 荧光有机物的变化图 3为VUV/PS及其对照体系降解EOM的三维荧光谱图。原EOM溶液中3个荧光团的峰值分别位于激发/发射波长(Ex/Em)为280/340 nm(峰T)、280/430 nm(峰A)和350/430 nm(峰C)处,分别代表溶解的微生物代谢物、类富里酸物质和类腐殖酸物质[21]。其中,峰T的荧光强度最高,表明EOM中含有较高浓度的微生物代谢物。UV和VUV辐照30 min后(图 3(c)、(d)),特征峰T消失,特征峰A和C的荧光强度显著下降,且峰C荧光强度最高。这一现象表明,与类腐殖酸物质相比,类富里酸物质、芳香蛋白和溶解的微生物代谢物更容易被转化。在UV/PS和VUV/PS体系中(图 3(e)、(f))),所有荧光峰几乎完全消失,表明EOM中的荧光物质被有效去除。
|
图 3 VUV/PS及其对照体系中EOM的EEM谱图 Fig. 3 EEM spectra of EOM in VUV/PS and control systems |
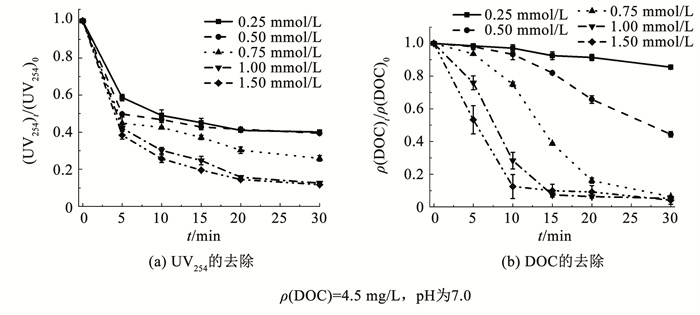
PS的初始投加量是影响VUV/PS工艺性能的重要因素之一。如图 4所示,EOM的去除率随PS投加量的增大而增加。当PS投加量增加到1.5 mmol/L时,UV254和DOC的去除率最高,分别为88.3%和95.9%。这是因为随着PS投加量的增加,溶液中产生了更多的ROS,从而更有效地降解了EOM。
|
图 4 PS投加量对VUV/PS体系去除EOM的影响 Fig. 4 Effect of PS dosage on the removal of EOM in VUV/PS system |
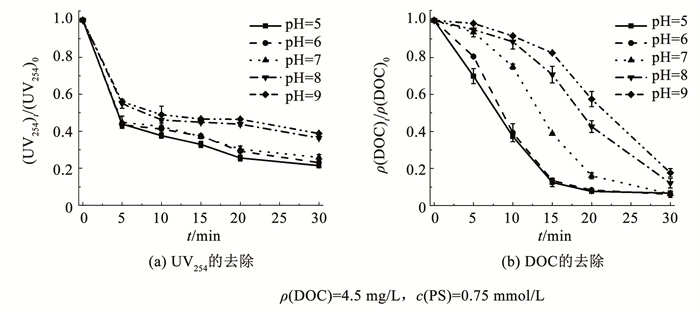
研究了VUV/PS体系中pH为5.0~9.0时EOM的去除率,结果如图 5所示。随着初始pH由5.0增加至9.0,UV254的去除率由78.6%降低至61.2%,DOC的去除率也从93.3%下降到82.3%。显然,酸性条件更有利于EOM的去除。
|
图 5 溶液初始pH对VUV/PS体系去除EOM的影响 Fig. 5 Effect of initial pH on removal of EOM in VUV/PS system |
在VUV/PS体系中,酸性条件下SO4· -是主要的ROS[16],其强氧化性促进了EOM的降解。随着pH升高,溶液碱性增强,SO4· -与OH-反应生成HO· (式(8))。但HO· 在碱性条件下氧化还原电位减弱[22],且HO2-和OH-清除作用增强,导致HO· 解离为低氧化能力的O · -(式(9))和O2· -(式(10)~(12))[23],从而降低了EOM的去除率。
| $ \mathrm{SO}_4^{·-}+\mathrm{OH}^{-} \rightarrow \mathrm{HO}^{·}+\mathrm{SO}_4^{2-}, k=6.5 \times 10^7 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (8) |
| $ \mathrm{HO}^{·}+\mathrm{OH}^{-} \rightarrow \mathrm{O}^{\cdot-}+\mathrm{H}_2 \mathrm{O}, k=1.2 \times 10^{10} \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (9) |
| $ \mathrm{HO}^{\cdot}+\mathrm{HO}^{\cdot} \rightarrow \mathrm{H}_2 \mathrm{O}_2, k=4.0 \times 10^9 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (10) |
| $ \mathrm{H}_2 \mathrm{O}_2+\mathrm{OH}^{-} \rightleftharpoons \mathrm{H}_2 \mathrm{O}+\mathrm{HO}_2^{-}, \mathrm{p} K_{\mathrm{a}}=11.62 $ | (11) |
| $ \mathrm{HO}^{·}+\mathrm{HO}_2^{-} \rightarrow \mathrm{O}_2^{·-}+\mathrm{H}_2 \mathrm{O}, k=7.5 \times 10^9 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (12) |
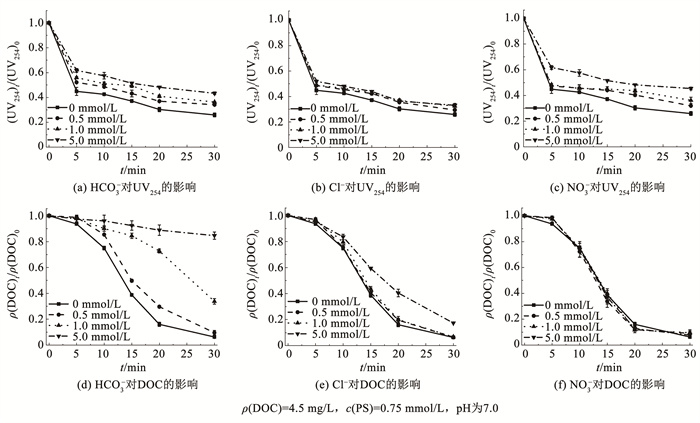
天然水体中普遍存在的无机阴离子对AOPs去除有机污染物可能造成影响[24],因此,研究了3种典型阴离子(HCO3-、Cl-和NO3-)对VUV/PS体系去除EOM的影响。如图 6所示,HCO3-和Cl-显著抑制EOM去除。当HCO3-和Cl-浓度从0增至5.0 mmol/L时,UV254的去除率分别下降至56.6%和66.9%,DOC的去除率也分别下降至15.3%和82.6%。HCO3-和Cl-的抑制作用主要源于两方面:一是HCO3-和Cl-在185 nm处的摩尔吸收系数分别为464、3 036 L/(mol · cm),能够与PS竞争VUV光子(式(13)),干扰了EOM的直接光解和ROS的产生;二是HCO3-和Cl-的自由基清除作用,能捕获SO4· -和HO· 生成氧化能力较低的CO3· -、Cl· 、Cl2· -和ClOH · -(式(14)~(18))[25],进而降低EOM的降解效率。与HCO3-和Cl-相比,NO3-对VUV/PS体系的影响较小。如图 6(c)、(f)所示,NO3-浓度从0增加到5.0 mmol/L,UV254的去除率从74.1%下降到54.6%,而DOC的去除率仅从93.7%下降到90.4%。这是由于NO3-具有较强的紫外光屏蔽效果,降低了EOM在254 nm处的紫外吸收,使得UV254的去除率降低。然而,NO3-可以通过光解产生HO· (式(19)、(20)),因此,NO3-对DOC去除的影响并不明显。
| $ \mathrm{HCO}_3^{-} / \mathrm{CO}_3^{2-} \xrightarrow{185 \mathrm{~nm}} \mathrm{CO}_3^{·-}+\mathrm{e}_{\mathrm{aq}}^{-} $ | (13) |
| $ \mathrm{HO}^{\cdot}+\mathrm{HCO}_3^{-} \rightarrow \mathrm{CO}_3^{\cdot-}+\mathrm{H}_2 \mathrm{O}, k=8.5 \times 10^6 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (14) |
| $ \mathrm{SO}_4^{·-}+\mathrm{HCO}_3^{-} \rightarrow \mathrm{CO}_3^{·-}+\mathrm{HSO}_4^{-}, k=9.1 \times 10^6 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (15) |
| $ \mathrm{HO} \cdot+\mathrm{Cl}^{-} \rightarrow \mathrm{ClOH}^{·-}, k=4.3 \times 10^9 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (16) |
| $ \mathrm{SO}_4^{·-}+\mathrm{Cl}^{-} \rightarrow \mathrm{Cl}^{·}+\mathrm{SO}_4^{2-}, k=3.1 \times 10^8 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (17) |
| $ \mathrm{Cl}^{·}+\mathrm{Cl}^{-} \rightarrow \mathrm{Cl}_2^{·-}, k=8.5 \times 10^9 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (18) |
| $ \mathrm{NO}_3^{-} \xrightarrow{h v} \mathrm{NO}_2^{·}+\mathrm{O}^{·-} $ | (19) |
| $ \mathrm{O}^{\cdot-}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{HO}^{·}+\mathrm{OH}^{-} $ | (20) |
|
图 6 共存阴离子对VUV/PS体系去除EOM的影响 Fig. 6 Effect of coexisting anions on removal of EOM in VUV/PS system |
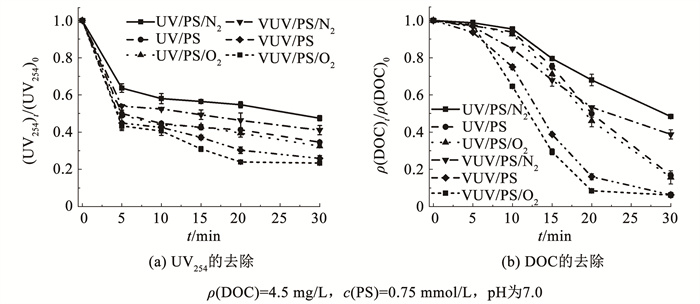
研究表明,溶解氧质量浓度的增加可有效促进VUV-AOPs及PS-AOPs中污染物的降解[26-27]。因此,在不同曝气条件下,研究了溶解氧对VUV/PS体系去除EOM的影响。采用便携式溶解氧测定仪监测溶解氧质量浓度,在曝氧气、不曝气和曝氮气时,溶解氧质量浓度在实验过程中均保持稳定,分别为0.3、7.9、35.4 mg/L。如图 7所示,UV254的去除率随着溶解氧质量浓度的增大而增加,分别为58.9%、74.1%和76.6%;DOC的去除率也同样随着溶解氧质量浓度的增大而增加,EOM矿化的kobs分别为0.033 9、0.100 0、0.108 1。在UV/PS工艺中,UV254和DOC的去除也遵循以下规律:曝氧气>不曝气>曝氮气。结果表明,溶解氧质量浓度的增加促进了EOM的降解。但EOM的去除率与溶解氧质量浓度不成正比,这可能与不同曝气条件下ROS的产量有关。因此,在2.3.2节中详细探讨了溶解氧对VUV/PS体系的影响机制。
|
图 7 曝气条件对EOM去除的影响 Fig. 7 Effect of bubbling gases on removal of EOM |
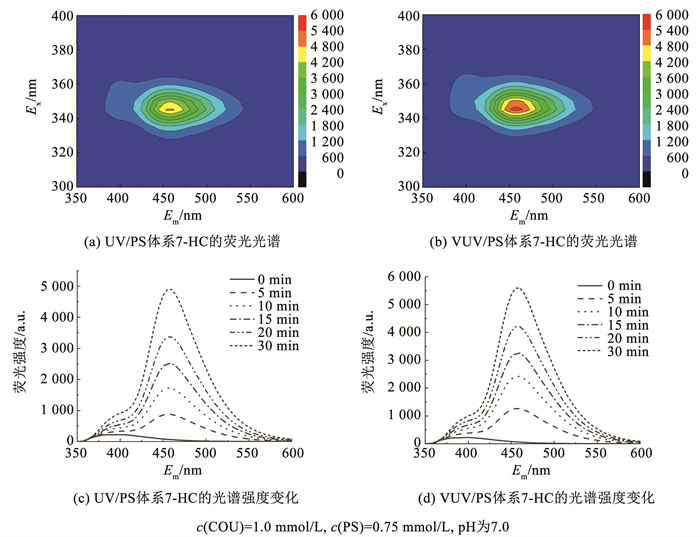
采用香豆素(COU)作为HO· 的荧光探针[15],检验VUV/PS体系生成HO· 的能力。如图 8所示,在UV/PS和VUV/PS体系中都检测到了香豆素与HO· 反应生成的特征荧光产物——7-羟基香豆素(7-HC),说明两个系统中均产生了HO· ,且其荧光强度均随着反应时间的延长而增加,HO· 可以在这两个体系中持续生成。此外,VUV/PS体系中7-HC的荧光强度超过了UV/PS体系,证明VUV辐照能够促进HO· 的产生。
|
图 8 VUV/PS及UV/PS体系中7-羟基香豆素的荧光光谱和荧光发射光谱强度变化 Fig. 8 Fluorescence EEM spectra and changes of fluorescence intensity of 7-hydroxycoumarin in VUV/PS and UV/PS systems |
NB和mTA被用作HO· 和SO4· -的特征探针化合物[16, 18],HO· 和SO4· -的稳态浓度(c(HO· )ss和c(SO4· -)ss)可根据式(21)~(25)计算。k体系,探针化合物为各体系中NB和mTA降解的拟一级动力学常数。NB和HO· 反应的二级速率常数为kHO·, NB=3.90×109 L/(mol · s),mTA与HO· 和SO4· -反应的二级速率常数分别为kHO·, mTA=7.60×109 L/(mol · s)和kSO4· -, mTA=2×109 L/(mol · s)[28-29]。
| $ c\left(\mathrm{HO}^·\right)_{\mathrm{ss}, \mathrm{VUV}}=\frac{k_{\mathrm{VUV}, \mathrm{NB}}-k_{\mathrm{VUV}, \mathrm{NB}, \mathrm{TBA}}}{k_{\mathrm{HO} ^·, \mathrm{NB}}} $ | (21) |
| $ c\left(\mathrm{HO}^·\right)_{\mathrm{ss}, \mathrm{UV} / \mathrm{PS}}=\frac{k_{\mathrm{UV} / \mathrm{PS}, \mathrm{NB}}-k_{\mathrm{UV}, \mathrm{NB}}}{k_{\mathrm{HO}^·, \mathrm{NB}}} $ | (22) |
| $ c\left(\mathrm{HO}^·\right)_{\mathrm{ss}, \mathrm{VUV} / \mathrm{PS}}=\frac{k_{\mathrm{VUV} / \mathrm{PS}, \mathrm{NB}}-k_{\mathrm{VUV}, \mathrm{NB}, \mathrm{TBA}}}{k_{\mathrm{HO} ^·, \mathrm{NB}}} $ | (23) |
| $ c\left(\mathrm{SO}_4^{·-}\right)_{\mathrm{ss}, \mathrm{UV} / \mathrm{PS}}=\frac{k_{\mathrm{UV} / \mathrm{PS}, \mathrm{mTA}}-k_{\mathrm{UV}, \mathrm{mTA}}-k_{\mathrm{HO}^·, \mathrm{mTA}} c\left(\mathrm{HO}^·\right)_{\mathrm{ss}, \mathrm{UV} / \mathrm{PS}}}{k_{\mathrm{SO}_{4}{^{·-},\mathrm{mTA}}}} $ | (24) |
| $ c\left(\mathrm{SO}_4^{·-}\right)_{\mathrm{ss}, \mathrm{VUV} / \mathrm{PS}}=\frac{k_{\mathrm{VUV} / \mathrm{PS}, \mathrm{mTA}}-k_{\mathrm{VUV}, \mathrm{mTA}, \mathrm{TBA}}-k_{\mathrm{HO}^{\cdot}, \mathrm{mTA}^{-}} c\left(\mathrm{HO}^{·}\right)_{\mathrm{ss}, \mathrm{VUV} / \mathrm{PS}}}{k_{\mathrm{SO}_4^{·-}, \mathrm{mTA}}} $ | (25) |
在VUV/PS体系中,测得c(HO· )ss和c(SO4· -)ss分别为4.78×10-13、1.51×10-11 mol/L;在UV/PS体系中,测得c(HO· )ss和c(SO4· -)ss分别为2.95×10-13、0.84×10-11 mol/L。VUV/PS体系中的c(HO· )ss和c(SO4· -)ss均为UV/PS体系的1.6倍,表明185 nm VUV辐照促进了ROS的生成。具体来说,H2O强烈吸收VUV辐照生成HO· 、H· 和eaq-(式(1)、(2)),eaq-进一步与PS反应生成SO4· -(式(6))。同时,254 nm UV辐照和185 nm VUV辐照均可活化PS生成SO4· -(式(4)、(5)),随后与H2O反应生成HO· (式(7))。由于185 nm VUV辐照的贡献,VUV/PS体系中的ROS生成能力较UV/PS体系更强。
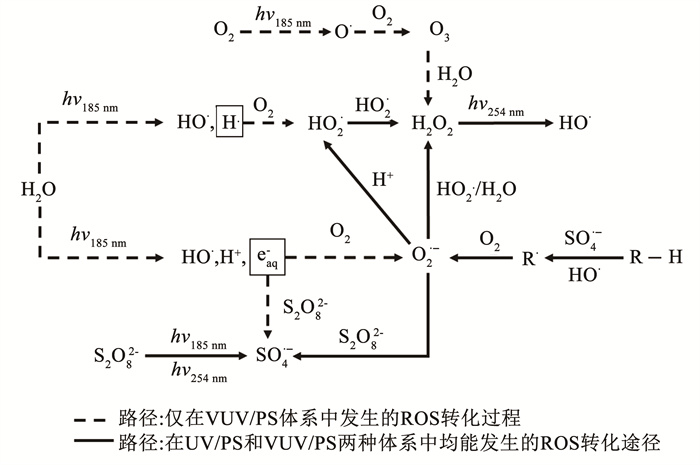
2.3.2 溶解氧对VUV/PS体系降解EOM的影响机制溶解氧可以明显促进EOM的降解,这可能与VUV/PS体系中ROS生成与转化有关。图 9展示了VUV/PS工艺中有关O2参与的ROS可能的产生与转化机制。因此,通过测定不同曝气条件下HO· 和SO4· -的稳态浓度,进一步探究了溶解氧对VUV/PS体系的影响机制。
|
图 9 VUV/PS体系ROS的转化途径 Fig. 9 Transformation pathways of ROS in VUV/PS system |
由图 10(a)可知,无氧(曝氮气)条件下c(HO· )ss最低,有氧条件下(不曝气及曝空气)c(HO· )ss明显增加。在VUV辐照下,无氧时HO· 主要源于VUV辐照对H2O的裂解(式(1)、(2));而有氧条件下,O2与H· 和eaq-反应生成H2O2(式(26)~ (31)),或吸收VUV辐照生成O3(式(32)),再由O3光解生成H2O2(式(33))。H2O2进而光解产生HO· (式(34))。因此,VUV体系中HO· 产量顺序为:曝氧气>不曝气>曝氮气。UV/PS和VUV/PS体系中c(HO· )ss比VUV高一个数量级,主要归因于PS的光解(式(4)~(8))。此外,在基于SO4· -的高级氧化工艺中,O2可以转化为O2· -和HO·2[30];同时,HO· 和SO4· -可以与包含芳环、胺类、羧酸盐等官能团的有机物生成相应的有机自由基(R· )(式(39)、(40)),R· 再与O2生成O2· -和HO·2(式(41)、(42))[30],进而转化为HO· (式(29)~(31)、(34))。因此,UV/PS和VUV/PS体系中HO· 产量随溶解氧质量浓度升高而增加。
| $ \mathrm{O}_2+\mathrm{e}_{\mathrm{aq}}^{-} \rightarrow \mathrm{O}_2^{\cdot-}, k_{15}=2.0 \times 10^{10} \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (26) |
| $ \mathrm{O}_2+\mathrm{H}^{\cdot} \rightarrow \mathrm{HO}_2^{\cdot}, k_{16}=2.1 \times 10^{10} \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (27) |
| $ \mathrm{HO}_2^{·}+\mathrm{HO}_2 \rightleftharpoons \mathrm{H}_3 \mathrm{O}^{+}+\mathrm{O}_2^{·-}, \mathrm{p} K_{\mathrm{a}}=4.8 $ | (28) |
| $ \begin{gathered} 2 \mathrm{O}_2^{·-}+\mathrm{HO}_2^{\cdot}+\mathrm{H}_3 \mathrm{O}^{+} \rightarrow \mathrm{H}_2 \mathrm{O}_2+\mathrm{O}_2+\mathrm{H}_2 \mathrm{O}, \\ k_{18}=9.7 \times 10^7 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) \end{gathered} $ | (29) |
| $ 2 \mathrm{O}_2^{·-}+2 \mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{H}_2 \mathrm{O}_2+\mathrm{O}_2+\mathrm{HO}^{-}, k_{19}=0.3 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (30) |
| $ 2 \mathrm{HO}^·_2 \rightarrow \mathrm{H}_2 \mathrm{O}_2+\mathrm{O}_2, k_{20}=2.0 \times 10^6 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (31) |
| $ \mathrm{O}_2 \xrightarrow{185 \mathrm{~nm}} \mathrm{O}^· \xrightarrow{+\mathrm{O}_2} \mathrm{O}_3 $ | (32) |
| $ \mathrm{O}_3+\mathrm{H}_2 \mathrm{O} \xrightarrow{254 \mathrm{~nm}} \mathrm{H}_2 \mathrm{O}_2+\mathrm{O}_2 $ | (33) |
| $ \mathrm{H}_2 \mathrm{O}_2 \xrightarrow{254 \mathrm{~nm}} \mathrm{HO}^·, \varPhi_{\mathrm{HO}^·}=0.5 $ | (34) |
| $ \mathrm{H}_2 \mathrm{O}_2+\mathrm{HO}^{·} \rightarrow \mathrm{HO}_2^{·}+\mathrm{H}_2 \mathrm{O}, k_{24}=2.7 \times 10^7 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (35) |
| $ \mathrm{H}_2 \mathrm{O}_2+\mathrm{e}_{\mathrm{aq}}^{-} \rightarrow \mathrm{HO}^{·}+\mathrm{HO}^{-}, k_{25}=1.3 \times 10^{10} \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (36) |
| $ \mathrm{H}_2 \mathrm{O}_2+\mathrm{H}^{\cdot} \rightarrow \mathrm{HO}^{\cdot}+\mathrm{H}_2 \mathrm{O}, k_{26}=5.0 \times 10^7 \mathrm{~L} /(\mathrm{mol} \cdot \mathrm{~s}) $ | (37) |
| $ \mathrm{S}_2 \mathrm{O}_8^{2-}+\mathrm{O}_2^{\cdot-} \rightarrow \mathrm{SO}_4^{\cdot-}+\mathrm{SO}_4^{2-}+\mathrm{O}_2 $ | (38) |
| $ \mathrm{HO}^{·}+\mathrm{R}-\mathrm{H} \rightarrow \mathrm{H}_2 \mathrm{O}+\mathrm{R}^{·} $ | (39) |
| $ \mathrm{SO}_4^{·-}+\mathrm{R}-\mathrm{H} \rightarrow \mathrm{HSO}_4^{-}+\mathrm{R}^{·} $ | (40) |
| $ \mathrm{R}^{\cdot}+\mathrm{O}_2 \rightarrow \mathrm{O}_2^{·-}+\mathrm{R}^{+} $ | (41) |
| $ \mathrm{O}_2^{·-}+\mathrm{H}^{+} \rightleftharpoons \mathrm{HO}_2^{·} $ | (42) |
|
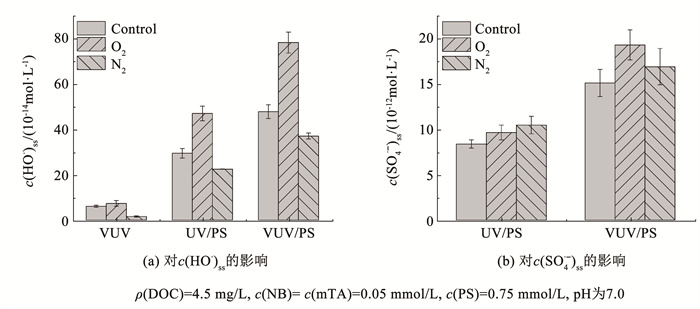
图 10 曝气条件对EOM去除及自由基稳态浓度的影响 Fig. 10 Effect of bubbling gases on removal of EOM and steady-state concentration of ROS |
如图 10(b)所示,在UV/PS和VUV/PS体系中,曝氧气和氮气条件下c(SO4· -)ss均高于不曝气条件。在VUV/PS体系中,无氧时eaq-主要与PS反应生成SO4· -(式(6));在有氧条件下,eaq-与O2反应生成O2· -(式(26)),O2· -部分转化为HO· (式(29)~(31)、(34)),部分与PS反应生成SO4· -(式(38))。因此,随着溶解氧质量浓度从0.3 mg/L(曝氮气)增加至7.9 mg/L(不曝气),eaq-的转化由主要生成SO4· -转变为同时生成SO4· -和HO· ,c(SO4· -)ss从1.69×10-11 mol/L下降到1.51×10-11 mol/L。当溶解氧增加至35.4 mg/L,O2· -生成量增加,其与PS反应生成SO4· -的产量也随之提升(式(38))。因此,曝氧气时c(SO4· -)ss(1.93×10-11 mol/L)最高。
基于以上分析可以得出,EOM在VUV/PS体系中的高效矿化主要归因于HO· 和SO4· -,溶解氧通过促进以HO· 和SO4· -为主的ROS生成,促进了EOM的降解。
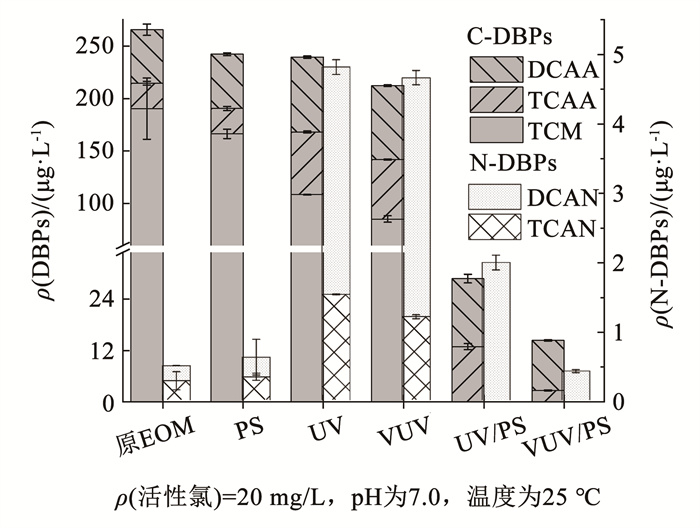
2.4 VUV/PS体系对EOM生成DBPs的影响鉴于EOM是DBPs的重要前体物,进一步考察了经VUV/PS及其对照体系处理后,EOM在后续氯消毒过程中DBPs的生成情况。如图 11所示,未经处理的原EOM溶液经氯消毒后C-DBPs和N-DBPs生成量分别为265.53、0.50 μg/L,经PS处理后,C-DBPs和N-DBPs生成量分别变为242.23、0.62 μg/L,PS对DBPs的形成没有显著影响。经过UV、VUV、UV/PS和VUV/PS处理后,C-DBPs生成量分别下降至239.50、212.32、28.82、14.35 μg/L,N-DBPs生成量分别为4.82、4.66、1.99、0.42 μg/L,3个对照体系中N-DBPs的生成量反而显著增加。在VUV/PS体系中DBPs总生成量最低,表明VUV/PS体系是控制DBPs生成的有效手段。
|
图 11 VUV/PS和其对照体系对DBPs生成量的影响 Fig. 11 Effect of VUV/PS and its control systems on formation of DBPs |
深入分析DBPs的构成,TCM和TCAA占比最高,这可能与EOM中丰富的蛋白质为氯化反应生成TCM和TCAA提供了充足的反应位点有关[31]。尽管UV辐照后C-DBPs的总量有所减少,但仅TCM质量浓度降低,而DCAA和TCAA的质量浓度增加,这可能与EOM特性的变化有关。UV和VUV辐照有效降解蛋白质和类腐殖酸有机物(图 2(c)、(d)),进而降低TCM生成量[32]。部分大分子有机物在此过程中转化为更易与氯反应的小分子有机物,生成更多DCAA和TCAA[33]。UV/PS和VUV/PS处理后,所有C-DBPs的质量浓度显著降低,归因于这两种体系优越的矿化效果。
EOM中,蛋白质和氨基酸作为主要有机氮源,是形成N-DBPs的重要前体物。UV及VUV辐照能将大分子有机物转化为游离氨基酸和脂肪酸等小分子[34],进而促进与氯反应生成N-DBPs[35]。UV/PS处理后,被氧化的氨基酸与氯反应生成更多有机氯胺(-NHCl2和-NCl2)[32],其后续降解导致N-DBPs质量浓度增加。此外,UV/PS体系中仅观察到DCAN生成,表明DCAN比TCAN更易形成。VUV/PS体系中N-DBPs生成量最低,可能是大部分N-DBPs前体物被矿化为无机物所致。
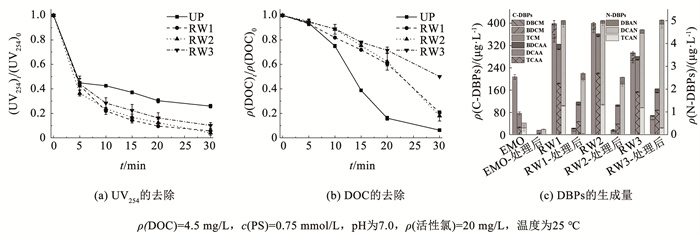
2.5 VUV/PS体系在天然含藻水中的应用藻华期间,EOM在水源中普遍积累。为评估VUV/PS体系在实际水体中去除EOM的效能,从3个发生藻华的饮用水源地采集了水样(RW 1~3)。如图 12(a)、(b)所示,RW 1和RW 2水样中UV254和DOC的去除率与超纯水相近,表明低浓度的阴离子(表 1)对EOM去除影响较小。但RW 3水样中,高浓度阴离子显著抑制DOC和UV254的去除,特别是Cl-和SO42-的浓度分别高达0.47、0.46 mmol/L。尽管如此,3个水样中DOC和UV254均呈下降趋势,表明VUV/PS体系对天然水中EOM降解具有显著效果。
|
图 12 VUV/PS体系对天然含藻水中EOM的去除及DBPs生成的影响 Fig. 12 Effect of VUV/PS system on the EOM removal and generation of DBPs formation in natural algal-containing water |
如图 12(c)所示,进一步研究了VUV/PS体系对DBPs生成的影响。由于实际水样中存在溴离子(Br-),检测到Br-DBPs的形成。经VUV/PS处理后,RW 1和RW 2水样中C-DBPs和N-DBPs生成量分别下降80.9%和46.6%以上;而在RW 3水样中,C-DBPs生成量下降59.8%,但N-DBPs产量增加9.1%。这表明VUV/PS体系对N-DBPs前体物的去除能力相对较弱。在RW 1-RW 3水样中,DBPs总量分别下降了81.2%、83.9%和59.8%,表明VUV/PS体系可有效减少天然含藻水中DBPs的形成,具有实际应用潜力。
3 结论1)VUV/PS体系在EOM降解和矿化方面表现优异,UV254和DOC的去除率分别为74.1%和93.7%。EOM的有效矿化主要归因于HO· 和SO4· -的氧化作用。在随后的氯化消毒过程中,DBPs的形成也得到了有效控制。
2)PS投加量的增加可以促进EOM的降解,溶液初始pH升高、HCO3-及Cl-浓度的增加会抑制EOM的降解,NO3-对EOM的矿化没有明显影响。
3)在VUV/PS体系中,溶解氧促进了ROS的产生,进而促进了EOM的去除。当溶解氧质量浓度从0.3 mg/L增加到35.4 mg/L时,c(HO· )ss从3.71×10-13 mol/L增加到7.83×10-13 mol/L,c(SO4· -)ss从1.69×10-11 mol/L增加到1.93×10-11 mol/L。
4)VUV/PS体系能够有效去除天然含藻水中的有机物,且显著降低DBPs的生成量。
| [1] |
邢加建. 紫外/氯预处理控制超滤膜污染的效能与机制研究[D]. 哈尔滨: 哈尔滨工业大学, 2021 XING Jiajian. Efficiency and mechanism of UV/chlorine based pretreatments for ultrafiltration membrane fouling control[D]. Harbin: Harbin Institute of Technology, 2021 |
| [2] |
LEPPARD G G. Colloidal organic fibrils of acid polysaccharides in surface waters: electron-optical characteristics, activities and chemical estimates of abundance[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 1997, 120(1): 1. DOI:10.1016/S0927-7757(96)03676-X |
| [3] |
JIE Xu, ZHAO Yanxia, GAO Baoyu, et al. The influence of algal organic matter produced by microcystis aeruginosa on coagulation-ultrafiltration treatment of natural organic matter[J]. Chemosphere, 2018, 196: 418. DOI:10.1016/j.chemosphere.2017.12.198 |
| [4] |
CHENG Xiaoxiang, SONG Wenxin, TAN Fengxun, et al. Novel calcium hypochlorite/ferrous iron as an ultrafiltration membrane pretreatment process for purifying algae-laden water[J]. Environmental Research, 2024, 240: 117572. DOI:10.1016/j.envres.2023.117572 |
| [5] |
方晶云. 蓝藻细胞及藻类有机物在氯化消毒中副产物的形成机理与控制[D]. 哈尔滨: 哈尔滨工业大学, 2010 FANG Jingyun. Formation and control of disinfection by-products in chlorination of B-G algae and algal organic matter (AOM)[D]. Harbin: Harbin Institute of Technology, 2010 |
| [6] |
杜锦滢. 真空紫外/臭氧处理藻类有机物缓解超滤膜污染过程机制研究[D]. 重庆大学: 重庆大学, 2022 DU Jinying. Study on process mechanism of vacuum ultraviolet/ozone for algal organic matter treatment to alleviate ultrafiltration membrane fouling[D]. Chongqing: Chongqing University, 2022 |
| [7] |
陈轶群. 紫外/过硫酸盐除藻及对消毒副产物生成影响研究[D]. 武汉: 华中科技大学, 2017 CHEN Yiqun. Removal of algae and the impact on subsequent formation of disinfection byproducts using UV/persulfate process[D]. Wuhan: Huazhong University of Science and Technology, 2017 |
| [8] |
陈徐庆, 唐玉朝, 伍昌年, 等. 真空紫外协同Co2+催化过硫酸氢钾降解罗丹明B[J]. 环境科学研究, 2024, 37(4): 822. CHEN Xuqing, TANG Yuchao, WU Changnian, et al. Degradation of Rhodamine B by potassium peroxymonosulfate synergistically catalyzed by vacuum ultraviolet and Co2+[J]. Research of Environmental Sciences, 2024, 37(4): 822. |
| [9] |
KRISTIN Z, BOERNICK H, WORCH E. Vacuum-UV radiation at 185 nm in water treatment:a review[J]. Water Research, 2014, 52: 131. DOI:10.1016/j.watres.2013.12.034 |
| [10] |
GHOLAMREZA M, POURAKBAR M, AGHAYANI E, et al. Investigating the aerated VUV/Ps process simultaneously generating hydroxyl and sulfate radicals for the oxidation of cyanide in aqueous solution and industrial wastewater[J]. Chemical Engineering Journal, 2018, 350: 673. DOI:10.1016/j.cej.2018.05.178 |
| [11] |
SUN Yuqing, CHO Dongwan, NIGEL J D, et al. Degradation of antibiotics by modified vacuum-UV based processes: mechanistic consequences of H2O2 and K2S2O8 in the presence of halide ions[J]. Science of the Total Environment, 2019, 664: 312. DOI:10.1016/j.scitotenv.2019.02.006 |
| [12] |
刘明, 黄妍妍, 史金玉, 等. 真空紫外/紫外/过硫酸盐工艺降解水中全氟辛酸[J]. 环境工程学报, 2023, 17(5): 1409. LIU Ming, HUANG Yanyan, SHI Jinyu, et al. Aquatic perfluorooctanoic acid degradation by a vacuum-ultraviolet/ ultraviolet/ persulfate process[J]. Chinese Journal of Environmental Engineering, 2023, 17(5): 1409. |
| [13] |
LUO Jinming, LIU Tongcai, ZHANG Danyu, et al. The individual and co-exposure degradation of benzophenone derivatives by UV/H2O2 and UV/PDS in different water matrices[J]. Water Research, 2019, 159: 102. DOI:10.1016/j.watres.2019.05.019 |
| [14] |
YANG Laxiang, LI Mengkai. A green method to determine VUV (185 nm) fluence rate based on hydrogen peroxide production in aqueous solution[J]. Photochemistry and Photobiology, 2018, 94(4): 821. DOI:10.1111/php.12913 |
| [15] |
CHEN Shengnan, ZHAO Zhiwei, CUI Fuyi, et al. Comparative study of UV/chlorine and VUV/chlorine as ultrafiltration membrane pretreatment techniques: performance, mechanisms and DBPs formation[J]. Journal of Hazardous Materials, 2023, 459: 132249. DOI:10.1016/j.jhazmat.2023.132249 |
| [16] |
XIAO Yongjun, ZHANG Lifeng, ZHANG Wei, et al. Comparative evaluation of iodoacids removal by UV/persulfate and UV/H2O2 processes[J]. Water Research, 2016, 102: 629. DOI:10.1016/j.watres.2016.07.004 |
| [17] |
DONG Feilong, LIN Qiufeng, LI Cong, et al. Impacts of pre-oxidation on the formation of disinfection byproducts from algal organic matter in subsequent chlor(am)ination: a review[J]. Science of the Total Environment, 2021, 754: 141955. DOI:10.1016/j.scitotenv.2020.141955 |
| [18] |
LIU Yudan, WU Jingke. The overlooked role of UV185 induced high-energy excited states in the dephosphorization of organophosphorus pesticide by VUV/persulfate[J]. Chemosphere, 2023, 334: 138993. DOI:10.1016/j.chemosphere.2023.138993 |
| [19] |
TIAN Jiayu, WU Cuiwei, YU Huarong, et al. Applying ultraviolet/persulfate (UV/PS) pre-oxidation for controlling ultrafiltration membrane fouling by natural organic matter (NOM) in surface water[J]. Water Research, 2018, 132: 190. DOI:10.1016/j.watres.2018.01.005 |
| [20] |
CHANG Xinqiang, LIN Tao, MO Jiachen, et al. Coagulation combined with ultraviolet irradiation activated sodium percarbonate as pretreatment prior to ultrafiltration: analysis of free radical oxidation mechanism and membrane fouling control[J]. Chemosphere, 2022, 287: 132049. DOI:10.1016/j.chemosphere.2021.132049 |
| [21] |
NAOMI H, BAKER A, REYNOLDS D. Fluorescence analysis of dissolved organic matter in natural, waste and polluted waters:a review[J]. River Research and Applications, 2007, 23(6): 631. DOI:10.1002/rra.1005 |
| [22] |
WANG Chuang, ZHAO Zhiwei, DENG Xiaoyong, et al. Ultrafast oxidation of emerging contaminants by novel VUV/Fe2+/PS process at wide pH range: performance and mechanism[J]. Chemical Engineering Journal, 2021, 426: 131921. DOI:10.1016/j.cej.2021.131921 |
| [23] |
WANG Dong, DUAN Xiaodi, HE Xuexiang, et al. Degradation of dibutyl phthalate (DBP) by UV-254 nm/H2O2 photochemical oxidation: kinetics and influence of various process parameters[J]. Environmental Science and Pollution Research, 2016, 23(23): 23772. DOI:10.1007/s11356-016-7569-1 |
| [24] |
YU Yang, LI Ning, LU Xukai, et al. Co/N co-doped carbonized wood sponge with 3D porous framework for efficient peroxymonosulfate activation: performance and internal mechanism[J]. Journal of Hazardous Materials, 2022, 421: 126735. DOI:10.1016/j.jhazmat.2021.126735 |
| [25] |
DU Jinying, WANG Chuang, ZHAO Zhiwei, et al. Mineralization, characteristics variation, and removal mechanism of algal extracellular organic matter during vacuum ultraviolet/ozone process[J]. Science of the Total Environment, 2022, 820: 153298. DOI:10.1016/j.scitotenv.2022.153298 |
| [26] |
LIU Haizhou, BRUTON T A, LI Wei, et al. Oxidation of benzene by persulfate in the presence of Fe(Ⅲ)-and Mn(Ⅳ)-containing oxides: stoichiometric efficiency and transformation products[J]. Environmental Science & Technology, 2016, 50(2): 890. DOI:10.1021/acs.est.5b04815 |
| [27] |
TSUTOMU T, WADA T, FUJIMOTO K, et al. Degradation of methyl orange using short-wavelength UV irradiation with oxygen microbubbles[J]. Journal of Hazardous Materials, 2009, 162(2/3): 1103. DOI:10.1016/j.jhazmat.2008.05.162 |
| [28] |
NETA P V, ZEMEL M H. Rate constants and mechanism of reaction of sulfate radical anion with aromatic compounds[J]. Journal of the American Chemical Society, American Chemical Society, 1977, 99(1): 163. DOI:10.1021/ja00443a030 |
| [29] |
BUXTON G V, GREENSTOCK C L. Critical review of rate constants for reactions of hydrated electrons, hydrogen atoms and hydroxyl radicals (· OH/ · O-) in aqueous solution[J]. Journal of Physical and Chemical Reference Data, 1988, 17(2): 513. DOI:10.1063/1.555805 |
| [30] |
XU Xiyan, PLIEGO G, JUAN A, et al. Mineralization of naphtenic acids with thermally-activated persulfate: the important role of oxygen[J]. Journal of Hazardous Materials, 2016, 318: 355. DOI:10.1016/j.jhazmat.2016.07.009 |
| [31] |
ZHANG Hua, QU Jiuhui, LIU Huijuan, et al. Characterization of isolated fractions of dissolved organic matter from sewage treatment plant and the related disinfection by-products formation potential[J]. Journal of Hazardous Materials, 2009, 164(2): 1433. DOI:10.1016/j.jhazmat.2008.09.057 |
| [32] |
DONG Feilong, LIN Qiufeng, DENG Jing, et al. Impact of UV irradiation on Chlorella sp. damage and disinfection byproducts formation during subsequent chlorination of algal organic matter[J]. Science of the Total Environment, 2019, 671: 519. DOI:10.1016/j.scitotenv.2019.03.282 |
| [33] |
ZAHRA A, MOUSSAVI G, MOHAMMADI S, et al. Development of a VUV-UVC/peroxymonosulfate, continuous-flow advanced oxidation process for surface water disinfection and natural organic matter elimination: application and mechanistic aspects[J]. Journal of Hazardous Materials, 2021, 408: 124634. DOI:10.1016/j.jhazmat.2020.124634 |
| [34] |
JOHNSON W P, BAO G B, JOHN W. Specific UV absorbance of aldrich humic acid: changes during transport in aquifer sediment[J]. Environmental Science and Technology, 2002, 36(4): 608. DOI:10.1021/es010920x |
| [35] |
HOW Z T, LINGE K L, BUSETTI F, et al. Organic chloramines in drinking water: an assessment of formation, stability, reactivity and risk[J]. Water Research, 2016, 93: 65. DOI:10.1016/j.watres.2016.02.006 |
 2024, Vol. 56
2024, Vol. 56


