2. 太原科技大学 材料科学与工程学院,太原 030024
2. School of Material Science & Engineering, Taiyuan University of Science and Technology, Taiyuan 030024, China
阳极键合技术作为一种清洁型连接工艺已经广泛应用于同种或异种材料的连接当中,其优点为键合温度低、键合时间短、键合强度高、产生键合应力小、可在不添加任何辅助材料的基础上实现有效键合等[1-2]。目前,阳极键合技术大规模应用于MEMS(微机电系统)器件的封装环节,而随着微型器件功能丰富化及工况复杂化,MEMS器件对封装质量和封装材料的要求也进一步提高[3]。固体电解质是一种具有离子导电性的有机高分子功能材料,拥有质轻、耐蚀、可塑性强等特点,同时又有良好的经济性[4-5]。聚乙二醇(PEG)作为一种固体电解质基体材料,其结构具有良好的空间配位,可提供高密度给电子基团,同时又具有良好的柔性聚醚链段,其醚氧基团易于阳离子相互作用使其溶剂化,易形成均匀体系,这为掺杂改性PEG,从而提高其键合性能提供了良好的结构基础[6-7]。无机颗粒在固体电解质中不仅能够提高基体的机械性能,同时还能够改善离子导电性,拓宽其电化学稳定窗口,增加界面稳定性,常见的无机颗粒有SiO2、Al2O3、ZnO、ZrO2、TiO2、NaCl等[8-9]。而近年来,稀土元素已在一些超导材料中展露头角,其具有的不饱和3d和4f壳层拥有极其丰富的物理及化学特性。CeO2为一种常见的非磁稀土氧化物,其结构稳定,在软化温度以下不发生相变,这也是其优于其他无机颗粒的一个方面。目前,利用PEG为基体进行改性后作为封装键合材料的研究还鲜有报道,本文以PEG为基体,制备出适于阳极键合封装的固体电解质材料,并研究其与Al的键合性能,该研究拓展了PEG基固体电解质材料在键合封装中的应用。
1 实验 1.1 样品制备实验原材料:聚乙二醇(PEG),分子量为4 000,纯度>99.6%,平均粒径<70 mm;高氯酸锂(LiClO4),纯度>99.6%,平均粒径<50 mm;二氧化硅(SiO2),纯度>90%,平均粒径<500 nm;氧化铈(CeO2),纯度>99%,平均粒径<500 nm;无水乙醇。
制备样品前先将PEG放置在50 ℃真空箱中干燥48 h。将LiClO4、SiO2和CeO2放置在120 ℃真空箱中干燥48 h。令PEG-LiClO4-SiO2和PEG-LiClO4-CeO2按照一定比例分别放入球磨罐,以少量无水乙醇作为研磨剂进行球磨,球磨介质为比例为1 ∶1 ∶1, 直径分别为3、5、8 mm的玛瑙球。球磨参数为:转速240 r/min,时间12 h,球料比为7 ∶1。原材料在高能球磨过程中经历强烈的冲击、研磨、挤压和搅拌等作用,新生原子表面不断产生冷焊结合,并发生复杂的络合反应。球磨过程结束后,将粉末材料干燥并筛分,而后将其加热至熔融状态,最后将得到的泥浆状混合物在圆柱型模具中压制成直径为20 mm、厚度为2 mm的(PEG)10LiClO4-SiO2和(PEG)10LiClO4-CeO2圆形片材,压好后将其放入干燥箱中备用[10-11]。
1.2 交流阻抗实验将所制备PEG基复合固体电解质材料放置于两个不锈钢电极间,采用CHI604C电化学工作站进行阻抗分析,测试频率范围0.1 Hz~1 MHz。通过交流阻抗测试所制备材料的本体电阻及离子导电率。
1.3 X-射线衍射实验为研究不同制备方法及无机填料含量对材料的影响,利用X′Pert PRO型X-射线衍射分析仪对所制备PEG基复合固体电解质材料进行实验,实验参数为Cu-Ka辐射源、波长λ=0.154 06 nm、管流为20 mA、管压30 kV、扫描速度2θ=5°/min、扫描范围10°至60°。
1.4 DSC实验对所制备PEG基复合固体电解质进行热性能分析,采用DSC204-F1型热分析系统进行DSC测试。将5 mg样品放入坩埚中,测试温度范围10~120 ℃,升温速率10 ℃/min,得到测试材料相转变温度、结晶度等信息。
1.5 力学性能实验采用P10-10型电液伺服疲劳试验机对样品进行室温下力学性能测试,设备规格为10 kN,精度等级为0.5。
屈服强度测试。测试试样尺寸为10 mm ×10 mm ×5 mm,水平放置于设备载物平面,调整压力头初始位置,设置下压速率为0.02 mm/s。
拉伸强度测试。将测试试样裁剪成尺寸为10 mm ×10 mm×2 mm,由于试样尺寸较小,不易加工成标准试件,将试样上下表面,即电解质材料及铝箔表面先分别粘结一个贴片,而后在贴片上放置AB胶,粘接至设备上下两个拉伸头,注意在粘结过程中保持试样水平粘接,等待15 min,AB胶干透后,开始进行拉伸试验,直至界面完全拉开,设置拉伸速率为0.02 mm/s。
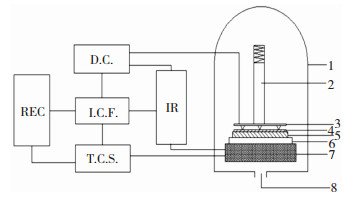
1.6 阳极键合实验将金属铝箔(Al)浸泡在50 g/L的NaOH溶液中5 min,去除表面氧化膜,再用丙酮清洗表面残留杂质,当丙酮溶液完全挥发后,将Al与所制备(PEG)10LiClO4-SiO2和(PEG)10LiClO4-CeO2分别重合并放入键合设备中,其中Al连接阳极,所制备PEG基固体电解质连接阴极,如图 1所示,调整压力后关闭键合炉,准备进行键合实验,键合实验在氮气保护下进行[12]。实验过程中记录键合温度、键合电流、键合电压随时间的变化[13]。
|
图 1 阳极键合设备示意图 Fig.1 Schematic diagram of anode bonding equipment 1-键合炉; 2-压力器; 3-阳极; 4-铝箔; 5-PEG基固体电解质; 6-阴极; 7-加热装置(DC: 直流电源、IR: 数据采集系统、REC: 记录计算模块、ICF: 调节保护系统、TCS: 温度控制系统); 8-保护气 1-bonding furnace; 2-pressor; 3-anode; 4-aluminum foil; 5-PEG-based solid electrolyte; 6-cathode; 7-heating device (DC: direct current power supply; IR: data acquisition system; REC: record calculation module; ICF: regulation protection system; TCS: temperature control system); 8-protective gas |
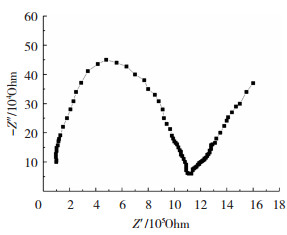
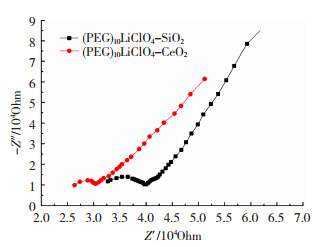
用全电化学分析系统和电化学界面进行交流阻抗实验,频率范围为0.1 Hz~1 MHz。图 2和图 3分别为PEG和(PEG)10LiClO4-SiO2、(PEG)10LiClO4-CeO2在室温下的交流阻抗谱图,可以看到,3条曲线均可分为两部分:即在高频部分显示为一个不对称的半圆,其表示材料的本体电阻;而低频部分为一条因扩散阻抗而引起的倾斜直线。当PEG与LiClO4-SiO2和LiClO4-CeO2络合后,高频部分的半圆半径变小,说明改性后的DSPE较纯PEG体系本体电阻变小,同时通过计算也可以得出,改性后材料在室温下的离子导电率提高了4个数量级,如表 1所示。
|
图 2 PEG在室温下的交流阻抗谱 Fig.2 AC impedance spectrum of PEG at room temperature |
|
图 3 (PEG) 10LiClO4-SiO2、(PEG)10LiClO4-CeO2在室温下的交流阻抗谱 Fig.3 AC impedance spectrum of (PEG)10LiClO4-SiO2 and (PEG)10LiClO4-CeO2 at room temperature |
| 表 1 不同DSPE室温下的离子导电率 Table 1 Ionic conductivity of different DSPE at room temperature |
在测试中,(PEG)10LiClO4-CeO2的本体电阻较低且离子导电率较高,说明CeO2纳米粒子加入后,Ce4+破坏了PEG与锂离子配位,形成(-CH2-CH2-O-Ce-)n,促进了锂离子的解离,增加了自由移动锂离子的数量。Ce4+比Si4+更充分地“释放”了锂离子,而阳极键合正是利用自由移动的离子在键合界面形成键合层,达到两种材料的连接,因此,CeO2的引入有利于阳极键合,进而提高键合封装质量[14]。
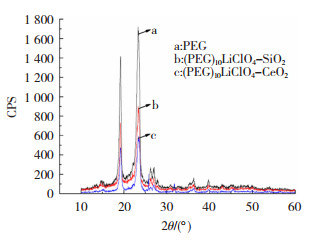
2.2 X射线衍射结果与分析图 4为PEG及所制备样品的XRD衍射谱图,可以看到,纯PEG材料的X衍射曲线在18°及23°两处有很强的衍射峰,说明在未加入锂盐及无机填料时PEG有着很强的结晶性。当加入LiClO4-SiO2或LiClO4-CeO2时,样品衍射峰的位置没有改变,但强度有所降低,说明(PEG)10LiClO4-CeO2、(PEG)10LiClO4-SiO2络合体系均有效降低了PEG的结晶性,而CeO2纳米颗粒引入后衍射峰值更低,则表明CeO2比SiO2更有效地破坏了PEG分子链原有的规则结构,使链段无序化[15]。
|
图 4 XRD衍射谱图 Fig.4 XRD diffraction spectrum |
PEG的结晶主要分为两部分,即晶核的形成与生长,而晶核的生长需要材料内部有序分子链热运动供能。当LiClO4-CeO2引入PEG时,改变了PEG原有的有序分子结构,降低了有序链段运动的总能量,因而无法提供晶核生长所需能量,降低了结晶度,提高了基体无定型区含量。而阳极键合过程中的离子迁移主要是在无定型区完成,降低材料内部结晶度就意味着扩展了传输的通道,从而促进离子迁移,提高键合效率。
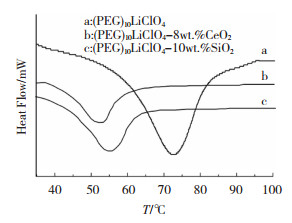
2.3 热性能分析聚乙二醇(PEG)的分子结构单元为(CH2-CH2-O)n,这样的线性高分子长链,其两端为羟基结构,易结晶且相变焓较大,热力学性质十分复杂。图 5与表 2分别为所制备样品的DSC曲线及对应的热力学性能表,PEG的标准熔融焓ΔHm*为203 J/g。
|
图 5 固体聚合物电解质的DSC曲线 Fig.5 DSC curve of solid polymer electrolyte |
| 表 2 所制备固体聚合物电解质的热力学性能 Table 2 Thermodynamic properties of the DSPE |
纯PEG在室温下具有很高的结晶性,当PEG加入LiClO4后,其内部结构发生改变,体系无定型含量增加,(PEG)10LiClO4的结晶度降低至47.71%。当SiO2、CeO2加入到复合体系中时,体系内部分子结构进一步发生改变,无机颗粒与PEG中醚氧基团相互作用,降低了分子间作用力,抑制结晶行为,(PEG)10LiClO4-8wt. %CeO2复合体系结晶度为35.16%,与不含改性颗粒的电解质相比降低了12.55%,说明CeO2的存在可有效降低PEG的结晶性。
改性颗粒的引入为体系内部提供了大量的Si4+、Ce4+,一定程度上减少了Li+与PEG中醚氧基团的络合作用。在实际的阳极键合过程中,需要有一定数量的自由移动离子进行迁移来完成键合,在体系内部可以理解为是Li+与PEG基体之间的“络合-解络合-再络合-再解络合”的一个离子迁移过程,而无机粒子的存在刚好可促进这一过程,释放出更多可自由移动的Li+参与键合,提高材料键合性能。
2.4 强度分析将样品裁剪成10 cm×10 cm×10 cm的形状并固定,测试样品在室温下的力学性能。从表 3中可以看到,(PEG)10LiClO4-CeO2和(PEG)10LiClO4-SiO2的强度明显高于纯PEG。纯PEG在受到外力时,内部分子链趋于外力方向运动,通过分子链的分段移动实现延伸,然而纯PEG的分子链在承受一定作用力时易于断裂。通过引入的锂盐和无机填料与PEG络合在一起,在受到外力时,CeO2和SiO2可以有效分散和转移应力,吸收断裂所需的断裂变形能,避免了分子链出现大规模断裂,这样的络合体系使得SPE机械强度显著提高,并有利于提高阳极键合质量。
| 表 3 室温下DSPE强度 Table 3 DSPE intensity at room temperature |
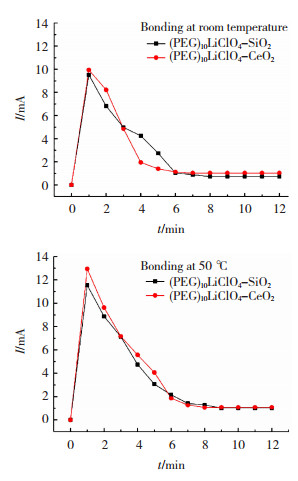
将所制备固体电解质与金属铝箔相互重合,同时铝箔连接到阳极,固体电解质材料连接阴极,放入阳极键合设备中,键合电压750 V,在室温及50 ℃下进行阳极键合实验,键合时间为10 min,整个键合过程通入氮气保护[15],阳极键合过程中时间-电流曲线如图 6所示。由图 6可以看到,在键合初始时,两种材料的键合电流瞬间增大到峰值,随着键合时间增加,键合电流逐渐降低并最终趋于稳定。
|
图 6 不同DSPE与Al键合过程中时间-电流曲线 Fig.6 Time-current curve in the bonding process of different DSPE and Al |
键合初期,随着锂离子的解离、聚集并在强静电场作用下,自由移动的离子不断向键合界面迁移形成电流;随着键合过程的进行,离子迁移达到饱和,电流下降,最终电流值趋于零。对比峰值电流发现,无论在室温或50 ℃键合温度下,(PEG)10LiClO4-CeO2均比(PEG)10LiClO4-SiO2更快达到峰值且峰值更高,这说明CeO2的存在更有利于降低络合体系结晶度,能够“释放”更多自由移动的锂离子,提高材料阳极键合性能。
2.6 键合界面表征将PEG基复合固体电解质与铝箔阳极键合界面进行表征,图 7为键合连接界面微观SEM图,可以看到,两种材料与铝箔之间明显存在一层有别于两边的键合层,其与两边的键合材料相连接,连接处未出现明显空隙和裂纹。键合材料中荷电粒子在静电场及温度场作用下向键合界面定向迁移,并在键合界面处发生了不可逆转的化学反应,产生键合层[14-19]。

|
图 7 键合界面SEM图 Fig.7 SEM image of bonding interface |
图 8、9分别为不同DSPE与铝箔阳极键合后,键合界面在室温下的拉伸断口形貌图,可以看到(PEG)10LiClO4-10wt. %SiO2与铝箔键合界面,断口铝箔一侧有部分位置未参与键合,参与键合的部分有白色薄膜状物质残留,分析为键合层,说明其断裂发生在键合层;而(PEG)10LiClO4-8wt. %CeO2与铝箔键合界面,铝箔一侧表面残留有部分大尺寸白色物质,而相应的聚合物表面有大小不一的凹陷坑,说明此时拉伸断裂有部分发生在键合母材,键合强度高, 见如表 4,键合质量较好。

|
图 8 键合界面拉伸断口形貌: (a)Al; (b)(PEG)10LiClO4-10wt. %SiO2 Fig.8 Tensile fracture morphology of bonding interface |

|
图 9 键合界面拉伸断口形貌: (a)Al; (b)(PEG)10LiClO4-8wt. %CeO2 Fig.9 Tensile fracture morphology of bonding interface |
| 表 4 室温下键合界面拉伸强度 Table 4 Tensile strength of bonding interface at room temperature |
1) 通过阻抗、XRD及热分析实验可知,PEG与LiClO4-SiO2/CeO2形成的络合体,能够有效抑制体系内部的结晶行为,打开了荷电粒子传输通道,并可促进碱金属离子的解离,释放更多可自由移动的Li+,提高复合材料离子导电率。
2) PEG基固体电解质经纳米颗粒(SiO2/CeO2) 改性后,其分子强化机制明显,能够有效促进应力的分散和转移,提高材料力学性能。
3) 经SiO2/CeO2改性后的PEG基固体电解质阳极键合性能得到显著提高,当CeO2含量为8wt. %时,(PEG)10LiClO4-8wt. %CeO2与铝的阳极键合性能最佳。
4) 阳极键合实验及键合后对键合界面的分析测试结果表明,在相同键合条件下,(PEG)10LiClO4-8wt. %CeO2与铝的阳极键合质量最优,键合界面生成的键合层是键合成功的关键。
| [1] |
HOU L, WU P. Understanding the UCST-type transition of P (AAM-co-AN) in HM2O and D2O: Dramatic effects of solvent isotopes[J]. Soft Matter, 2015, 11(35): 7059-7065. DOI:10.1039/C5SM01745A |
| [2] |
杜超, 刘翠荣, 阴旭, 等. 阳极键合研究现状及影响因素[J]. 材料科学与工艺, 2018, 26(5): 82-88. DU Chao, LIU Cuirong, YIN Xu, et al. Research status and influencing factors of anodic bonding[J]. Materials Science and Technology, 2018, 26(5): 82-88. DOI:10.11951/j.issn.1005-0299.20170313 |
| [3] |
沈伟东, 吴亚明, 章岳光, 等. 电子束蒸发玻璃薄膜中间层的阳极键合研究[J]. 真空科学与技术学报, 2008, 28(2): 143-147. SHEN Weidong, WU Yaming, ZHANG Yueguang, et al. Anodic bonding of intermediate glass films grown by e-beam evaporation[J]. Chinese Journal of Vacuum Science and Technology, 2008, 28(2): 143-147. DOI: CNKI:SUN:ZKKX.0.2008-02-012 |
| [4] |
WOETZEL S, KESSLER E, DIEGEL M, et al. Low-temperature anodic bonding using thin films of lithium-niobate-phosphate glass[J]. Journal of Micromechanics & Microengineering, 2014, 24(9): 95-100. DOI:10.1088/0960-1317/24/9/095001 |
| [5] |
LI T, TANG H, WU P. Molecular evolution of poly(2-isopropyl-2-oxazoline) aqueous solution during the liquid-liquid phase separation and phase transition process[J]. Langmuir, 2015, 31(24): 6870-6878. DOI:10.1039/c8cc09835b |
| [6] |
YEN W, LIN Y. A Study on the bonding conditions and mechanism for glass-to-glass anodic bonding in field emission display[J]. Journal of Adhesion Science and Technology, 2009, 23(1): 151-162. DOI:10.1163/156856108X344577 |
| [7] |
CHENG S, SMITH D M, LI C Y. How does nanoscale crystalline structure affect ion transport in solid polymer electrolytes[J]. Macromolecules, 2014, 47(12): 3978-3986. DOI:10.1021/ma500734q |
| [8] |
XIONG H M, ZHAO X, CHEN J S. New polymer-inorganic nanocomposites PEO-ZnO and PEO-ZnO-LiClO4 films[J]. Journal of Physical Chemistry B, 2001, 105: 10169-10174. DOI:10.1021/jp0103169 |
| [9] |
PATIL S U, YAWALE S S, YAWALE S P. Conductivity study of PEO-LiClO4 polymer electrolyte dopedwith ZnO nanocomposite ceramic filler[J]. Bulletin of Material Science, 2014, 37: 1403-1409. DOI:10.1007/s12034-014-0089-z |
| [10] |
DU Chao, LIU Cuirong, YIN Xu. Polyethylene glycol-based solid polymer electrolytes: Encapsulation materials with excellent anodic bonding performance[J]. Journal of Inorganic and Organometallic Polymers and Materials, 2017, 27(5): 1521-1525. DOI:10.1007/s10904-017-0612-y |
| [11] |
DU Chao, LIU Cuirong, YIN Xu. Effect of cooling mode on anodic bonding properties of solid polymer electrolytes[J]. Journal of Inorganic and Organometallic Polymers and Materials, 2018, 28(1): 146-151. DOI:10.1007/s10904-017-0658-x |
| [12] |
李星, 陈立国, 王阳俊. 激光辅助阳极键合方法及实验研究[J]. 纳米技术与精密工程, 2017, 15(1): 67-71. LI Xing, CHEN Liguo, WANG Yangjun. Method and experimental study on laser assisted anodic bonding[J]. Nanotechnology and Precision Engineering, 2017, 15(1): 67-71. DOI:10.13494/j.npe.20160058 |
| [13] |
JOYCE R, SINGH K, VARGHESE S, et al. Stress reduction in silicon/oxidized silicon-Pyrex glass anodic bonding for MEMS device packaging: RF switches and pressure sensors[J]. Journal of Materials Science: Materials in Electronics, 2015, 26(1): 411-423. DOI:10.1007/s10854-014-2415-z |
| [14] |
DU Chao, LIU Cuirong, YIN Xu, et al. Synthesis and bonding performance of conductive polymer containing rare earth oxides[J]. Journal of Inorganic and Organometallic Polymers and Materials, 2018, 28(3): 746-750. DOI:10.1007/s10904-017-0713-7 |
| [15] |
WU T, YAMASAKI T, HOKARI R. Spherical silicon micromirrors bent by anodic bonding[J]. Optics Express, 2011, 19(12): 11897-11905. DOI:10.1364/OE.19.011897 |
| [16] |
WOETZEL S, KESSLER E, DIEGEL M, et al. Low-temperature anodic bonding using thin films of lithium-niobate-phosphate glass[J]. Journal of Micromechanics & Microengineering, 2014, 24(9): 95-100. DOI:10.1088/0960-1317/24/9/095001 |
| [17] |
YIN X, LIU C R. Synthesis and properties of ionic conduction polymer for anodic bonding[J]. Chinese Chemical Letters, 2015, 26(3): 289-292. DOI:10.1016/j.cclet.2014.10.027 |
 2021, Vol. 29
2021, Vol. 29


